Содержание
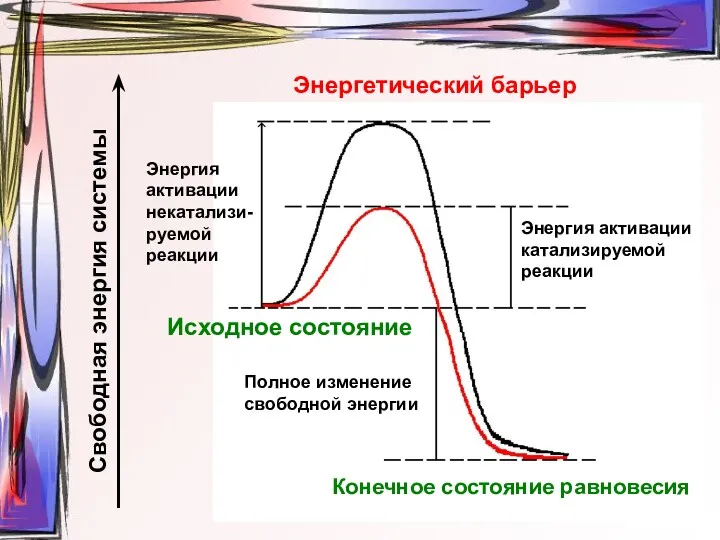
- 2. Энергия активации катализируемой реакции Полное изменение свободной энергии Энергия активации некатализи-руемой реакции Исходное состояние Конечное состояние
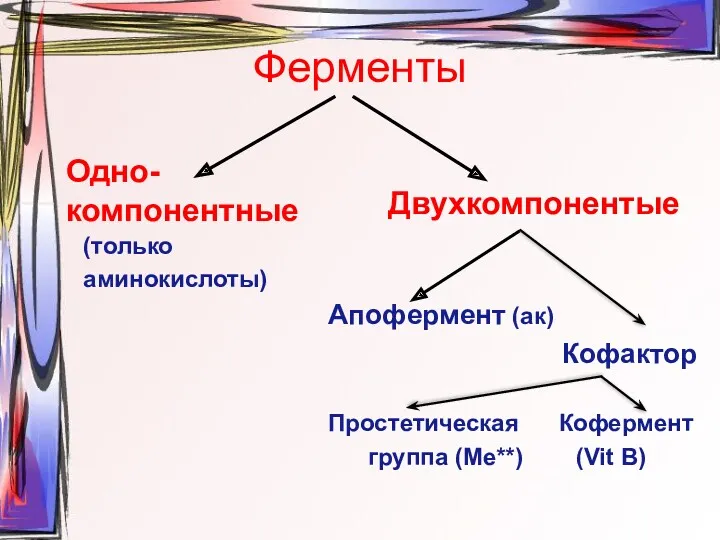
- 3. Ферменты Одно-компонентные (только аминокислоты) Двухкомпонентые Апофермент (ак) Кофактор Простетическая Кофермент группа (Ме**) (Vit В)
- 4. Собственные свойства ферментов Высокая биологическая активность Ферментная специфичность действия субстратная Иная зависимость от факторов, влияющих на
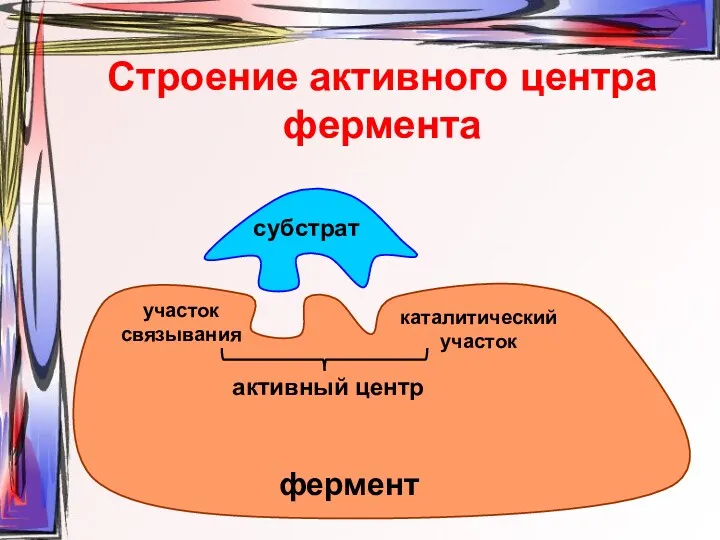
- 5. Строение активного центра фермента субстрат участок связывания каталитический участок активный центр фермент
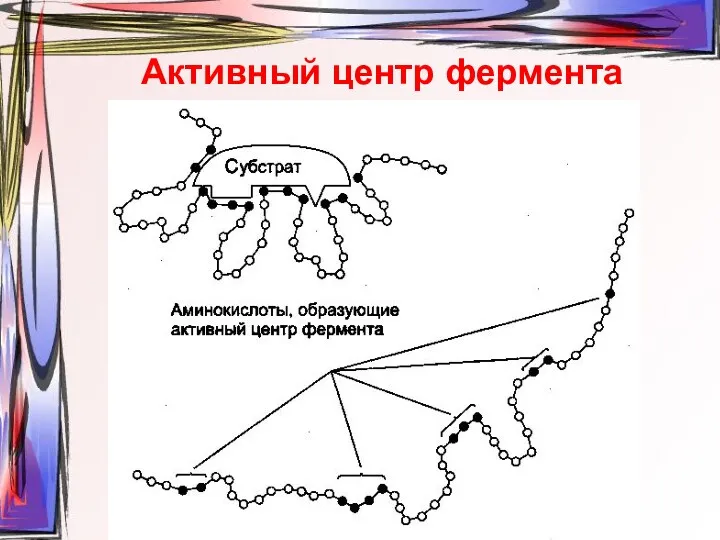
- 6. Активный центр фермента
- 7. Металлы, содержащиеся в ферментах
- 8. Каталитические центры ферментов Ко-А, глутатион, липоевая кислота пиридоксальфосфат тетрагидрофолиевая кислота флавины биотин тиаминпирофосфат НАД+ и НАДФ+
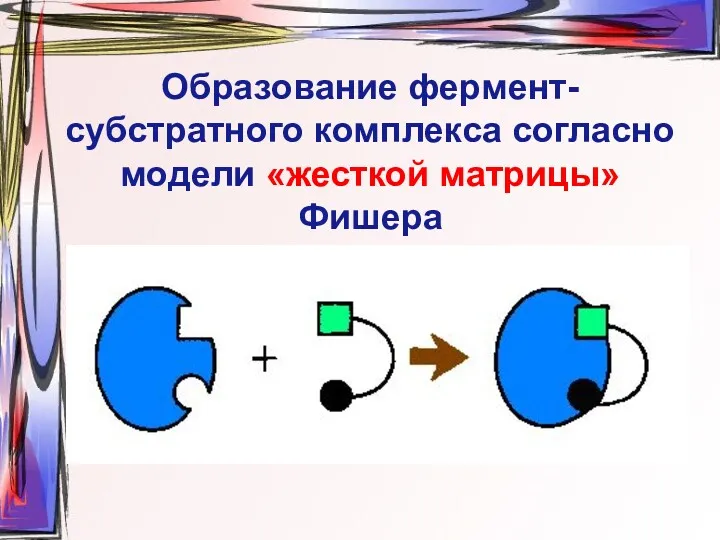
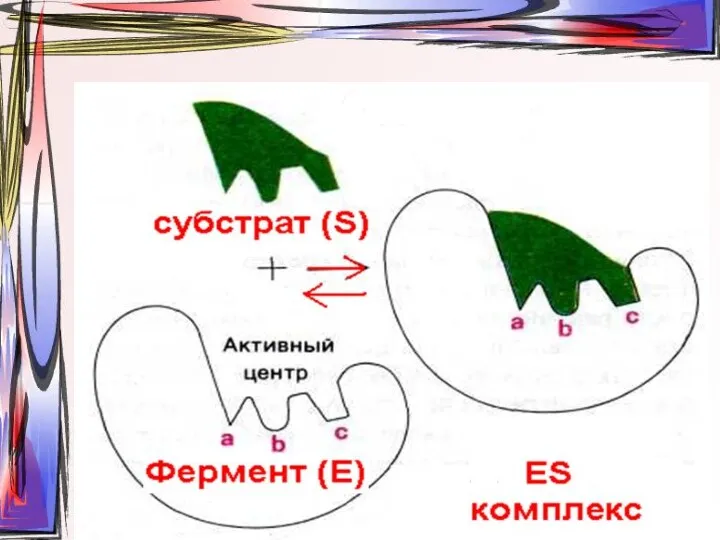
- 9. Образование фермент-субстратного комплекса согласно модели «жесткой матрицы» Фишера
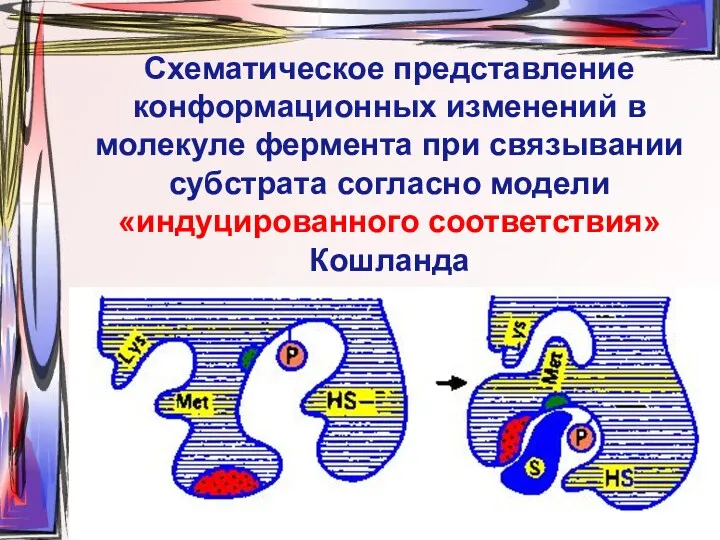
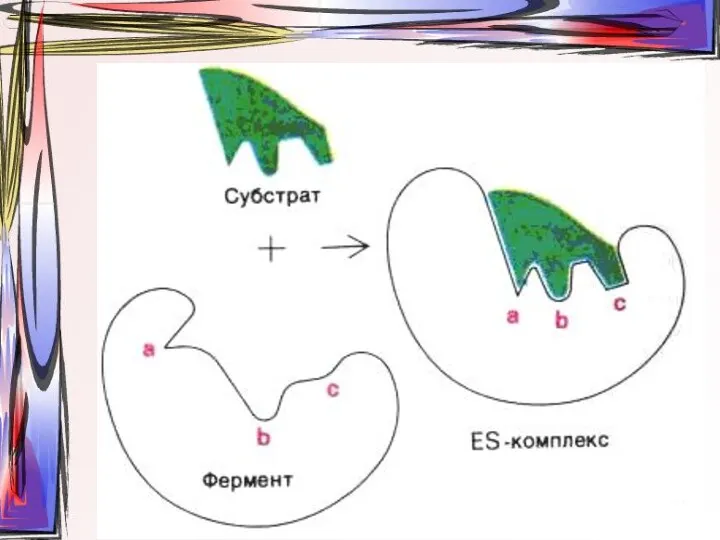
- 11. Схематическое представление конформационных изменений в молекуле фермента при связывании субстрата согласно модели «индуцированного соответствия» Кошланда
- 13. Общее уравнение ферментативной реакции: E + S ES EP E + P k2 k3 k1
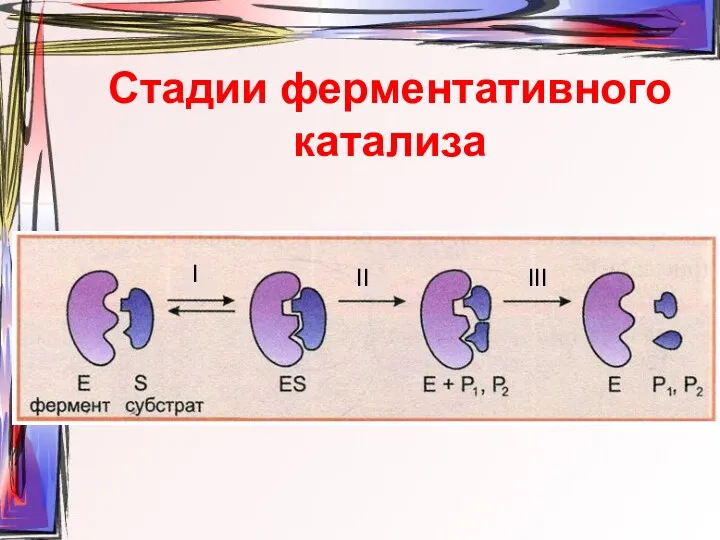
- 14. Стадии ферментативного катализа I III II
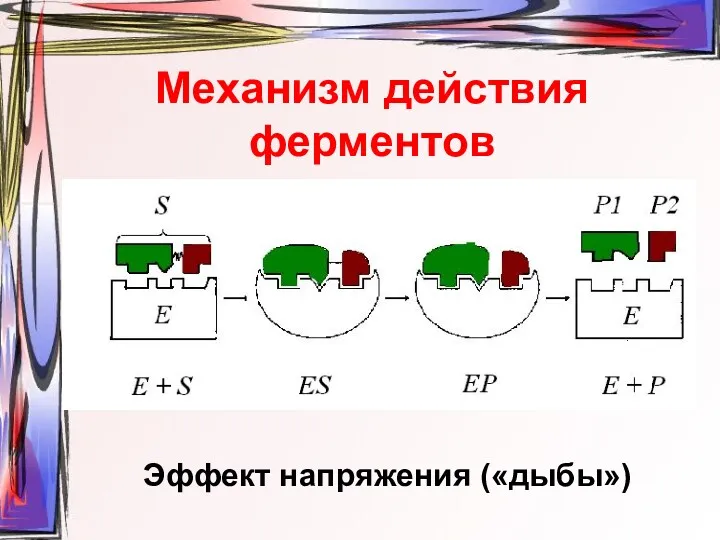
- 15. Механизм действия ферментов Эффект напряжения («дыбы»)
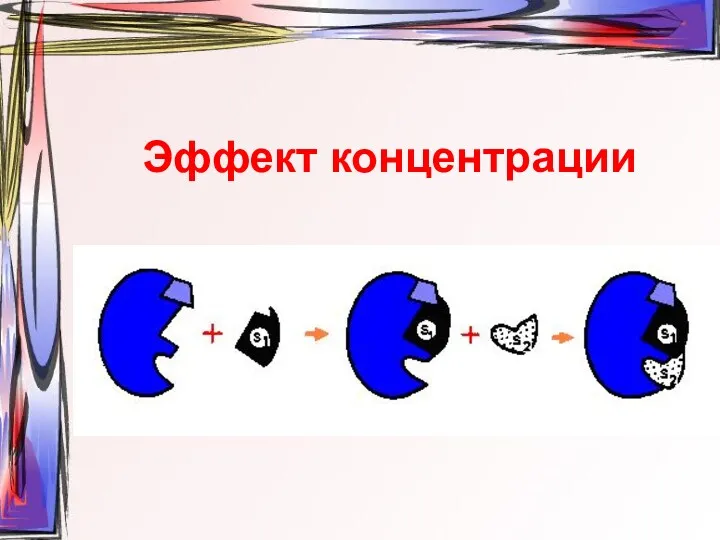
- 16. Эффект концентрации
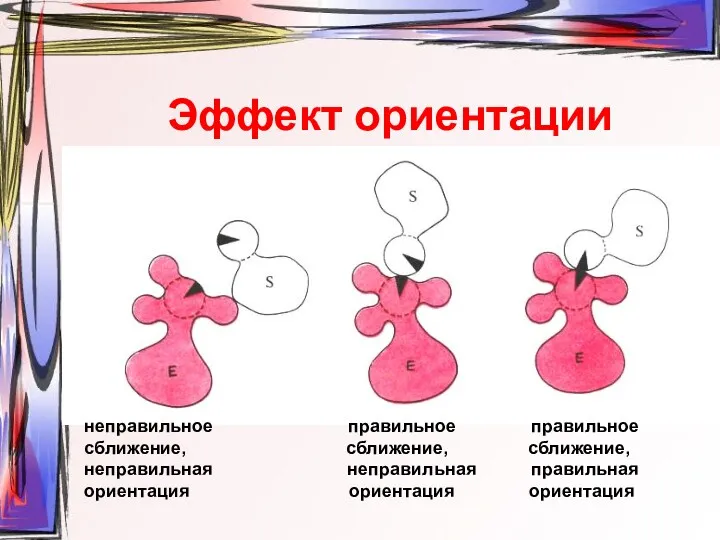
- 17. Эффект ориентации неправильное правильное правильное сближение, сближение, сближение, неправильная неправильная правильная ориентация ориентация ориентация
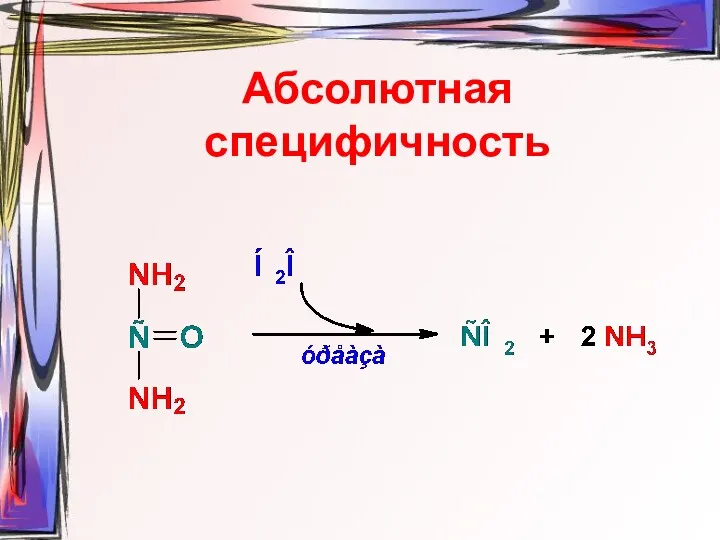
- 18. Абсолютная специфичность
- 19. Абсолютная специфичность
- 20. Относительная специфичность
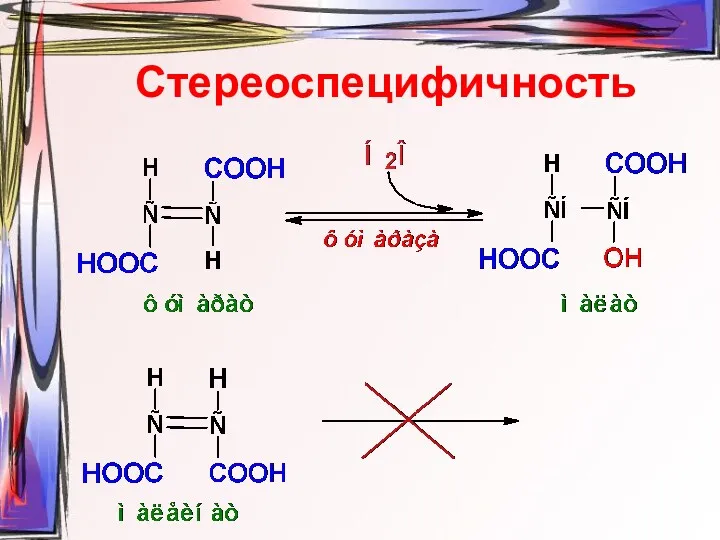
- 21. Стереоспецифичность
- 22. Общее уравнение ферментативной реакции: E + S ES EP E + P k2 k3 k1
- 23. Константа Михаэлиса
- 24. Зависимость скорости ферментативной реакции от концентрации субстрата
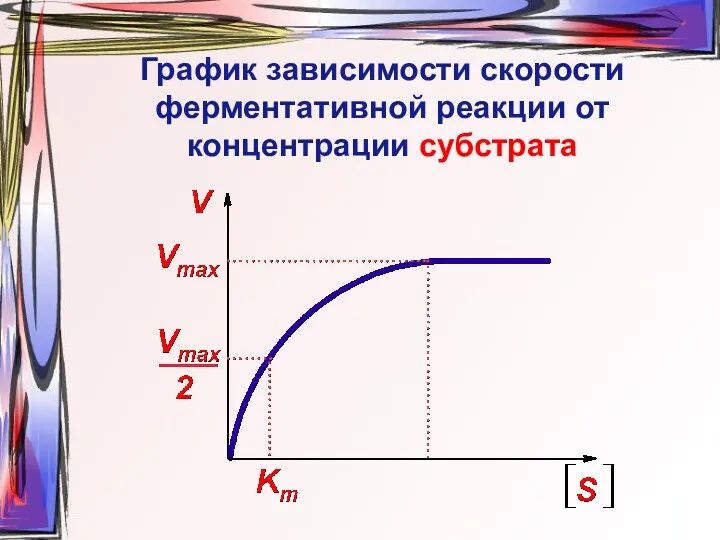
- 25. [S] >> Km; V = Vmax [S] [S] = Km; V = ½ Vmax
- 26. График зависимости скорости ферментативной реакции от концентрации субстрата
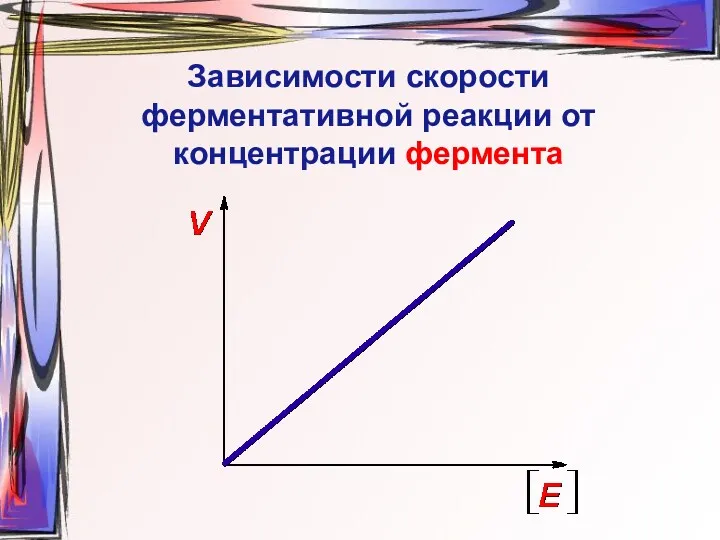
- 27. Зависимости скорости ферментативной реакции от концентрации фермента
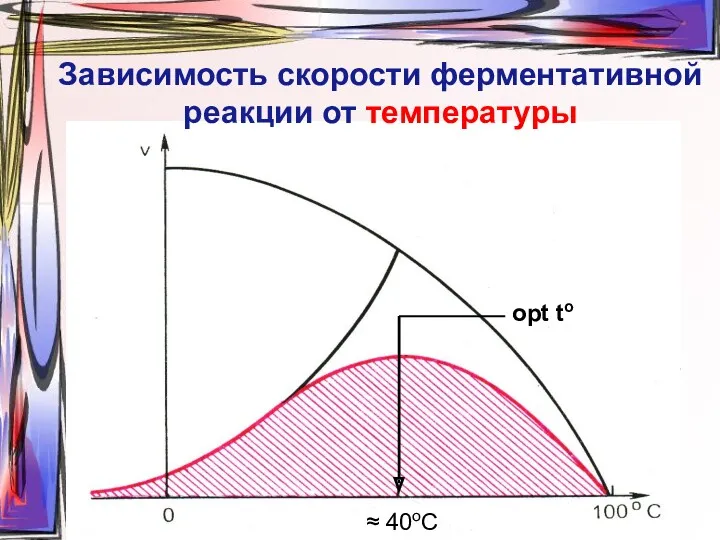
- 28. Зависимость скорости ферментативной реакции от температуры opt to ≈ 40oC
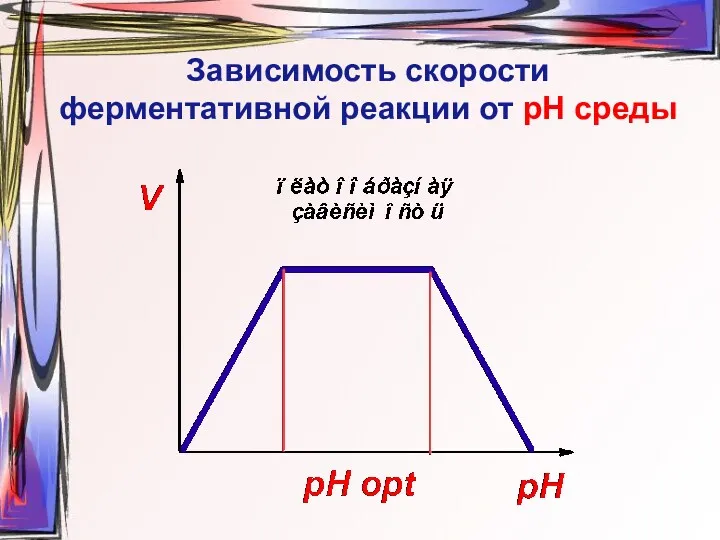
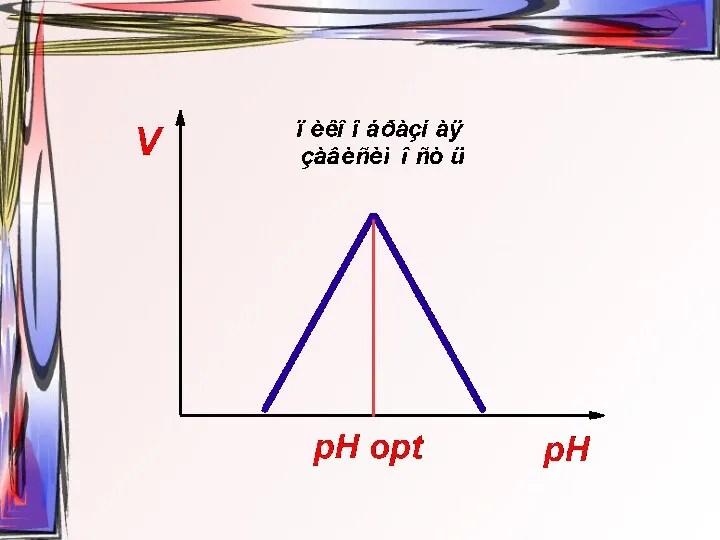
- 29. Зависимость скорости ферментативной реакции от рН среды
- 33. Скачать презентацию









![[S] >> Km; V = Vmax [S] [S] = Km; V = ½ Vmax](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270648/slide-24.jpg)

 Происхождение человека. Люди эпохи палеолита
Происхождение человека. Люди эпохи палеолита Жизнь в морях и океанах
Жизнь в морях и океанах Реализация генетической информации. Пластический обмен. Синтез белка
Реализация генетической информации. Пластический обмен. Синтез белка Физиология пищеварения
Физиология пищеварения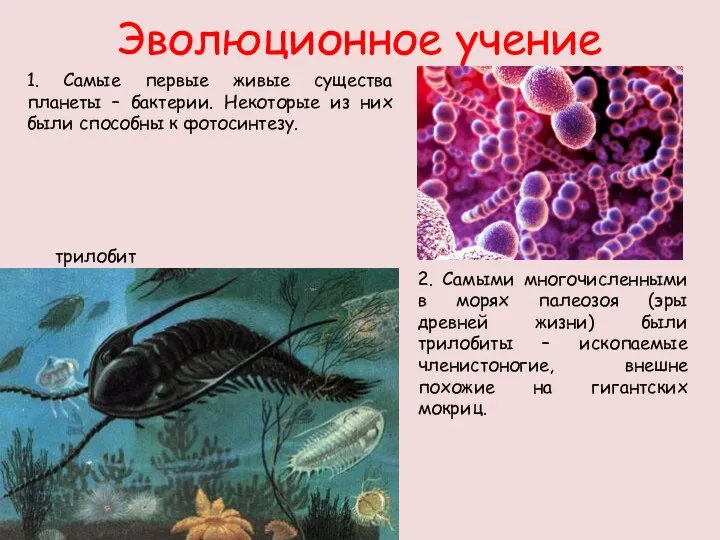 Биология. 7 класс. Эволюционное учение.
Биология. 7 класс. Эволюционное учение. Биохимия. Ферменты (Лекция№2)
Биохимия. Ферменты (Лекция№2) Насекомые. Игра Как стать миллионером
Насекомые. Игра Как стать миллионером Энергообразующие органоиды (лекция 7)
Энергообразующие органоиды (лекция 7) Цветковые растения
Цветковые растения Общая гистология. Ткань
Общая гистология. Ткань Анатомо-физиологические особенности репродуктивной системы человека
Анатомо-физиологические особенности репродуктивной системы человека Определение пола особи
Определение пола особи Царство животные. Тип хордовые. Класс пресмыкающиеся или рептилии
Царство животные. Тип хордовые. Класс пресмыкающиеся или рептилии Происхождение человека и становление общества
Происхождение человека и становление общества Семинар учителей биологии. Решение генетических задач
Семинар учителей биологии. Решение генетических задач Тип Членистоногие, класс Ракообразные
Тип Членистоногие, класс Ракообразные Структурные уровни организации живого. Свойства живого
Структурные уровни организации живого. Свойства живого певчие птицы россии
певчие птицы россии Папоротниктәрізділер, Қырықбуынтәрізділердің. Табиғаттағы, фармациядағы, медицинадағы маңызы
Папоротниктәрізділер, Қырықбуынтәрізділердің. Табиғаттағы, фармациядағы, медицинадағы маңызы Тип Хордовые. Подтипы: Бесчерепные и Черепные, или Позвоночные
Тип Хордовые. Подтипы: Бесчерепные и Черепные, или Позвоночные Решение задач на составление и анализ родословных
Решение задач на составление и анализ родословных Функциональная асимметрия мозга. Лекция 11
Функциональная асимметрия мозга. Лекция 11 Система движения. Поддержание позы и движения животного
Система движения. Поддержание позы и движения животного Экологические аспекты производства биопрепаратов
Экологические аспекты производства биопрепаратов Мікроскопічні гриби, що викликають хвороби у рослин
Мікроскопічні гриби, що викликають хвороби у рослин Биология клетки в культуре. Клеточная и генная инженерия 2
Биология клетки в культуре. Клеточная и генная инженерия 2 Общая физиология нервной системы и возбудимых тканей
Общая физиология нервной системы и возбудимых тканей Низшие растения водоросли
Низшие растения водоросли