Содержание
- 2. Ферменты от латинского fermentum брожение, закваска Энзимы от греческого enzyme ЭН – в, ЗИМ – закваска,
- 3. Практически все химические реакции в живых организмах протекают при участии ферментов. Для клетки ферменты абсолютно необходимы,
- 4. Ферменты – белки и РНК Первый кристаллический белок-фермент (уреаза) вы-делен в 1926 г американским биохимиком Д.Самнером
- 5. Общие свойства ферментов и химических катализаторов небелковой природы Не могут возбудить реакций, противоречащих законам термодинамики. Не
- 6. Отличительные признаки ферментативного и химического катализа Скорость ферментативного катализа намного выше, чем небиологического У ферментов высокая
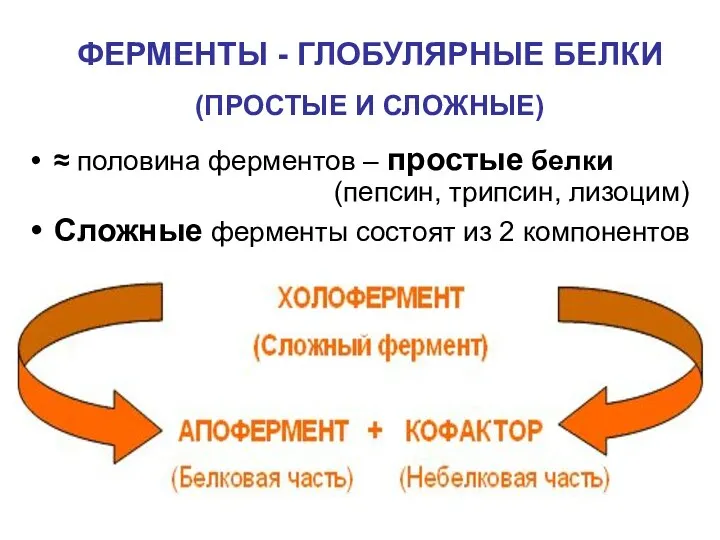
- 7. ФЕРМЕНТЫ - ГЛОБУЛЯРНЫЕ БЕЛКИ (ПРОСТЫЕ И СЛОЖНЫЕ) ≈ половина ферментов – простые белки (пепсин, трипсин, лизоцим)
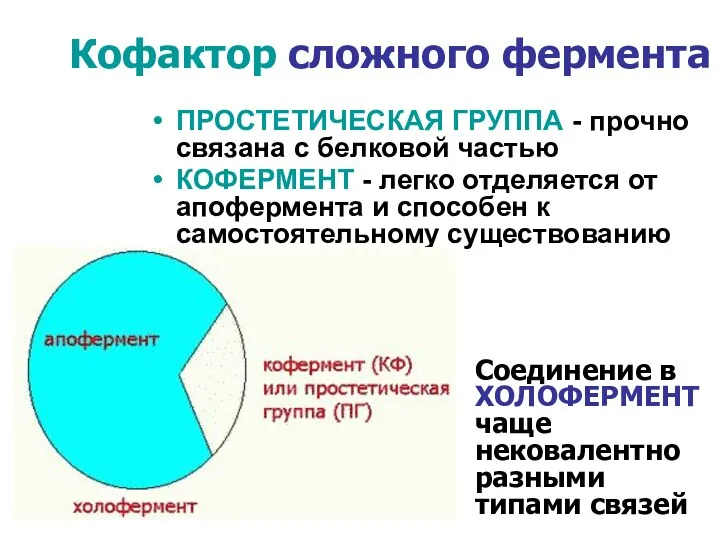
- 8. ПРОСТЕТИЧЕСКАЯ ГРУППА - прочно связана с белковой частью КОФЕРМЕНТ - легко отделяется от апофермента и способен
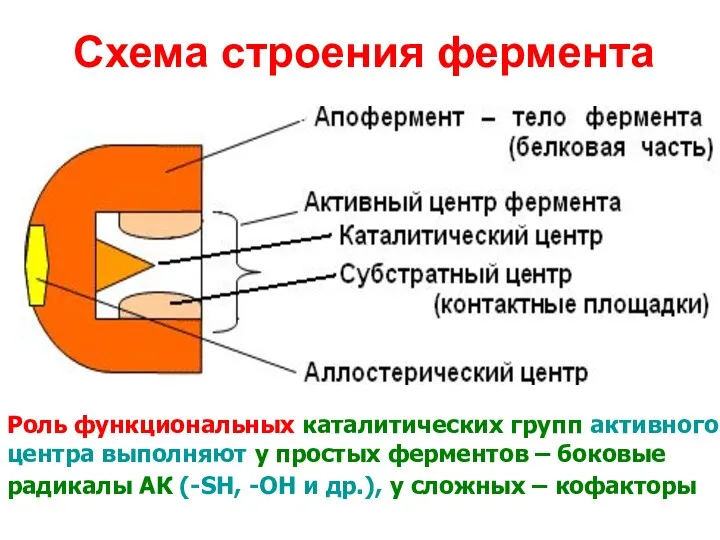
- 9. Схема строения фермента Роль функциональных каталитических групп активного центра выполняют у простых ферментов – боковые радикалы
- 10. 1. Участие в акте катализа 2. Осуществление контакта между энзимом и субстратом 3. Стабилизация апофермента роль
- 11. КЛАССИФИКАЦИЯ КОФАКТОРОВ 1.витамины, их производные Большинство витаминов или соединений, построенных с участием витаминов - тиаминовые (В1
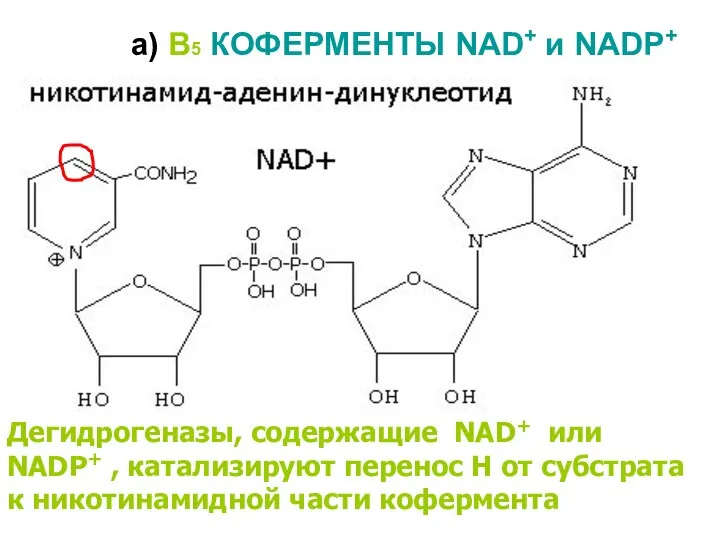
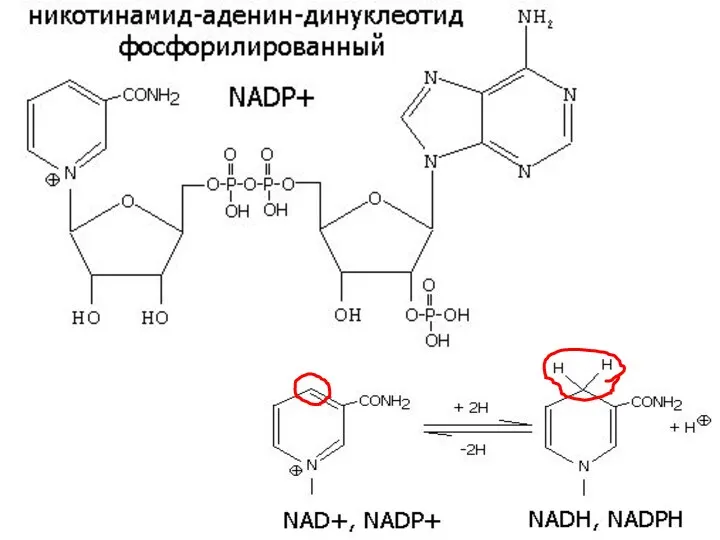
- 12. а) В5 КОФЕРМЕНТЫ NAD+ и NADP+ Дегидрогеназы, содержащие NAD+ или NADP+ , катализируют перенос Н от
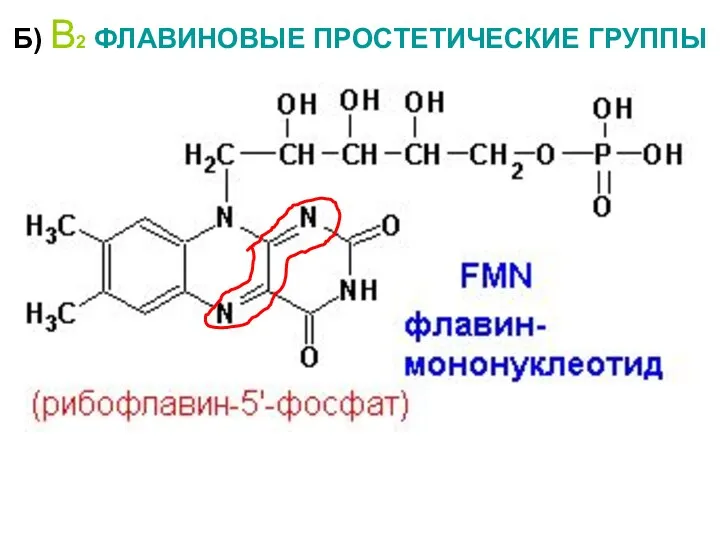
- 14. Б) В2 ФЛАВИНОВЫЕ ПРОСТЕТИЧЕСКИЕ ГРУППЫ
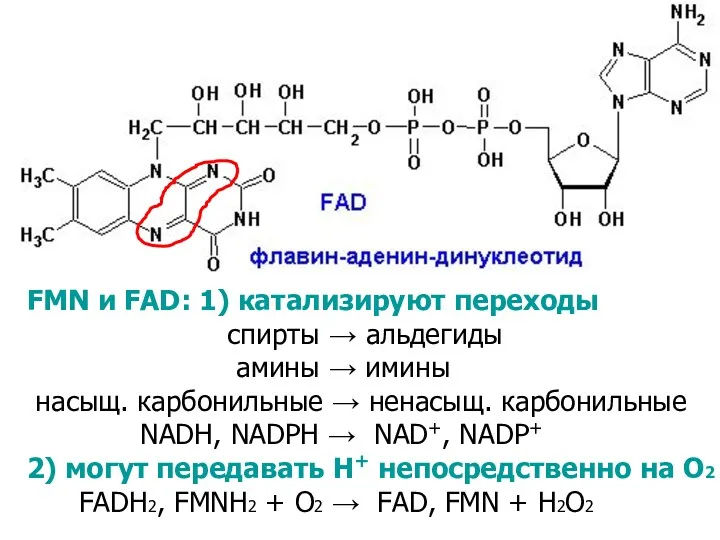
- 15. FMN и FAD: 1) катализируют переходы спирты → альдегиды амины → имины насыщ. карбонильные → ненасыщ.
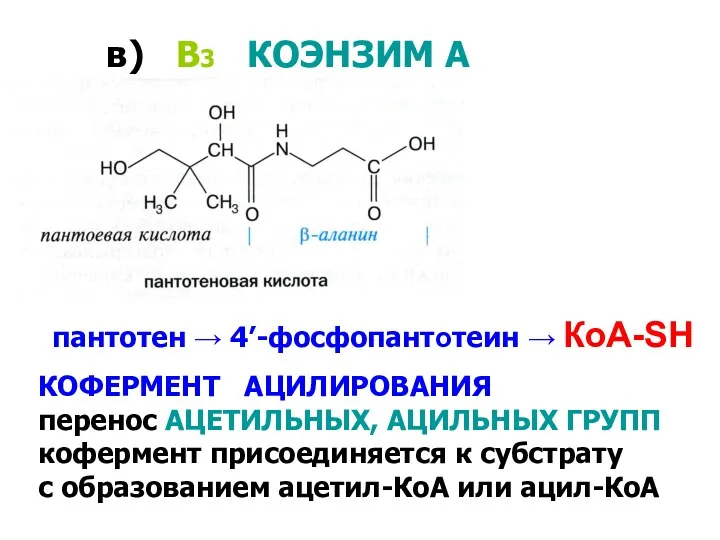
- 16. в) В3 КОЭНЗИМ А КОФЕРМЕНТ АЦИЛИРОВАНИЯ перенос АЦЕТИЛЬНЫХ, АЦИЛЬНЫХ ГРУПП кофермент присоединяется к субстрату с образованием
- 17. 2. невитаминные 1) нуклеотидного типа: нуклеотиды и их производные реакции переноса, ферменты – трансферазы а) НУКЛЕОЗИД-ТРИФОСФАТЫ
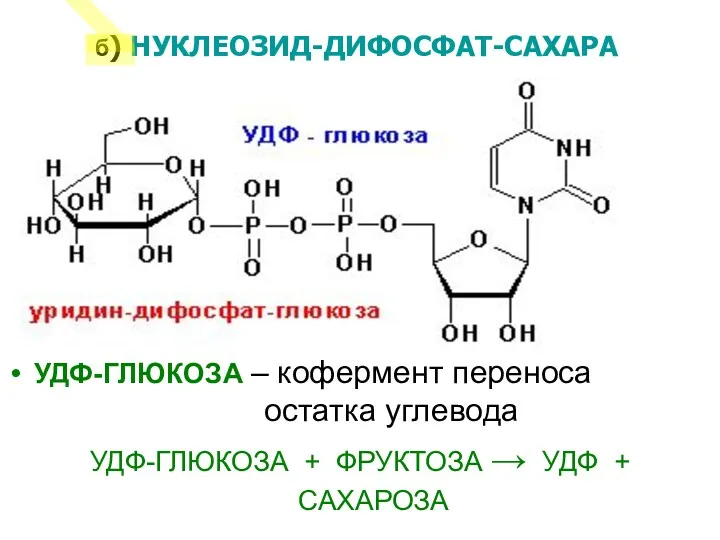
- 18. УДФ-ГЛЮКОЗА – кофермент переноса остатка углевода УДФ-ГЛЮКОЗА + ФРУКТОЗА → УДФ + САХАРОЗА б) НУКЛЕОЗИД-ДИФОСФАТ-САХАРА
- 19. К невитаминным кофакторам также относят 2) металлопорфириновые (гем у каталазы, пероксидаз) 3) фосфорные эфиры некоторых моносахаридов
- 20. Классификация и НОМЕНКЛАТУРА ФЕРМЕНТОВ Вначале называли по случайным признакам (тривиальная номенклатура – пепсин, трипсин…) Сейчас используется
- 21. Международная класификация Утверждена в 1961 г. КФ - русскоязычная, ЕС - англоязычная В её основе механизм
- 22. КЛАССЫ ФЕРМЕНТОВ Всё многообразие реакций сводится к 6 типам (СМ реакции в приложении к ПРАКТИКУМУ!!!) 1.
- 23. 2. Трансферазы Подклассы: Метил-, Карбоксил- и карбамоил-, Ацил-, Гексозил-, Амино-, Фосфотрансферазы … реакции переноса различных групп
- 24. 4. Лиазы или Синтазы Подклассы: Лиазы связи С-О, Лиазы связи С-N, Лиазы связи С-S и другие.
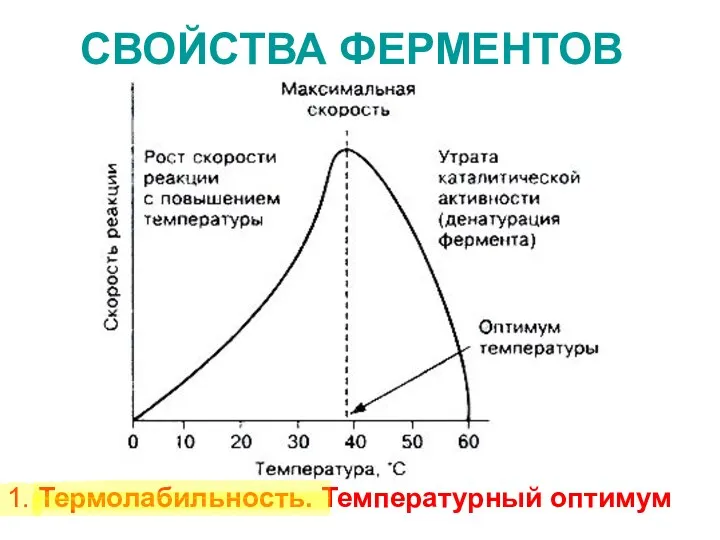
- 25. СВОЙСТВА ФЕРМЕНТОВ 1. Термолабильность. Температурный оптимум
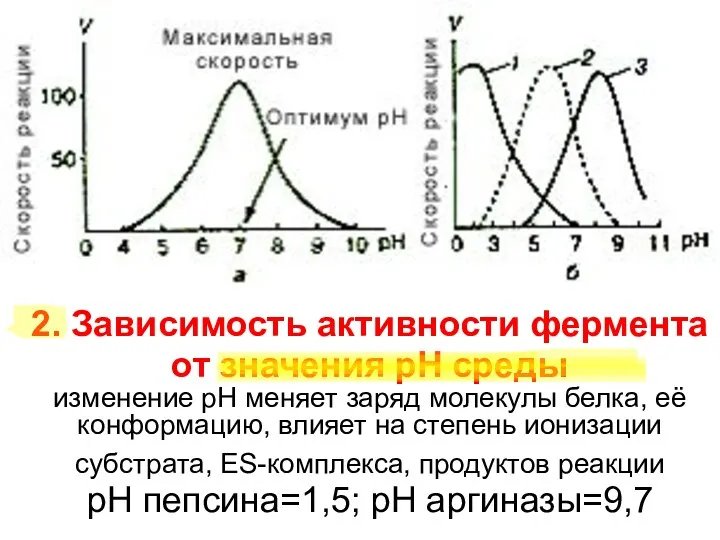
- 26. 2. Зависимость активности фермента от значения рН среды изменение рН меняет заряд молекулы белка, её конформацию,
- 27. 3. Зависимость скорости ферментативной реакции от концентрации субстрата [S] Кm - константа Михаэлиса
- 28. Зависимость скорости ферментативной реакции от концентрации субстрата может быть описана уравнением: V - скорость ферментативной реакции,
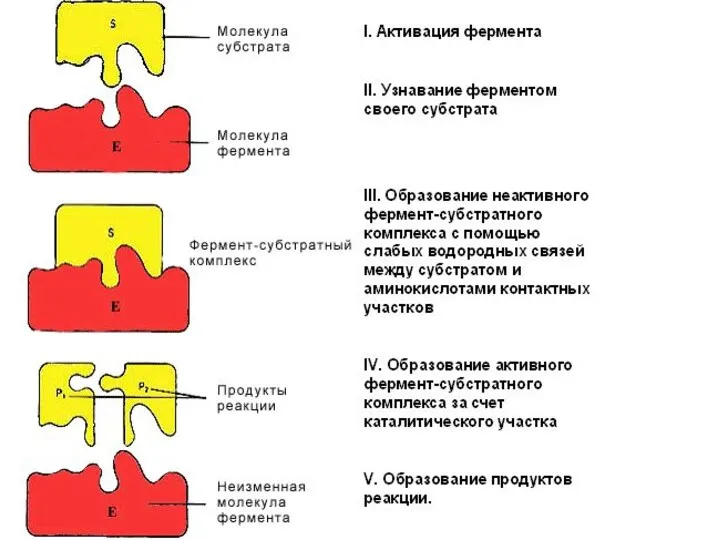
- 29. 4. Специфичность фермента Основана на строгой комплементарности структуры субстрата и активного центра Абсолютная катализ определенного типа
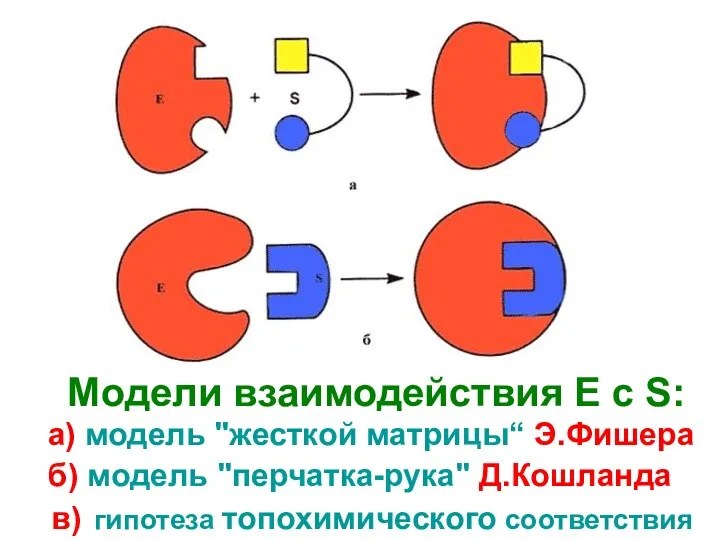
- 30. Модели взаимодействия Е с S: а) модель "жесткой матрицы“ Э.Фишера б) модель "перчатка-рука" Д.Кошланда в) гипотеза
- 31. Статическая гипотеза Э. Фишера 1894 г. – фермент подходит к субстрату, как "ключ к замку". Абсолютная
- 33. Механизмы катализа Известно 6 видов катализа 1) кислотно-основный 2) ковалентный 3) с участием ионов металлов 4)
- 34. Примеры механизмов катализа 1. Кислотно-основный катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков,
- 35. Кинетика – учение о скорости химических реакций организма и факторах, влияющих на неё Скорость реакции –
- 36. КИНЕТИКА ФЕРМЕНТАТИВНОГО КАТАЛИЗА Е + S ↔ [ES*] → Е + Р фермент субстрат продукт E-S
- 37. Регуляция активности ферментов I. эффекторами: а) активаторы б) ингибиторы II. в том числе аллостерические механизмы III.
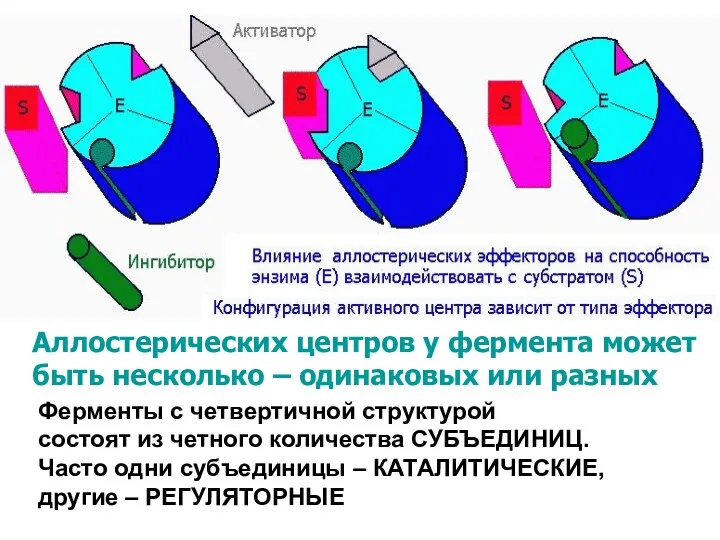
- 38. аллостерическая регуляция allos - другой, steros – пространство, чужой структура АЛЛОСТЕРИЧЕСКИЙ ЦЕНТР – пространственно отделённый от
- 39. Ферменты с четвертичной структурой состоят из четного количества СУБЪЕДИНИЦ. Часто одни субъединицы – КАТАЛИТИЧЕСКИЕ, другие –
- 40. Активаторы ферменты переходят в активную форму под влиянием активаторов. Например, Ионы. Ионы хлора – активаторы амилазы
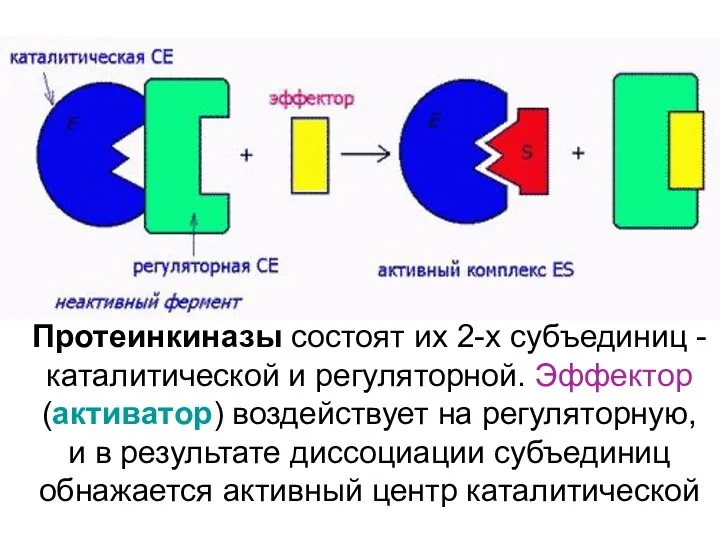
- 41. Протеинкиназы состоят их 2-х субъединиц - каталитической и регуляторной. Эффектор (активатор) воздействует на регуляторную, и в
- 42. Ингибиторы Необратимые связываются ковалентно Обратимые связываются нековалентно Ингибирование бывает: Конкурентное – ингибитор по структуре похож на
- 43. двойные обратные координаты Лайнуивера-Берка (1/V0 -1/[S]) ОПРЕДЕЛЕНИЕ ТИПА ИНГИБИРОВАНИЯ КОНКУРЕНТНЫЙ ингибитор увеличивает Кm, не меняет Vmax
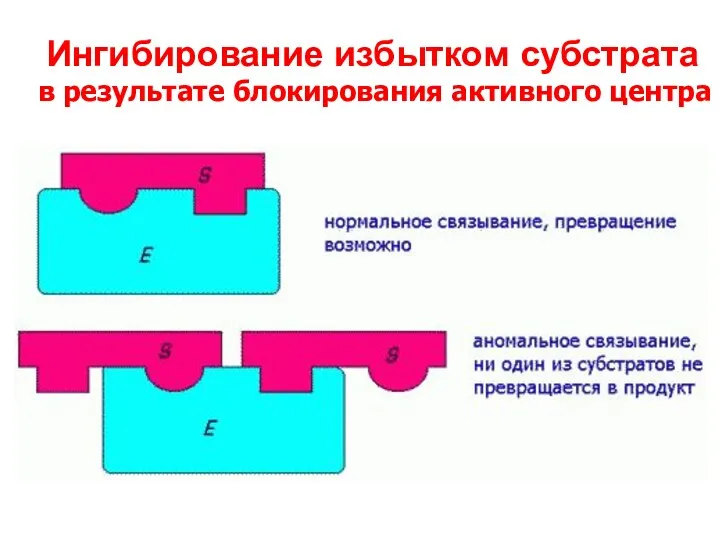
- 44. Ингибирование избытком субстрата в результате блокирования активного центра
- 45. КООПЕРАТИВНЫЙ ЭФФЕКТ Характерен для ферментов, имеющих две и более субъединиц Присоединение субстрата или эффектора к одной
- 46. Регуляция по механизму ковалентной модификации ОГРАНИЧЕННЫЙ ПРОТЕОЛИЗ (частичный точечный протеолиз) Автокатализ протеолитических ферментов пищеварения (пепсин, трипсин).
- 47. Регуляция ферментов за счёт их компартментализации Компартментализация – локализация ферментов и их субстратов в одном компартменте
- 48. ферментативный спектр органов и тканей внутриклеточные - действуют в тех же клетках, где синтезируются внеклеточные -
- 49. 1. ИЗОФЕРМЕНТЫ - отличаются по структуре (α-, β-, γ- субъединицы), но выполняют одну и ту же
- 50. Принципы определения активности ферментов Активность фермента (удельная) – скорость накопления продукта или скорость убыли субстрата в
- 51. Единицы активности Е (стандартные единицы) - количество фермента, которое превращает 1 микромоль субстрата за 1 минуту
- 52. Энзимодиагностика заболеваний 1) При энзимодиагностике болезней оценивают выход ферментов из поврежденных структур клеток и тканей АсАТ
- 53. Энзимотерапия ферменты и регуляторы их активности (ингибиторы, активаторы) могут быть средствами заместительной и функциональной терапии -
- 54. Применение ИНГИБИТОРОВ ФЕРМЕНТОВ блокадой АЦЕТАЛЬДЕГИДДЕГИДРОГЕНАЗЫ в стационарах лечат хронический алкоголизм сульфаниламидные препараты (БИСЕПТОЛ, его аналоги) блокируют
- 55. недостатки в применении ферментативных препаратов Проявление антигенных свойств Ненаправленное проявление агрессивных свойств Трудность доставки к поражённым
- 56. Энзимопатии первичные - недостаточность или полное отсутствие отдельных ферментов - избыточность действия того или иного фермента
- 58. Скачать презентацию














![3. Зависимость скорости ферментативной реакции от концентрации субстрата [S] Кm - константа Михаэлиса](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336595/slide-26.jpg)






![КИНЕТИКА ФЕРМЕНТАТИВНОГО КАТАЛИЗА Е + S ↔ [ES*] → Е](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336595/slide-35.jpg)




![двойные обратные координаты Лайнуивера-Берка (1/V0 -1/[S]) ОПРЕДЕЛЕНИЕ ТИПА ИНГИБИРОВАНИЯ КОНКУРЕНТНЫЙ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336595/slide-42.jpg)












 Лист. Внешнее и внутреннее строение
Лист. Внешнее и внутреннее строение Гипотезы возникновения жизни. 9 класс
Гипотезы возникновения жизни. 9 класс Растения и животные леса
Растения и животные леса Біологічні основи ембріонального розвитку організмів. Лекція 7
Біологічні основи ембріонального розвитку організмів. Лекція 7 Пищеварение в ротовой полости
Пищеварение в ротовой полости Ведьмины мётлы
Ведьмины мётлы Первый и второй Законы Г. Менделя
Первый и второй Законы Г. Менделя Головоногие моллюски
Головоногие моллюски Интегративная (высшая нервная) деятельность организма
Интегративная (высшая нервная) деятельность организма Презентация к уроку биологии 5 класс Зачем живые организмы запасают питательные вещества?
Презентация к уроку биологии 5 класс Зачем живые организмы запасают питательные вещества? Строение живой клетки, химический состав и физико-химические свойства цитоплазмы
Строение живой клетки, химический состав и физико-химические свойства цитоплазмы Арнайы қозғалыстағы магниттік қозғалыстар
Арнайы қозғалыстағы магниттік қозғалыстар Строение и работа сердца
Строение и работа сердца Биология как наука
Биология как наука Класс насекомые. Муравьи
Класс насекомые. Муравьи Нервная система. Строение и функции
Нервная система. Строение и функции Цветущие листопадные кустарники
Цветущие листопадные кустарники Ткани, органы, системы органов
Ткани, органы, системы органов Введение в физиологию. Физиология клетки
Введение в физиологию. Физиология клетки Строение коры больших полушарий
Строение коры больших полушарий Продолговатый мозг и мост. Процессы регуляции вегетативных функций
Продолговатый мозг и мост. Процессы регуляции вегетативных функций Сердечно-сосудистая система
Сердечно-сосудистая система 20190217_tsvetok_stroenie_i_znachenie
20190217_tsvetok_stroenie_i_znachenie Абиотические факторы среды. Влажность
Абиотические факторы среды. Влажность Анатомия спинного мозга (medulla spinalis)
Анатомия спинного мозга (medulla spinalis) Дыхание. Типы дыхания
Дыхание. Типы дыхания Увеличительные приборы
Увеличительные приборы Эмбриоселекция
Эмбриоселекция