Содержание
- 2. Сло́жные белки́ (протеиды, холопротеины) — двухкомпонентные белки) — двухкомпонентные белки, в которых помимо пептидных цепей (простого
- 3. Сложный белок, состоящий из белковой части (апопротеин) и небелковой части (простетическая группа), называют «холопротеин». Простетическая группа
- 4. Классификация сложных белков – зависит от строения простетической группы Гликопротеины (содержат углеводы) Липопротеины (содержат липиды) Фосфопротеины
- 5. Количество и порядок соединения протомеров в белке называется четвертичной структурой Многие белки в своем составе имеют
- 6. Количество протомеров в структуре олигомерных белков Олигомерный белок состоит из протомеров, количество которых составляет от 2
- 7. Сборка протомеров в олигомерный белок. Комплементарность протомеров Схема образования димерной белковой молекулы. Между протомерами А и
- 8. Функционирование белков. Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей
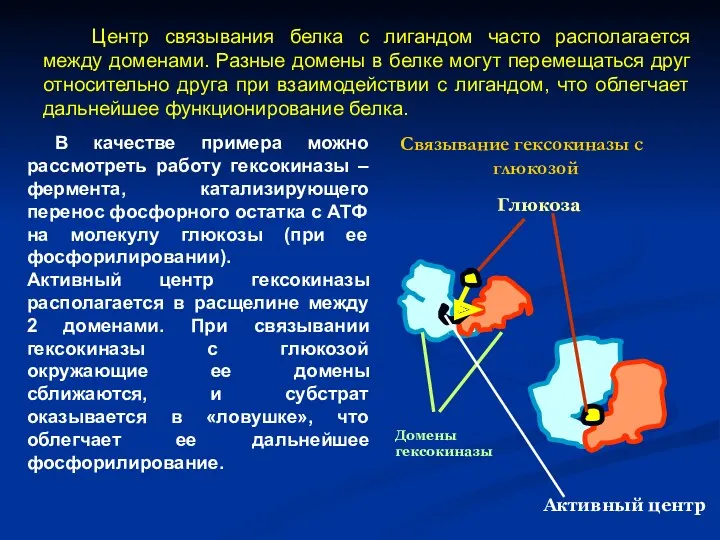
- 9. Центр связывания белка с лигандом часто располагается между доменами. Разные домены в белке могут перемещаться друг
- 10. Активный центр белков Это определенный участок белковой молекулы, как правило находящийся в ее углублении («кармане»), сформированный
- 11. В основе функционирования белков лежит их специфическое взаимодействие с лигандами. 50 000 индивидуальных белков, содержащих уникальные
- 12. Сродство активного центра лиганду Скорость взаимодействия белка с лигандом определяется концентрациями белка и лиганда в растворе,
- 13. Когда скорости образования и распада комплекса равны, то говорят, что система находится в состоянии равновесия: [Р][L]К1=[РL]К-1
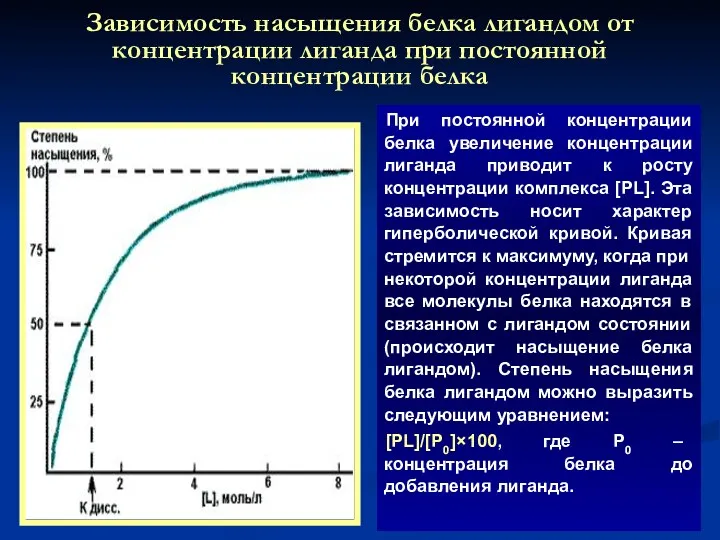
- 14. Зависимость насыщения белка лигандом от концентрации лиганда при постоянной концентрации белка При постоянной концентрации белка увеличение
- 15. Зависимость между образованием комплекса [PL] и концентрацией белка при избытке лиганда При возрастающей концентрации лиганда насыщение
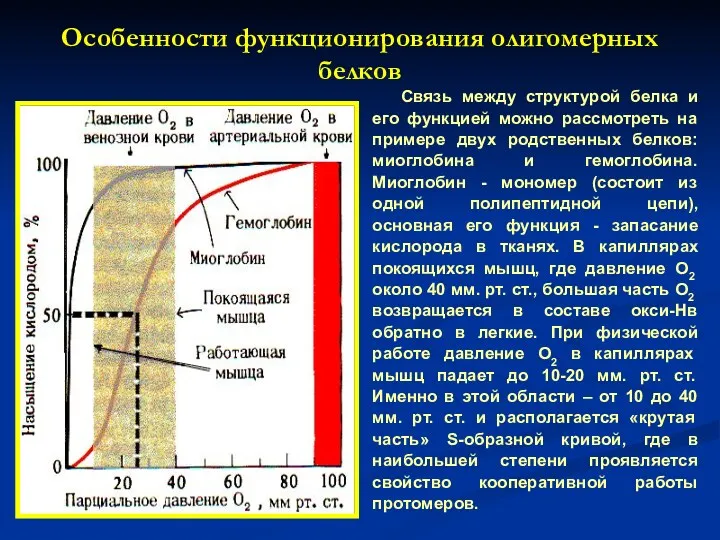
- 16. Особенности функционирования олигомерных белков Связь между структурой белка и его функцией можно рассмотреть на примере двух
- 17. Следовательно, благодаря уникальной структуре каждый из рассмотренных белков приспособлен выполнять свою функцию: миоглобин – присоединять О2,
- 18. Взаимодействие обоих белков (Мв и Нв) с кослородом зависит от его парциального давления в тканях. Нв
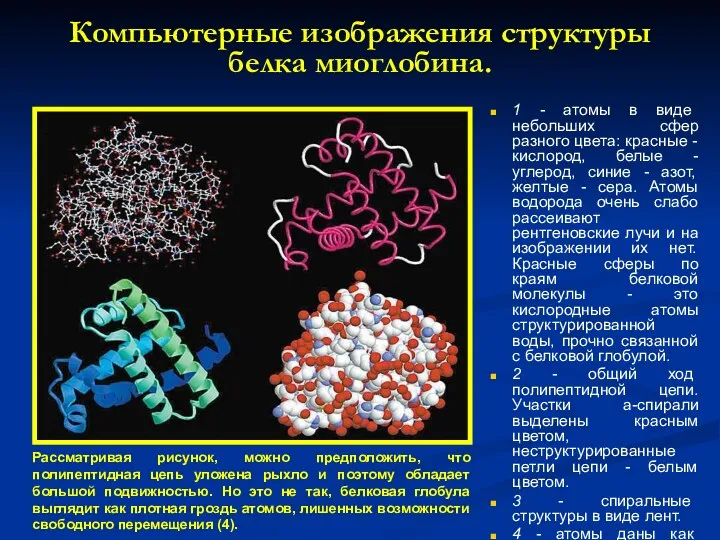
- 19. Компьютерные изображения структуры белка миоглобина. 1 - атомы в виде небольших сфер разного цвета: красные -
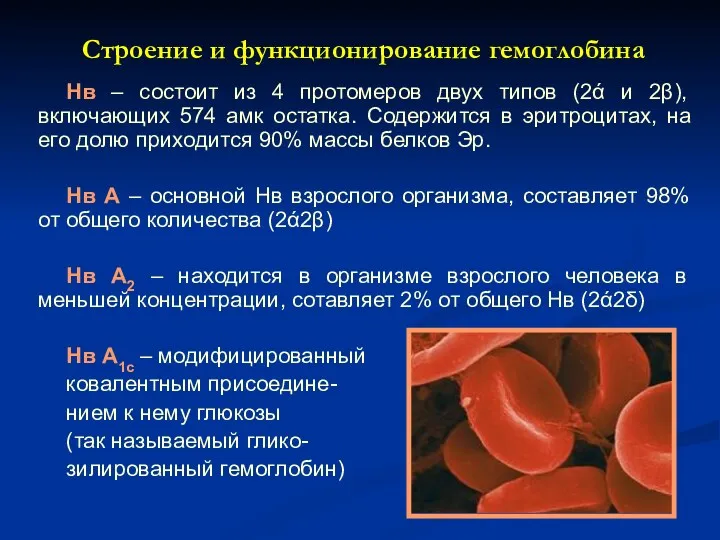
- 20. Строение и функционирование гемоглобина Нв – состоит из 4 протомеров двух типов (2ά и 2β), включающих
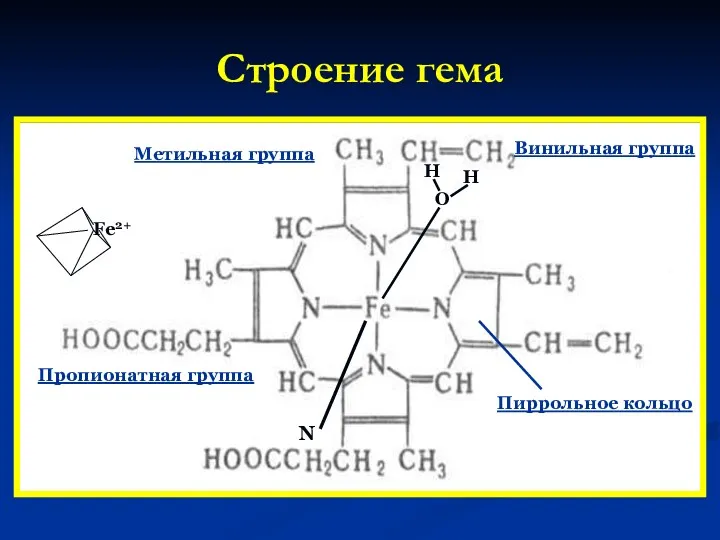
- 21. Строение гема Винильная группа Метильная группа Пропионатная группа Пиррольное кольцо Fe2+ О Н Н N
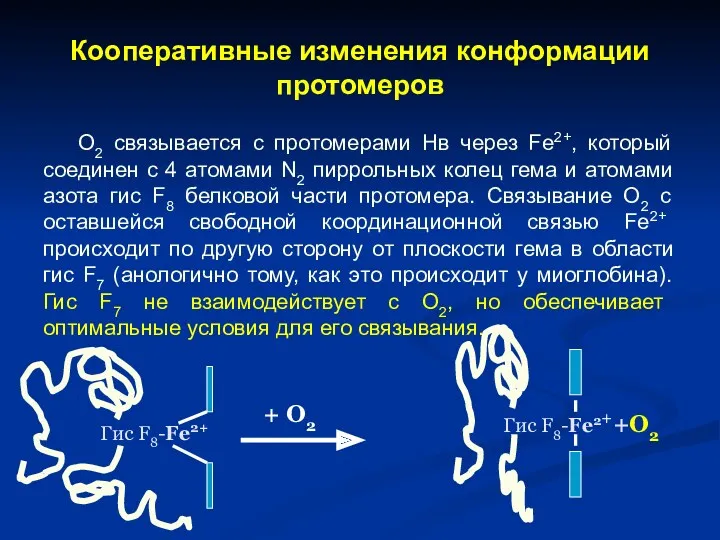
- 22. Кооперативные изменения конформации протомеров О2 связывается с протомерами Нв через Fe2+, который соединен с 4 атомами
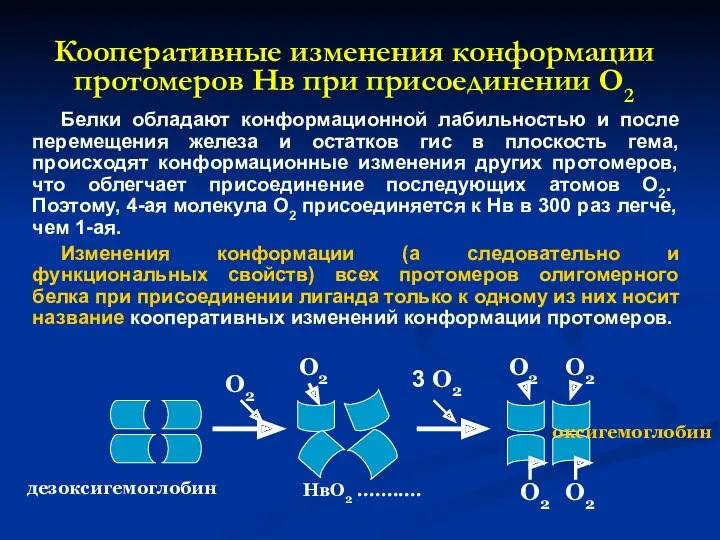
- 23. Кооперативные изменения конформации протомеров Нв при присоединении О2 Белки обладают конформационной лабильностью и после перемещения железа
- 24. Гем присоединяется к неполярным радикалам активного центра своими пиррольными циклами, а также к радикалу гистидина с
- 25. Эмбриональный и фетальный гемоглобин Эмбриональный гемоглобин синтезируется в эмбриональном желточном мешке через несколько недель после оплодотворения.
- 26. Формы гемоглобина Оксигемоглобин (НвО2) – полностью оксигенированный Нв; Дезоксигемоглобин (Нв) – незамещенная 6 координационная связь железа;
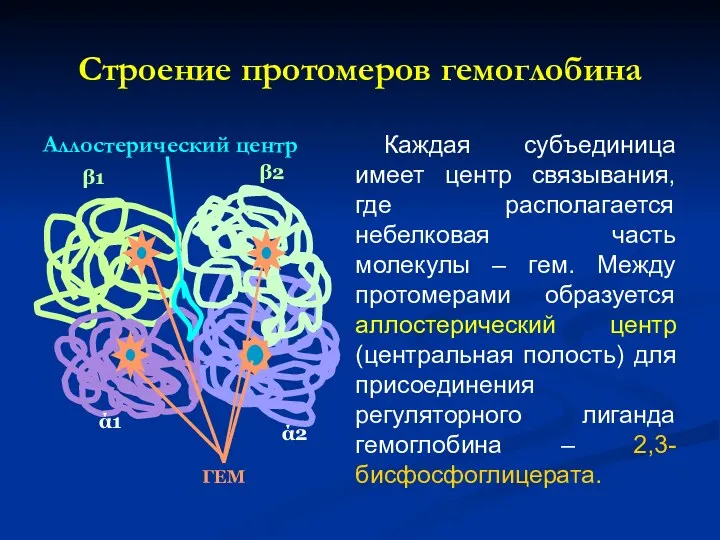
- 27. Строение протомеров гемоглобина Аллостерический центр Каждая субъединица имеет центр связывания, где располагается небелковая часть молекулы –
- 28. Таким образом: 1. в центре тетрамерной молекулы Нв находиться полость, которую образуют амк остатки всех 4
- 29. 2,3-Бисфосоглицерат (БФГ) – вещество, синтезируемое в Эр из промежуточного продукта окисления глюкозы – 1,3-бисфосфоглицерата. В нормальных
- 30. Изменение концентрации БФГ – как механизм адаптации организма к гипоксии. Концентрация БФГ в Эр людей, живущих
- 31. Аллостерическими регуляторами активности Нв, которые присоединяются к аллостерическим центрам (пространственно удаленным от активного центра), помимо 2,3-БФГ
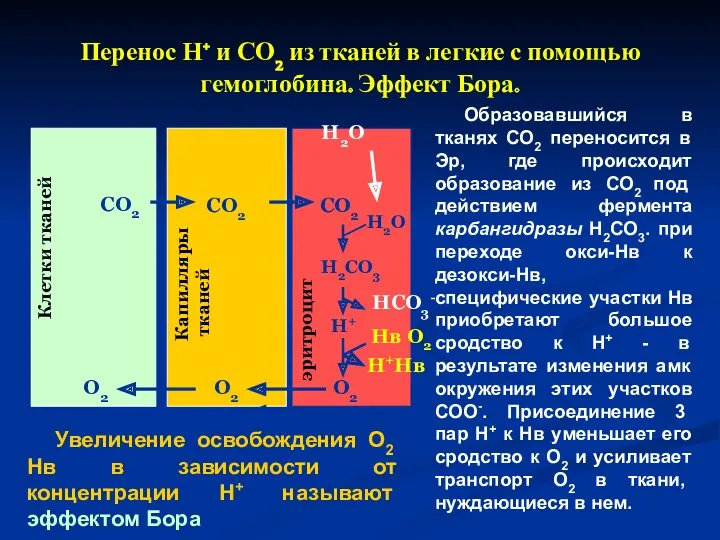
- 32. Перенос Н+ и СО2 из тканей в легкие с помощью гемоглобина. Эффект Бора. Увеличение освобождения О2
- 33. Оксигенирование дезоксигемоглобина в легких, образование и выделение СО2. Увеличение концентрации протонов в среде снижает сродство О2
- 34. Нуклеопротеины - широко распространённые в природе комплексы нуклеиновых кислот с белками. В зависимости от характера входящей
- 35. Гистоны - ядерные белки, упаковывающие хромосомную ДНК в компактную структуру. Все ДНК-связывающие белки эукариот подразделяются на
- 36. 1853 Коссель Альбрехт - немецкий биохимик (Kossel, Albrecht) (1853–1927), немецкий биохимик, удостоенный в 1910 Нобелевской премии
- 37. Анализ результатов двадцатилетних исследований, направленных на разработку методов построения моделей трехмерных биологических полипептидов и нуклеопротеидов, исходя
- 38. Нуклеопротеидный комплекс. Желтым показана р РНК, синим – белки. • Комплекс нуклеосомы с гистоном Н1 Устойчивость
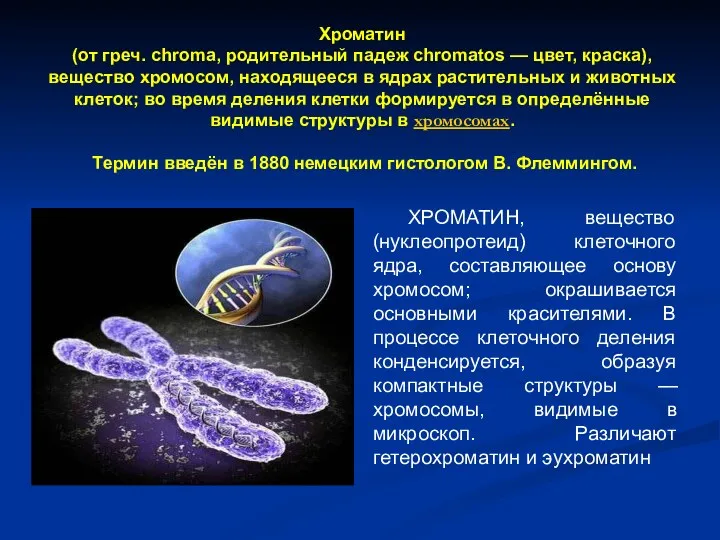
- 39. Хроматин (от греч. chroma, родительный падеж chromatos — цвет, краска), вещество хромосом, находящееся в ядрах растительных
- 40. Нуклеиновые кислоты Н.К. – высокомолекулярные линейные гетерополимеры с мМ от 250 до 1,2 • 105 кДа.
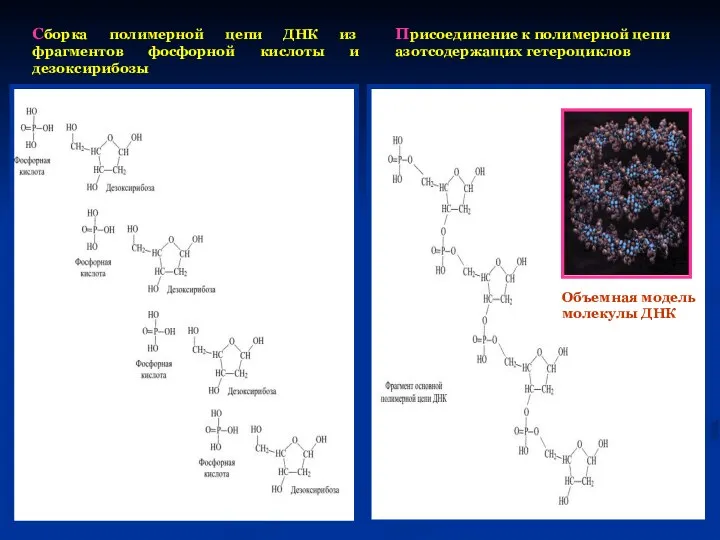
- 41. Сборка полимерной цепи ДНК из фрагментов фосфорной кислоты и дезоксирибозы Присоединение к полимерной цепи азотсодержащих гетероциклов
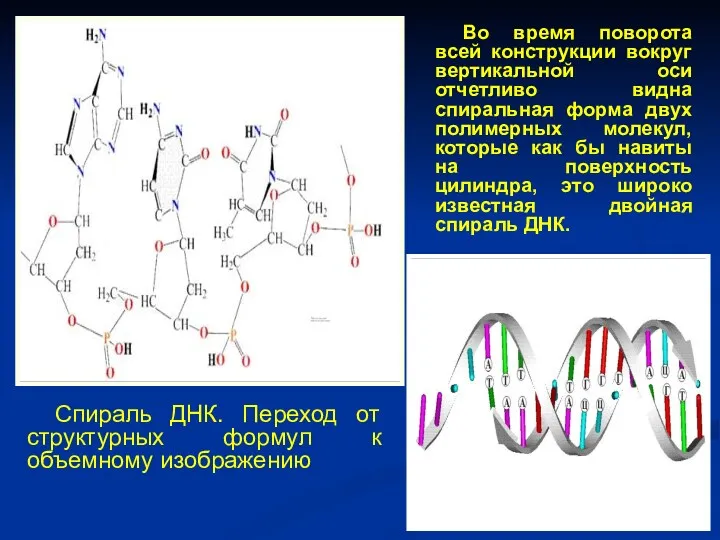
- 42. Спираль ДНК. Переход от структурных формул к объемному изображению Во время поворота всей конструкции вокруг вертикальной
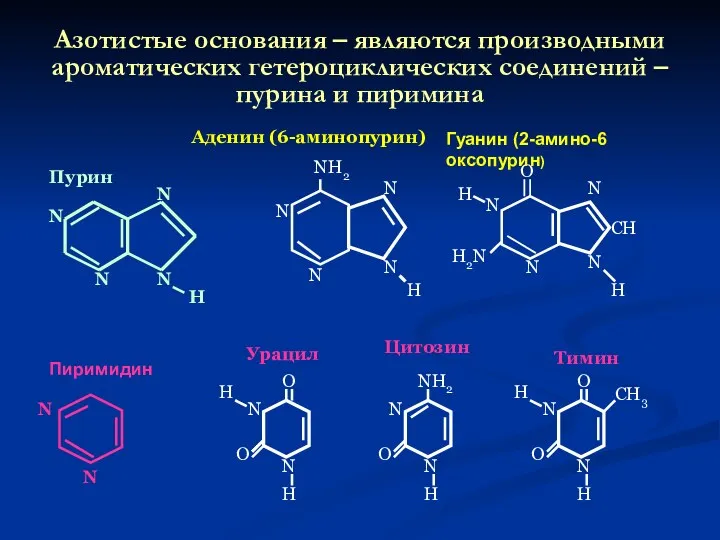
- 43. Азотистые основания – являются производными ароматических гетероциклических соединений – пурина и пиримина N N N N
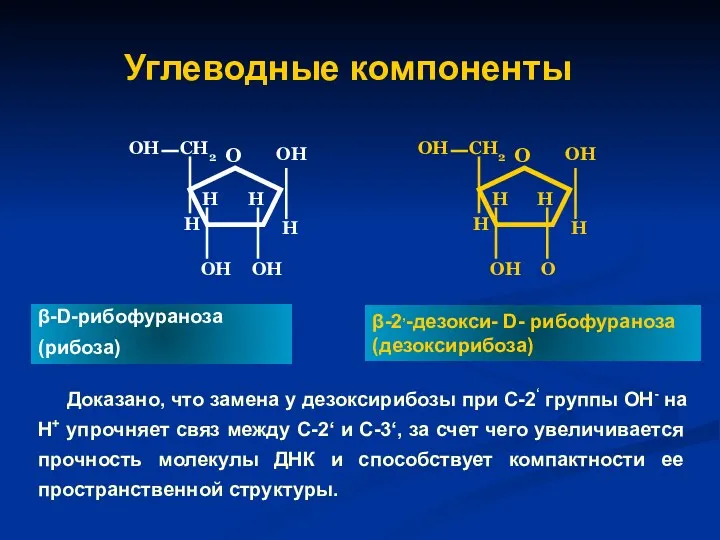
- 44. Углеводные компоненты Доказано, что замена у дезоксирибозы при С-2‘ группы ОН- на Н+ упрочняет связ между
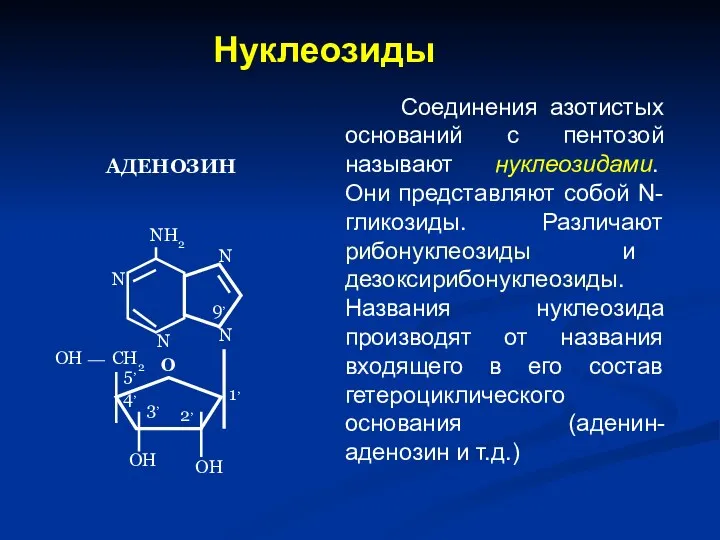
- 45. Нуклеозиды Соединения азотистых оснований с пентозой называют нуклеозидами. Они представляют собой N-гликозиды. Различают рибонуклеозиды и дезоксирибонуклеозиды.
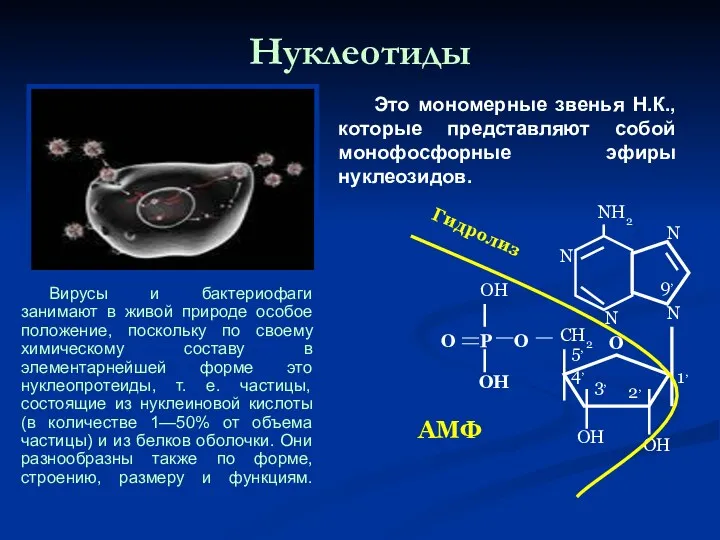
- 46. Нуклеотиды Вирусы и бактериофаги занимают в живой природе особое положение, поскольку по своему химическому составу в
- 47. Олиго- и полинуклеотиды Остатки фосфорной кислоты могут связываться за счет образования фосфоангидридной связи. Следовательно, два нуклеотида
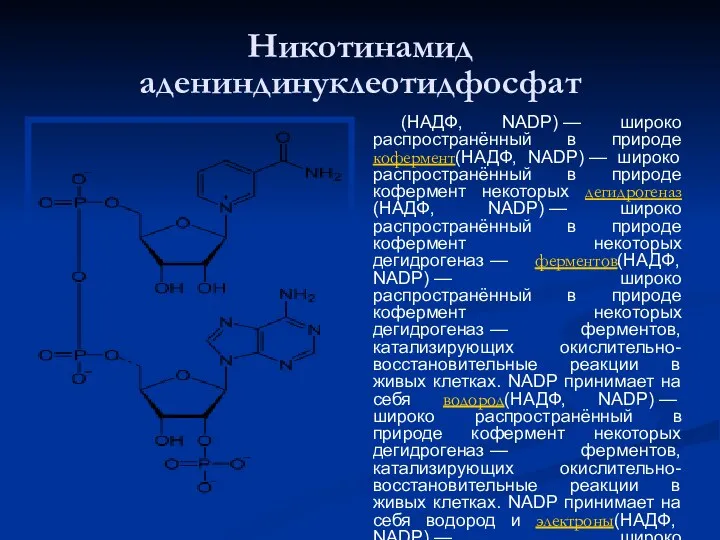
- 48. Никотинамид адениндинуклеотидфосфат (НАДФ, NADP) — широко распространённый в природе кофермент(НАДФ, NADP) — широко распространённый в природе
- 49. Основные мононуклеотиды Мононуклеотиды РНК: аденозин -3‘ и 5‘-фосфаты (адениловые кислоты), цитидин -3‘ и 5‘-фосфаты (цитидиловые кислоты),
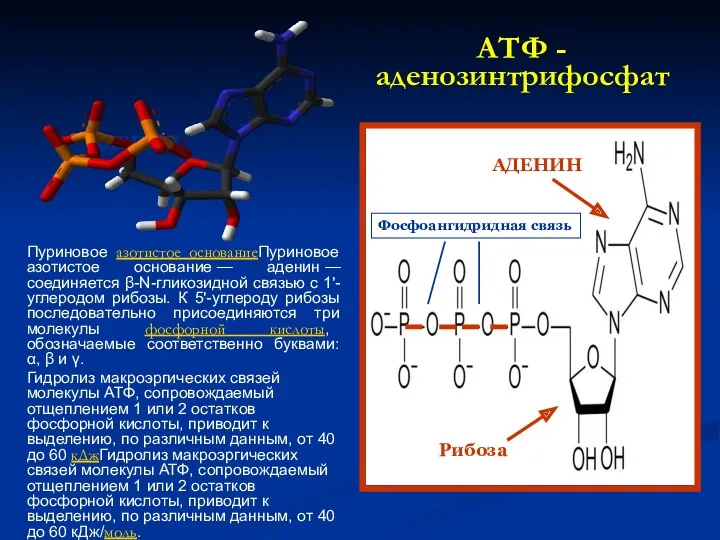
- 50. АТФ - аденозинтрифосфат Пуриновое азотистое основаниеПуриновое азотистое основание — аденин — соединяется β-N-гликозидной связью с 1'-углеродом
- 51. Строение АТФ Благодаря присутствию в молекуле АТФ атомов фосфора, связанных между собой ангидридными связями, эти молекулы
- 53. Скачать презентацию










![Зависимость между образованием комплекса [PL] и концентрацией белка при избытке](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/343853/slide-14.jpg)



















 Өсімдіктердің вегетативті көбею тәсілдерін зерттеу
Өсімдіктердің вегетативті көбею тәсілдерін зерттеу Молекулярні механізми впливу канцерогенів на організм людини
Молекулярні механізми впливу канцерогенів на організм людини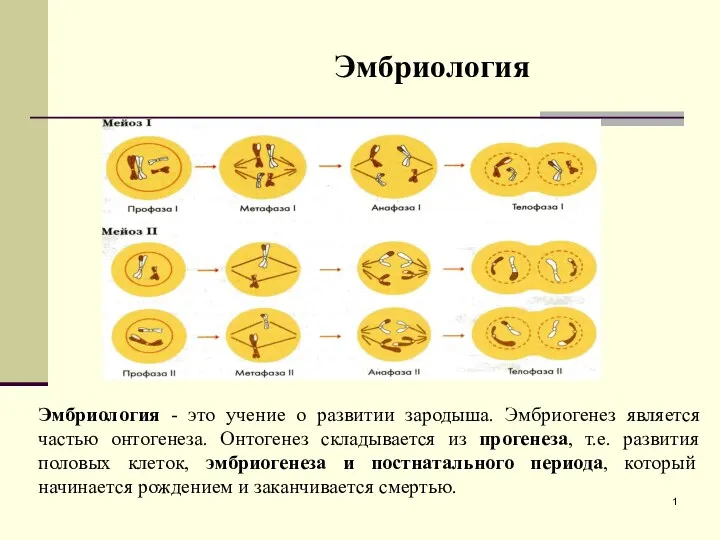 Учение о развитии зародыша - эмбриология
Учение о развитии зародыша - эмбриология Голосеменные растения
Голосеменные растения Презентации к урокам 9 - 11 класс
Презентации к урокам 9 - 11 класс Викторина по биологии Что? Где? Когда?
Викторина по биологии Что? Где? Когда? Немного о бобрах
Немного о бобрах Технологія виробництва м’яса бройлерів
Технологія виробництва м’яса бройлерів Генетика, как наука. Взаимосвязь процессов наследственности и изменчивости
Генетика, как наука. Взаимосвязь процессов наследственности и изменчивости Модификациялық өзгергіштік
Модификациялық өзгергіштік Сырдарияның гидробиологиялық режимі
Сырдарияның гидробиологиялық режимі Вегетативное размножение растений
Вегетативное размножение растений Домашние кошки
Домашние кошки Представители парнокопытных
Представители парнокопытных Формы естественного отбора
Формы естественного отбора Основные группы рыб, их роль в природе и практическое значение
Основные группы рыб, их роль в природе и практическое значение Отряд Чешуйчатые. Подотряд Ящерицы
Отряд Чешуйчатые. Подотряд Ящерицы Биометрические системы контроля доступа
Биометрические системы контроля доступа Всероссийская проверочная работа по биологии. 5 класс, 3 вариант
Всероссийская проверочная работа по биологии. 5 класс, 3 вариант Генно-инженерно-модифицированные организмы. Методы детекции и идентификации
Генно-инженерно-модифицированные организмы. Методы детекции и идентификации Здоровьесберегающий подход к выбору туалетного мыла
Здоровьесберегающий подход к выбору туалетного мыла Бактерии
Бактерии Наследственность и изменчивость как основа способности к развитию и эволюции
Наследственность и изменчивость как основа способности к развитию и эволюции 10 самых необычных растений мира
10 самых необычных растений мира Царство Вирусы
Царство Вирусы Фауна, животные (урок 14)
Фауна, животные (урок 14) Цианеи (сине-зелёные водоросли)
Цианеи (сине-зелёные водоросли) Основы гистологии. Ткани, виды тканей, соединительная ткань
Основы гистологии. Ткани, виды тканей, соединительная ткань