Содержание
- 2. Основные вопросы лекции: Макроэргтік қосылыстар.Тіндік тыныс алу боитотығу туралы түсінік Тотығып фосфорлану, Р/0 коэффициенті және АДФ/О.Тіндік
- 3. Специфические и общие пути катаболизма . Катаболитикалық процесстер екіге бөлінеді: - катаболизмнің өзіндік жолы, барлық класстарға
- 5. Пирожүзім қышқылының тотығып декарбоксильденуі Пирожүзім қышқылының тотығып декарбоксильденуі митохондрияның ішкі мембрананасында орналасқан мультиэнзимді пируват-дегидрогеназды комплекспен катализденеді.
- 6. катаболизмнің жалпы жолына кіреді: - Пирожүзім қышқылының тотығып декарбоксильденуі - Үш карбон қышқылы циклінде ацетил-КоА айналуы
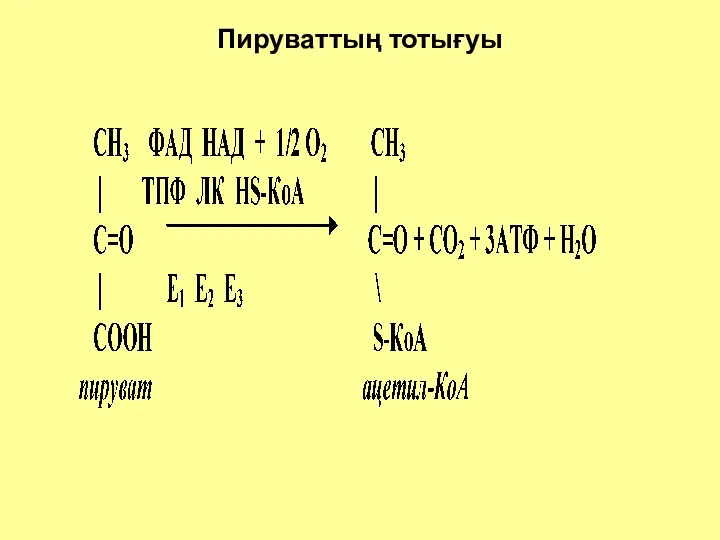
- 7. Пируваттың тотығуы
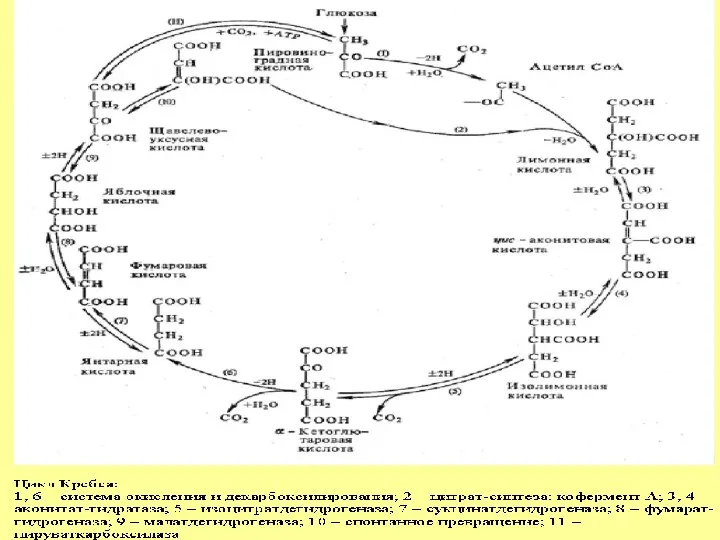
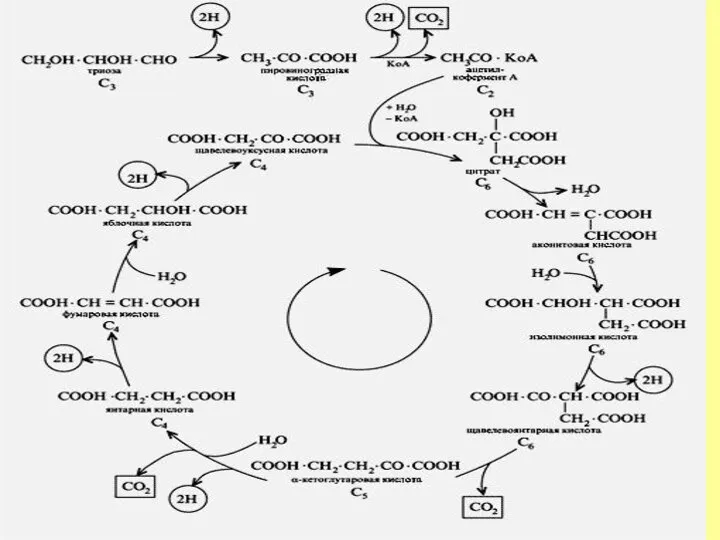
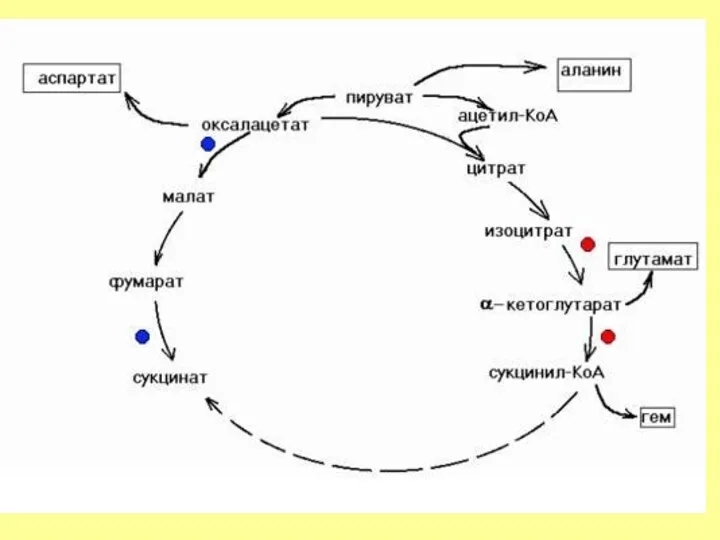
- 11. Үш карбон қышқылы циклі
- 12. Цикл трикарбоновых кислот
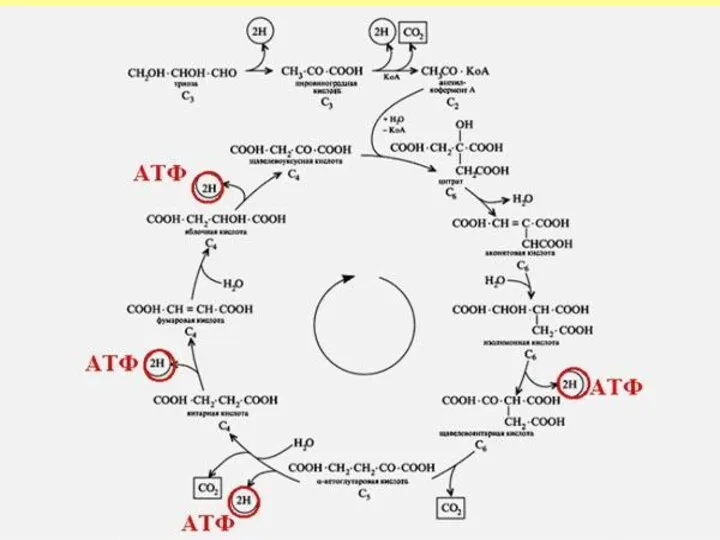
- 14. Энергия шығымы Дегидрогеназалармен төрт реакцияда субстрат дегидрирленуі жүреді изоцитратдегидрогеназа, кофермент НАД, альфа-кетоглутаратдегидрогеназалар, кофактор НАД сукцинатдегидрогеназа, кофермент
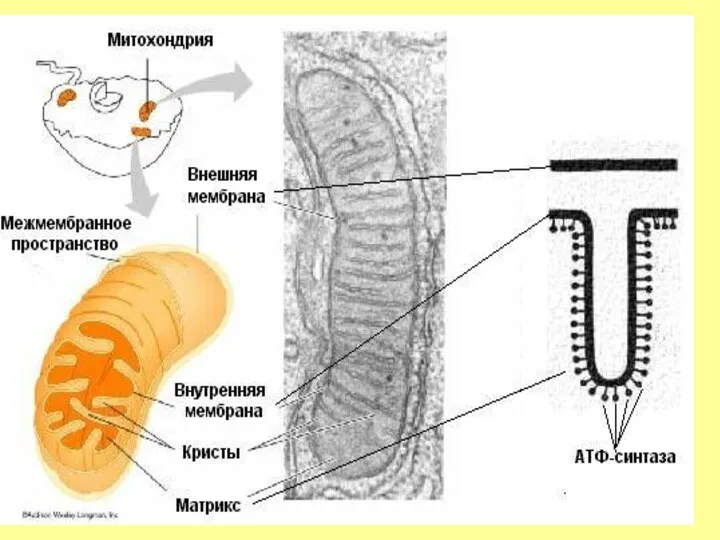
- 18. Челночные механизмы транспорта Своеобразным вариантом групповой транслокации является механизм переноса протонов (Н+) через митохондриальные мембраны. Мембраны
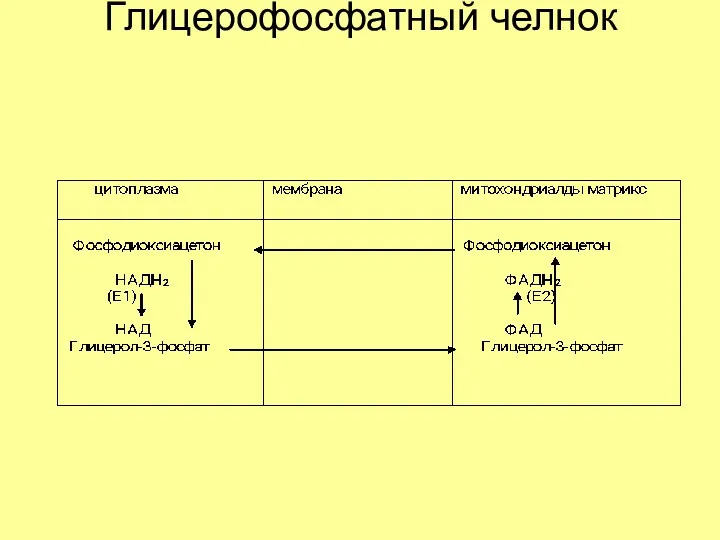
- 19. Глицерофосфатный челнок
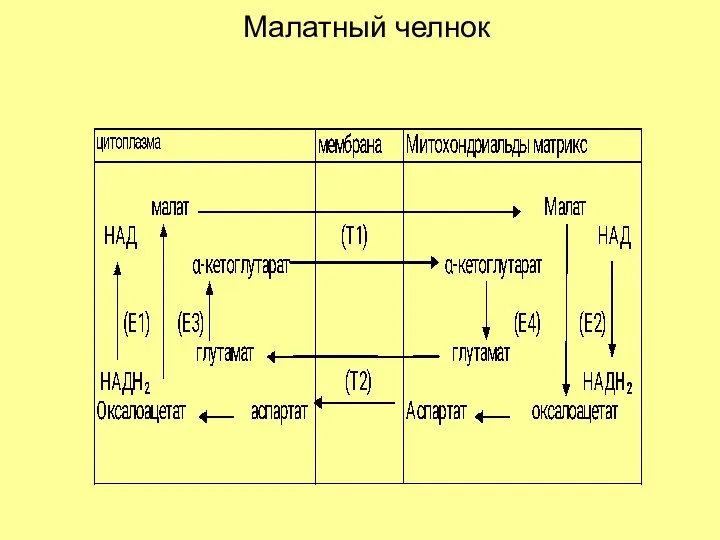
- 20. Малатный челнок
- 21. Основные типы окисления Реакции катаболизма органических соединений (субстратов), сопряженные с высвобождением свободной энергии в биосистемах, в
- 22. Маркоэрги К энергетическим субстратам для клеток животного организма относятся углеводы, липиды и аминокислоты. Удельная калорийность углеводов
- 23. Механизмы трансформация энергии в клетке Высвобождение свободной энергии при катаболизме углеводов, липидов и аминокислот может происходить
- 25. Механизм биологического окисления
- 26. Основной функцией этого процесса является обеспечение организма энергией в доступной для использования форме (прежде всего в
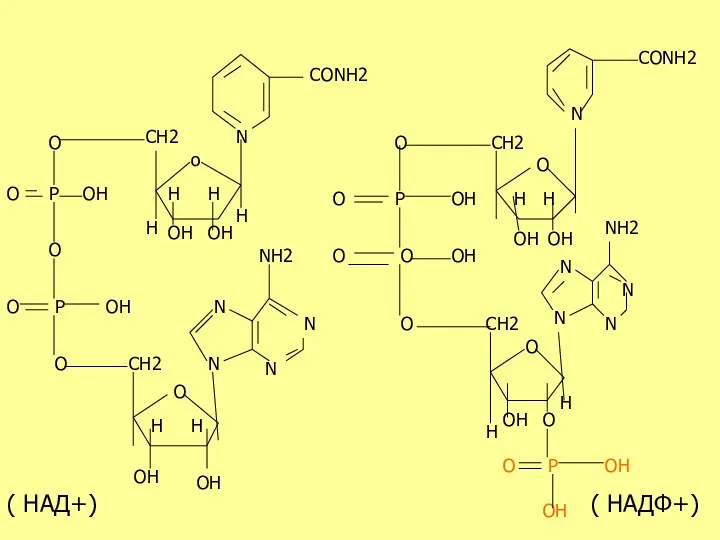
- 27. Анаэробные дегидрогеназы Эти ферменты катализируют реакции переноса атомов водорода (протоны и электроны) на любой акцептор кроме
- 28. N o H OH OH H CH2 O P OH O O P OH O O
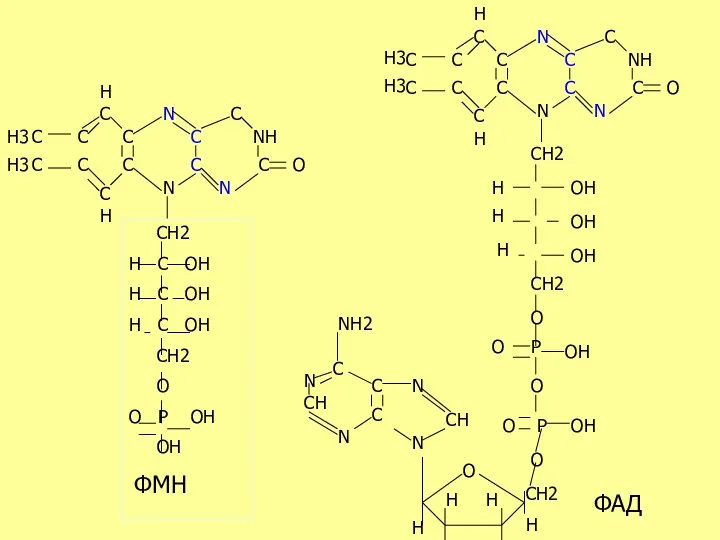
- 29. АЭРОБНЫЕ ДЕГИДРОГЕНАЗЫ Эти ферменты катализируют реакции переноса атомов водорода (протоны и электроны) на любой акцептор в
- 30. С С С С С С С С С С С С H H H3 H3
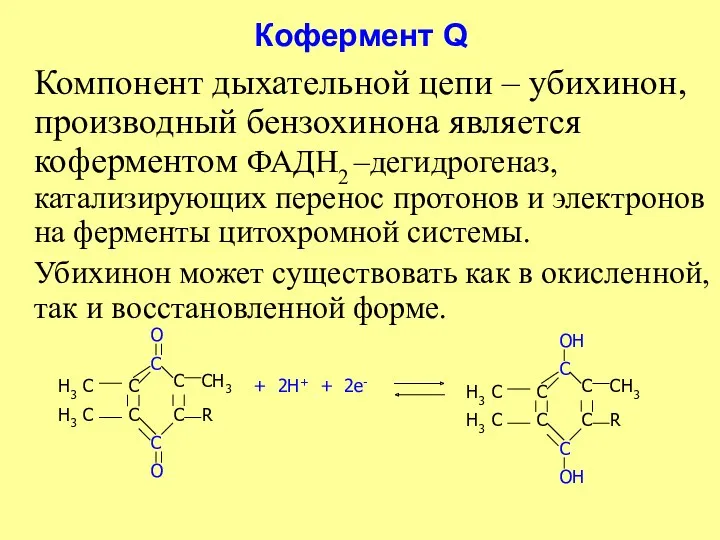
- 31. Кофермент Q Компонент дыхательной цепи – убихинон, производный бензохинона является коферментом ФАДН2 –дегидрогеназ, катализирующих перенос протонов
- 32. ЦИТОХРОМЫ Дальнейший перенос электронов от убихинона на кислород осуществляет система цитохромов: b, c1, c, a- a3.
- 33. Механизм действия цитохромов в окислительно-восстановительных реакциях Fe3+ + e- Fe2+ Fe2+ - e - Fe3+ Cu2+
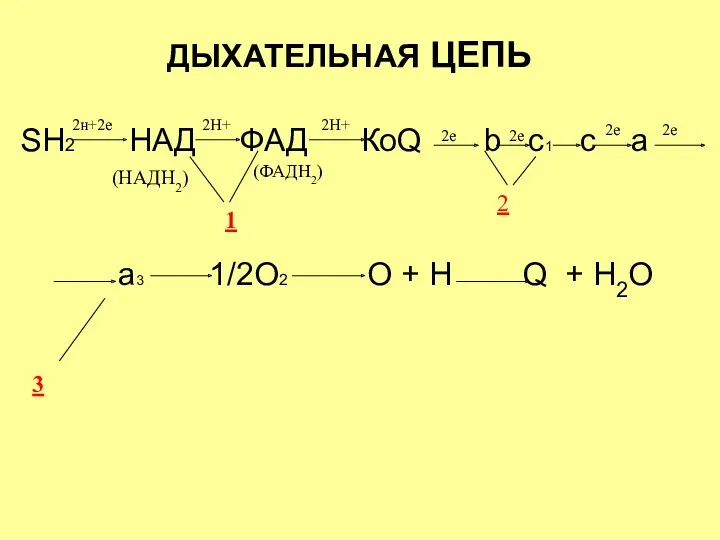
- 34. СТРУКТУРА ДЫХАТЕЛЬНОЙ ЦЕПИ Перенос электронов и протонов в митохондриальной дыхательной цепи происходит по градиенту их окислительно-восстановительного
- 35. ДЫХАТЕЛЬНАЯ ЦЕПЬ SH2 НАД ФАД КоQ b c1 c a a3 1/2O2 O + H Q
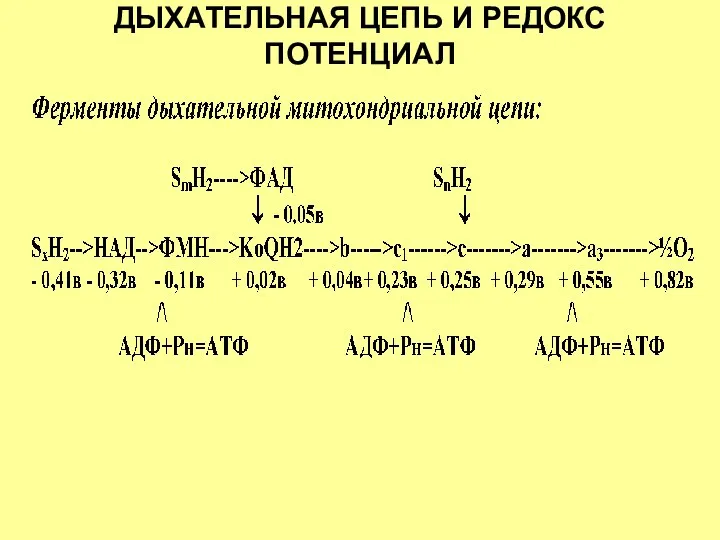
- 36. ДЫХАТЕЛЬНАЯ ЦЕПЬ И РЕДОКС ПОТЕНЦИАЛ
- 37. ПУНКТЫ ФОСФОРИЛИРОВАНИЯ Первый пункт фосфорилирования находится между ферментами НАД и ФАД, где разность их потенциала равна
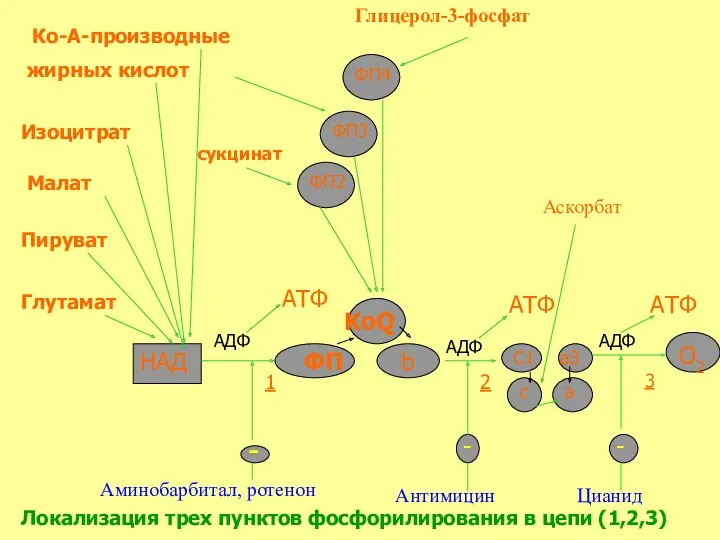
- 38. Ко-А-производные жирных кислот Изоцитрат Малат Пируват Глутамат НАД ФП b КоQ АТФ АДФ - Аминобарбитал, ротенон
- 39. Окислительное фосфорилирование При окислении одной молекулы субстрата на один атом поглощенного митохондриями кислорода может использоваться от
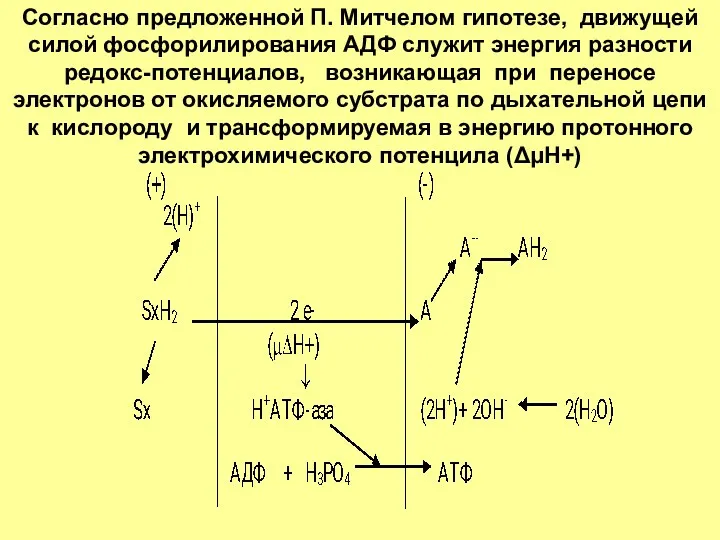
- 41. Согласно предложенной П. Митчелом гипотезе, движущей силой фосфорилирования АДФ служит энергия разности редокс-потенциалов, возникающая при переносе
- 43. Скачать презентацию

























 Биологическая эффективность гербицида Miuris 125 в борьбе с однодольными сорными растениями в посевах сой
Биологическая эффективность гербицида Miuris 125 в борьбе с однодольными сорными растениями в посевах сой Биологическая память. Лекция № 31
Биологическая память. Лекция № 31 Способы размножения животных. Оплодотворение
Способы размножения животных. Оплодотворение Аптека под ногами
Аптека под ногами Высшая нервная деятельность. Лекция № 28
Высшая нервная деятельность. Лекция № 28 Травы и цветы полей и лугов
Травы и цветы полей и лугов Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10)
Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10) Мейоз. Деление мейоза
Мейоз. Деление мейоза Как размножаются живые организмы
Как размножаются живые организмы Неклеточные формы жизни. Вирусы и бактериофаги.
Неклеточные формы жизни. Вирусы и бактериофаги. Методы биологии
Методы биологии Бактерии
Бактерии Постэмбриональный период развития человека
Постэмбриональный период развития человека Кровь, кроветворение
Кровь, кроветворение Хим.состав клетки
Хим.состав клетки Пищевые цепи. Взаимосвязи организмов в природных сообществах
Пищевые цепи. Взаимосвязи организмов в природных сообществах Ферменты. АЛТ и АСТ
Ферменты. АЛТ и АСТ витамины
витамины Способность к размножению у животных
Способность к размножению у животных Дополнительный_материал_11.40_05.02.2024_eb5cb3bf (1)
Дополнительный_материал_11.40_05.02.2024_eb5cb3bf (1) Органеллы эукариотической клетки
Органеллы эукариотической клетки Экология и фитодизайн школьного кабинета биологии
Экология и фитодизайн школьного кабинета биологии Барханная кошка
Барханная кошка Клас ссавці
Клас ссавці Строение пластид. Фотосинтез
Строение пластид. Фотосинтез Адромискус. Семейство – толстянковые
Адромискус. Семейство – толстянковые Мутация. Геномдық мутация. Хромосомалық мутация. Гендік мутация. Мутацияның типтері
Мутация. Геномдық мутация. Хромосомалық мутация. Гендік мутация. Мутацияның типтері Что же такое трава?
Что же такое трава?