Слайд 2

Кислотно–щелочное равновесие – сложная система регуляции концентраций водородных ионов (Н+)
Кислота –
это вещество, которое при растворении выделяет Н+
Основание – это вещество, которое при растворении связывает Н+
Буфер – это вещество, которое либо связывает, либо выделяет Н+ в зависимости от концентрации Н+ во внутренней среде
Слайд 3
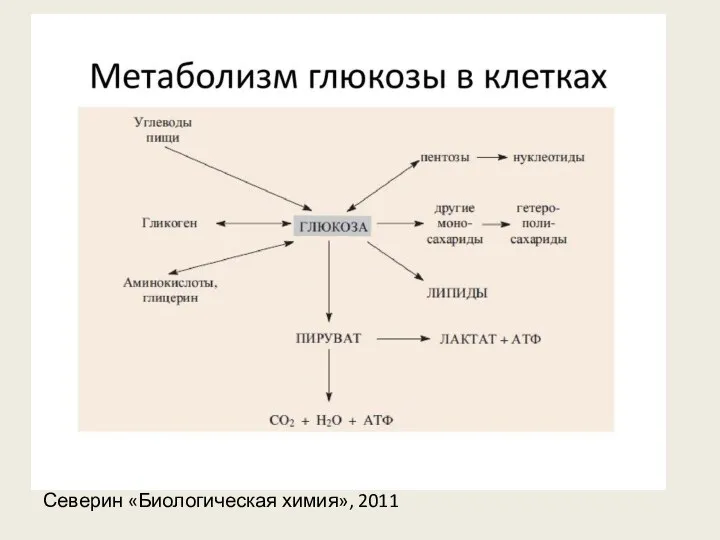
Северин «Биологическая химия», 2011
Слайд 4

Основные показатели КЩС
pH крови – отрицательный десятичный логарифм концентрации H+
pH =
- log H+
Норма pH 7,35 – 7, 45
Iain A M Hennessey, Alan G Japp «Arterial Blood Gases Made Easy»
Слайд 5

Поддержание pH
Внутриклеточные буферные системы (белковая, фосфатная)
Внеклеточные буферные системы (белки плазмы, гемоглобин,
угольная кислота/бикарбонат)
Экскреторная функция почек и легких
Слайд 6

Основные показатели КЩС
Парциальное давление СO2 в арт. крови (раСО2)
32-48 мм рт
ст
Парциальное давление кислорода в арт. крови (раО2)
83-108 мм рт ст
Стандартный бикарбонат плазмы крови (standard bicarbonate, SB)
24,0 ± 2,0 ммоль/л
Буферные основания крови (buffer base, ВВ)
48,0 ± 2,0 ммоль/л
Избыток (или дефицит) оснований (base excess, ВЕ)
± 2,3 ммоль/л
Анионный промежуток = (Na++ K+) – (CL-+HCO3-)
10-18 ммоль/л
Слайд 7
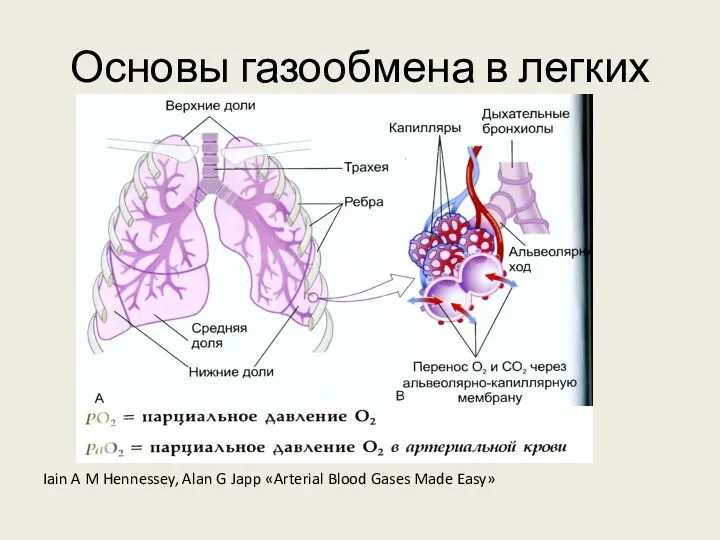
Основы газообмена в легких
Iain A M Hennessey, Alan G Japp
«Arterial Blood Gases Made Easy»
Слайд 8
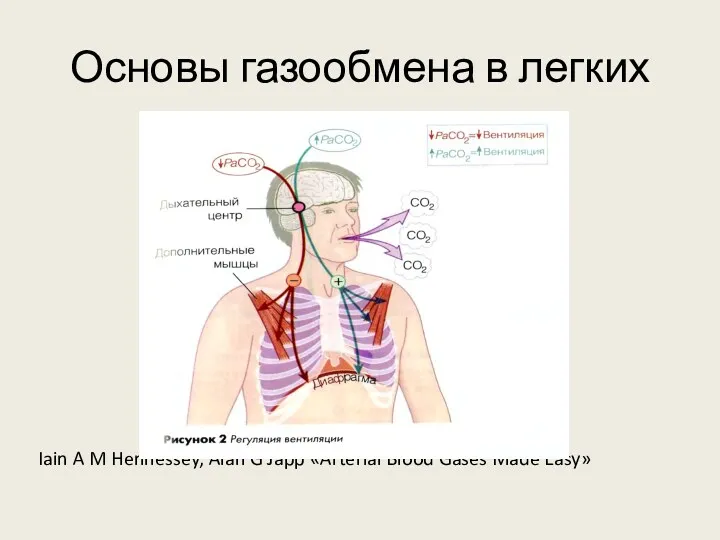
Основы газообмена в легких
Iain A M Hennessey, Alan G Japp
«Arterial Blood Gases Made Easy»
Слайд 9

Основы газообмена в легких
Iain A M Hennessey, Alan G Japp
«Arterial Blood Gases Made Easy»
Слайд 10

Основы газообмена в легких
paO2 не отражает содержания О2 в крови.
Эта величина дет представление только о свободных, несвязанных молекулах О2.
Почти все молекулы О2 связаны с Hb.
Слайд 11

Основы газообмена в легких
Содержание O2 определяется двумя параметрами:
Концентрация Hb: определяет
способность крови к переносу О2
Сатурация Hb кислородом: процент доступных мест связывания на Hb, которые несут молекулы O2
Слайд 12
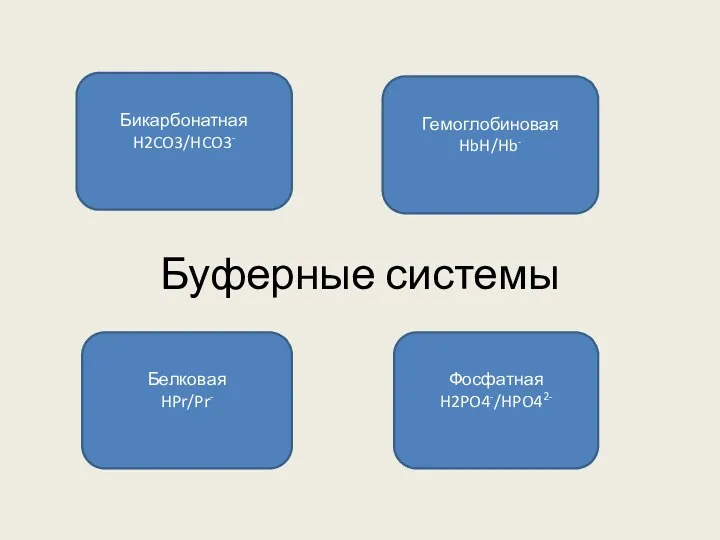
Буферные системы
Бикарбонатная
H2CO3/HCO3-
Гемоглобиновая
HbH/Hb-
Белковая
HPr/Pr-
Фосфатная
H2PO4-/HPO42-
Слайд 13

Бикарбонатная буферная система
Кровь
(карбоангидраза)
СО2 + H2O ↔ H2CO3 ↔ H+
+ HCO3 -
дыхательный механизм почечный мех-м
Уникальность этой системы состоит в том, что концентрация ее компонентов - угольной кислоты/бикарбоната – могут изменяться независимо друг от друга посредством почечного и легочного механизмов компенсации.
рН зависит не от абсолютных количеств СО2 и HCO3- , а от отношения СО2 к HCO3-
Слайд 14

Патофизиология, Новицкий,т.1
Слайд 15

3 пути экскреции ионов H+ почками
Основной путь – регулирование количества бикарбоната,
реабсорбируемого в проксимальных трубочках
Реакция HPO42-+ H+ → H2PO4-
Связывание ионов аммиака с ионами H+
Слайд 16
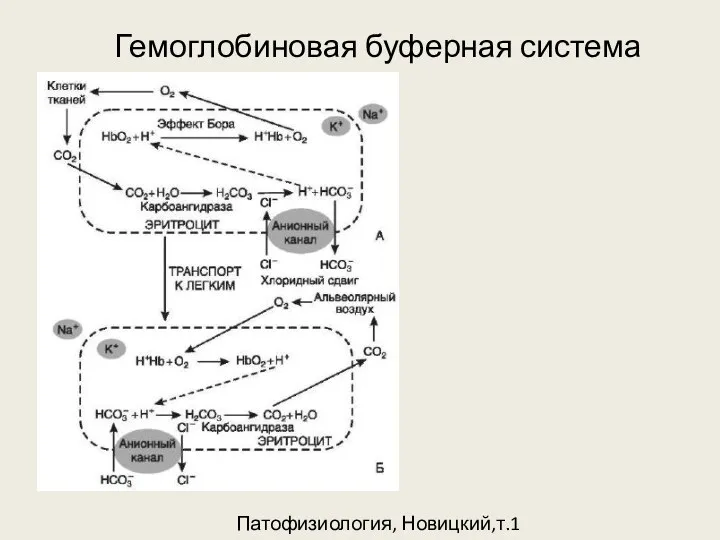
Гемоглобиновая буферная система
Патофизиология, Новицкий,т.1
Слайд 17
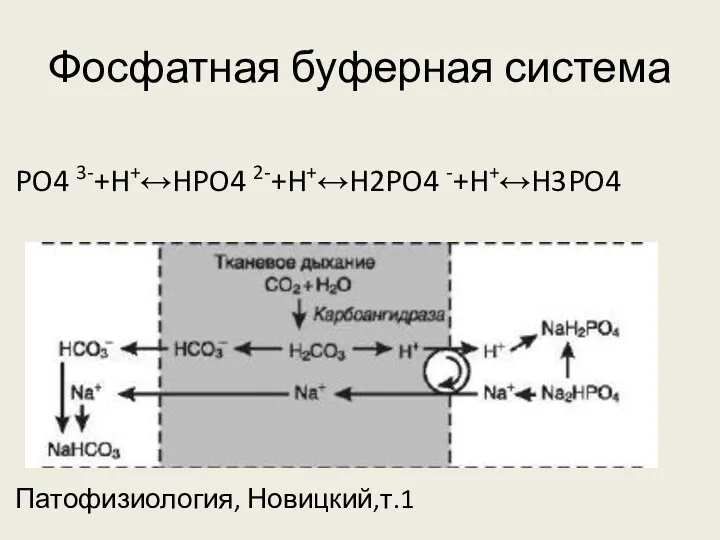
Фосфатная буферная система
PO4 3-+H+↔HPO4 2-+H+↔H2PO4 -+H+↔H3PO4
Патофизиология, Новицкий,т.1
Слайд 18
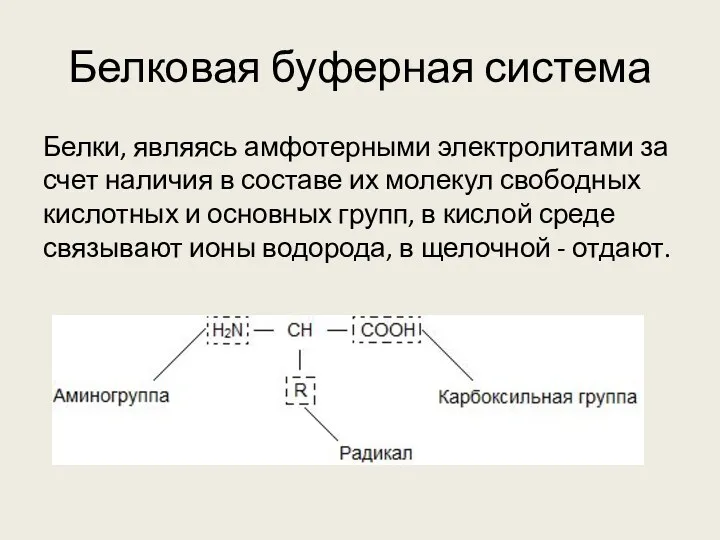
Белковая буферная система
Белки, являясь амфотерными электролитами за счет наличия в составе
их молекул свободных кислотных и основных групп, в кислой среде связывают ионы водорода, в щелочной - отдают.

















 Биологическая эффективность гербицида Miuris 125 в борьбе с однодольными сорными растениями в посевах сой
Биологическая эффективность гербицида Miuris 125 в борьбе с однодольными сорными растениями в посевах сой Биологическая память. Лекция № 31
Биологическая память. Лекция № 31 Способы размножения животных. Оплодотворение
Способы размножения животных. Оплодотворение Аптека под ногами
Аптека под ногами Высшая нервная деятельность. Лекция № 28
Высшая нервная деятельность. Лекция № 28 Травы и цветы полей и лугов
Травы и цветы полей и лугов Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10)
Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10) Мейоз. Деление мейоза
Мейоз. Деление мейоза Как размножаются живые организмы
Как размножаются живые организмы Неклеточные формы жизни. Вирусы и бактериофаги.
Неклеточные формы жизни. Вирусы и бактериофаги. Методы биологии
Методы биологии Бактерии
Бактерии Постэмбриональный период развития человека
Постэмбриональный период развития человека Кровь, кроветворение
Кровь, кроветворение Хим.состав клетки
Хим.состав клетки Пищевые цепи. Взаимосвязи организмов в природных сообществах
Пищевые цепи. Взаимосвязи организмов в природных сообществах Ферменты. АЛТ и АСТ
Ферменты. АЛТ и АСТ витамины
витамины Способность к размножению у животных
Способность к размножению у животных Дополнительный_материал_11.40_05.02.2024_eb5cb3bf (1)
Дополнительный_материал_11.40_05.02.2024_eb5cb3bf (1) Органеллы эукариотической клетки
Органеллы эукариотической клетки Экология и фитодизайн школьного кабинета биологии
Экология и фитодизайн школьного кабинета биологии Барханная кошка
Барханная кошка Клас ссавці
Клас ссавці Строение пластид. Фотосинтез
Строение пластид. Фотосинтез Адромискус. Семейство – толстянковые
Адромискус. Семейство – толстянковые Мутация. Геномдық мутация. Хромосомалық мутация. Гендік мутация. Мутацияның типтері
Мутация. Геномдық мутация. Хромосомалық мутация. Гендік мутация. Мутацияның типтері Что же такое трава?
Что же такое трава?