Содержание
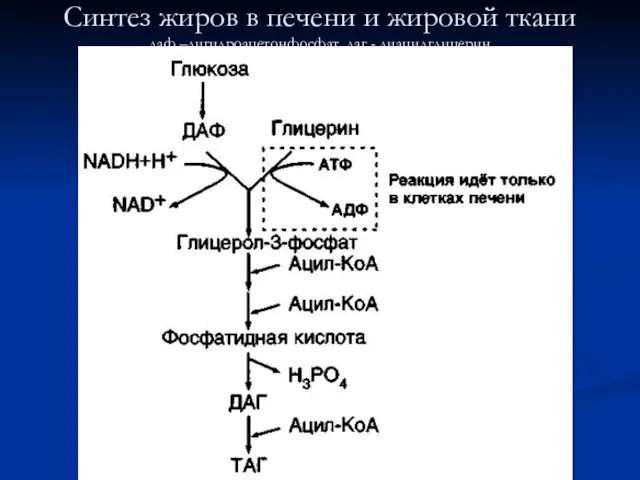
- 2. Синтез жиров в печени и жировой ткани даф –дигидроацетонфосфат, даг - диацилглицерин
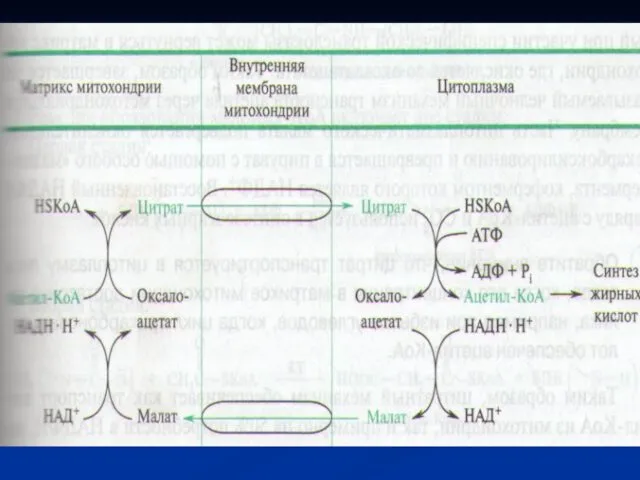
- 3. Биосинтез жирных кислот Источником углерода для синтеза жирных кислот служит ацетил-КоА, образующийся при распаде глюкозы в
- 5. Синтез жирных кислот Синтез жирных кислот имеет ряд особенностей: в отличие от окисления синтез локализован в
- 6. Из ацетил-КоА образуется малонил-КоА:
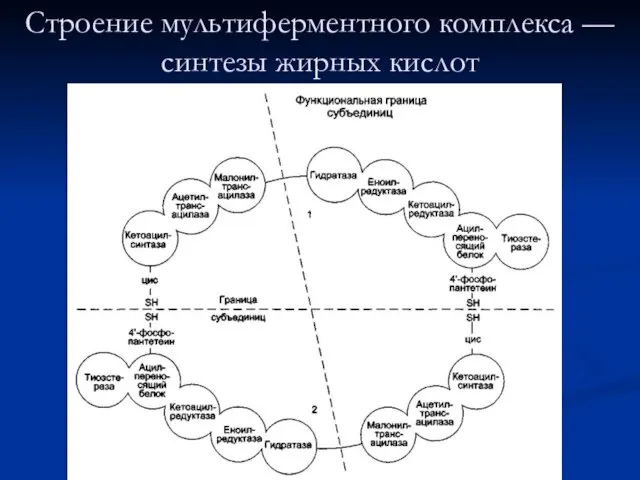
- 7. Строение мультиферментного комплекса — синтезы жирных кислот
- 8. Синтез пальмитиновой кислоты Синтаза жирных кислот: в первом протомере SH-группа принадлежит цистеину, во втором — фосфопантетеину.
- 9. Общая схема реакций синтеза пальмитиновой кислоты
- 10. Образование двойных связей в радикалах жирных кислот Включение двойных связей в радикалы жирных кислот называется десатурацией.
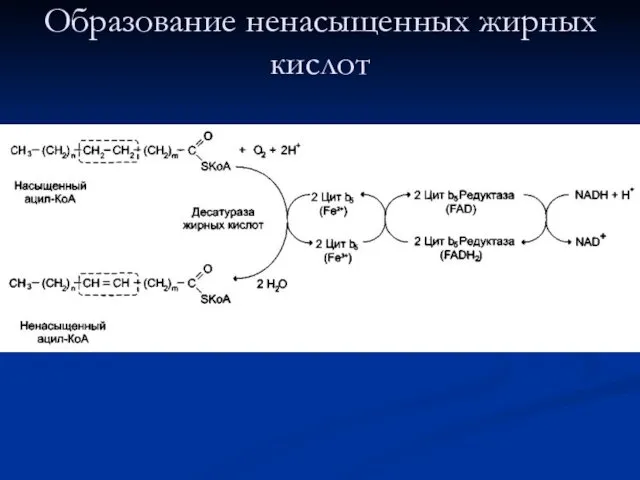
- 11. Образование двойных связей Для образования двойной связи в радикале жирной кислоты требуется молекулярный кислород, NADH, цитохром
- 12. Образование ненасыщенных жирных кислот
- 13. Регуляция липидного обмена 1. Внешние факторы (тип питания): избыток углеводов в рационе усиливает процессы синтеза жиров
- 14. 2. Внутренние факторы: гормоны, усиливающие процессы липогенеза: - инсулин; гормоны, усиливающие процессы липолиза (распада липидов): -
- 15. Патология липидного обмена 1. Ожирение Причины: гипофункция щитовидной железы (по тироксину); недостаток липотропного гормона гипофиза.
- 16. 2. Нарушения переваривания и усвоения липидов: заболевания поджелудочной железы (недостаточная секреция и активность панкреатической липазы); нарушение
- 17. 3. Кетозы – характеризуются кетонемией и кетонурией. Причины: недостаток инсулина; В3-авитаминоз (недостаток НS-КоА); недостаток ЩУК –
- 18. 4. Атеросклероз: увеличение в крови свободных жирных кислот; увеличение в крови ЛПОНП и ЛПНП.
- 19. Обмен белков
- 20. Белки Белки – биологические полимерные молекулы, мономерами которых являются аминокислоты, соединенные пептидными связями. Индивидуальность белковых молекул
- 21. Функции белков. Каталитическая – ферменты Пластическая – структурные белки Регуляторная – гормоны, ферменты Сократительная – белки
- 22. Содержание белков в тканях, % Животные Организм – 18-21 Мышцы – 19-23 Печень – 18-19 Почки
- 23. Простые белки а) альбумины б) глобулины в) гистоны г) протамины д) глютелины е) проламины ж) склеропротеины
- 24. Сложные белки а) нуклеопротеины б) хромопротеины в) фосфоропротеины г) гликопротеины д) липопротеины е) металлопротеины
- 25. Аминокислоты Заменимые Глицин Аланин Серин Цистеин Аспарагиновая кислота Глютаминовая кислота Тирозин Пролин Аспарагин Глютамин Незаменимые Треонин
- 26. Классификация белков по их полноценности Полноценные белки содержат все незаменимые аминокислоты. К ним относят белки животного
- 27. АЗОТИСТЫЙ БАЛАНС Азотистый баланс — разница между количеством азота, усвоенного организмом, и количеством азота, выделенного в
- 28. Виды азотистого баланса Положительный: количество усвоенного азота больше, чем количество выделенного азота, т.е. процессы анаболизма преобладают
- 29. Отрицательный азотистый баланс: количество выделенного азота больше, чем количество усвоенного азота, т.е. процессы катаболизма в организме
- 30. Азотистое равновесие (нулевой баланс): количество усвоенного и выделенного азота равно. Это наблюдается у здоровых непродуктивных, закончивших
- 31. Белковая недостаточность Известно, что даже длительное исключение из рациона человека жиров или углеводов не вызывает тяжёлых
- 32. Белковый минимум Это наименьшее количество белка в рационе, которое обеспечивает восполнение всех его потребностей, т.е. при
- 33. Нормы протеина в рационе Они расчитываются с учетом вида животного, возраста, направления продуктивности и других факторов
- 34. В организме человека в сутки распадается на аминокислоты около 400 г белков, примерно такое же количество
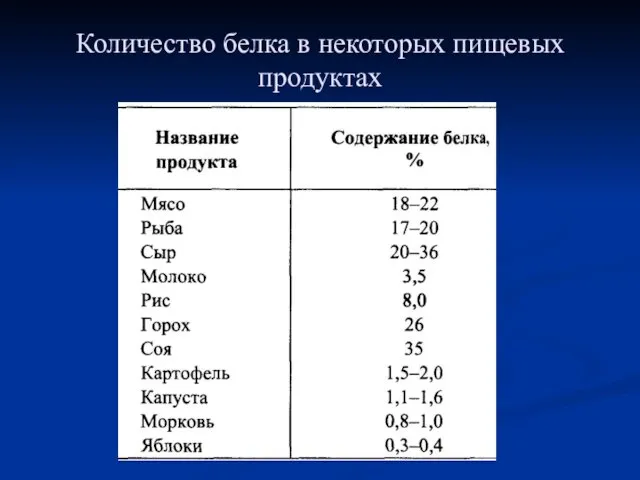
- 35. Количество белка в некоторых пищевых продуктах
- 36. Переваривание белков Основной смысл переваривания белков состоит в их гидролизе до свободных аминокислот, в ходе которого
- 37. Переваривание белков осуществляется комплексом пищеварительных ферментов, которые называются протеолитическими или протеазами. Протеазы относят к классу Гидролазы,
- 38. Переваривание белков в желудке Желудочный сок — продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка
- 39. Под действием НС1 происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей
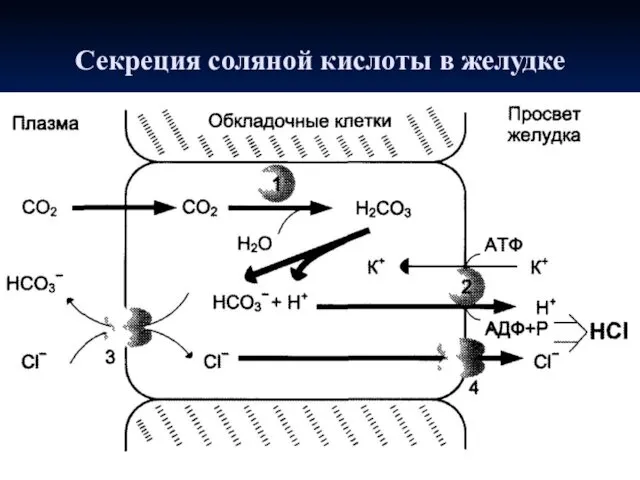
- 40. Секреция соляной кислоты в желудке
- 41. Механизм активации пепсина Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена
- 42. Особенности переваривания белков в желудке у молодых животных В молочный период вскармливания животных в сычуге (желудке)
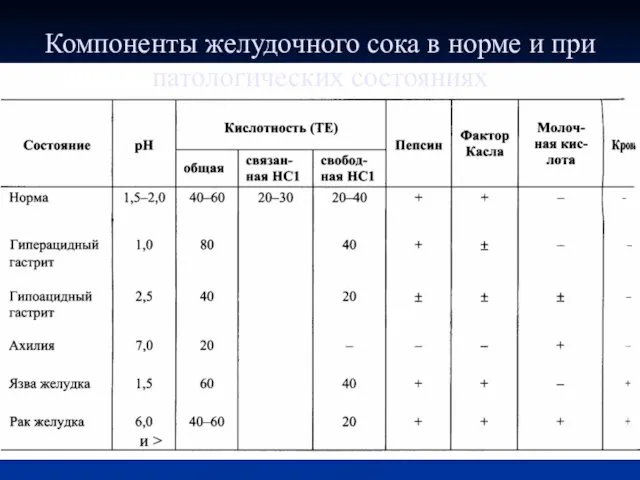
- 43. Компоненты желудочного сока в норме и при патологических состояниях
- 44. Механизм действия пепсина Белки рациона + НОН → высокомолекулярные полипептиды Пепсин гидролизует внутренние пептидные связи, в
- 45. Активация панкреатических ферментов В поджелудочной железе синтезируются проферменты ряда протеаз: трипсиноген, химотрипсиноген, проэластаза, прокарбоксипептидазы А и
- 46. - Активация трипсиногена происходит под действием фермента эпителия кишечника энтеропептидазы (энтерокиназы): Энтеропептидаза Трипсиноген + НОН →
- 47. - Образовавшийся трипсин активирует химотрипсиноген: трипсин Химотрипсиноген + НОН → Химотрипсин (неактивная форма) (активная форма) -
- 48. Активация химотрипсиногена
- 49. Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного протеолиза.
- 50. Карбоксипептидазы А и В — цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно
- 51. Аминопептидазы последовательно отщепляют N-концевые аминокислоты пептидной цепи. Наиболее известна лейцинаминопептидаза — Zn2+ - или Мn2+ -
- 52. Механизм действия экзопептидаз
- 53. Защита клеток от действия протеаз Клетки поджелудочной железы защищены от действия пищеварительных ферментов тем, что: эти
- 54. Защита от действия протеаз В полости желудка и кишечника протеазы не контактируют с белками клеток, поскольку
- 55. Механизм всасывания аминокислот в кишечнике
- 56. В настоящёе время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для
- 57. Гниение белков в толстом отделе кишечника БЕЛКИ АМИНОКИСЛОТЫ гнилостные бактерии ЯДОВИТЫЕ ВЕЩЕСТВА аммиак, сероводород, путресцин, кадаверин,
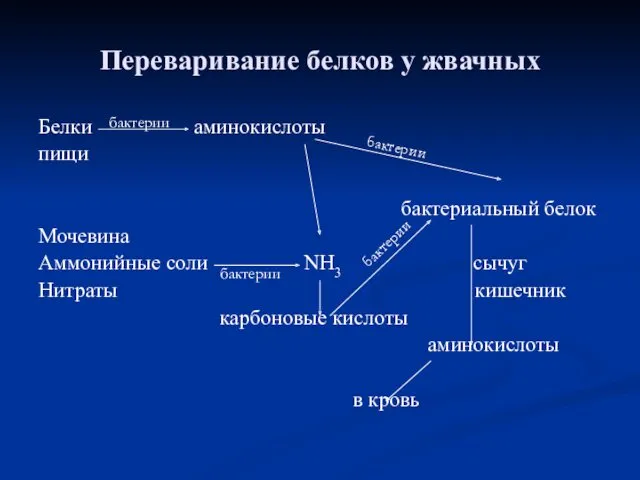
- 58. Переваривание белков у жвачных Белки аминокислоты пищи бактериальный белок Мочевина Аммонийные соли NH3 сычуг Нитраты кишечник
- 59. Фонд свободных аминокислот организма составляет примерно 35 г. Содержание свободных аминокислот в крови в среднем равно
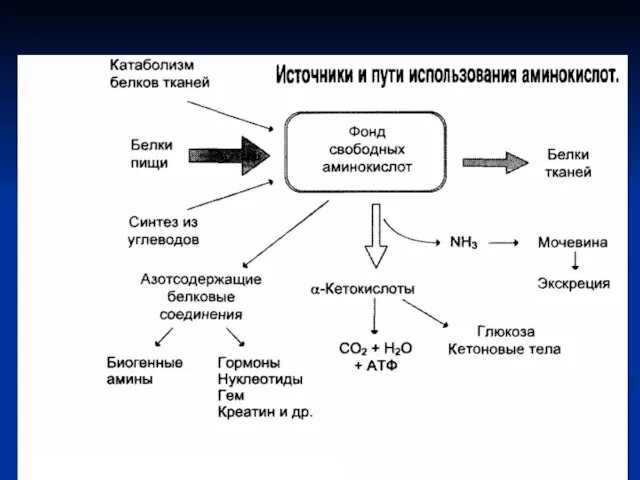
- 60. Источники аминокислот 1. Белки корма (экзогенные аминокислоты). 2. Белки тканей при распаде в процессе их обновления
- 61. Пути использования аминокислот в организме Биосинтез белков, специфичных для данного организма. Синтез биологически активных веществ (ферментов,
- 63. КАТАБОЛИЗМ АМИНОКИСЛОТ Аминокислоты, образующиеся при переваривании белков и поступающие в клетки тканей, подвергаются катаболизму и анаболизму,
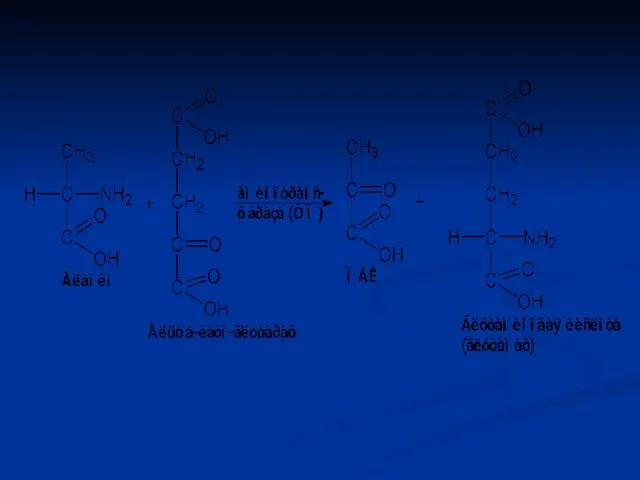
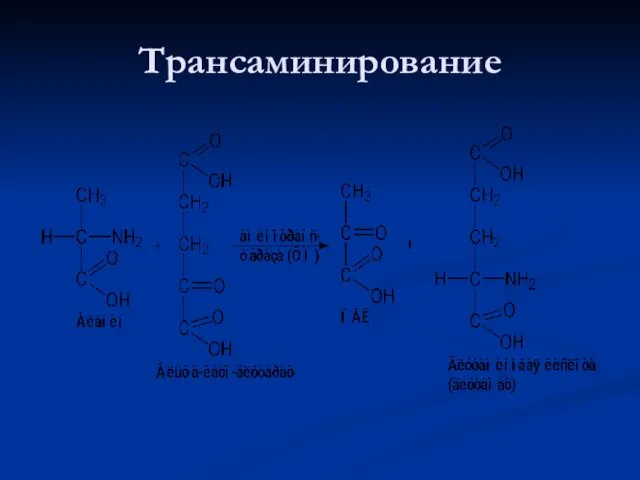
- 64. Трансаминирование Трансаминирование — реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая кетокислота
- 65. Реакция трансаминирования
- 66. Аминотрансферазы Аминотрансферазы обнаружены как в цитоплазме, так и в митохондриях клеток эукариот. Причём митохондриальные и цитоплазматические
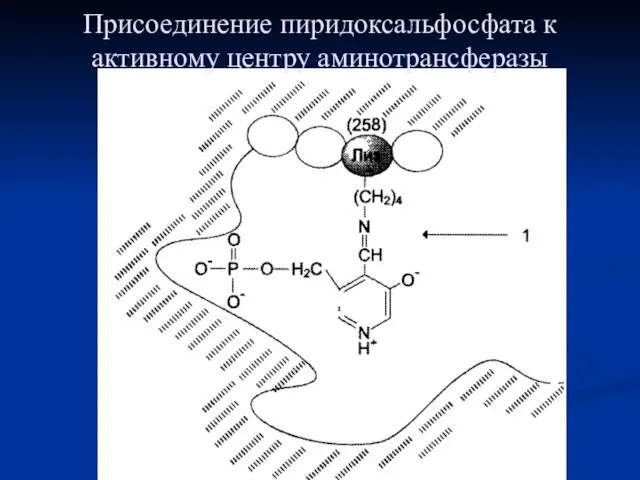
- 67. Присоединение пиридоксальфосфата к активному центру аминотрансферазы
- 68. Основной путь трансаминирования Чаще всего в реакциях трансаминированиш участвуют аминокислоты, содержание которых в тканях значительно выше
- 70. Аминотрансферазы обладают субстратной специфичностью к разным аминокислотам. В тканях человека обнаружено более 10 разных аминотрансфераз. Наиболее
- 71. Аланинаминотрансфераза АЛТ (АлАТ) катализирует реакцию трансаминирования между аланином и α-кетоглутаратом. Локализован этот фермент в цитозоле клеток
- 72. ACT (АсАТ) катализирует реакцию трансаминирования между аспартатом и α-кетоглутаратом аналогично предыдущей. В результате образуются оксалоацетат и
- 73. Биологическое значение трансаминирования Реакции трансаминирования играют большую роль в обмене аминокислот. Поскольку этот процесс обратим, ферменты
- 74. Дезаминирование аминокислот Дезаминирование аминокислот — реакция отщепления α-аминогруппы от аминокислоты, в результате чего образуется соответствующая α-кетокислота
- 75. Виды дезаминирования Окислительное (идет в две ступени); Восстановительное; Гидролитическое; Внутримолекулярное; Трансаминирование.
- 76. Окислительное дезаминирование Наиболее активно в тканях происходит деза-минирование глутаминовой кислоты. Реакцию катализирует фермент глутаматдегидрогеназа, коферментом глутаматдегидрогеназы
- 77. Дезаминирование глутамата
- 78. Непрямое дезаминирование (трансдезаминирование) Большинство аминокислот не способно дезаминироваться в одну стадию, подобно Глу. Аминогруппы таких аминокислот
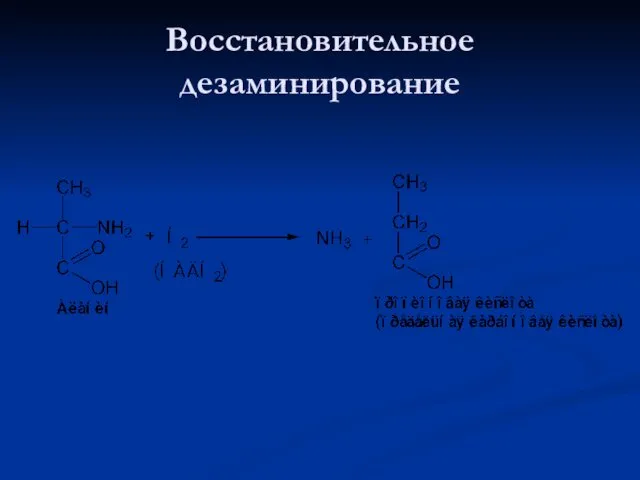
- 79. Восстановительное дезаминирование
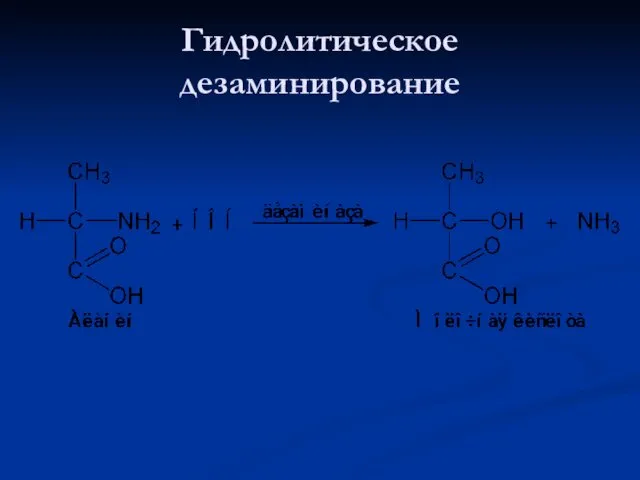
- 80. Гидролитическое дезаминирование
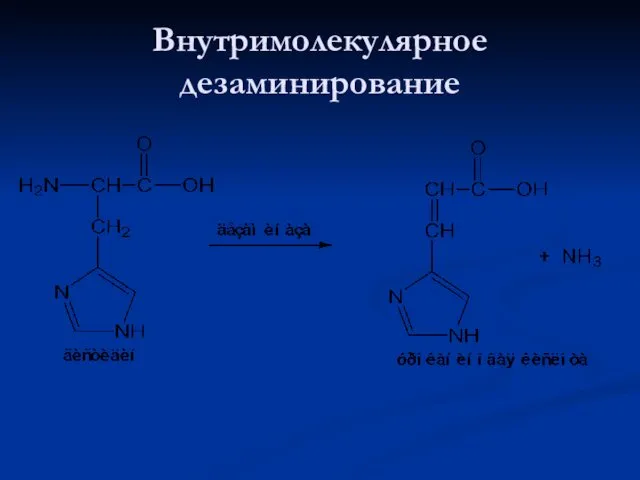
- 81. Внутримолекулярное дезаминирование
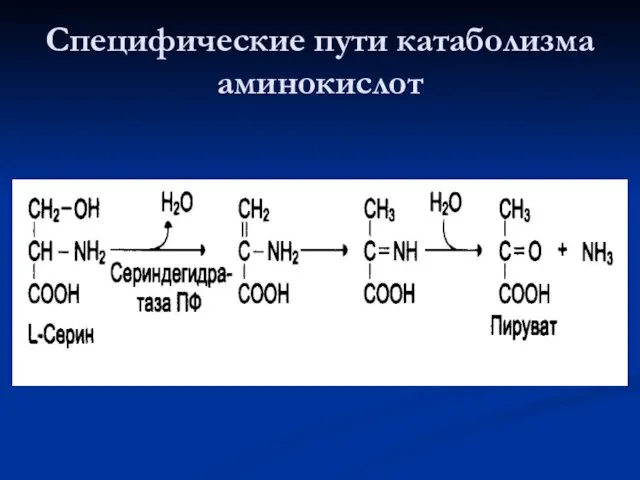
- 82. Специфические пути катаболизма аминокислот
- 83. Специфические пути катаболизма аминокислот
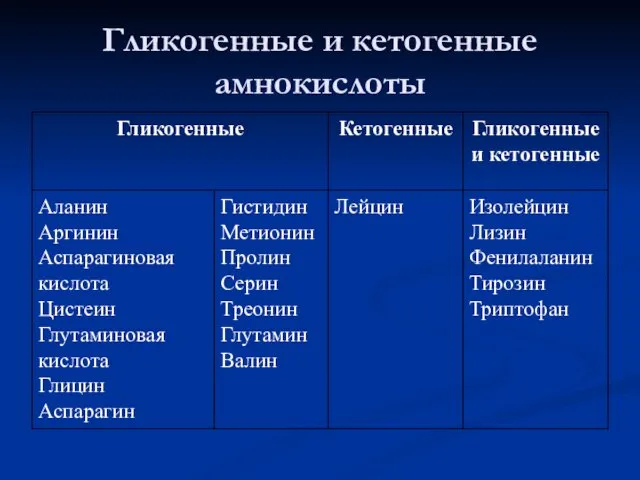
- 84. Гликогенные и кетогенные аминокислоты Аминокислоты, которые в процессе катаболизма превращаются в пируват, оксалоацетат (ЩУК) и фосфоенолпируват,
- 85. Гликогенные и кетогенные амнокислоты
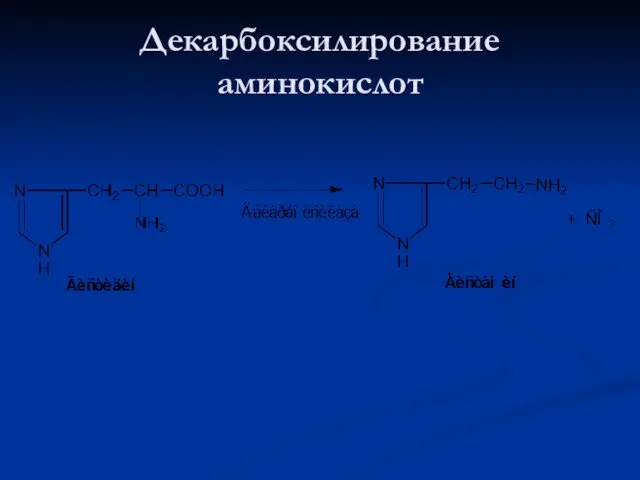
- 86. Декарбоксилирование аминокислот
- 87. Биологическая роль гистамина Много образуется в очаге воспаления: обладает сосудорасширяющим действием, ускоряет приток лейкоцитов и активирует
- 88. Декарбоксилирование аминокислот
- 89. Токсичность аммиака Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глутаматдегидрогеназой,
- 90. Токсичность аммиака Повышение концентрации аммиака в крови сдвигает рН в щелочную сторону (вызывает алкалоз). Это, в
- 91. Пути обезвреживания аммиака Временное обезвреживание (во всех тканях): - образование аммонийных солей; - образование амидов дикарбоновых
- 92. R R COOH +NH3 COONH4 органическая аммонийная кислота соль органич. к-ты
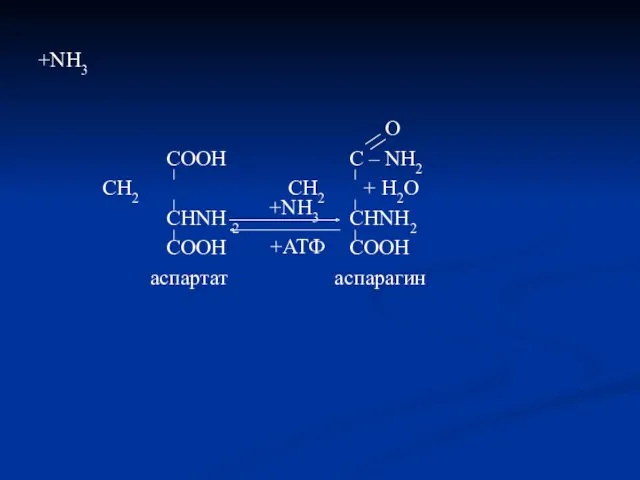
- 93. +NH3 O COOH C – NH2 CH2 CH2 + H2O CHNH 2 CHNH2 COOH COOH аспартат
- 94. Связывание аммиака Основной реакцией связывания аммиака, протекающей во всех тканях организма, является синтез глутамина под действием
- 95. Глутамин — основной донор азота в организме. Высокий уровень глутамина в крови и лёгкость его поступления
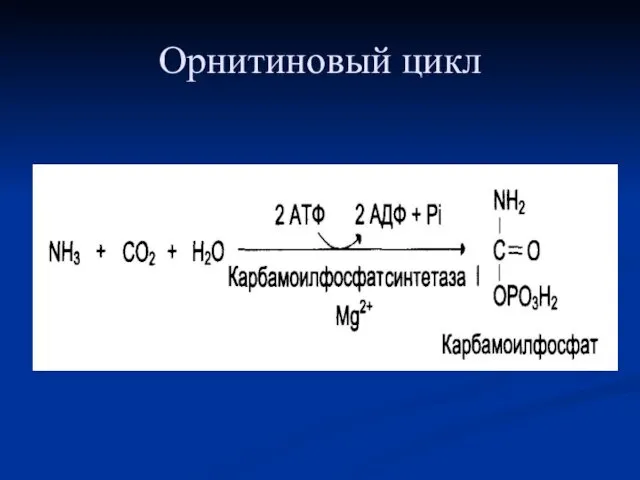
- 96. Орнитиновый цикл Мочевина — основной конечный продукт азотистого обмена, в составе которого из организма выделяется до
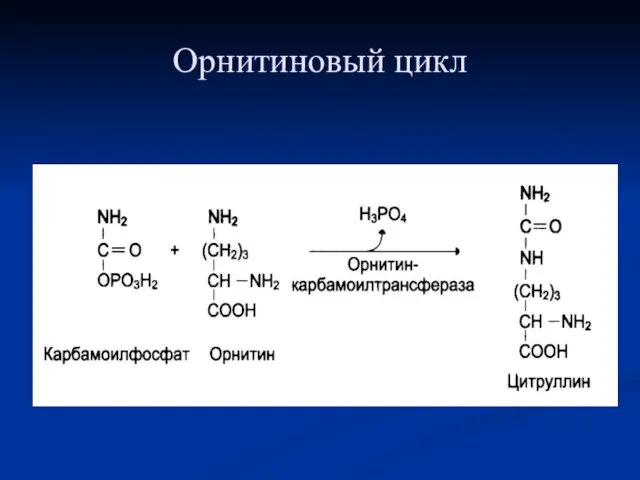
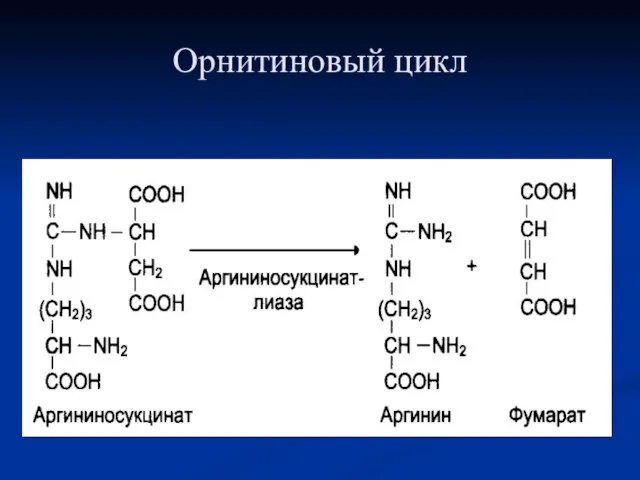
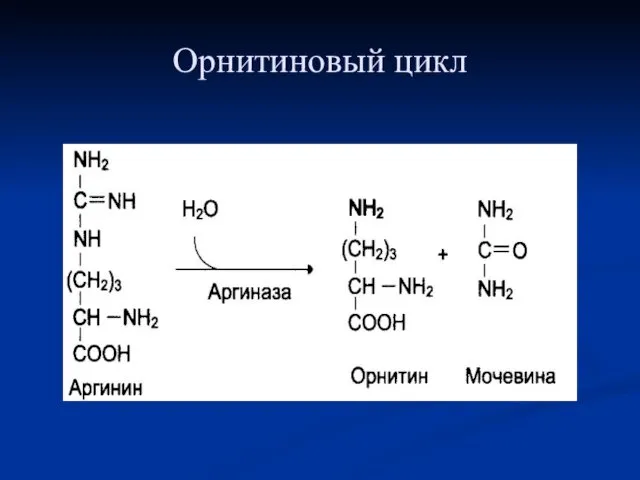
- 97. Орнитиновый цикл
- 98. Орнитиновый цикл
- 99. Орнитиновый цикл
- 100. Орнитиновый цикл
- 101. Орнитиновый цикл
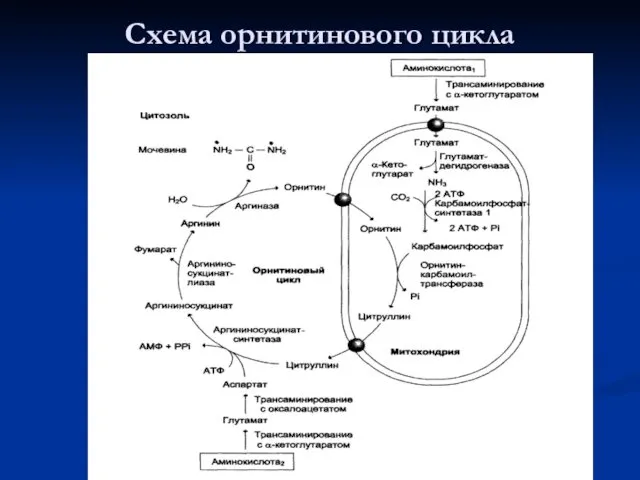
- 102. Схема орнитинового цикла
- 103. При образовании мочевины используется А) аммиак – одна молекула Б) СО2 – одна молекула В) аминогруппа
- 104. Анаболическая фаза обмена белков Синтез заменимых аминокислот. Синтез специфических белков. Синтез азотсодержащих веществ: -биогенные амины; -гормоны
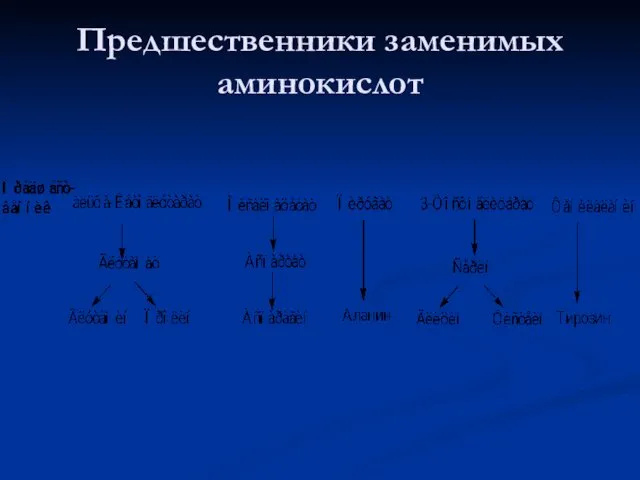
- 105. Синтез заменимых аминокислот Углеродный скелет заменимых аминокислот образуется из промежуточных метаболитов гликолиза, пентозофосфатного пути, цикла трикарбоновых
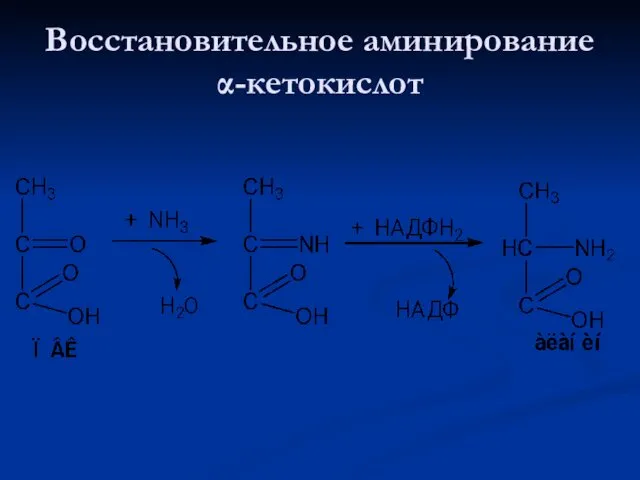
- 106. Восстановительное аминирование α-кетокислот
- 107. Трансаминирование
- 108. Предшественники заменимых аминокислот
- 110. Скачать презентацию

















































































 Многообразие и происхождение пресмыкающихся
Многообразие и происхождение пресмыкающихся Наука биология
Наука биология Антибиотические отношения. Паразитизм
Антибиотические отношения. Паразитизм водоплавающие птицы Дальнего Востока
водоплавающие птицы Дальнего Востока Инвазионные виды в результате деятельности человека
Инвазионные виды в результате деятельности человека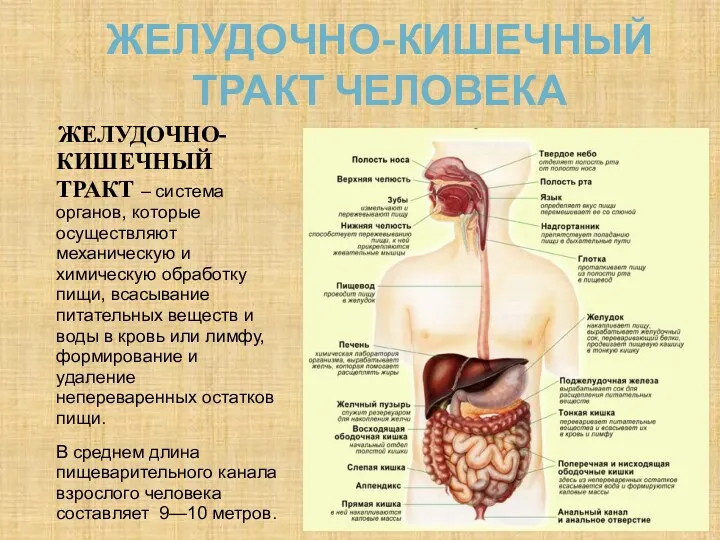 Желудочно-кишечный тракт человека
Желудочно-кишечный тракт человека Значення мікробів в кругообігу речовин в природі
Значення мікробів в кругообігу речовин в природі Дистанционное обучение - биология 11 класс
Дистанционное обучение - биология 11 класс Биология как наука
Биология как наука Дикие и домашние животные. (2 класс)
Дикие и домашние животные. (2 класс) Задания ЕГЭ по теме Клетка
Задания ЕГЭ по теме Клетка Научная работа о медведях
Научная работа о медведях Рецепция. Өткізгіш жолдардың жүйелік ұйымдасуы
Рецепция. Өткізгіш жолдардың жүйелік ұйымдасуы Витамины жирорастворимые и водорастворимые
Витамины жирорастворимые и водорастворимые Общая физиология сенсорных систем
Общая физиология сенсорных систем Генетика микроорганизмов
Генетика микроорганизмов Технологическая карта урока
Технологическая карта урока Чипсы, вред или польза
Чипсы, вред или польза b4bc0cef0f934965a9c12b2fa1f5e8ea
b4bc0cef0f934965a9c12b2fa1f5e8ea Кожно-двигательный, зрительный, слуховой,вестибулярный, обонятельный и вкусовой анализаторы
Кожно-двигательный, зрительный, слуховой,вестибулярный, обонятельный и вкусовой анализаторы Витамины - источники жизни
Витамины - источники жизни Элективный курс Репродуктивное здоровье
Элективный курс Репродуктивное здоровье Методы исследования генетики человека
Методы исследования генетики человека Фізіологічні механізми адаптації організму людини до фізичних навантажень. (Лекція 3)
Фізіологічні механізми адаптації організму людини до фізичних навантажень. (Лекція 3) Общие свойства живых организмов
Общие свойства живых организмов Органы чувств
Органы чувств Современные представления об эволюции органического мира
Современные представления об эволюции органического мира Биологическая мотивация: пищевая, половая, оборонительная
Биологическая мотивация: пищевая, половая, оборонительная