Слайд 2
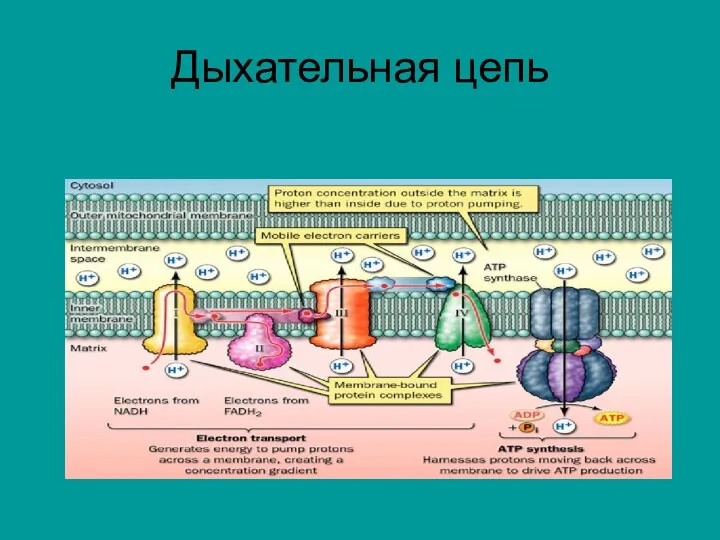
Слайд 3
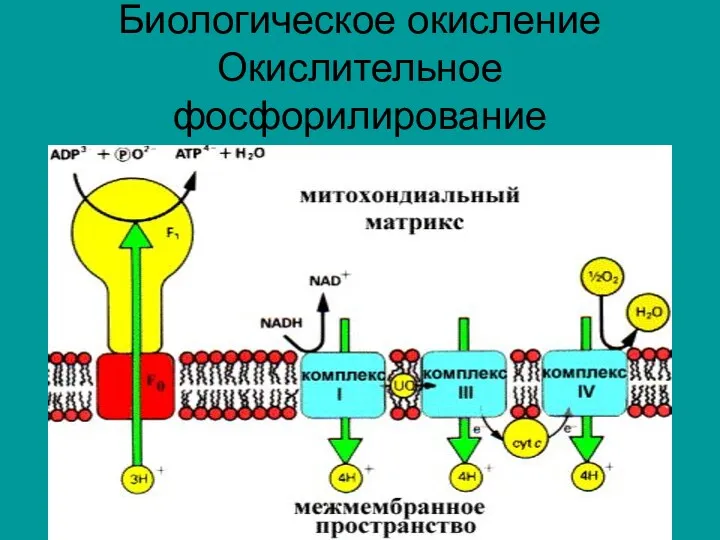
Биологическое окисление Окислительное фосфорилирование
Слайд 4

В пище человека нет готовых первичных доноров водорода, которые могут служить
субстратами для дегидрогеназ. Они образуются в ходе катаболизма пищевых веществ.
Слайд 5

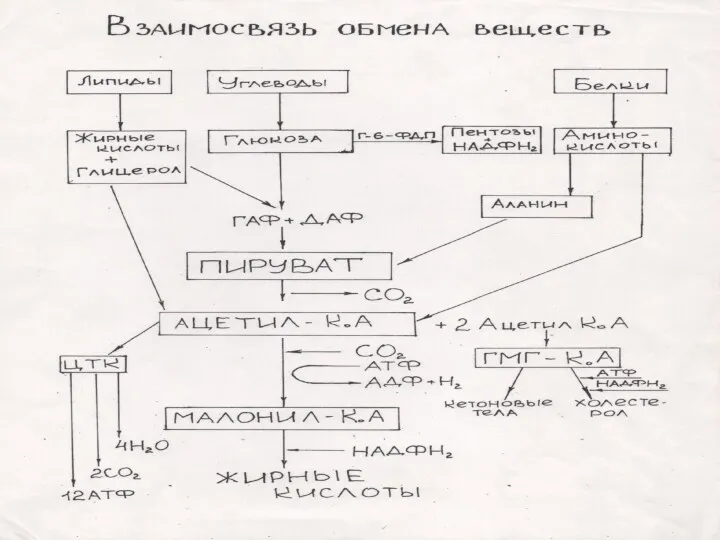
В ходе метаболизма У , Ж и Б образуются 2 центральных
метаболита:
1) ПВК (пировиноградная кислота) и
2) ацетил-КоА.
Слайд 6
Слайд 7
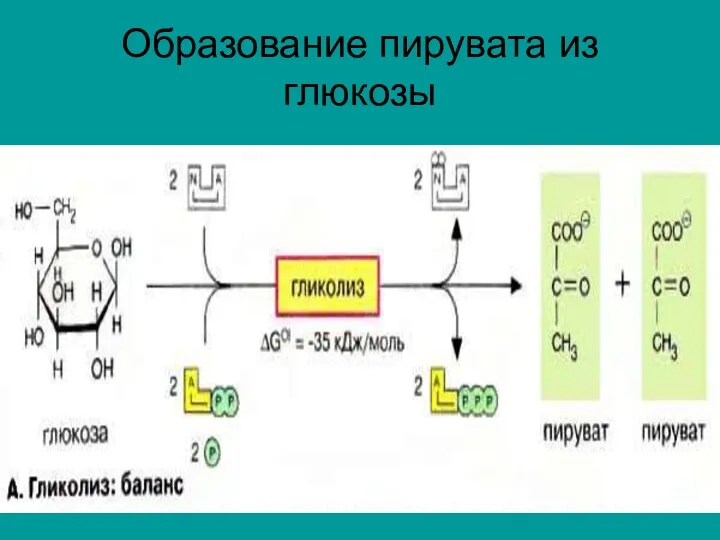
Образование пирувата из глюкозы
Слайд 8
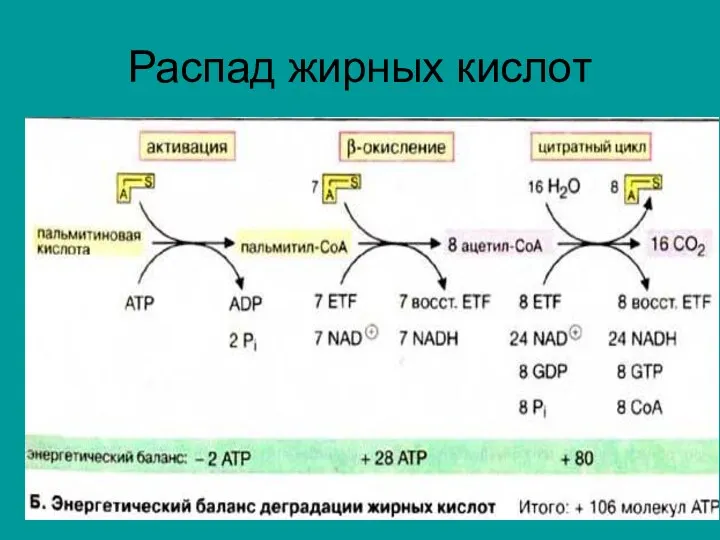
Слайд 9

Различают специфические пути катаболизма (разные для разных классов веществ) и
Общие пути
катаболизма, которые являются единым продолжением специфических путей.
Слайд 10
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
В МАТРИКСЕ МИТОХОНДРИЙ
Слайд 11

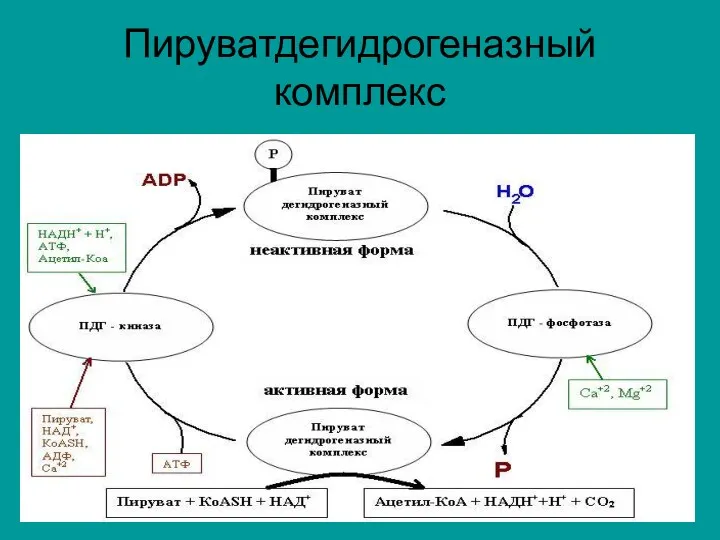
Окислительное декарбоксилирование пирувата
пируватдегидрогеназный мультиферментный комплекс:
3 фермента:
пируватдегидрогеназа (декарбоксилирующая) -
Е1-ТПФ,
дигидролипоилацетилтрансфераза –
Е2-ЛК,
Дигидролипоилдегидрогеназа – Е3-ФАД.
Слайд 12

5 коферментов:
1)Тиаминдифосфат (ТДФ) с Е1,
2) Липоевая кислота (ЛК) с
Е2,
Слайд 13

3) ФАД в виде простетической группы на Е3.
4) НАД+
5) кофермент А
Слайд 14

Е2-ЛК составляет ядро пируватдегидрогеназного комплекса, вокруг которого расположены пируватдегидрогеназа и
дигидролипоилдегидрогеназа.
Слайд 15

Суммарная реакция:
Пируват + НАД+ + HS-KoA
–>Ацетил-КоА +
НАДН + Н+ + СO2.
Слайд 16
Пируватдегидрогеназный комплекс
Слайд 17
Слайд 18

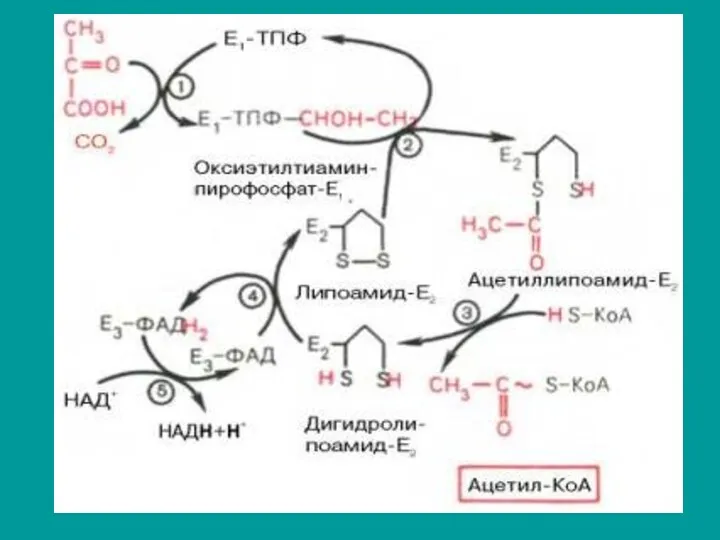
На I стадии пируват теряет свою карбоксильную группу в результате взаимодействия
с ТПФ в составе активного центра E1-ТПФ.
Слайд 19

На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной
группы, которая переносится на ЛК, связанную с ферментом Е2-ТПФ.
Слайд 20

Этот фермент катализирует III стадию – перенос ацетильной группы на
коэнзим КоА (HS-KoA) с образованием ацетил-КоА.
Слайд 21

На IV стадии образуется окисленная форма ЛК из восстановленного комплекса Е2-ЛК.
При участии фермента дигидролипоилдегидрогеназы (Е3-ФАД) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоевой кислоты на ФАД.
Слайд 22

На V стадии восстановленный ФАДН2 дигидролипоилдегидрогеназы передает водороды на кофермент
НАД с образованием НАДН + Н+.
Слайд 23

Суммарная реакция, катализируемая пируватдегидрогеназным комплексом:
Пируват + НАД+ + HS-KoA
–>Ацетил-КоА + НАДН + Н+ + СO2.
Слайд 24
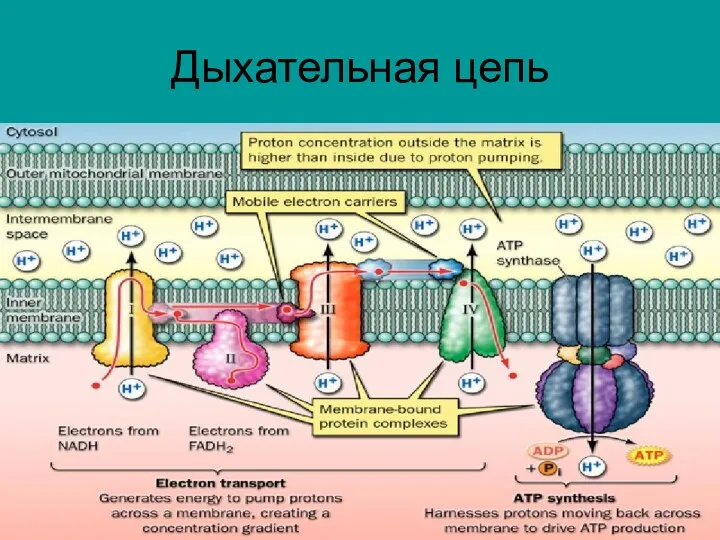
Слайд 25

Образовавшийся в процессе окислительного декарбоксилирования ацетил-КоА подвергается дальнейшему окислению с образованием
СО2 и Н2О в цикле трикарбоновых кислот (цикл Кребса).
Слайд 26

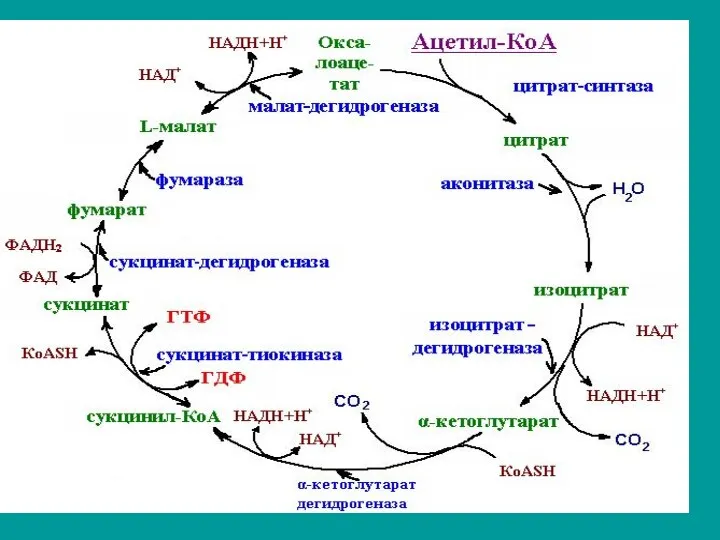
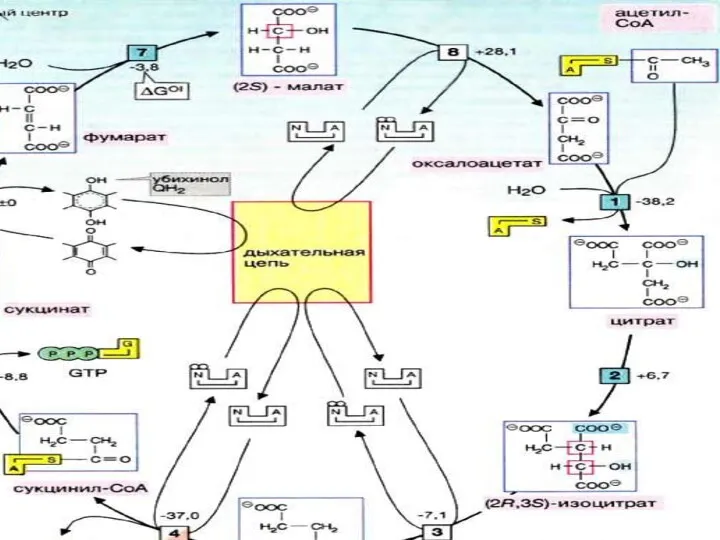
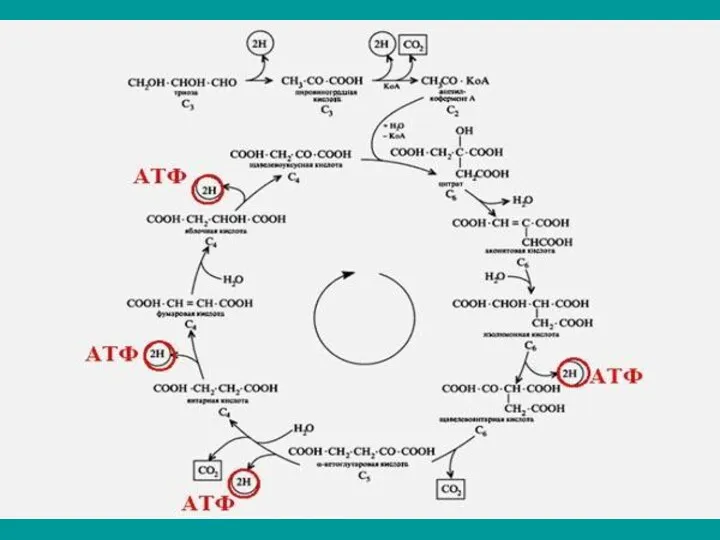
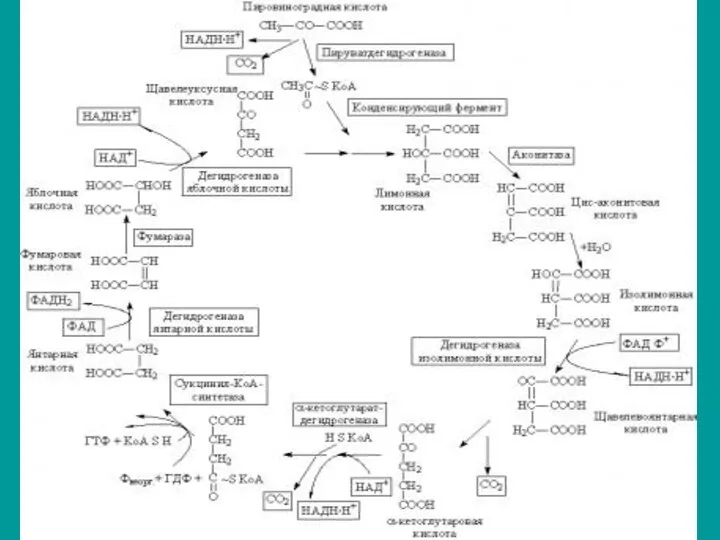
Цикл трикарбоновых кислот
Полное «сгорание» как жирных кислот, так и углеводов требует
окисления до СО2 и Н2О ацетильного остатка, связанного с коферментом А.
Слайд 27

ЦТК – цикл Кребса
Сгорание происходит в цикле трикарбоновых кислот — циклом
Кребса. Как и окислительное декарбо-ксилирование пирувата, происходит в МХ клеток.
Слайд 28

Первая реакция
Присоединение ацетильного остатка ацетилкофермента А к оксалоацетату с образованием трикарбоновой
лимонной кислоты — цитрата.
Слайд 29

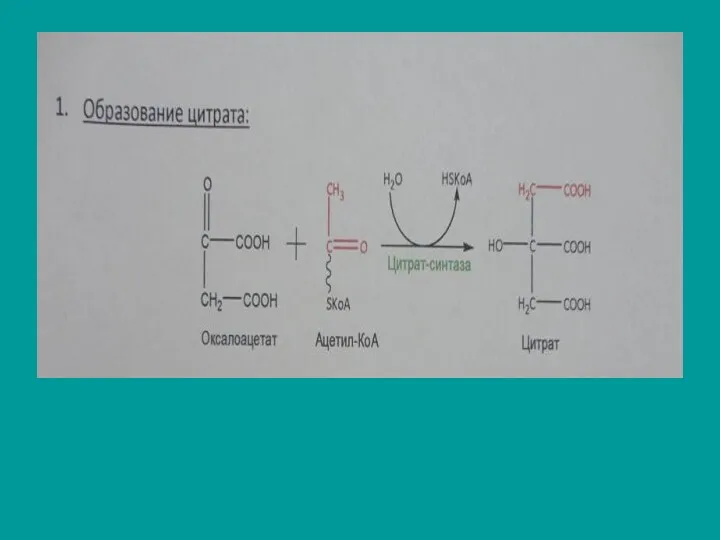
Первая стадия
Взаимодействие ацетилкофермента А с оксалоацетатом, катализируемое ферментом цитратсинтазой:
Слайд 30
Слайд 31

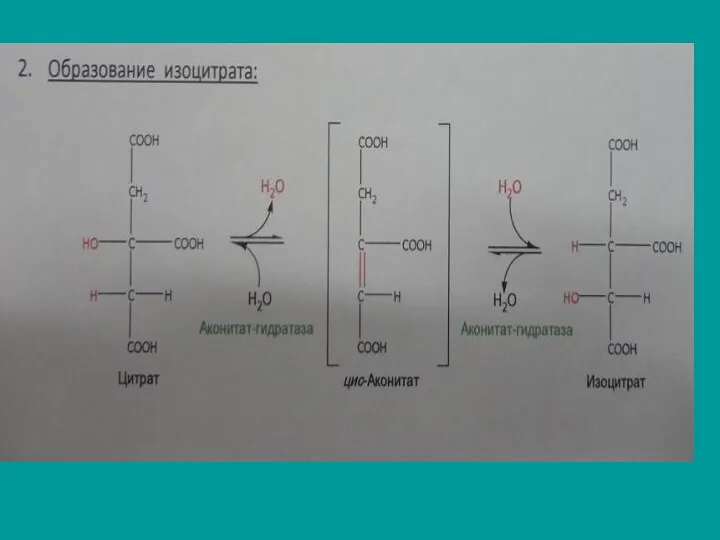
Вторая стадия
Изомеризация цитрата в изоцитрат, катализируется аконитазой.
Проходит через образование аконитата путем
дегидратации цитрата и последующей гидратации аконитата с превращением его в изоцитрат:
Слайд 32
Слайд 33

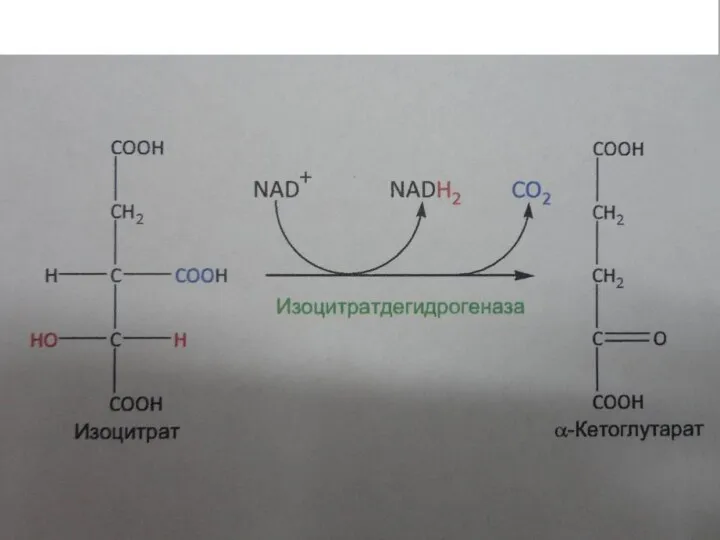
Третья стадия
3. Окисление гидроксигруппы изоцитрата до карбонильной группы с помощью NAD+,
сопровождается элиминацией карбоксильной группы в бета-положении изоцитратдегидрогеназой:
Слайд 34
Слайд 35

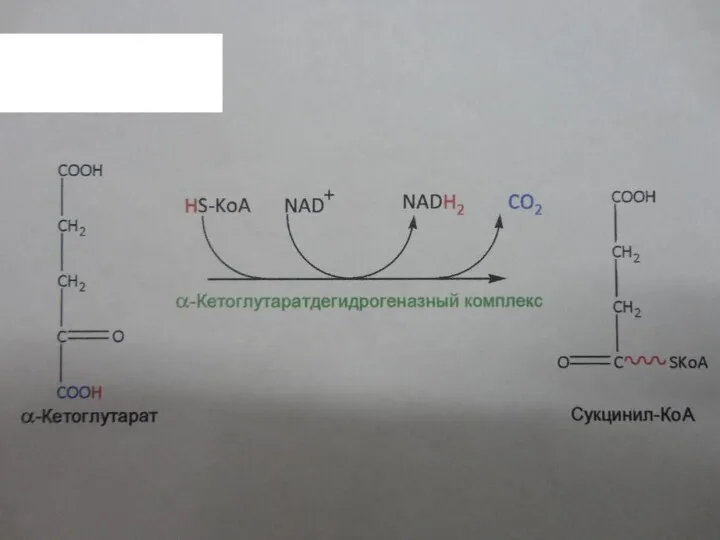
Четвертая стадия
4. Окислительное декарбоксилирование
aльфа-кетоглутарата, катализируется aльфа‑кетоглутаратдегидрогеназным комплексом. Образуется сукцинилкофермент А
и выделяется вторая молекула CO2:
Слайд 36
Слайд 37

Пятая стадия
5. Фосфорилирование GTP, сопряженное с гидролизом макроэргической тиоэфирной связи в
сукцинилкоферменте А, катализируется сукцинатСоА лиазой:
Слайд 38

Слайд 39

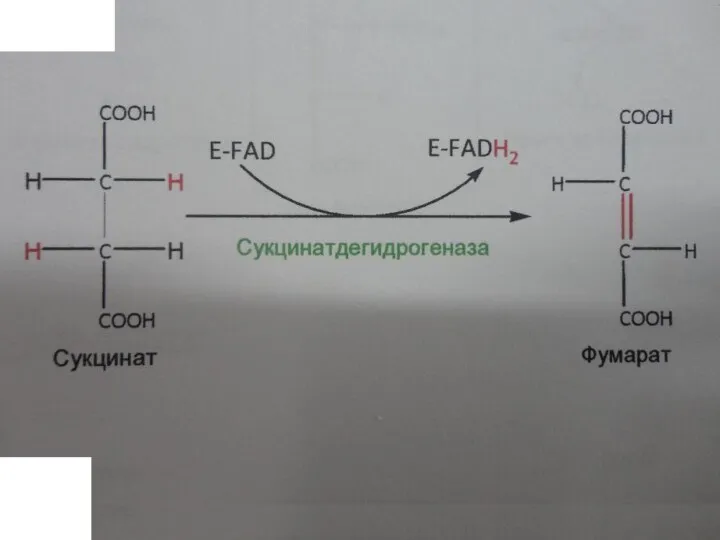
Шестая стадия
6. Превращение сукцината в фумарат, катализируется сукцинатдегидрогеназой,
( в
составе комплекса II ЦПЭ с коферментом Q в качестве акцептора электронов:
Слайд 40
Слайд 41

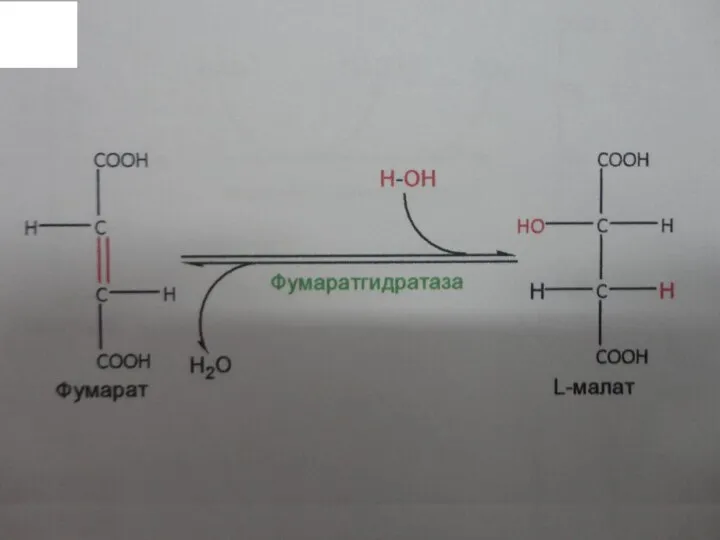
Седьмая стадия
7. Гидратация двойной связи фумарата с образованием малата, катализируется фумарат-
гидратазой:
Слайд 42
Слайд 43

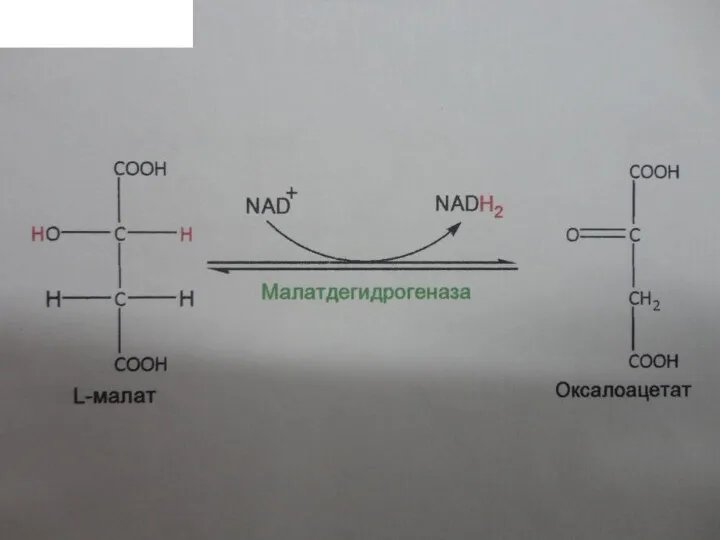
Восьмая стадия
8. Окисление гидроксигруппы малата до кетогруппы, приводит к регенерации оксалоацетата,
катализируется малатдегидрогеназой:
Слайд 44
Слайд 45

Значение ЦТК
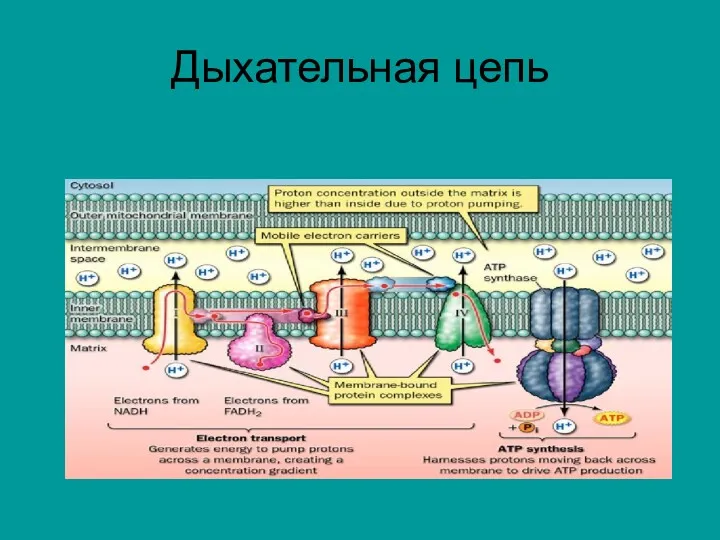
В ходе ЦТК восстанавливается до НАДH три молекулы НАД+, пара
электронов посылается в комплексы III и IV цепи переноса электронов от ФАДН2 через кофермент Q и образуется одна макроэргическая связь в молекуле GТР.
Слайд 46
Слайд 47

Энергетика ЦТК
С учетом АТФ, образующихся в ЦПЭ при окислении НАДH2 и
ФАДH2, сгорание ацетильного остатка в ЦТК сопровождается образованием 11 молекул АТФ и одной ГТФ, т.е. - 12 макроэргиче-ских связей.
Слайд 48

Роль ЦТК для анаболизма
При стационарном функционировании ЦТК никакие компоненты цикла не
расходуются. Некоторые компоненты ЦТК необходимы для биосинтетических процессов (синтез некоторых аминокислот и нуклеотидов).
Слайд 49
Слайд 50
Слайд 51
Слайд 52



















































 Науки о человеке: анатомия, физиология, гигиена
Науки о человеке: анатомия, физиология, гигиена Биология оқыту әдістемесі ғылым ретінде. Биология оқыту әдістемесінің пәні
Биология оқыту әдістемесі ғылым ретінде. Биология оқыту әдістемесінің пәні Грегор Мендель. Закон единообразия гибридов
Грегор Мендель. Закон единообразия гибридов Микроскопические методы исследования морфологии микроорганизмов
Микроскопические методы исследования морфологии микроорганизмов Этапы эволюции человека
Этапы эволюции человека Как определить птицу
Как определить птицу Пути воздействия организмов на среду обитания
Пути воздействия организмов на среду обитания Організмовий рівень організації генетичної інформації. Взаємодія генів
Організмовий рівень організації генетичної інформації. Взаємодія генів Продуктивность кукурузы в зависимости от приемов выращивания в центральной зоне Краснодарского края
Продуктивность кукурузы в зависимости от приемов выращивания в центральной зоне Краснодарского края Сердечно-сосудистая система
Сердечно-сосудистая система Презентация по биологии Семейство крестоцветные
Презентация по биологии Семейство крестоцветные Бактериофаги. Строение бактериофагов
Бактериофаги. Строение бактериофагов Дикие и домашние животные
Дикие и домашние животные По грибы. Классный час, возраст: 7-10 лет
По грибы. Классный час, возраст: 7-10 лет Двигательные системы
Двигательные системы Индивидуальное развитие организмов (онтогенез)
Индивидуальное развитие организмов (онтогенез) Урок 8 класс. Осанка. Первая помощь при травмах скелета
Урок 8 класс. Осанка. Первая помощь при травмах скелета Характеристика класса птицы. Внешнее строение птиц
Характеристика класса птицы. Внешнее строение птиц Конспект открытого урока по теме : Опорно-двигательная система. Биология 8 класс.
Конспект открытого урока по теме : Опорно-двигательная система. Биология 8 класс. Царство животные
Царство животные Життя риб навесні. 2 клас
Життя риб навесні. 2 клас Анатомия женских половых органов (1)
Анатомия женских половых органов (1) V.A. Motsart hayoti va ijodi
V.A. Motsart hayoti va ijodi Гиповитаминозы животных
Гиповитаминозы животных Отряды насекомых
Отряды насекомых Презентация непрямой онтогенез
Презентация непрямой онтогенез В поисках витамина С. 2 класс
В поисках витамина С. 2 класс Гіпотези виникнення життя на землі
Гіпотези виникнення життя на землі