Содержание
- 2. ПЛАН 1. Дисперсійні системи молока і формування полідисперсійної системи 2. Молоко як емульсія 3. Молоко як
- 3. Дисперсійна система – система, яка формується з однієї чи декількох речовин, що тонко розприділені в дисперсійному
- 4. Класифікації дисперсійних систем За просторовою відокремленістю: дискретні (інкогерентні) і компактні (когерентні) За агрегатним станом: піни, емульсії,
- 5. Приклади Молоко: інкогерентна, тонкодисперсійна + суспензія + справжній розчин, емульсія (суспензія, піна, аерозоль) Коагульований казеїн: когерентна,
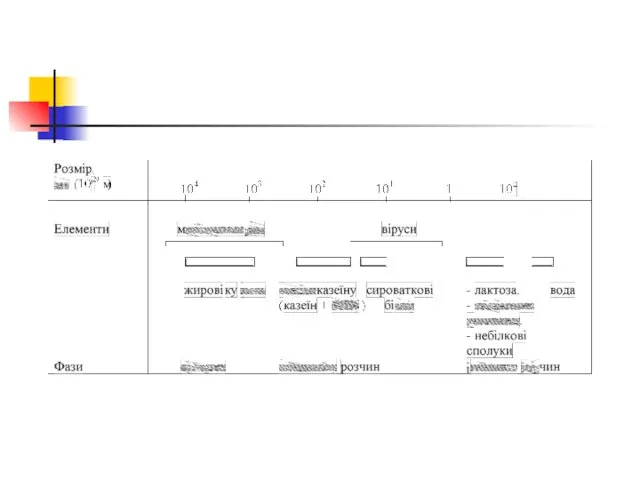
- 6. Молоко – корпускулярна полідисперсійна система: часточки різні за розмірами
- 7. Молоко – інкогерента, корпускулярна, полідисперсійна система, в якій жир емульгований, білки (а також частина мінеральних солей)
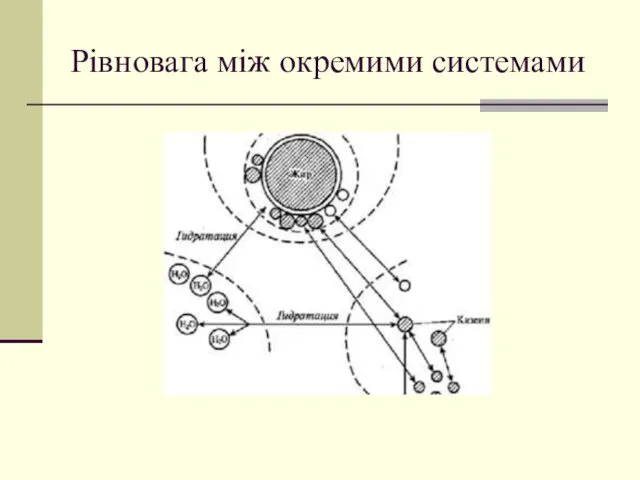
- 8. Рівновага між окремими системами: Встановлюється під час синтезу молока (розчин солей Са стабілізує колоїдну систему казеїнів;
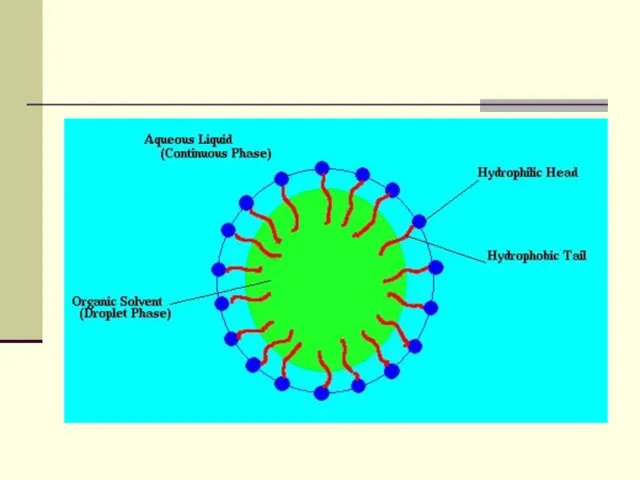
- 10. Система емульсії Молоко – типова природна емульсія Значення: з т.з. фізіології харчування новонароджених; з т. з.
- 11. Класифікація емульсій: За полярністю За концентрацією
- 12. Діаметр жирових кульок: 1- 10 мкм В 1 мл молока – 1,5 – 3 млрд. жирових
- 13. Стабільність емульсії Структурно-механічний бар'єр – оболонка Термодинамічний бар'єр – заряд поверхні Стабільність відносна через надлишок поверхневої
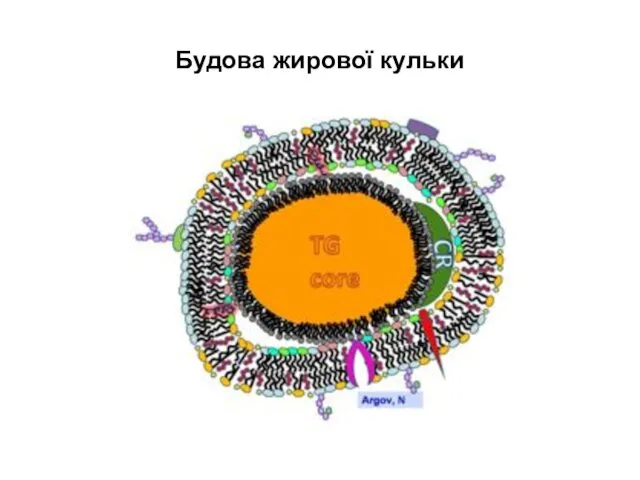
- 14. Будова жирової кульки
- 15. Схема синтезу жиру і секреції жирової глобули
- 16. Склад оболонок жирових кульок Білки + ліпіди (1:1) У мг/100 г жиру: Протеїни 1800 Фосфоліпіди 650
- 17. Ліпідна фракція Полярні ліпіди (в напіврідкому, але наближеному до твердого стані): Фосфатидилхолін (36%) Фосфатидилетаноламін (27%) Фосфатидилінозитол
- 18. Білкова фракція Структурні або трансмембранні білки (погано розчинні) – глікопротеїди, пронизують оболонку жирової кільки, частина, яка
- 19. Мінеральні елементи Cu, Fe, Mo, Zn, Co, Mg, Se, Na, K Утворюють комплекси з білками а
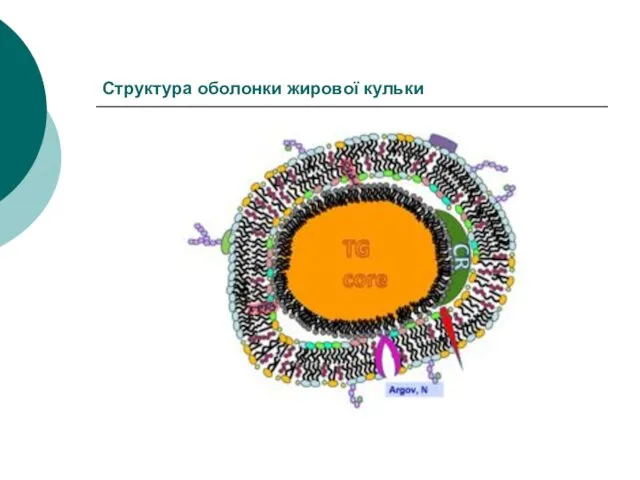
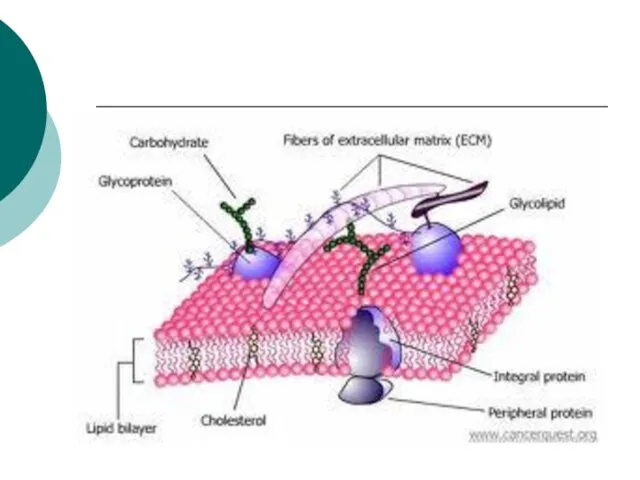
- 20. Структура оболонки жирової кульки
- 21. Існуюча модель – динамічна мозаїчна модель, за якою молекули білків занурені із двох сторін мембрани на
- 22. Оболонка жирових кульок складається з: Внутрішнього тонкого шару 10 нм (власне плазматична мембрана) І зовнішнього рихлого
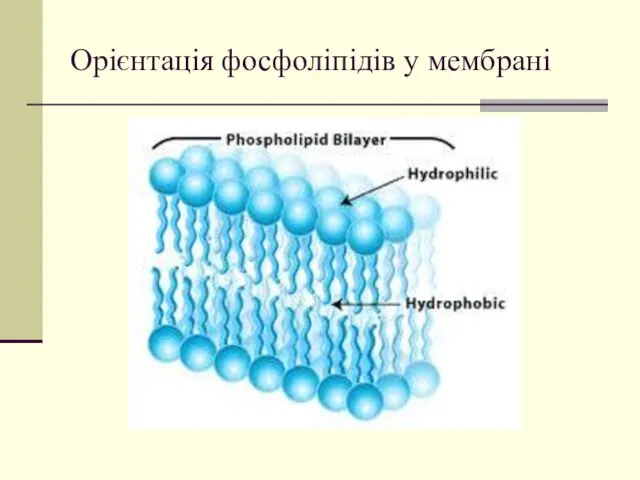
- 24. Орієнтація фосфоліпідів у мембрані
- 26. Сили відповідальні за цілісність структури Гідрофобні взаємодії: ФЛ, білки Електростатичні: заряджені групи амінокислот, вуглеводневих груп
- 27. Зміна оболонки під час обробки Свіже молоко – поверхня доволі значної товщини, нерівна Механічна обробка (перемішування,
- 28. Стабільність емульсії Залежить від величини енергії взаємодії, яка складається з суми енергії електростатичного відштовхування і енергії
- 29. Енергетичний бар'єр – заряд поверхні + гідратна оболонка (ПЕШ) Частинки в цілому електричнонейтральні, але при наближенні
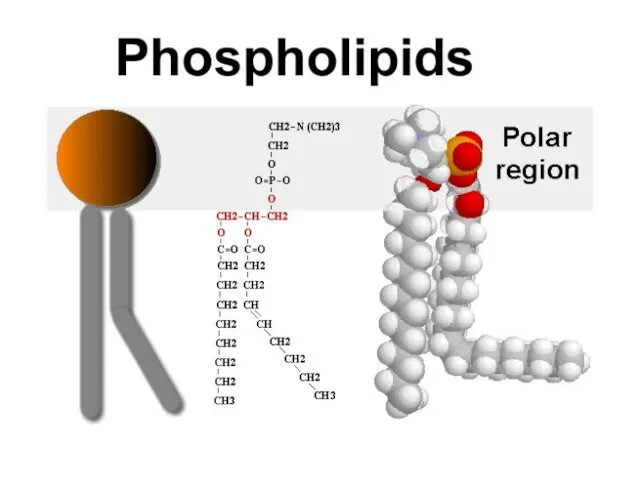
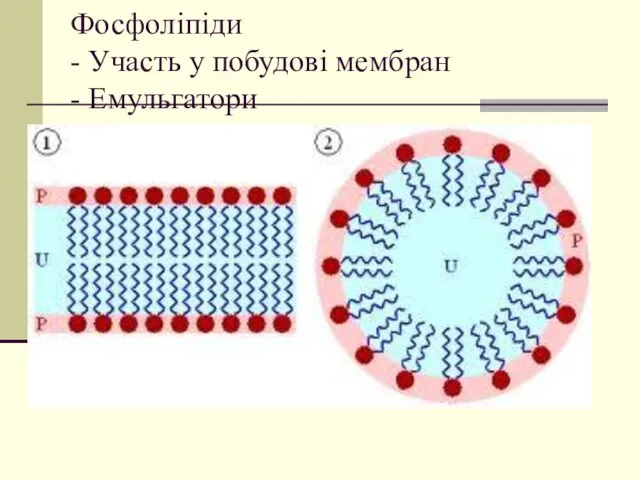
- 30. Фосфоліпіди - Участь у побудові мембран - Емульгатори
- 31. Емульгатор, абсорбуючись на поверхні – міжфазовій границі, знижує поверхневий натяг. Стабілізувальна функція емульгатора пояснюється створенням на
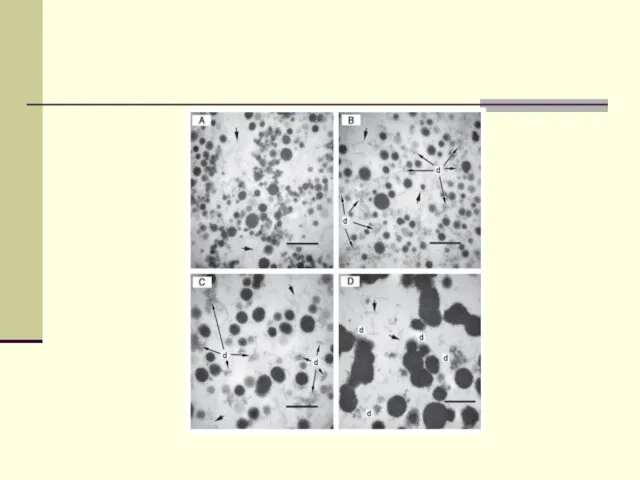
- 32. Обробка протеїназами і фосфоліпазами викликає коалесценцію
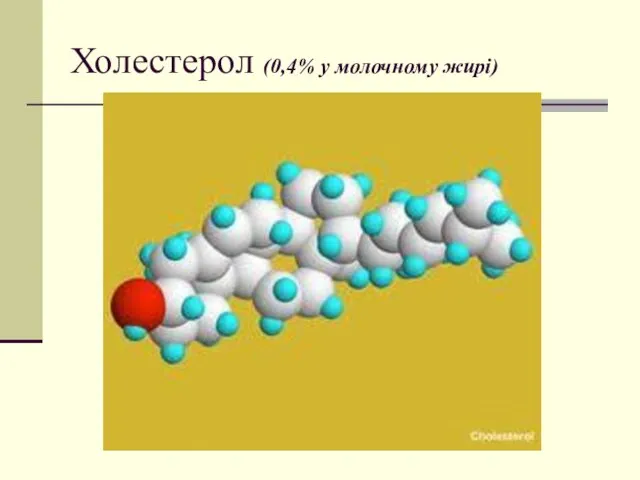
- 33. Холестерол (0,4% у молочному жирі)
- 34. Емульсія
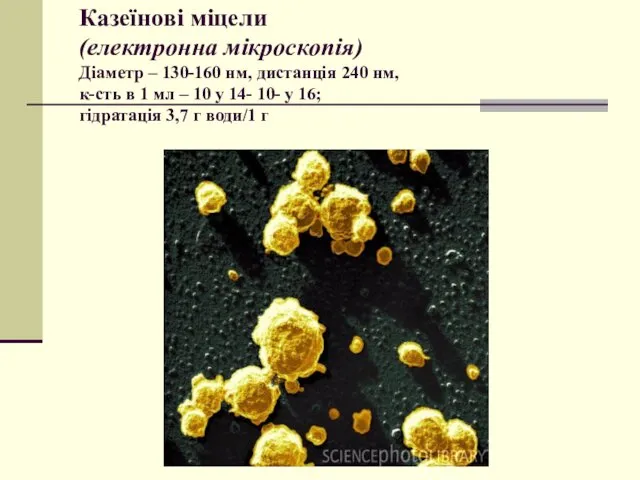
- 37. Казеїнові міцели (електронна мікроскопія) Діаметр – 130-160 нм, дистанція 240 нм, к-сть в 1 мл –
- 38. Хімічний склад казеїнових міцел (ККФК) αs1 -33% αs2 -11% β- 37% χ-11% Ca - 2,9% Mg
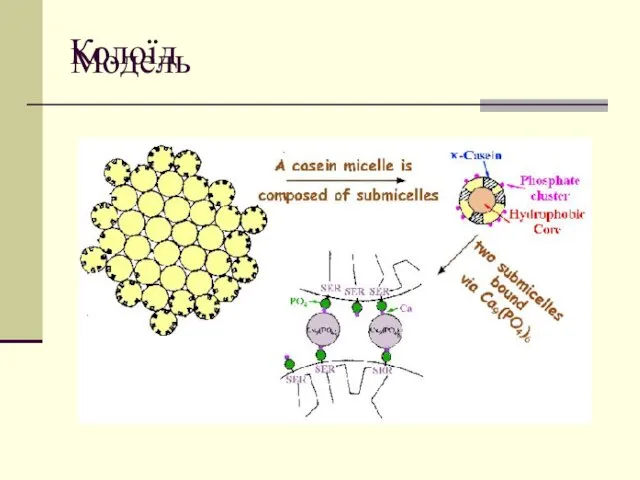
- 39. Модель Колоїд
- 40. Будова міцел субміцелярна Субміцели побудовані з 10-12 субодиниць, молекули з’єднані гідрофобними, електростатичними, водневими зв’язками і кальцієвими
- 41. Поверхня казеїнових міцел заряджена: Багато груп аспарагінової і глутамінової кислот, крім того, серину і треоніну з
- 42. Міцелярний казеїн є сильногідратованим, 1 г білка поглинає 2-3,7 г води Вода не тільки оточує міцеллу,
- 43. Поверхня казеїнової міцелли має приблизно 9600-12800 носіїв заряду (В міцеллі є біля 8000, біля 15-20% у
- 44. Фактори стійкості казеїнових міцел Теорія ДЛФО (Дерягін, Ландау, Фервей, Овербок): Стійкість і коагуляція частинок в колоїдних
- 45. Часточки сироваткових білків – або окремі молекули, або димери чи полімери (пентамери) Розміри колоїдних часточок β-Лактоглобуліну
- 46. Дестабілізація колоїдної системи молока: Зниження рН (к/м продукти; небажана при самовільному скисанні молока) Дія сильних електролітів
- 48. Коагуляцію сироваткових білків можна викликати шляхом теплової обробки. Термостійкість: Яєчний альбумін +56˚С Сироватковий альбумін молока +67˚С
- 49. Механізм теплової коагуляції сироваткових білків – теплова енергія приводить до розгортання поліпептидних ланцюгів після розриву водневих
- 50. Усі фактори, що знижують поверхневий заряд і міцність гідратної оболонки (зміна рН, додавання електролітів, дія протеолітичних
- 51. Система справжнього розчину Гомогенний розчин, що складається з розчинених сполук і води Солі Са, Na, K,
- 52. Частина цитратів і фосфатів Са, Mg у стані справжнього розчину Система справжнього розчину зумовлює осмотичний тиск,
- 53. Молочна сироватка – реальний (а не ідеальний розчин), в якому молекули здійснюють взаємний вплив – міжіонна
- 54. Рівновага між окремими системами
- 56. Скачать презентацию








































 Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения
Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения клетка
клетка فيتامين C بدون حركات
فيتامين C بدون حركات Решение задач по цитологии и генетике
Решение задач по цитологии и генетике Адамның рефлекторлық реакциясын зерттеу
Адамның рефлекторлық реакциясын зерттеу Растениеводство. Жизненный цикл зерновых хлебов
Растениеводство. Жизненный цикл зерновых хлебов Блеск и сила здоровых волос
Блеск и сила здоровых волос Пищеварение в желудке и кишечнике
Пищеварение в желудке и кишечнике Biochimia. Enzimele
Biochimia. Enzimele Презентация О великом женском секрете
Презентация О великом женском секрете презентация с аннимациями образование биоценоза Диск
презентация с аннимациями образование биоценоза Диск Строение волос
Строение волос Лекарственные растения в домашней аптечке (2 класс)
Лекарственные растения в домашней аптечке (2 класс) Red Wolf
Red Wolf презентация к разработке по внеклассного мероприятия теме вода
презентация к разработке по внеклассного мероприятия теме вода Многообразие одноклеточных организмов
Многообразие одноклеточных организмов Сn(Н2О)m. Углеводы
Сn(Н2О)m. Углеводы Путешествие с комнатными растениями
Путешествие с комнатными растениями Круговорот кислорода в природе
Круговорот кислорода в природе Охорона тварин
Охорона тварин Палеозойская эра
Палеозойская эра Какие бывают растения
Какие бывают растения Внеклассное мероприятие в рамках недели естественных наук КВН, автор учитель биологии Сизова С.В.
Внеклассное мероприятие в рамках недели естественных наук КВН, автор учитель биологии Сизова С.В. Работы Никитина Никиты уч-ся 7 класса
Работы Никитина Никиты уч-ся 7 класса Класс птицы. Птицы как высокоорганизованные представители хордовых животных
Класс птицы. Птицы как высокоорганизованные представители хордовых животных метапредметный подход и проекты в биологии
метапредметный подход и проекты в биологии Узамбарская фиалка
Узамбарская фиалка Удивительное животное. Дельфин
Удивительное животное. Дельфин