Содержание
- 2. Основные понятия биохимии МЕТАБОЛИЗМ (обмен веществ) - совокупность всех химических реакций в клетке. КАТАБОЛИЗМ - распад
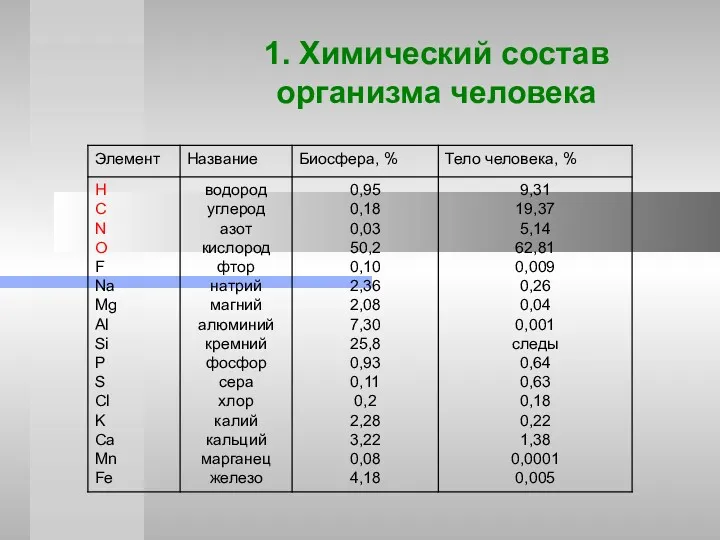
- 3. 1. Химический состав организма человека
- 4. Макробиогенные (выше1%) H,O,C,N Олигобиогенные (от 0,1 до 1%) Ca, P, K, Cl, S, Mg, Fe Микробиогенные
- 5. Структурная организация молекул в клетке Низкомолекулярные и промежуточные Н2О, СО2, Na+,K+, Ca2+,Mg 2+ и др. Органические
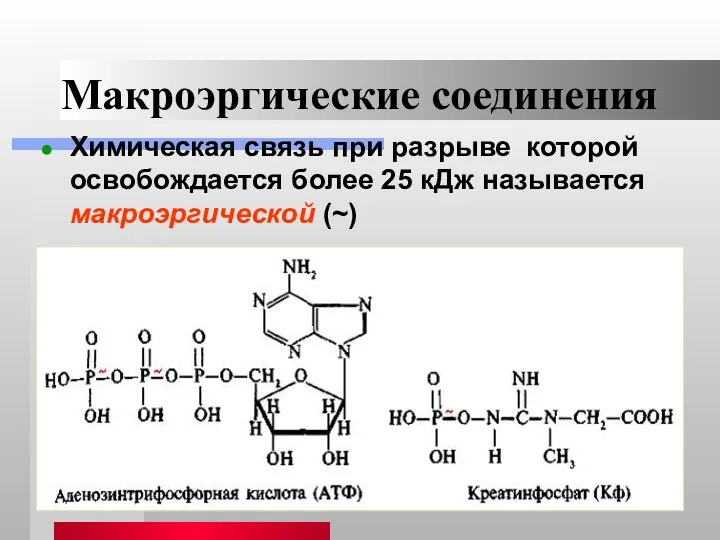
- 6. Макроэргические соединения Химическая связь при разрыве которой освобождается более 25 кДж называется макроэргической (~)
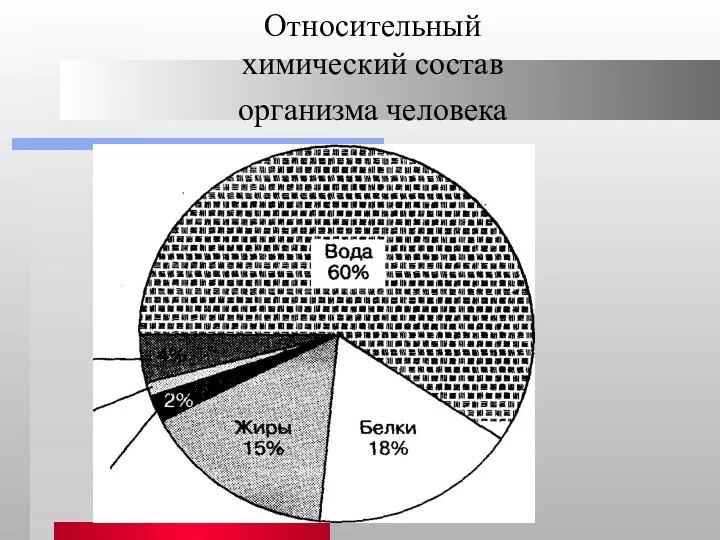
- 7. Относительный химический состав организма человека
- 8. 2. Внутренняя среда организма- вода (Н2О) - универсальный растворитель, - участник химических реакций (гидролиза и др.)
- 9. Свойства водных растворов Диффузия – основной механизм транспорта простых соединений в клетку. скорость = (с1-с2)/ диаметр
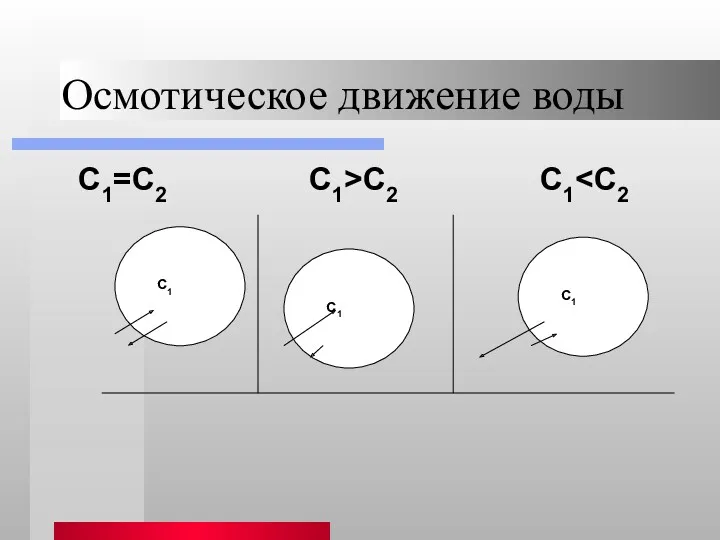
- 10. Осмотическое движение воды С1=С2 С1>С2 С1
- 11. Водородный показатель - рН рН связан с концентрацией ионов водорода: рН = - lg [H+] где
- 12. Буферные системы препятствуют изменению рН Основные буферные системы организма Фосфатный NaH2PO4 + Na2HPO4 Бикарбонатный NaHCO3 +
- 14. Скачать презентацию







 Вода – важный фактор окружающей среды. Значение, состав, свойства воды
Вода – важный фактор окружающей среды. Значение, состав, свойства воды Типы питания живых организмов
Типы питания живых организмов Интересные животные и растения Африки
Интересные животные и растения Африки Обмен веществ и энергии в клетке
Обмен веществ и энергии в клетке Растительный мир Дальнего Востока
Растительный мир Дальнего Востока Қоректік орта құрамындағы фитогормондар және оларды залалсыздандыру
Қоректік орта құрамындағы фитогормондар және оларды залалсыздандыру Водный обмен растений
Водный обмен растений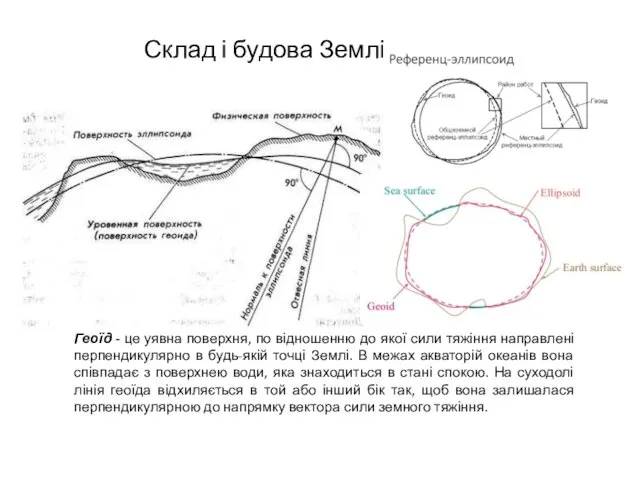 Склад і будова Землі. Лекція 2
Склад і будова Землі. Лекція 2 Біологічні основи поведінки
Біологічні основи поведінки Биологияны оқытуда жүргізілетін оқу – тәрбие жұмыстары
Биологияны оқытуда жүргізілетін оқу – тәрбие жұмыстары Хищники
Хищники Физиология и экология диатомовых водорослей
Физиология и экология диатомовых водорослей Физиология пищеварения
Физиология пищеварения Луг и его обитатели. Насекомые и животные
Луг и его обитатели. Насекомые и животные Биотические факторы среды
Биотические факторы среды Мінливість. Типи мінливості. Мутації і модифікації. Тема 7
Мінливість. Типи мінливості. Мутації і модифікації. Тема 7 Педагогика 21 века на пороге школы.
Педагогика 21 века на пороге школы. Glycolysis. Splitting glucose to jumpstart cellular respiration
Glycolysis. Splitting glucose to jumpstart cellular respiration презентация с аннимациями образование биоценоза Диск
презентация с аннимациями образование биоценоза Диск Состав и строение клеток
Состав и строение клеток Трансгенді ағзалар
Трансгенді ағзалар Оценка качества воздуха Удельного парка с помощью лихеноиндикации
Оценка качества воздуха Удельного парка с помощью лихеноиндикации Обмен веществ. Витамины
Обмен веществ. Витамины Почвоведение, как научная дисциплина
Почвоведение, как научная дисциплина Презентация к обобщающему уроку биологии по теме Развитие органического мира
Презентация к обобщающему уроку биологии по теме Развитие органического мира Половое размножение цветковых растений
Половое размножение цветковых растений Репликация ДНК. Элонгация репликации ДНК. (Лекция 4)
Репликация ДНК. Элонгация репликации ДНК. (Лекция 4) Иммобилизация ферментов
Иммобилизация ферментов