Слайд 2

Свойства ферментов. Сходство с неорганическими катализаторами
1. Повышают скорость химической реакции.
2. Не
сдвигают равновесие химической реакции.
3. Снижают энергию активации.
Слайд 3

Отличия от неорганических катализаторов
1. Ферменты обладают намного большей активностью.
2. Неорганические катализаторы
активны в очень жестких условиях, а ферменты работают в мягких условиях: t тела, атмосферное давление, нейтральное значение pH.
3. Ферменты обладают строгой специфичностью.
Слайд 4

Активность ферментов и неорганических катализиторов
Слайд 5

Виды специфичности ферментов
1. Абсолютная (индивидуальная).
2. Групповая (относительная).
3. Стереохимическая (оптическая: D-, L-;
геометрическая: цис-, транс-)
Слайд 6
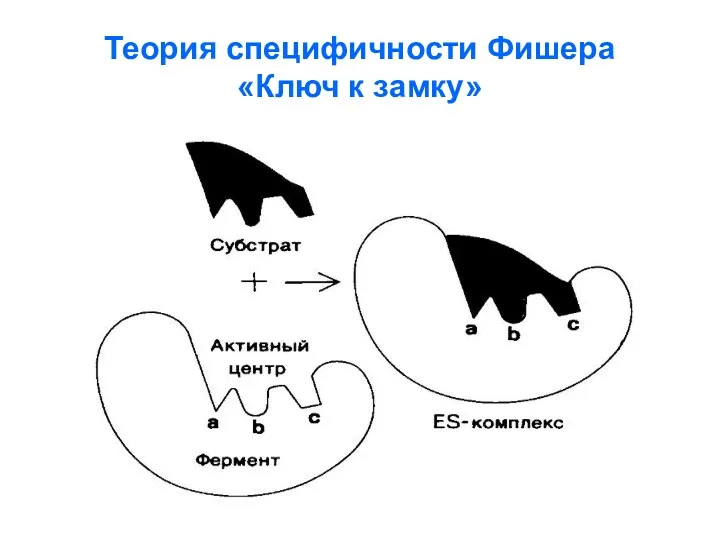
Теория специфичности Фишера
«Ключ к замку»
Слайд 7
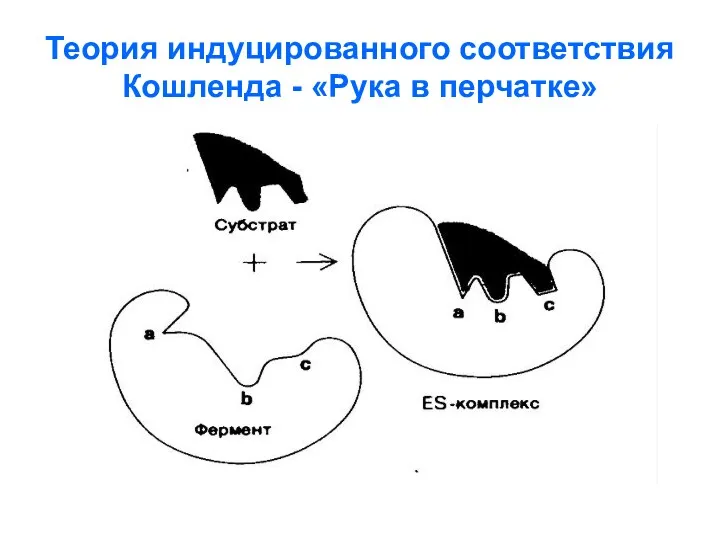
Теория индуцированного соответствия
Кошленда - «Рука в перчатке»
Слайд 8
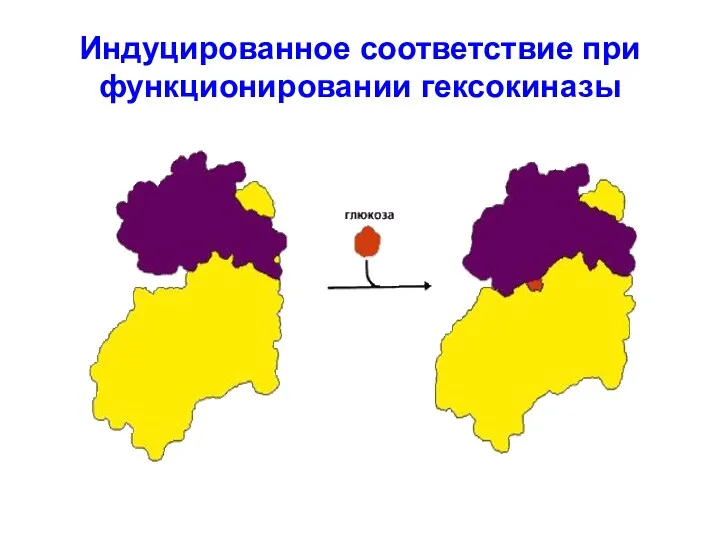
Индуцированное соответствие при функционировании гексокиназы
Слайд 9
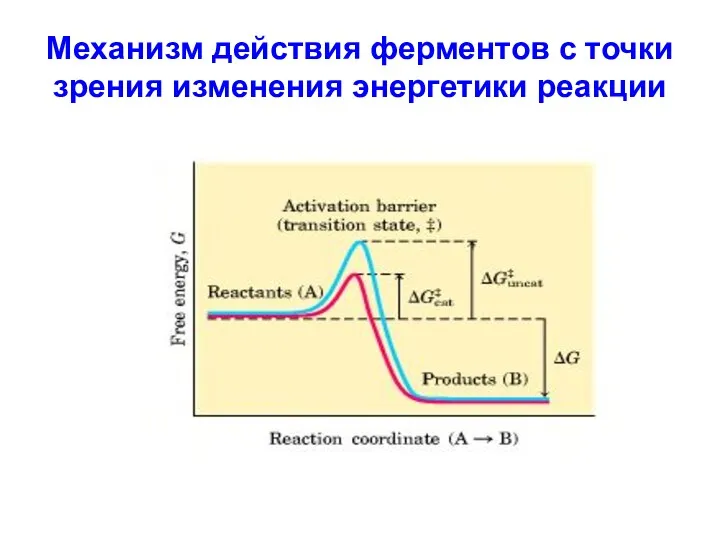
Механизм действия ферментов с точки зрения изменения энергетики реакции
Слайд 10
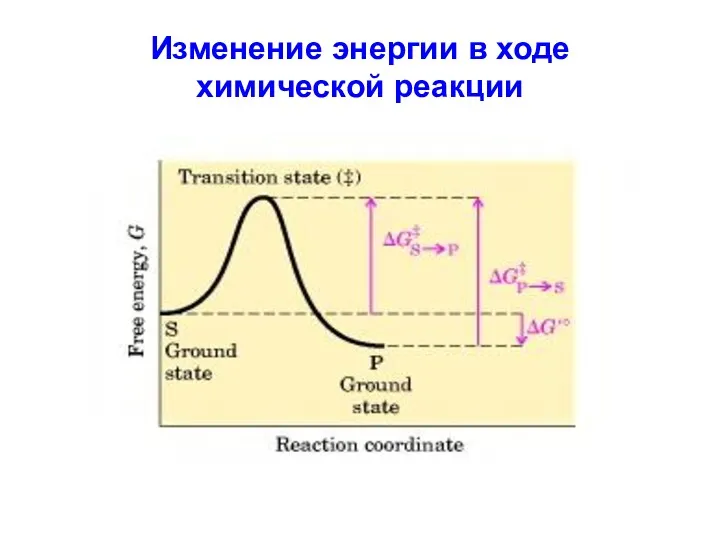
Изменение энергии в ходе
химической реакции
Слайд 11
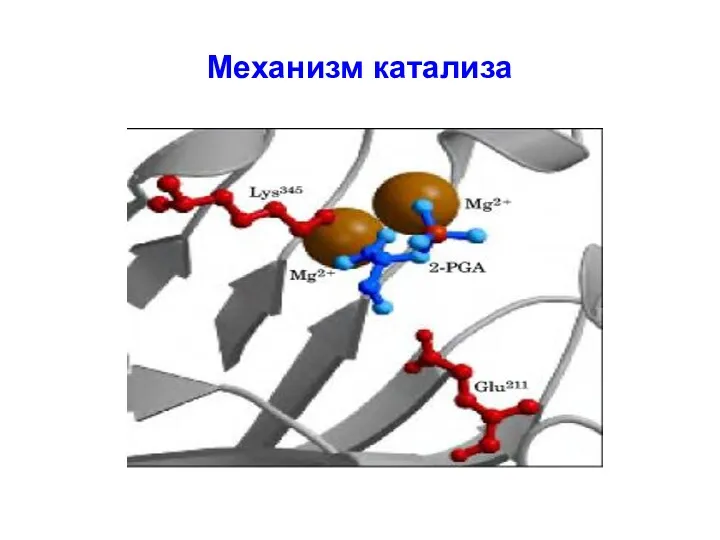
Слайд 12
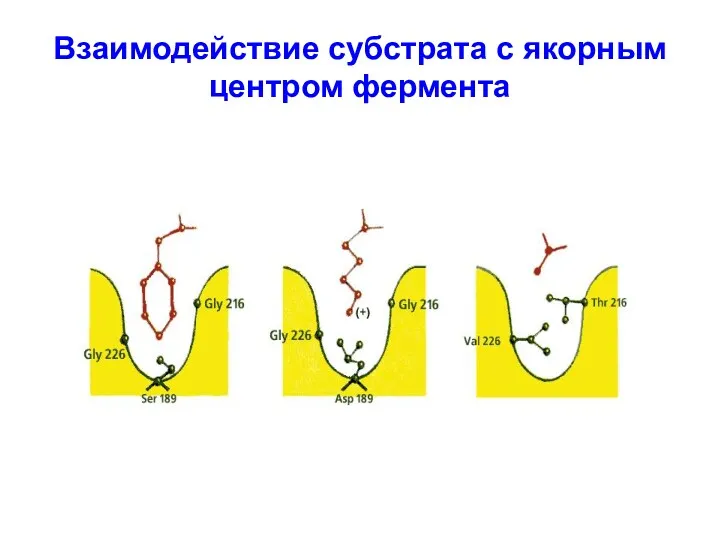
Взаимодействие субстрата с якорным центром фермента
Слайд 13
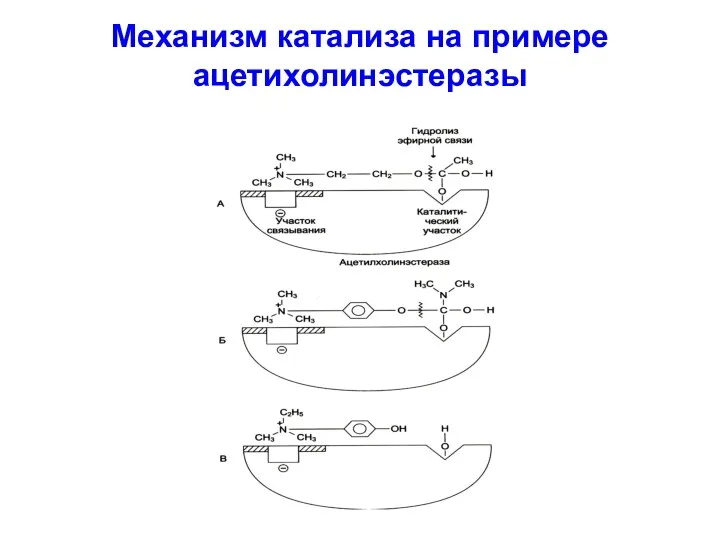
Механизм катализа на примере
ацетихолинэстеразы
Слайд 14
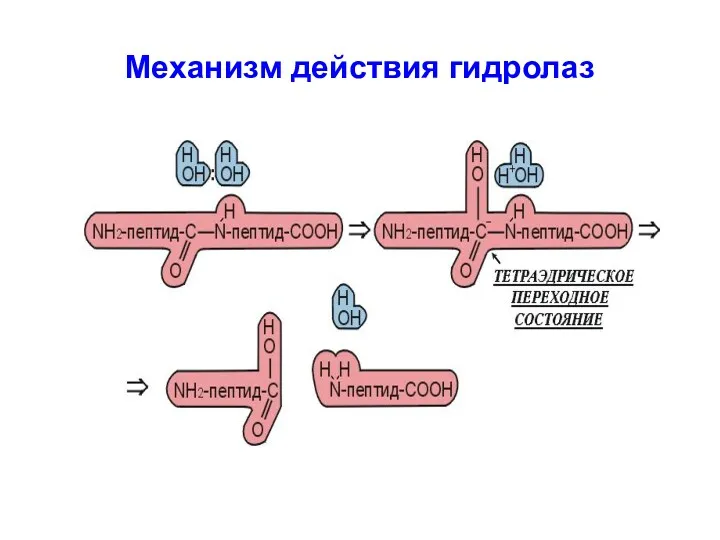
Механизм действия гидролаз
Слайд 15
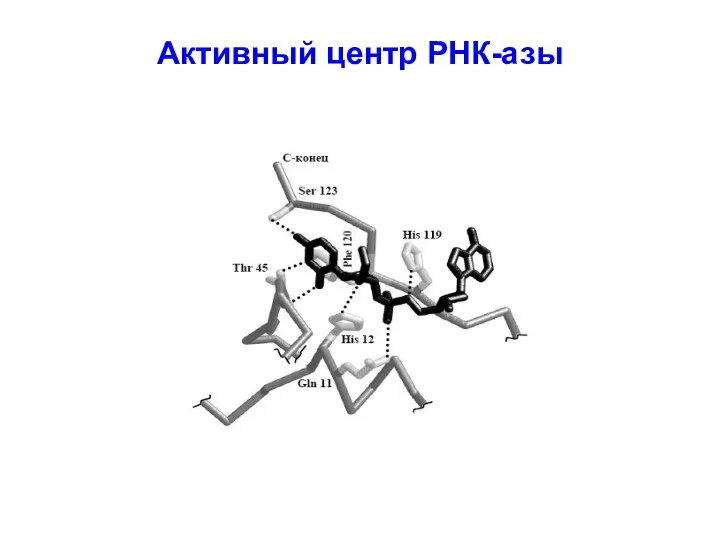
Слайд 16
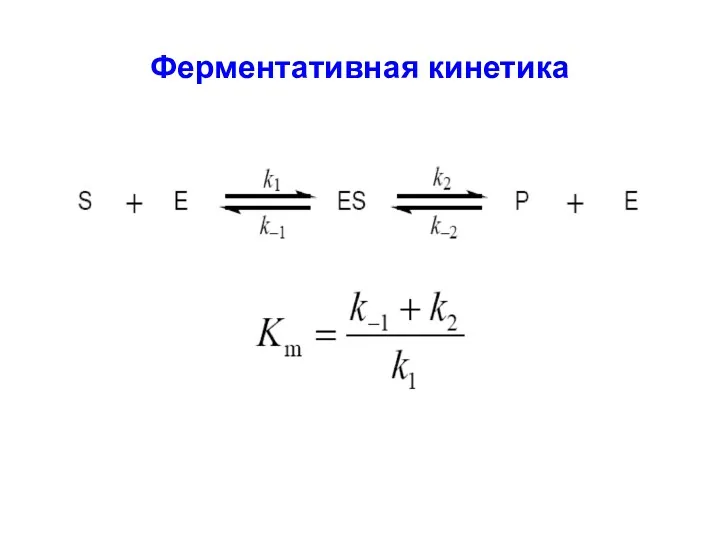
Слайд 17
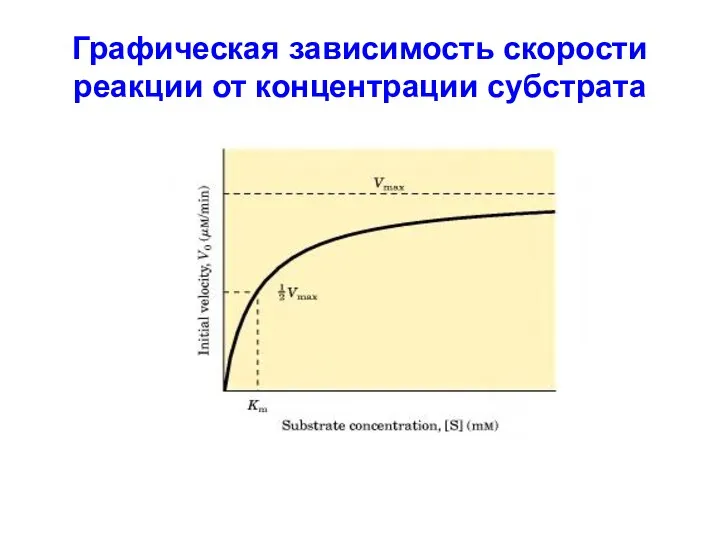
Графическая зависимость скорости реакции от концентрации субстрата
Слайд 18
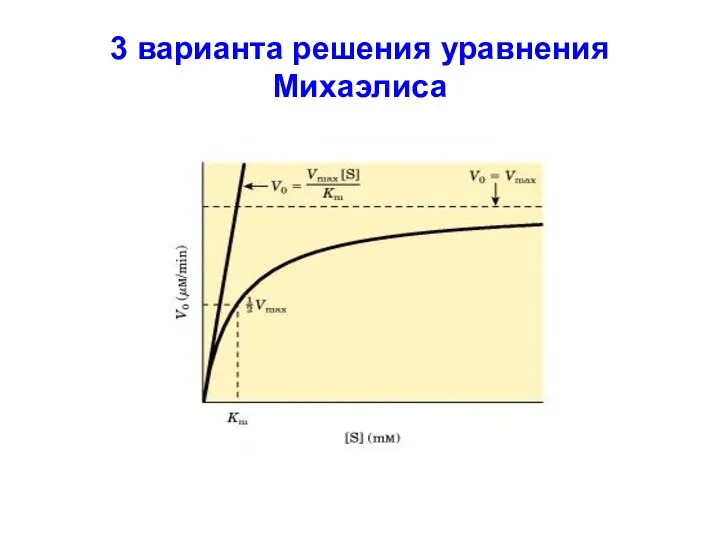
3 варианта решения уравнения Михаэлиса
Слайд 19
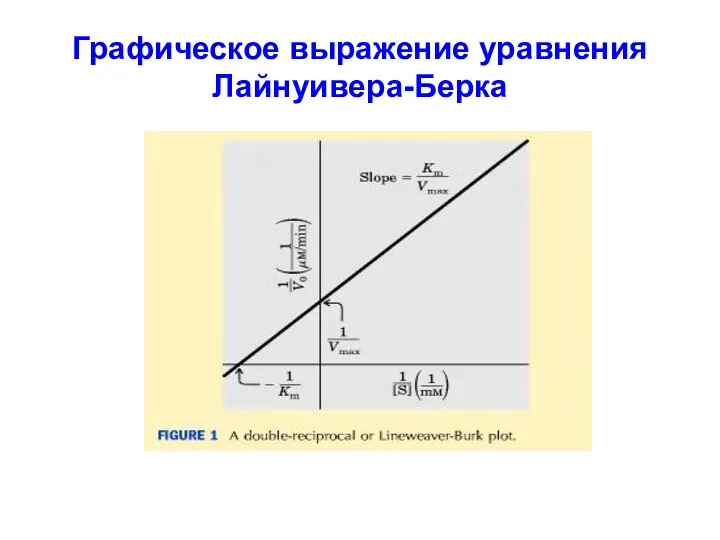
Графическое выражение уравнения Лайнуивера-Берка
Слайд 20
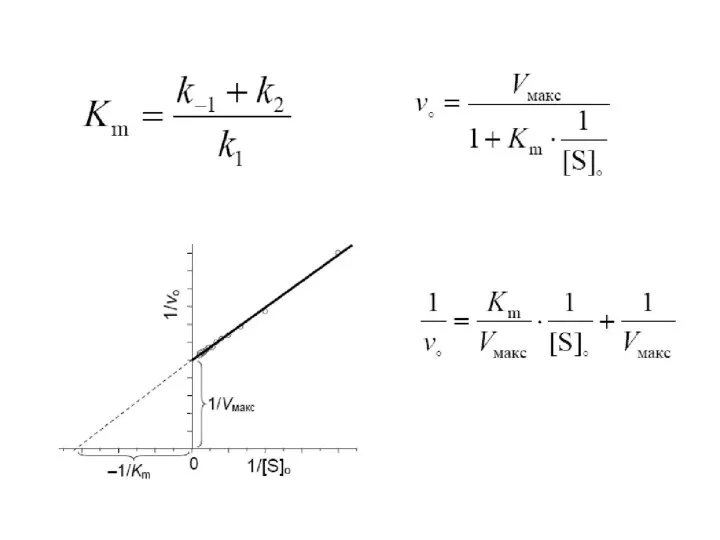
Слайд 21
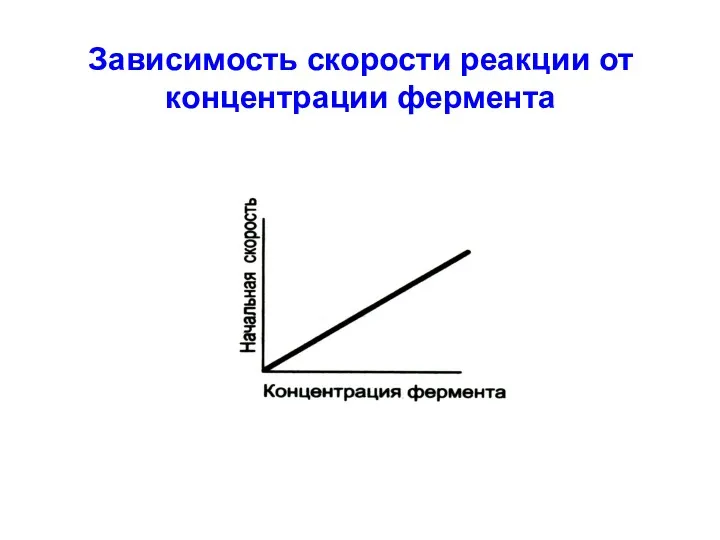
Зависимость скорости реакции от концентрации фермента
Слайд 22
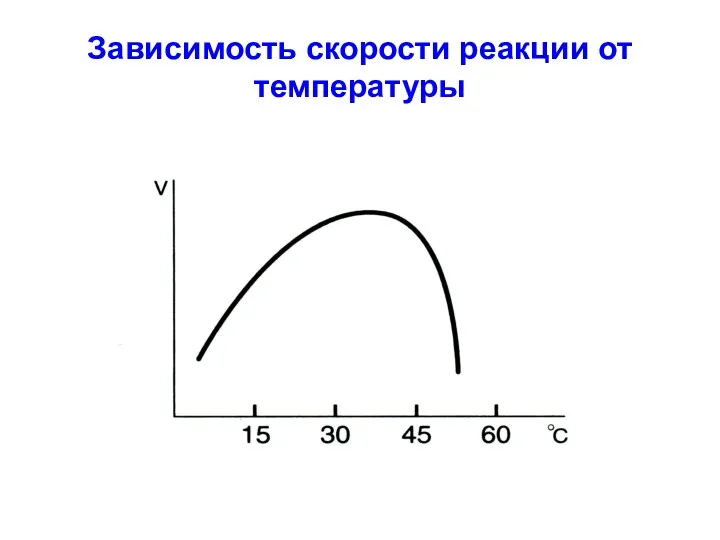
Зависимость скорости реакции от температуры
Слайд 23
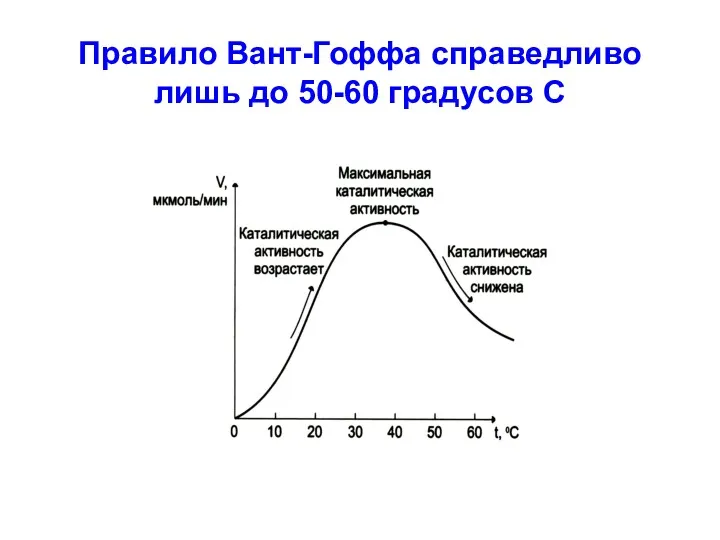
Правило Вант-Гоффа справедливо лишь до 50-60 градусов С
Слайд 24
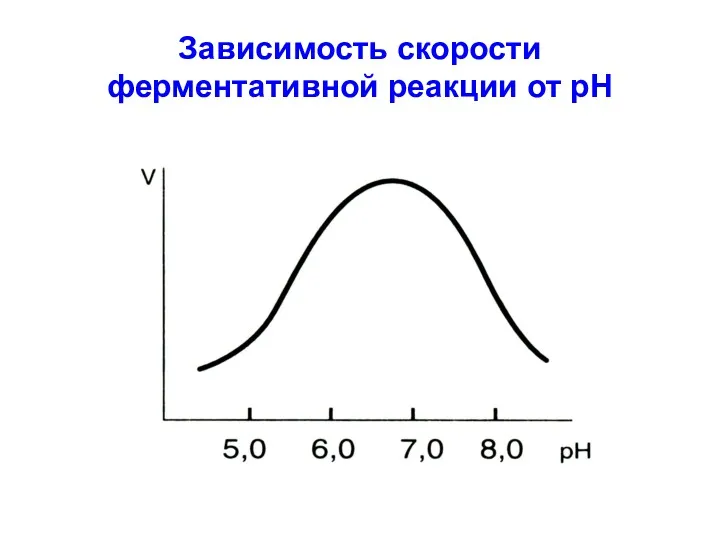
Зависимость скорости ферментативной реакции от рН
Слайд 25
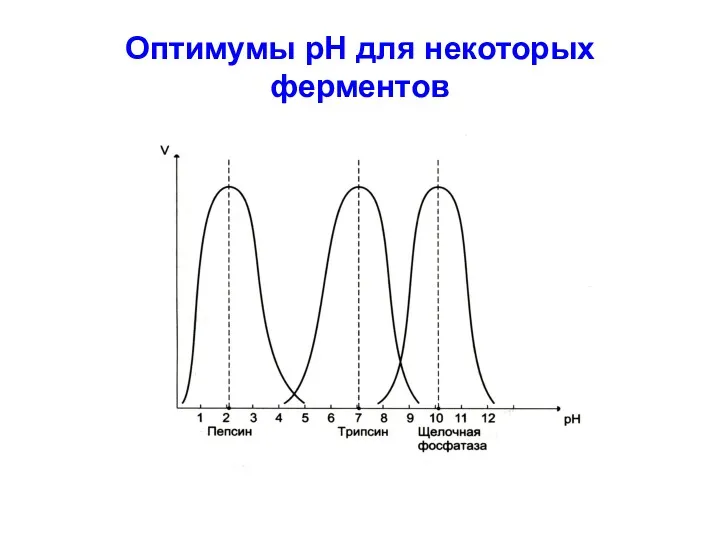
Оптимумы рН для некоторых ферментов
























 Онтоногенез — это индивидуальное развитие организма
Онтоногенез — это индивидуальное развитие организма Поверхневі структури бактерій
Поверхневі структури бактерій Омыртқалы және омыртқасыз жануарлардың тыныс алуы
Омыртқалы және омыртқасыз жануарлардың тыныс алуы Генетические аспекты селекции микроорганизмов
Генетические аспекты селекции микроорганизмов Учение об иммунитете
Учение об иммунитете Белки, жиры, углеводы
Белки, жиры, углеводы Скелет туловища. Позвоночный столб. Лекция № 9
Скелет туловища. Позвоночный столб. Лекция № 9 Бактериофаги
Бактериофаги Ашық тұқымдылар немесе Қарағайлар бөлімі (Gymnospermatophyta Pinophyta)
Ашық тұқымдылар немесе Қарағайлар бөлімі (Gymnospermatophyta Pinophyta) Плотоядные растения
Плотоядные растения Қосмекенділер немесе Амфибиялар
Қосмекенділер немесе Амфибиялар Отдел голосеменные. ОГЭ
Отдел голосеменные. ОГЭ Ялівець звичайний. 6 клас
Ялівець звичайний. 6 клас Қалқаншамаңы бездері,тимус(айырша без) және бүйрек үсті бездері
Қалқаншамаңы бездері,тимус(айырша без) және бүйрек үсті бездері Общая характеристика царства Растения
Общая характеристика царства Растения Домашние животные
Домашние животные Физиологические основы ПФИ: кожа человека
Физиологические основы ПФИ: кожа человека Состав белка. Нуклеиновые кислоты
Состав белка. Нуклеиновые кислоты Значение воды в жизни растений
Значение воды в жизни растений Отряд акулы
Отряд акулы Фармацевтична ботаніка. Аналіз буклету 2015 року
Фармацевтична ботаніка. Аналіз буклету 2015 року Мужская половая система
Мужская половая система презентация Интеллектуальный марафон
презентация Интеллектуальный марафон Общие принципы анатомического строения и закономерности регуляции функциональных систем организма
Общие принципы анатомического строения и закономерности регуляции функциональных систем организма Загадки о животных (1 класс)
Загадки о животных (1 класс) Ткани из растений. Классификация волокон
Ткани из растений. Классификация волокон Биология в схемах и таблицах
Биология в схемах и таблицах Получение кормовой добавки на основе выжимок томатов и рисовой мучки
Получение кормовой добавки на основе выжимок томатов и рисовой мучки