Содержание
- 2. Химический элемент Углерод — химический элемент, символизируемый буквой C и имеющий атомный номер 6. Элемент является
- 3. Признание элемента На рубеже XVII—XVIII вв. возникла теория флогистона, подразумевавшая наличие в каждом горючем теле особого
- 4. Разнообразие Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими свойствами за счет способности образовывать
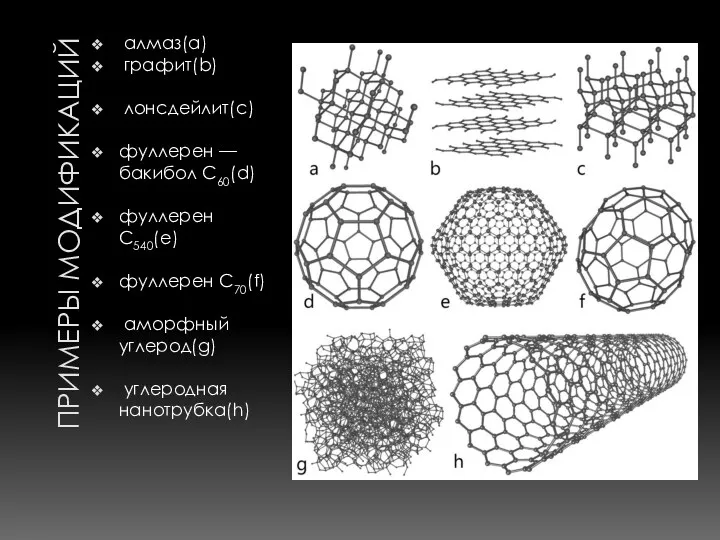
- 5. ПРИМЕРЫ МОДИФИКАЦИЙ алмаз(a) графит(b) лонсдейлит(c) фуллерен — бакибол C60(d) фуллерен C540(e) фуллерен C70(f) аморфный углерод(g) углеродная
- 6. Углерод в природе Свободный углерод находится в природе в виде алмаза и графита. Основная масса углерода
- 7. Органика Способность углерода образовывать полимерные цепочки порождает огромный класс соединений на основе углерода, которых значительно больше,
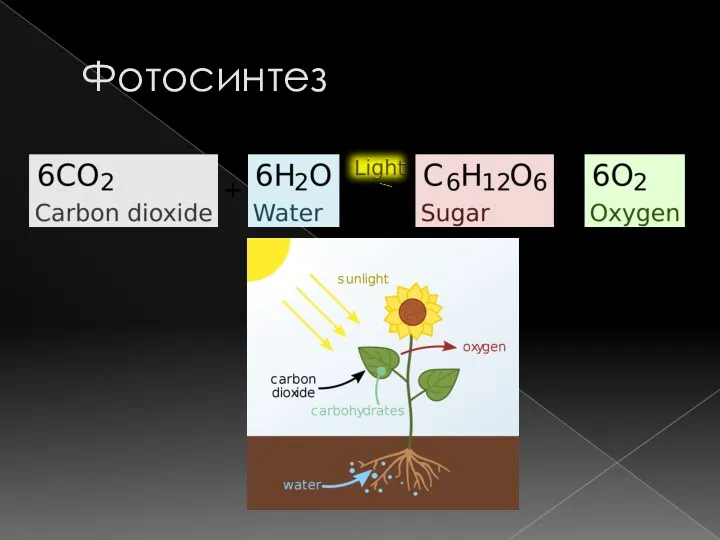
- 8. Фотосинтез
- 10. Скачать презентацию





 Чудесное превращение. Появление комара
Чудесное превращение. Появление комара Цели, задачи и методы науки селекции
Цели, задачи и методы науки селекции Север - богатый край.
Север - богатый край. Акселерация және ретардация реактивтілік және организмнің резистенттілігі
Акселерация және ретардация реактивтілік және организмнің резистенттілігі Рыбы. Внутреннее строение
Рыбы. Внутреннее строение Загальна характеристика біосфери. Вчення Вернадського про біосферу. Роль живих організмів у біосфері. Біомаса
Загальна характеристика біосфери. Вчення Вернадського про біосферу. Роль живих організмів у біосфері. Біомаса Презентация Дигибридное скрещивание. Третий закон Менделя.
Презентация Дигибридное скрещивание. Третий закон Менделя. Кожа и её производные
Кожа и её производные Отдел Моховидные. Общая характеристика, значение
Отдел Моховидные. Общая характеристика, значение Презентация Значение калия в организме
Презентация Значение калия в организме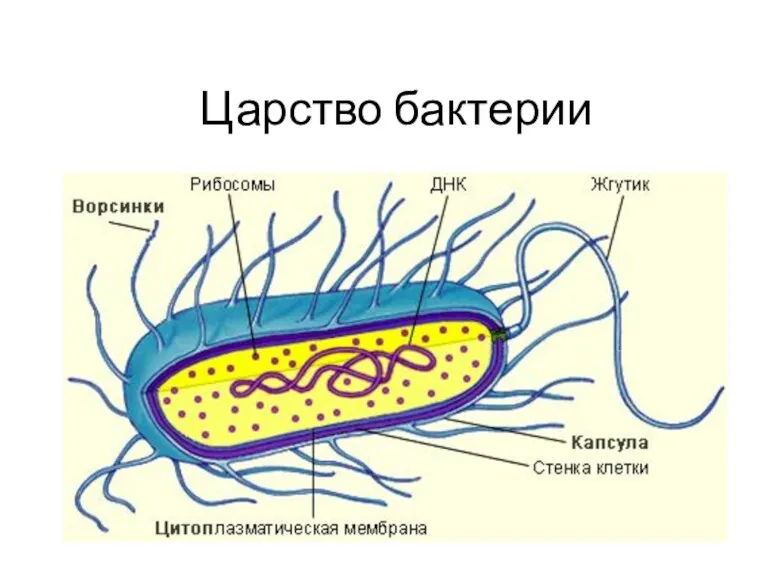 Царство Бактерии. 6 класс
Царство Бактерии. 6 класс презентация Цветок
презентация Цветок Пищевая микробиология. Превращения азотсодержащих веществ
Пищевая микробиология. Превращения азотсодержащих веществ Экология и природопользование. Экосистемы
Экология и природопользование. Экосистемы Кожа. Наружный покров
Кожа. Наружный покров ВИДЫ ВЕГЕТАТИВНОГО РАЗМНОЖЕНИЯ РАСТЕНИИ
ВИДЫ ВЕГЕТАТИВНОГО РАЗМНОЖЕНИЯ РАСТЕНИИ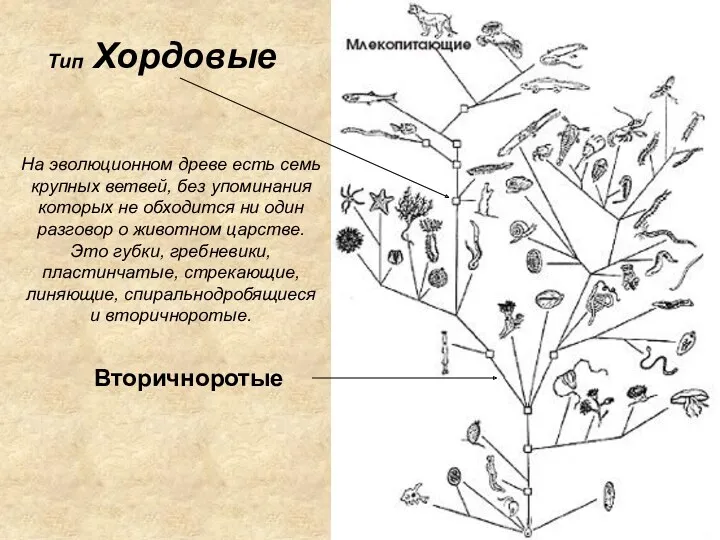 Тип Хордовые
Тип Хордовые Какие бывают животные? Окружающий мир. 2 класс
Какие бывают животные? Окружающий мир. 2 класс Вегетативное размножение растений
Вегетативное размножение растений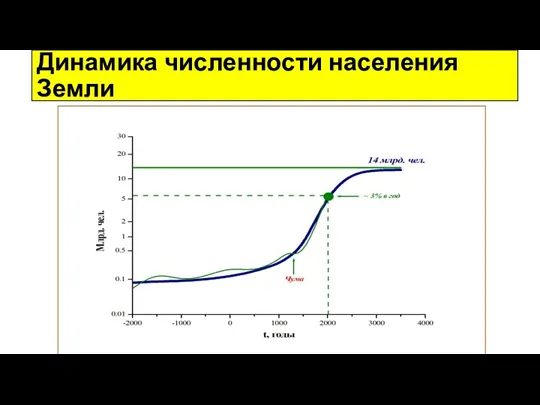 Динамика численности населения Земли
Динамика численности населения Земли Осторожно, борщевик!
Осторожно, борщевик! Среды обитания организмов
Среды обитания организмов Малина звичайна
Малина звичайна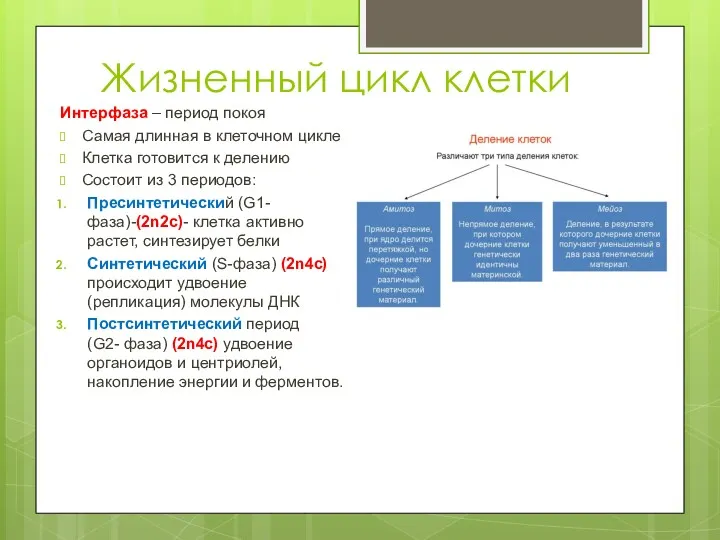 Жизненный цикл клетки
Жизненный цикл клетки Болотные птицы
Болотные птицы Общая характеристика грибов. Многообразие
Общая характеристика грибов. Многообразие Растения болот
Растения болот Международная классификация микроорганизмов по Берги
Международная классификация микроорганизмов по Берги