Содержание
- 2. Статистический характер необратимых процессов. Все естественно происходящие тепловые процессы – необратимы. При переходе в состояние т.д.
- 3. беспорядочном движении. Она может покинуть этот объем и оказаться в любом из пяти объемов, но может
- 4. А если взять большое число N молекул : - и процесс становится практически не обратимым, так
- 5. Таким образом, сам собой происходит переход к равно- весному состоянию, вероятность которого велика. Обратный переход к
- 6. Состояние, описанное таким образом, называется микросостоянием. При этом всякое перемещение молекул внутри ячейки не меняет микросостояние,
- 7. Мы условились считать макроскопическим состоянием число молекул в одной половине сосуда. Тогда окажутся возможными 5 различных
- 8. В каждой строке цифры слева и справа указывают номера молекул, размещенных соответственно в левой и в
- 9. макросостояния микросостояния
- 10. Можно видеть, что макросостояние, при котором все молекулы соберутся в одной половине сосуда существенно менее вероятно,
- 11. Ситуация при числе молекул 24 Ω математическая 224
- 12. Из таблиц видно, что наибольшее число способов раз- мещения соответствует состоянию, где слева и справа одинаковое
- 13. Легко убедиться, что при любом N: при , то есть система находится в равновесном состоянии. Термодинамическая
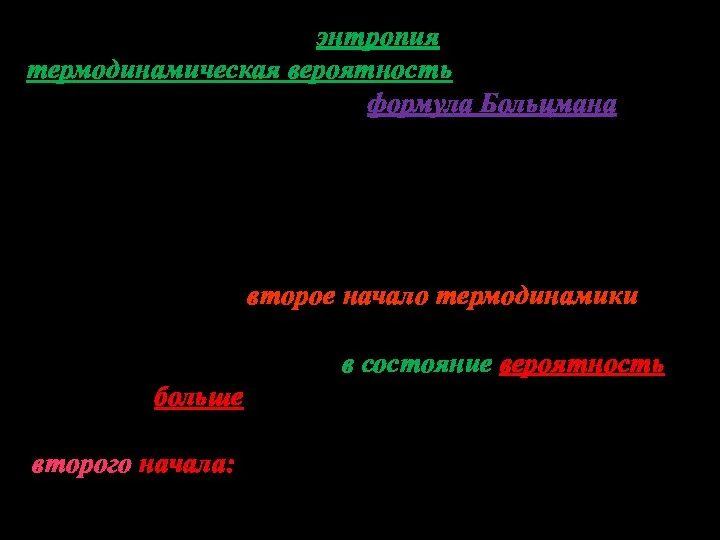
- 14. Формула Больцмана для энтропии Мы ввели понятие энтропии через приведенную теплоту. Посмотрим на энтропию с другой
- 15. Использовать статистический вес Ω в качестве величины, определяющей вероятность состояния, не- удобно, так как он неаддитивен
- 16. Согласно Больцману, энтропия системы и термодинамическая вероятность связаны между собой следующим образом (формула Больцмана): где k
- 17. Если система находится в каком-либо состоянии с данной энтропией, , то с подавляющей вероятностью следует ожидать,
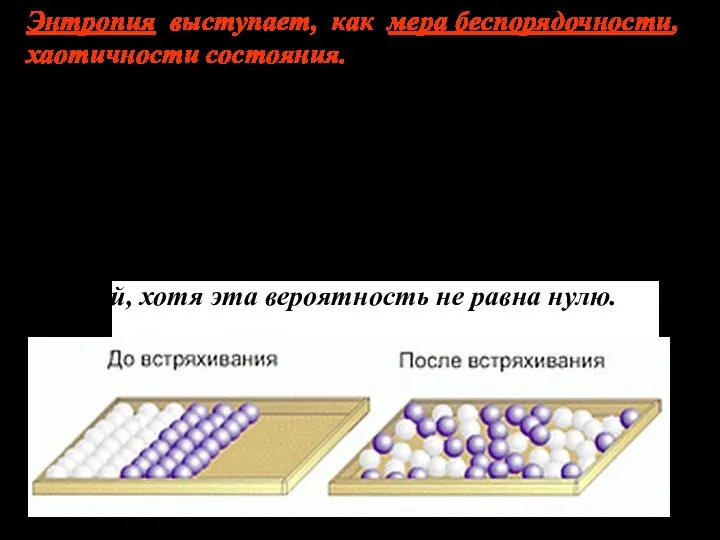
- 18. Статистический характер закона возрастания энтропии. Флуктуации. Второе начало термодинамики есть статисти-ческий закон, согласно которому отступления от
- 19. Например, в ящике сиреневые и белые шары. Они порознь, есть порядок и Ω невелика. После встряхивания
- 20. Клаузиус в 1867 г. выдвинул гипотезу о тепловой смерти Вселенной, согласно которой Вселенная рассматривается как замкнутая
- 21. Рассмотрим поведение энтропии при Т → 0 При стремлении температуры к абсолютному нулю ( Т= 0
- 22. Принцип Нернста был развит Планком, предположившим, что при абсолютном нуле температуры энергия системы минимальна и она
- 23. Основные свойства энтропии: 1. Энтропия является функцией состояния. 2. Для вычисления энтропии системы в данном состоянии
- 24. 5. Максимальное значение энтропии соответвует равновесному состоянию. 6. Энтропия непосредственно связана с вероятностью. Возрастание энтропии системы
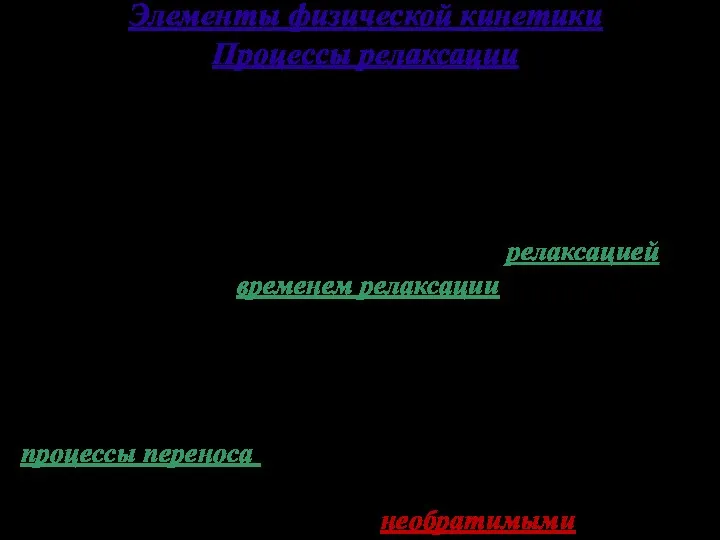
- 25. Элементы физической кинетики Процессы релаксации Если система не находится в термодинамическом равновесии, то она стремится к
- 26. Раздел физики, изучающий эти процессы, называется физической кинетикой. Для полного описания этих процессов необходимо учитывать большое
- 27. Роль столкновений. Газокинетический диаметр молекул. Средняя длина свободного пробега. Средняя скорость теплового движения молекул : Если
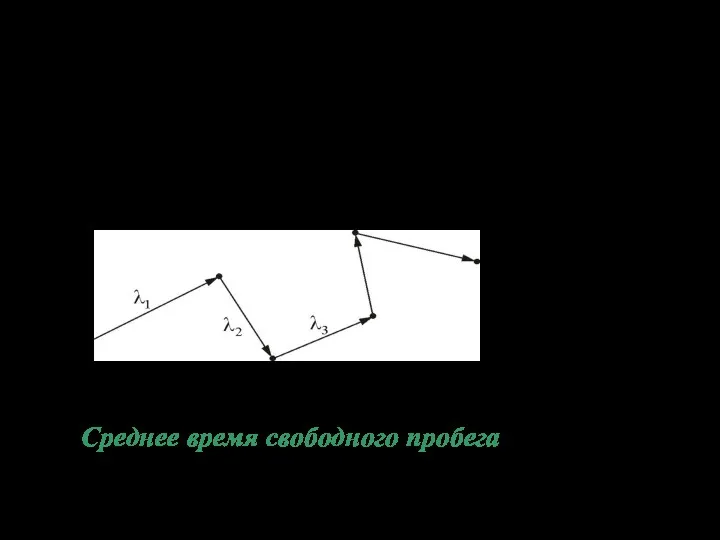
- 28. Свободно молекула пролетает короткое расстояние до следующего столкновения. В момент столкновения скорость молекулы испытывает резкое изменение
- 29. 2. Среднюю длину свободного пробега - среднее расстояние, которое пролетает молекула между соседними столкновениями. В данном
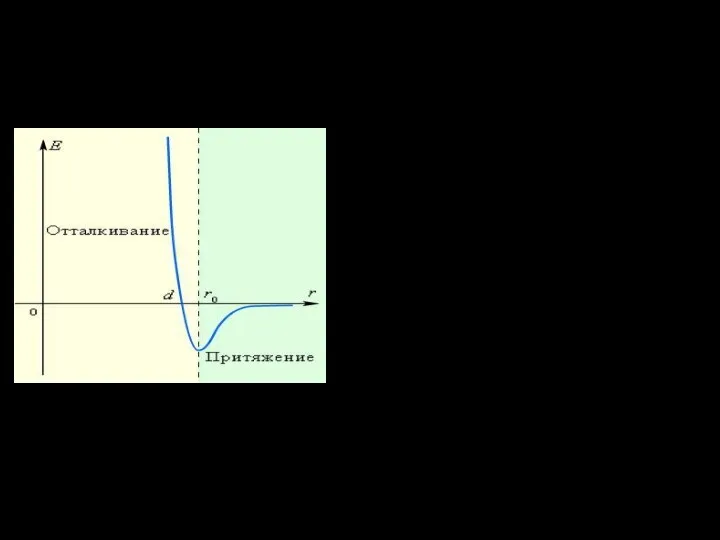
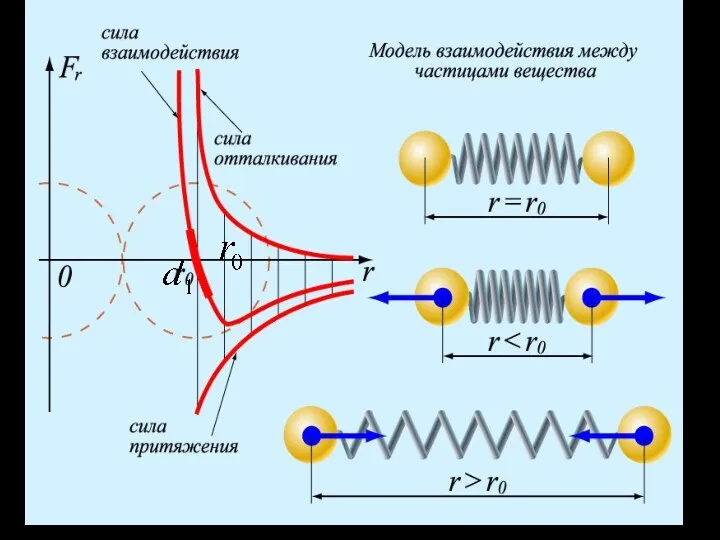
- 30. Рассмотрим взаимодействие двух молекул. Зависи-мость их потенциальной энергии Е от расстояния r между ними представлена на
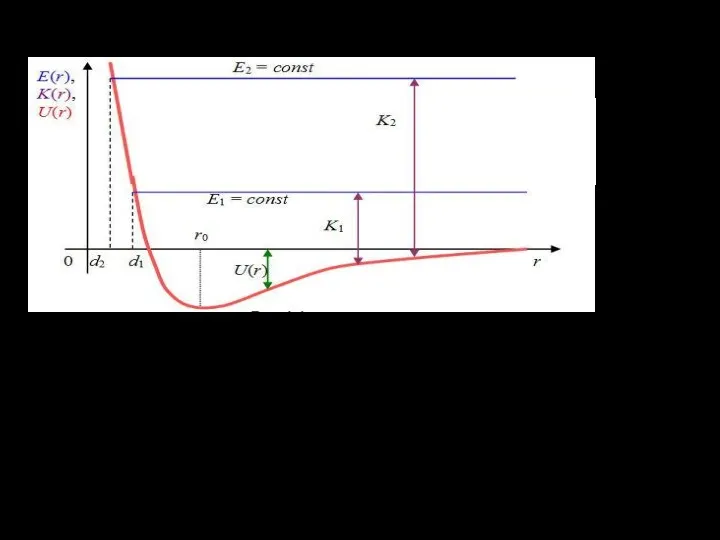
- 32. Пусть E - энергия системы при r = ∞ Закон сохранения энергии Е = К+U, где
- 33. Минимальное расстояние d, на которое сближаются центры двух молекул, называется эффективным (или газокинетическим) диаметром молекулы. Из
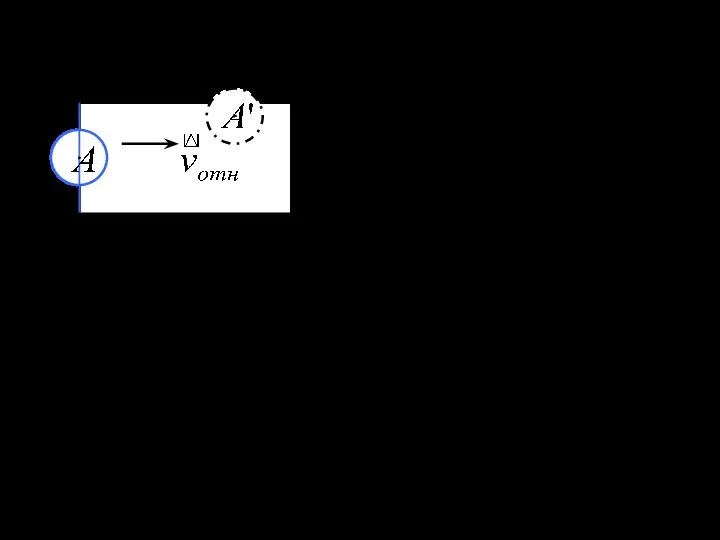
- 34. Модель твердых шаров. Молекула А движется со средней относительной скоростью по Отношению к молекуле . Мысленно
- 35. Можно показать, что . Тогда Если происходит одно столкновение (N=1 и ) Средняя длина свободного пробега
- 36. Из основного уравнения МКТ: , подставим в Число столкновений одной молекулы за 1 секунду: Полное число
- 38. Скачать презентацию



























 ВКР: Ручное изготовление изделия из группы сервировки стола с использованием традиционных материалов
ВКР: Ручное изготовление изделия из группы сервировки стола с использованием традиционных материалов Улаштування та технічне обслуговування паливного насосу високого тиску. ТО системи живлення дизельного двигуна (4)
Улаштування та технічне обслуговування паливного насосу високого тиску. ТО системи живлення дизельного двигуна (4) Растяжение и сжатие
Растяжение и сжатие Закон электромагнитной индукции
Закон электромагнитной индукции Влияние механических и тепловых воздействий на механические свойства материалов (прочность и пластичность)
Влияние механических и тепловых воздействий на механические свойства материалов (прочность и пластичность) Общие сведения о двигателях внутреннего сгорания
Общие сведения о двигателях внутреннего сгорания Шкала электромагнитных излучений
Шкала электромагнитных излучений Излучение и спектры (презентация)
Излучение и спектры (презентация) Компания Volat
Компания Volat Технологический процесс изготовления детали Соединительная втулка
Технологический процесс изготовления детали Соединительная втулка Полярне сяйво
Полярне сяйво Сила трения
Сила трения Реактивное движение. Ракеты
Реактивное движение. Ракеты Знакомство с энциклопедией атомной отрасли
Знакомство с энциклопедией атомной отрасли Приборы вакуумной электроники
Приборы вакуумной электроники Бесступенчатая коробка передач
Бесступенчатая коробка передач Механизмы управления. Рулевое управление
Механизмы управления. Рулевое управление Разработка урока физики в 7 классе по теме Строение твердых тел, жидкостей и газов
Разработка урока физики в 7 классе по теме Строение твердых тел, жидкостей и газов Плавление и отвердевание кристаллических тел. Удельная теплота плавления
Плавление и отвердевание кристаллических тел. Удельная теплота плавления Основы технической механики. Основы статики. Урок 1
Основы технической механики. Основы статики. Урок 1 Корпусные детали, смазочные и уплотняющие устройства
Корпусные детали, смазочные и уплотняющие устройства Электромагнетизм. Электр және магнит өрістері
Электромагнетизм. Электр және магнит өрістері Қозғалыс материяның ажырамас қасиеті. Материалдық нүкте. Санақ жүйесі. Салыстырмалы механикалық қозғалыс
Қозғалыс материяның ажырамас қасиеті. Материалдық нүкте. Санақ жүйесі. Салыстырмалы механикалық қозғалыс презентация физика 8 классРабота и мощность
презентация физика 8 классРабота и мощность Организация дистанционной формы обучения физике 7-9 классов обучащихся с ОВЗ
Организация дистанционной формы обучения физике 7-9 классов обучащихся с ОВЗ Механические свойства горных пород и массивов. Тема 6. Лекция № 9
Механические свойства горных пород и массивов. Тема 6. Лекция № 9 Механизмы поворота. Устройство и расчет. (Лекция № 5)
Механизмы поворота. Устройство и расчет. (Лекция № 5) Проблемное обучение в преподавании физики
Проблемное обучение в преподавании физики