Слайд 2

Давление, объем и температура являются основными параметрами состояния газа. Всякое изменение
состояния газа называется термодинамическим процессом. Термодинамические процессы, протекающие в газе постоянной массы при неизменном значении одного из параметров состояния газа, называются изопроцессами. И эти изопроцессы подчиняются газовым законам.
Слайд 3

Газовые законы определяют количественные зависимости между двумя параметрами газа при неизменном
значении третьего. Справедливы эти законы для любых газов и газовых смесей.
Слайд 4

Изопроцессы
Изотермический процесс
Изобарный процесс
Изохорный процесс
Слайд 5

Изотермический процесс
Изменения состояния газа, протекающие при постоянной температуре, называются изотермическим процессом.
Слайд 6

Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой
с большой системой – термостатом. Иначе температура газа будет меняться. Термостатом может служить атмосферный воздух, если температура его заметно не меняется на протяжении всего процесса. Для поддержания теплообмена процесс должен протекать медленно.
Слайд 7

Закон Бойля-Мариотта
Для газа данной массы произведение давления газа на его
объем постоянно, если температура газа не меняется.
Слайд 8

Графическое представление изотермического процесса:
График, отражающий изотермический процесс, называется изотермой. (математически
– это гипербола)
Слайд 9

Изохорный процесс
Процесс изменения состояния термодинамической системы макроскопических тел при постоянном объеме
называют изохорным.
Слайд 10

Закон Шарля
Для газа данной массы отношение давления газа к его температуре
постоянно, если объем газа не меняется.
Слайд 11

Графическое представление изохорного процесса:
График, отражающий изохорный процесс, называется изохорой.
(математически
– это линейная зависимость)
Слайд 12

Изобарный процесс
Изобарным процессом называются изменения состояния газа, протекающие при постоянном давлении.
Слайд 13

Давление газа зависит от числа ударов молекул о стенки сосуда.
При
повышении температуры скорость
движения молекул увеличивается, число ударов молекул о стенки сосуда увеличивается, и, следовательно, давление повышается.
При понижении температуры скорость
движения молекул уменьшается, число ударов молекул о стенки сосуда уменьшается, и, следовательно, давление понижается.
Слайд 14

Закон Гей – Люссака
Для данной массы газа при постоянном давлении
отношение объема газа к его температуре постоянно.













 Тепловые явления. Тепловое движение. Температура
Тепловые явления. Тепловое движение. Температура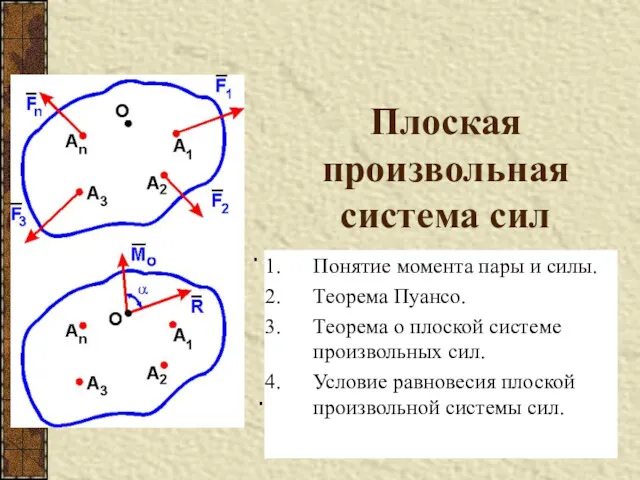 Плоская произвольная система сил
Плоская произвольная система сил Хроматографические методы. (Часть 2)
Хроматографические методы. (Часть 2) Атом. Состав атомного ядра
Атом. Состав атомного ядра Электромагнетизм. Электр және магнит өрістері
Электромагнетизм. Электр және магнит өрістері Гравитационное притяжение эллипсоидов
Гравитационное притяжение эллипсоидов Бытовая швейная машина. Первая машина с челночным механизмом
Бытовая швейная машина. Первая машина с челночным механизмом Детали Машин. Виды механизмов
Детали Машин. Виды механизмов История телескопов. Современные телескопы
История телескопов. Современные телескопы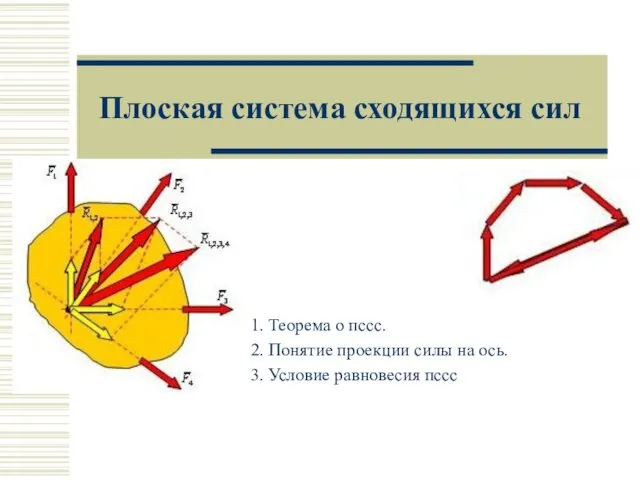 Плоская система сходящихся сил
Плоская система сходящихся сил Тепловое излучение тел
Тепловое излучение тел Продуктивність та виробіток машинно-тракторних агрегатів
Продуктивність та виробіток машинно-тракторних агрегатів Қозғалтқыш жалпы түсінік. Қозғалтқыштың құрылысы
Қозғалтқыш жалпы түсінік. Қозғалтқыштың құрылысы Последовательное и параллельное соединения проводников. Урок 37
Последовательное и параллельное соединения проводников. Урок 37 Физические основы радиоактивности
Физические основы радиоактивности Диэлектрики
Диэлектрики Законы постоянного тока
Законы постоянного тока Механические характеристики производственных механизмов
Механические характеристики производственных механизмов Автоматические коробки переключения передач
Автоматические коробки переключения передач Технологический процесс ремонта КПП М16А автомобиля Suzuki Liana
Технологический процесс ремонта КПП М16А автомобиля Suzuki Liana Архимедова сила
Архимедова сила Напряженность магнитного поля
Напряженность магнитного поля Изменение энергии нейтронов при рассеянии. Замедляющая способность вещества
Изменение энергии нейтронов при рассеянии. Замедляющая способность вещества Сила упругости. Закон Гука
Сила упругости. Закон Гука Сверлильные и расточные станки. (Тема 5)
Сверлильные и расточные станки. (Тема 5) Средства измерений
Средства измерений календарно тематическое планирование 11 класс
календарно тематическое планирование 11 класс Электростатика. Электр зарядтарының өзара әсерлесуі және сақталу заңы
Электростатика. Электр зарядтарының өзара әсерлесуі және сақталу заңы