Содержание
- 2. Атом Модель Томсона Первая попытка создания модели атома на основе накопленных экспериментальных данных (1903 г.) принадлежит
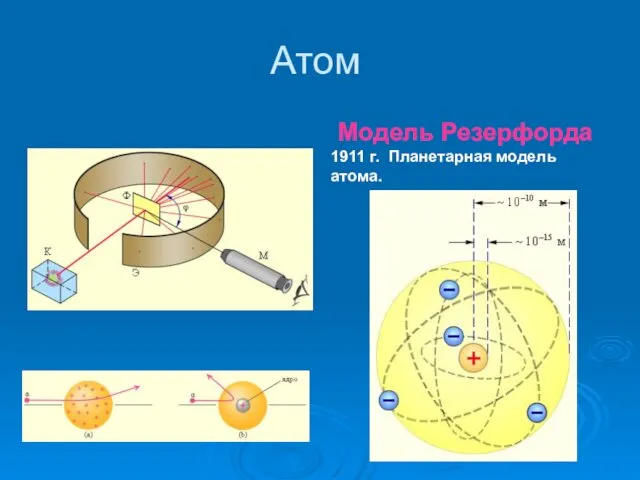
- 3. Атом Модель Резерфорда 1911 г. Планетарная модель атома.
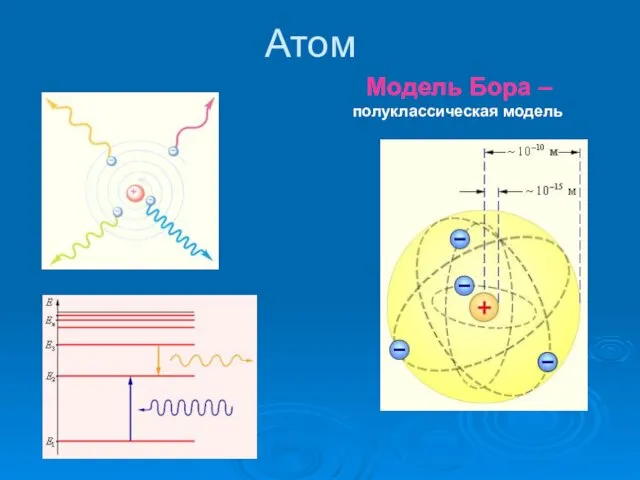
- 4. Атом Модель Бора – полуклассическая модель
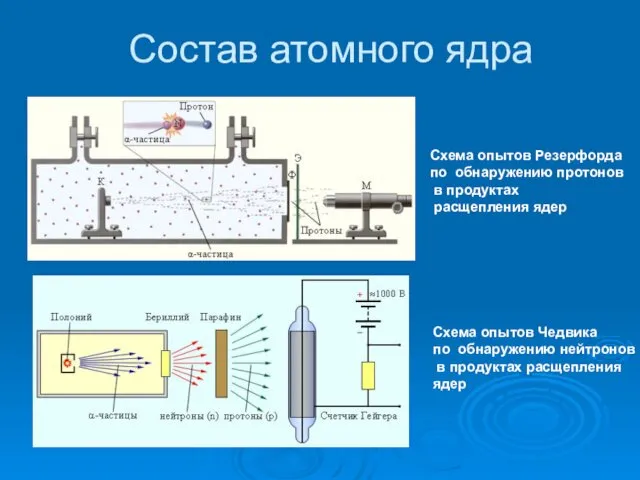
- 5. Состав атомного ядра Схема опытов Резерфорда по обнаружению протонов в продуктах расщепления ядер Схема опытов Чедвика
- 6. Атом Положительно заряженных (+) протонов, Незаряженных нейтронов и Отрицательно заряженных (-) электронов Атом состоит из: 1932
- 7. Ядро Протоны и нейтроны образуют ядро атома. Ядро определяет название элемента и его атомную массу. Протоны
- 8. Электроны Электроны – отрицательно заряженные частицы, которые окружают ядро, находясь на своих орбитах. Взаимодействие и обмен
- 9. Энергия связи электронов Электроны существуют в виде дискретных «оболочек» вокруг ядра (как планеты вокруг звезды) Каждая
- 10. Атомная единица массы Где 1 amu приблизительно равна 1.6605 x 10-24 грамма
- 11. Атомная единица массы Атомные массы протона и нейтрона приблизительно равны: Протон = 1.6726 x 10-24 г
- 12. Атомная единица массы Разницу в массах нейтрона и протона можно понять, если представить, что нейтрон состоит
- 13. Атомная единица массы Атомная масса электрона: Электрон = 9.1094 x 10-28 г = 0.00055 аем
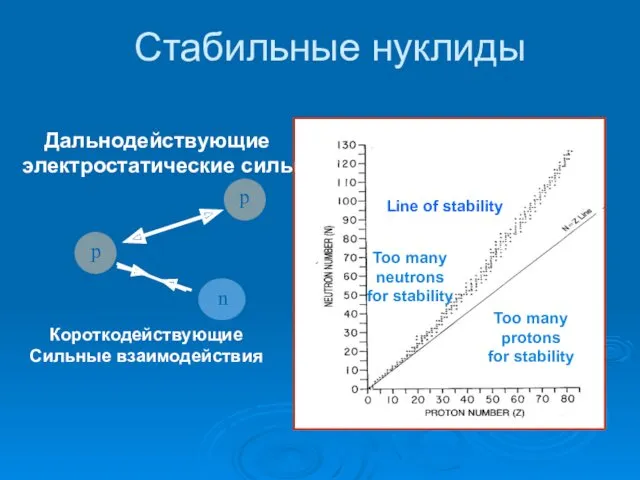
- 14. Стабильные нуклиды Дальнодействующие электростатические силы Короткодействующие Сильные взаимодействия Too many protons for stability Too many neutrons
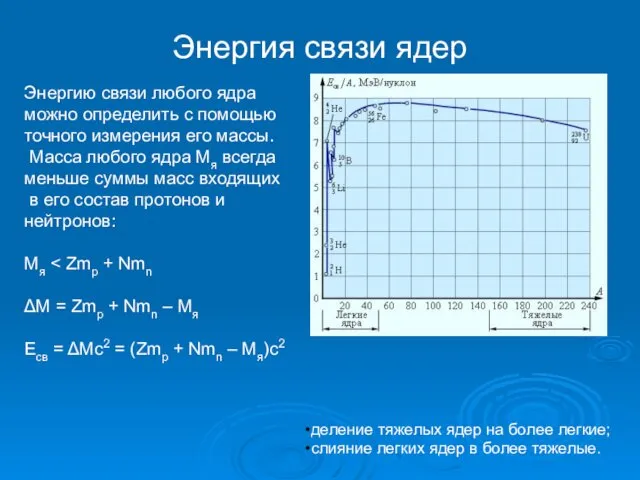
- 15. Энергия связи ядер деление тяжелых ядер на более легкие; слияние легких ядер в более тяжелые. Энергию
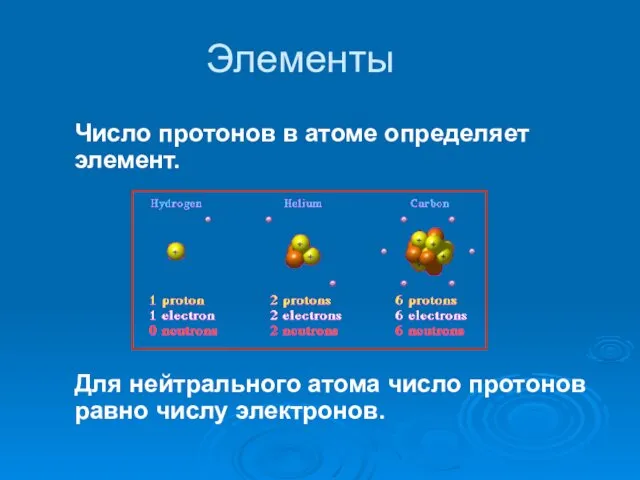
- 16. Элементы Число протонов в атоме определяет элемент. Для нейтрального атома число протонов равно числу электронов.
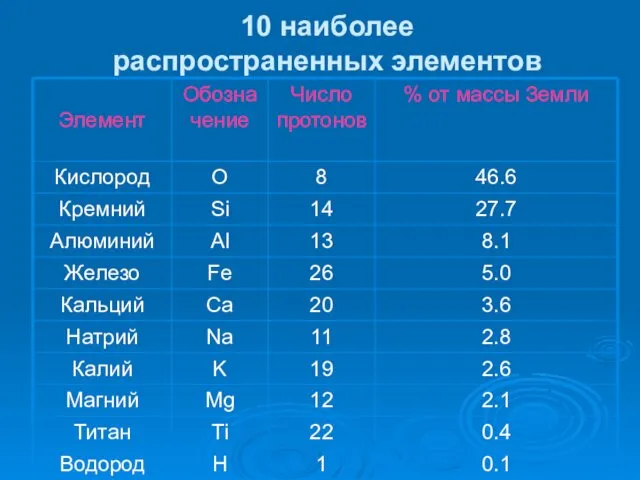
- 17. 10 наиболее распространенных элементов
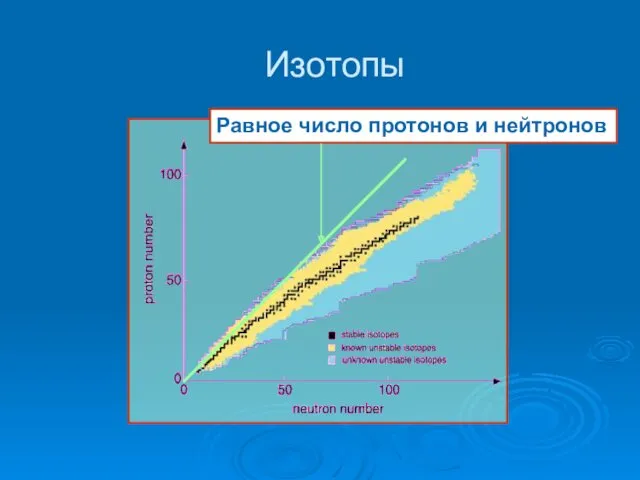
- 18. Изотопы Атомы элемента, которые имеют различное число нейтронов в ядре, называются изотопами этого элемента.
- 19. Изотопы
- 20. Радиоактивность
- 21. Радиоактивность атомных ядер : история, результаты… 1895 г. В.К. Рентген – открытие Х-лучей. 1896 г. Анри
- 22. Радиоактивность – определение и основные характеристики Радиоактивность - это самопроизвольное изменение свойств ядер со временем. Ядра,
- 23. Радиоактивность ядер, существующих в природных условиях, называют естественной. Радиоактивные ядра, синтезированные в лабораторных условиях искусственными способами
- 24. Виды радиоактивного распада Радиоактивные элементы испускают альфа-частицы, бета-частицы и гамма- кванты. При этом говорят о двух
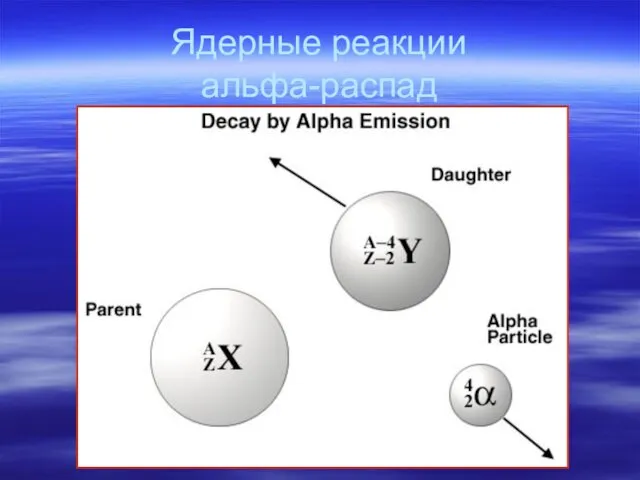
- 25. Ядерные реакции альфа-распад
- 26. Ядерные реакции альфа-распад 226Ra → 222Rn + 4He
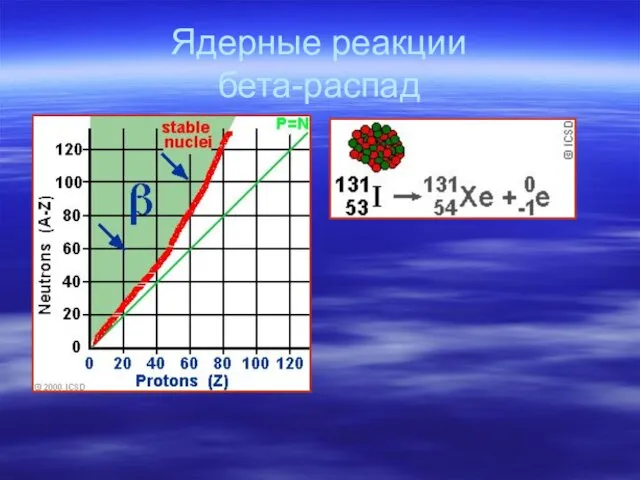
- 27. Ядерные реакции бета-распад
- 28. Ядерные реакции бета-распад
- 29. Спектр бета-частиц Eср. = 1/3 Emax
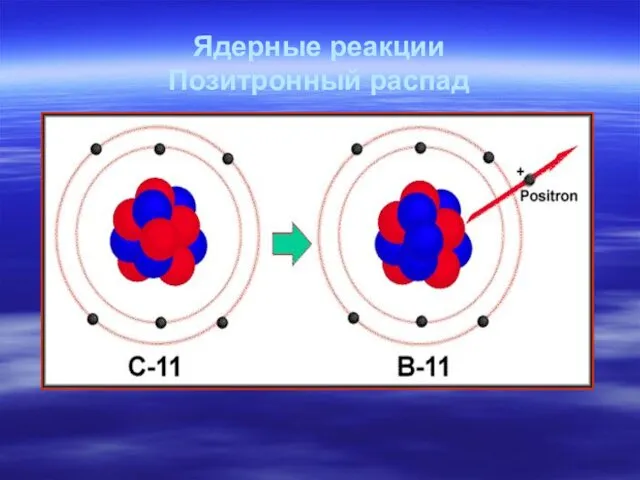
- 30. Ядерные реакции Позитронный распад
- 31. Ядерные реакции Позитронный распад
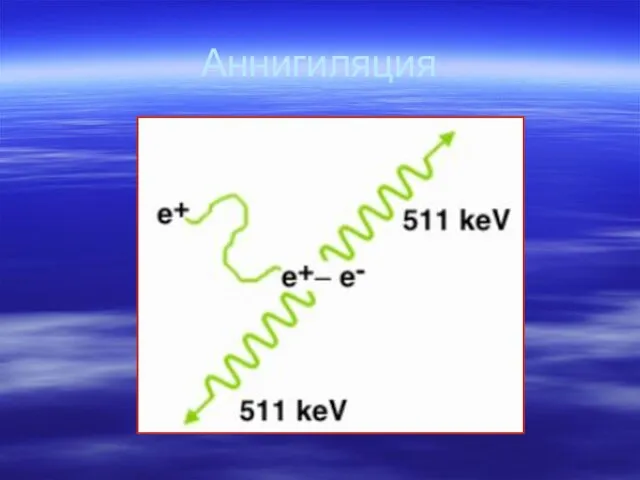
- 32. Аннигиляция
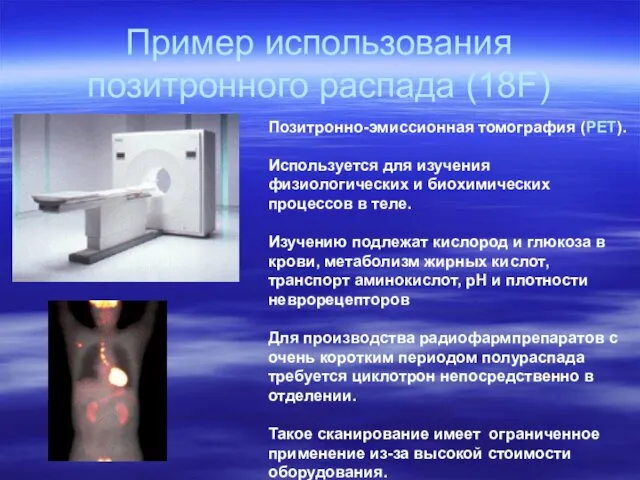
- 33. Пример использования позитронного распада (18F) Позитронно-эмиссионная томография (PET). Используется для изучения физиологических и биохимических процессов в
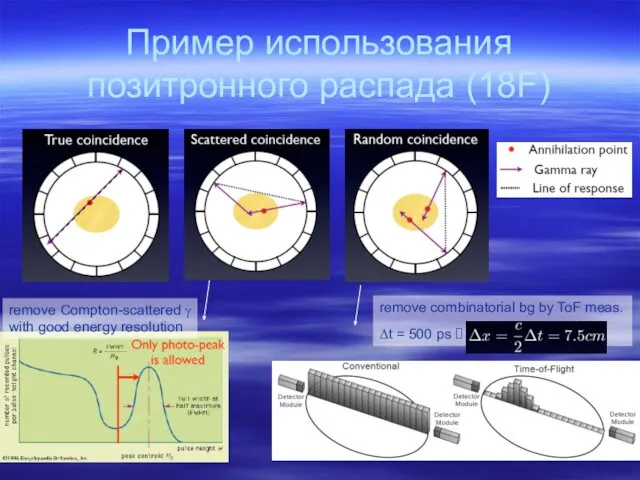
- 34. Пример использования позитронного распада (18F) remove Compton-scattered γ with good energy resolution remove combinatorial bg by
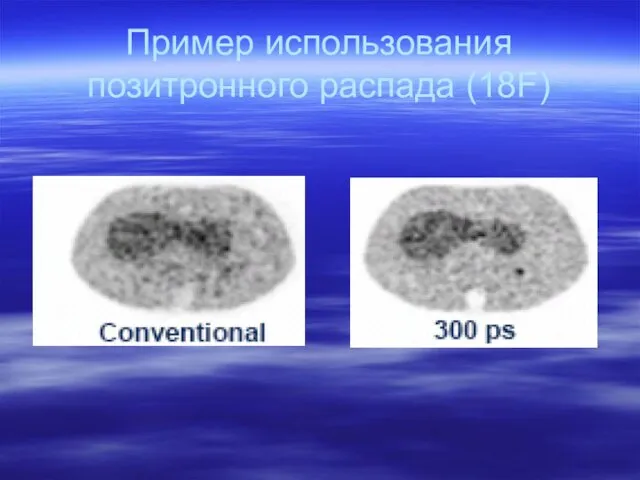
- 35. Пример использования позитронного распада (18F)
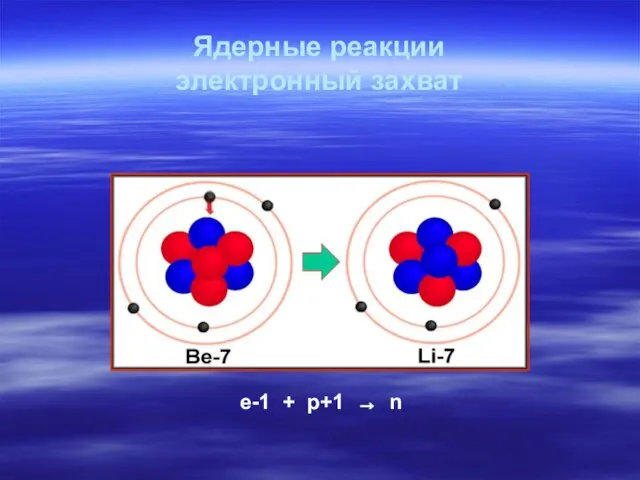
- 36. Ядерные реакции электронный захват Результат: Характеристическое рентгеновское излучение
- 37. Ядерные реакции электронный захват e-1 + p+1 → n
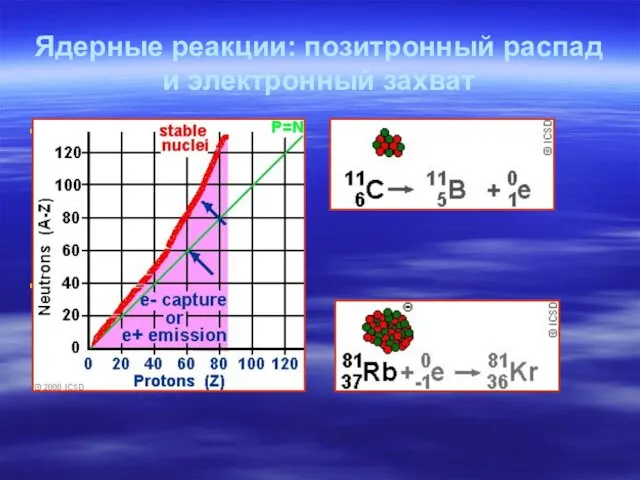
- 38. Ядерные реакции: позитронный распад и электронный захват позитронный распад электронный захват
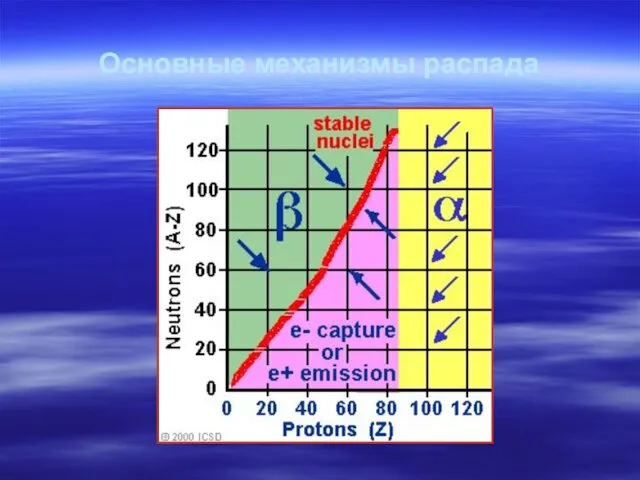
- 39. Основные механизмы распада
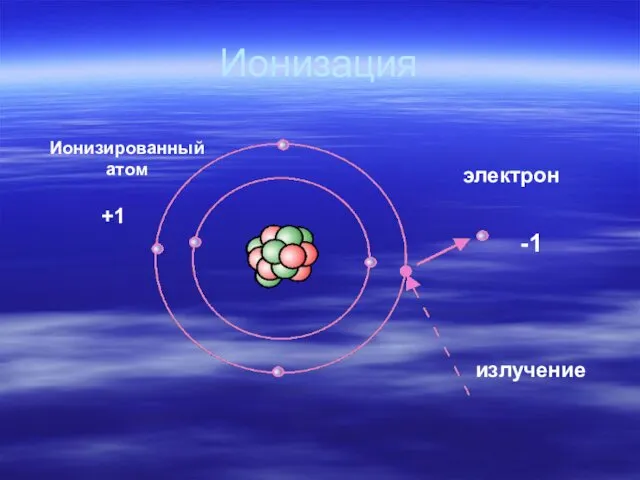
- 40. Ионизация излучение
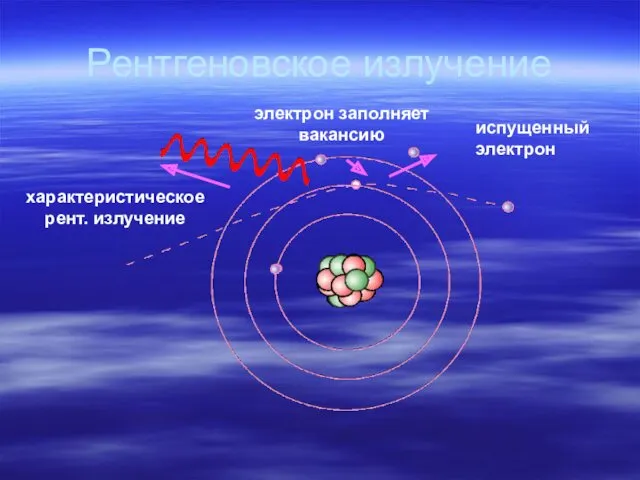
- 41. Рентгеновское излучение
- 42. Гамма-излучение Моноэнергетическое гамма-излучение испускается ядрами возбужденных атомов при радиоактивном распаде Освобождает ядра от избыточной энергии Имеет
- 43. Гамма-излучение
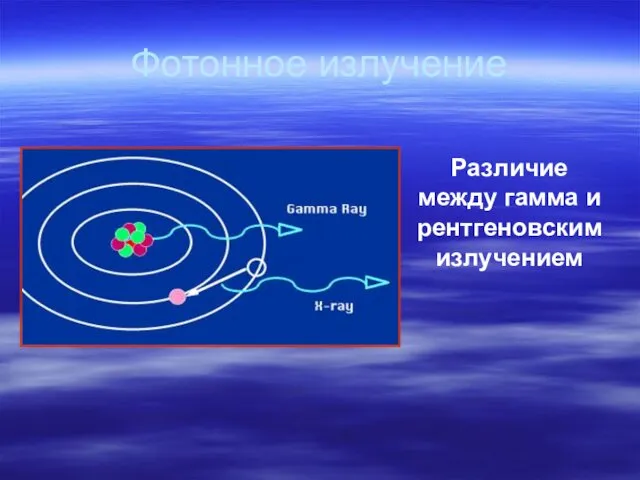
- 44. Фотонное излучение Различие между гамма и рентгеновским излучением
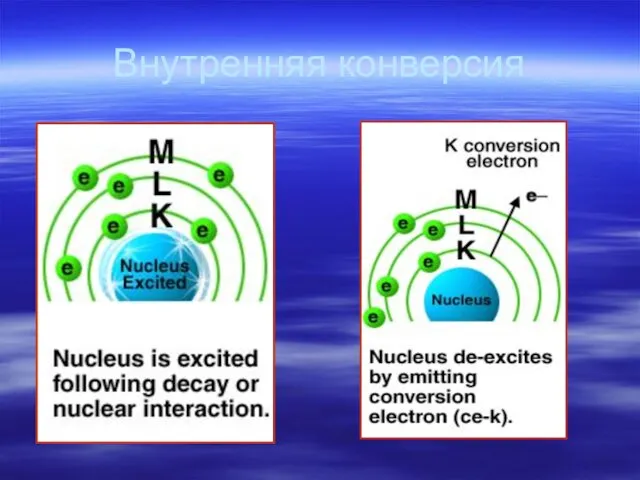
- 45. Внутренняя конверсия Процесс при котором возбужденные ядра высвобождают энергию возбуждения Ядро передает энергию возбуждения непосредственно орбитальными
- 46. Внутренняя конверсия
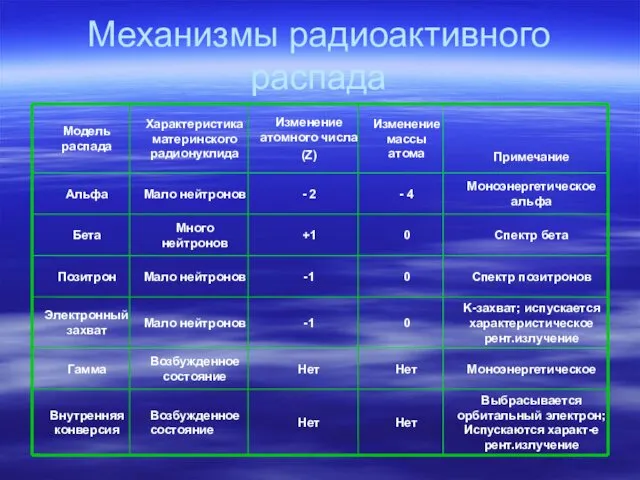
- 47. Механизмы радиоактивного распада
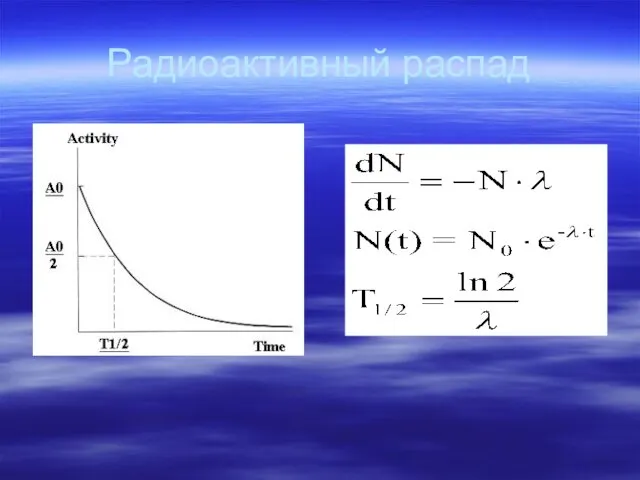
- 48. Радиоактивный распад
- 49. Дочки-матери A B C λ1 λ2
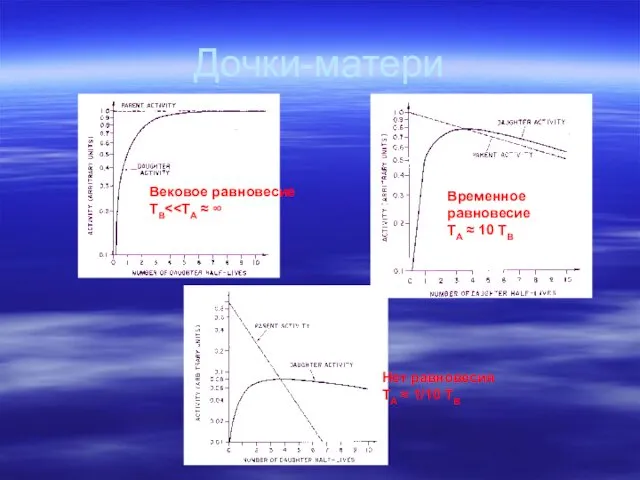
- 50. Дочки-матери Вековое равновесие TB Временное равновесие TA ≈ 10 TB Нет равновесия TA ≈ 1/10 TB
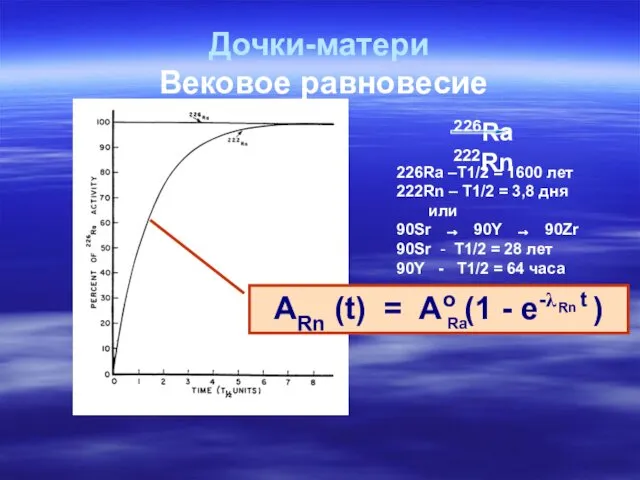
- 51. Дочки-матери Вековое равновесие ARn (t) = Ao (1 - e-λ t ) Rn Ra 226Ra 222Rn
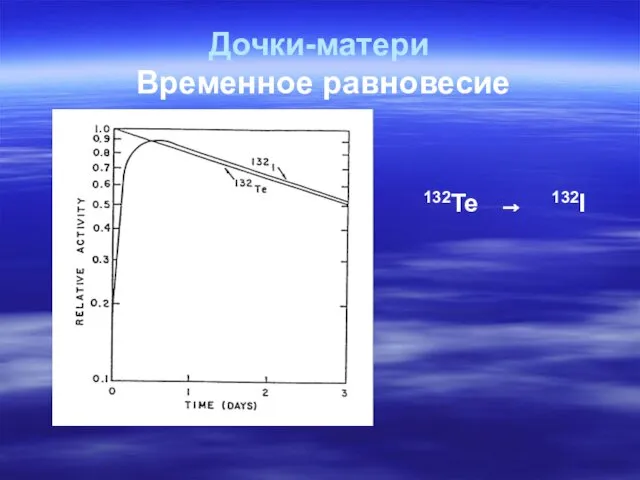
- 52. Дочки-матери Временное равновесие 132Te → 132I
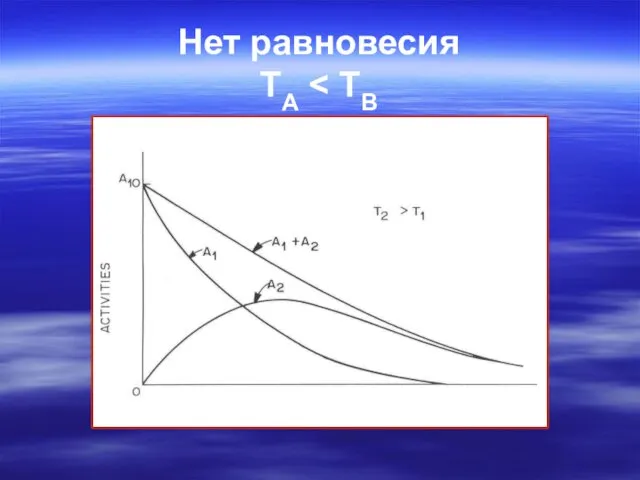
- 53. Нет равновесия TA
- 54. Ядерные реакции при бомбардировке ядер (n, зар.ч-ца) (n, гамма) (n, деление)
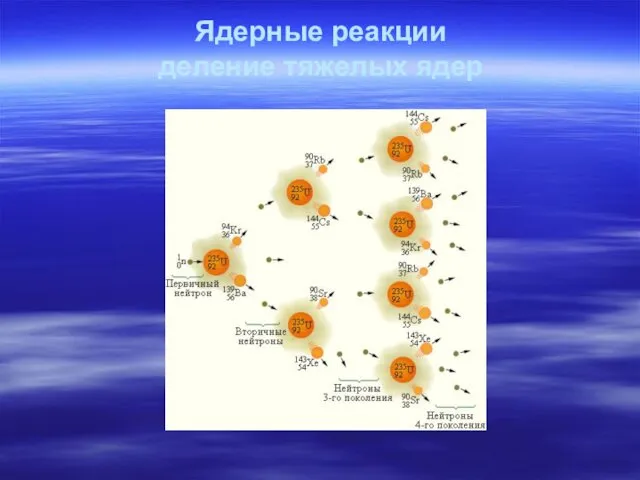
- 55. Ядерные реакции деление тяжелых ядер
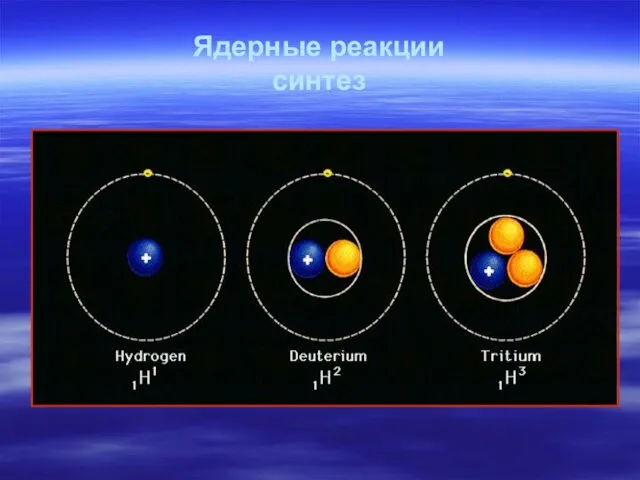
- 56. Ядерные реакции синтез
- 58. Скачать презентацию
























 Презентация к уроку физики Первый закон термодинамики
Презентация к уроку физики Первый закон термодинамики Потенциал. Решение задач
Потенциал. Решение задач Молекулярная физика. Молекулярно-кинетическая теория. Масса и размеры молекул
Молекулярная физика. Молекулярно-кинетическая теория. Масса и размеры молекул Определение элементного состава вещества методом рентгенофлуоресцентной спектроскопии
Определение элементного состава вещества методом рентгенофлуоресцентной спектроскопии Теоретическая механика. Кинематика. Курс лекций
Теоретическая механика. Кинематика. Курс лекций Виды спектров
Виды спектров Класифікація плугів. Класифікація фрез. Лекція 3
Класифікація плугів. Класифікація фрез. Лекція 3 Положительные лучи. Определение истинных масс атомов. Изотопы. АФ1.5
Положительные лучи. Определение истинных масс атомов. Изотопы. АФ1.5 Зат құрылысының атомдық теориясы
Зат құрылысының атомдық теориясы Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений
Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений Теорема об изменении импульса механической системы
Теорема об изменении импульса механической системы Работа и мощность электрического тока. Единицы работы электрического тока
Работа и мощность электрического тока. Единицы работы электрического тока Основы слесарно-сборочных и электромонтажных работ. Резка
Основы слесарно-сборочных и электромонтажных работ. Резка Физико-технические основы электроэнергетики. Лекция 11
Физико-технические основы электроэнергетики. Лекция 11 Импульс тела. Закон сохранения
Импульс тела. Закон сохранения Температура
Температура Урок по теме Квантовые постулаты Бора, 11 класс
Урок по теме Квантовые постулаты Бора, 11 класс Сложные электрические цепи
Сложные электрические цепи Общие свойства ионизирующих излучений ядерного взрыва
Общие свойства ионизирующих излучений ядерного взрыва Средства конвективного нагрева
Средства конвективного нагрева Проявление сил тяжести и упругости живой природе
Проявление сил тяжести и упругости живой природе Терморазведка. Тепловое поле
Терморазведка. Тепловое поле Nucleul atomic
Nucleul atomic Гироскопические приборы и устройства. (Модуль 2.7)
Гироскопические приборы и устройства. (Модуль 2.7) Сұйықтардың беттік керілуі
Сұйықтардың беттік керілуі Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении
Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении Принципы радиосвязи
Принципы радиосвязи Механические колебания. Кинематика и динамика колебательного движения
Механические колебания. Кинематика и динамика колебательного движения