Содержание
- 2. Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних
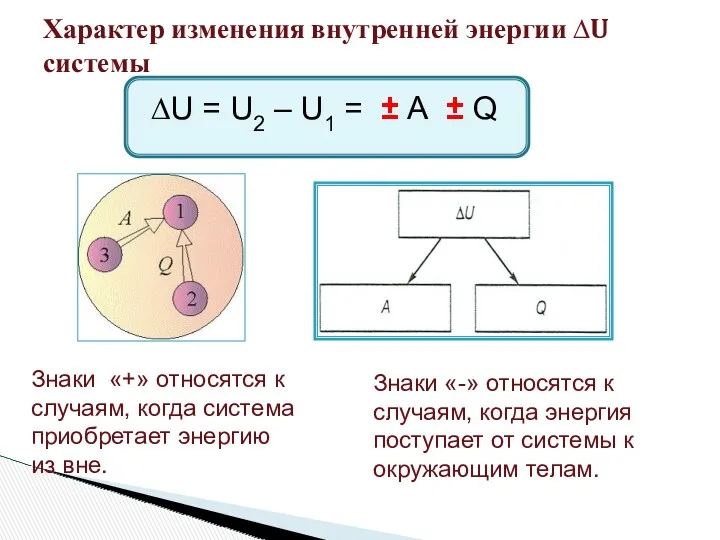
- 3. Характер изменения внутренней энергии ∆U системы ∆U = U2 – U1 = ± А ± Q
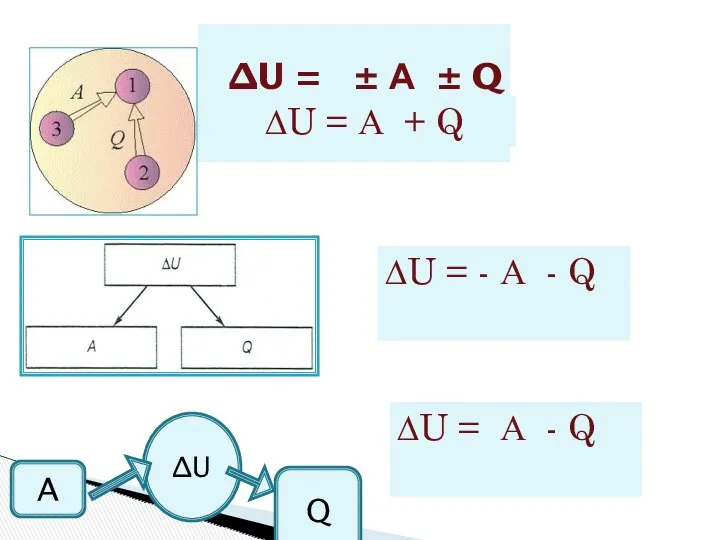
- 4. ∆U = ± А ± Q ∆U = А + Q ∆U = - А -
- 5. Внутренняя энергия Внутренняя энергия ΔU, основное понятие термодинамики, зависит от температуры и объема. Внутренняя энергия идеального
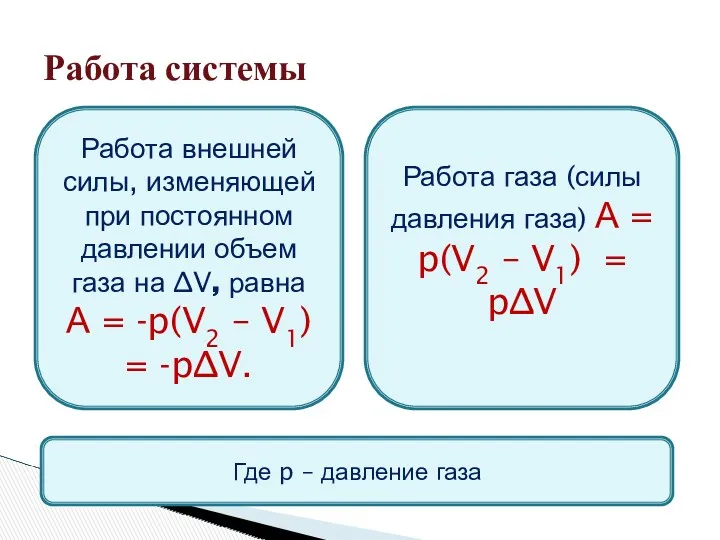
- 6. Работа системы Работа внешней силы, изменяющей при постоянном давлении объем газа на ∆V, равна А =
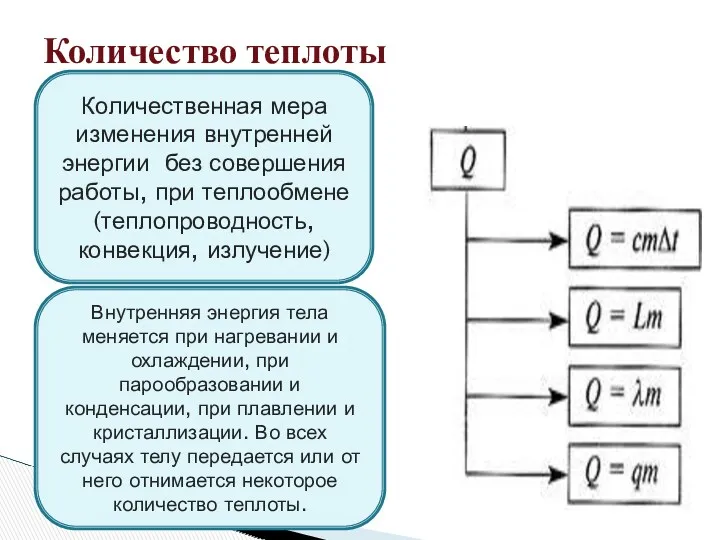
- 7. Количество теплоты Количественная мера изменения внутренней энергии без совершения работы, при теплообмене (теплопроводность, конвекция, излучение) Внутренняя
- 8. Первичное закрепление темы «Первый закон термодинамики»
- 9. №1.Газ в сосуде сжали, совершив работу 25 Дж. Внутренняя энергия газа при этом увеличилась на 30
- 10. Вопрос №1 Над телом совершена работа A внешними силами и телу передано количество теплоты Q. Чему
- 11. Вопрос №2 Газ получил количество теплоты 200 Дж, и при этом его внутренняя энергия увеличилась на
- 12. Вопрос №3 Какая физическая величина вычисляется по формуле ? Количество теплоты в идеальном газе Давление идеального
- 13. Вопрос №4 Выберите правильную формулировку первого закона термодинамики. А. Количество теплоты, преданное телу, равно сумме изменения
- 15. Скачать презентацию








 Технічні дані тепловозів
Технічні дані тепловозів Мир в магнитах. При поддержке туристической компании Колесница
Мир в магнитах. При поддержке туристической компании Колесница презентация на тему: Строение атома
презентация на тему: Строение атома Что изучает физика. Некоторые физические термины, наблюдения и опыты
Что изучает физика. Некоторые физические термины, наблюдения и опыты Электр тораптарын жіктеу, негізгі ұғымдар және анықтамалар
Электр тораптарын жіктеу, негізгі ұғымдар және анықтамалар Электрические машины постоянного тока
Электрические машины постоянного тока Элементы геометрической и электронной оптики
Элементы геометрической и электронной оптики Восстанавливающие моменты
Восстанавливающие моменты Законы трения скольжения
Законы трения скольжения Всероссийский турнир юных физиков. Катание на диске
Всероссийский турнир юных физиков. Катание на диске Мощностной баланс автомобиля
Мощностной баланс автомобиля Мастер-класс Применение технологии интерактивного обучения на уроках физики
Мастер-класс Применение технологии интерактивного обучения на уроках физики Автосцепные устройства
Автосцепные устройства Динамика кулисного механизма
Динамика кулисного механизма Сила. Види сил у механіці
Сила. Види сил у механіці Механика материалов
Механика материалов Физические величины и их математическая размерность
Физические величины и их математическая размерность История создания швейной машинки
История создания швейной машинки Ремонт выхлопной системы Ваз-2170. (Часть 2)
Ремонт выхлопной системы Ваз-2170. (Часть 2) Получение неразрывных соединений путем пайки
Получение неразрывных соединений путем пайки Истечение из отверстий и насадок
Истечение из отверстий и насадок Вводный урок 7 класс
Вводный урок 7 класс Спидометр
Спидометр Давление. Единицы давления. Способы уменьшения и увеличения давления. 7 класс
Давление. Единицы давления. Способы уменьшения и увеличения давления. 7 класс Физическая игра Счастливый случай. 8 класс
Физическая игра Счастливый случай. 8 класс ЕГЭ по физике за 2004 год
ЕГЭ по физике за 2004 год Законы автоматического регулирования
Законы автоматического регулирования Урок с использованием ИКТ по теме Электромагнитная индукция.
Урок с использованием ИКТ по теме Электромагнитная индукция.