Содержание
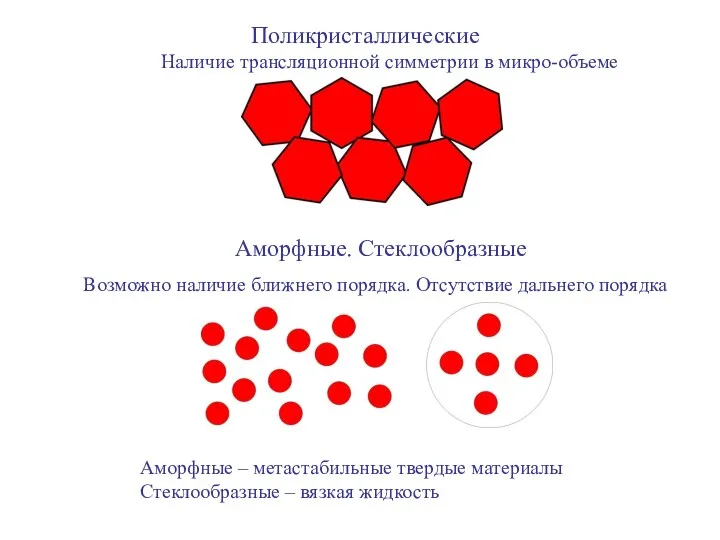
- 2. Поликристаллические Наличие трансляционной симметрии в микро-объеме Аморфные. Стеклообразные Возможно наличие ближнего порядка. Отсутствие дальнего порядка Аморфные
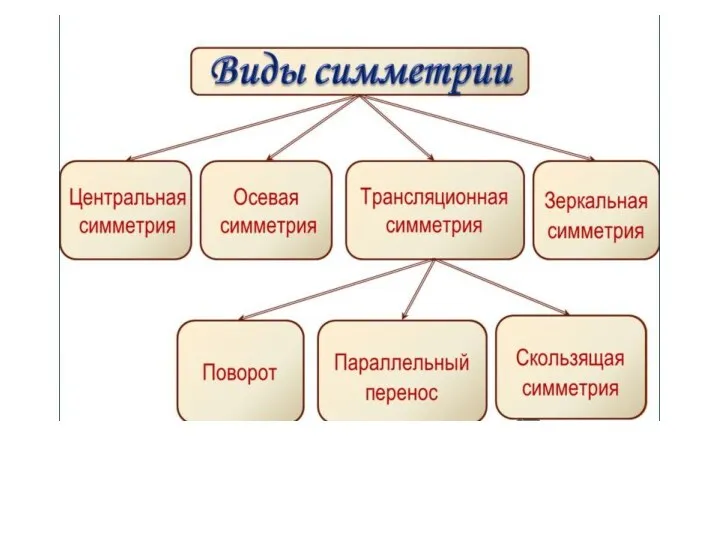
- 4. Виды симметрии 1 2 3 4 5 6 7 8 9 10
- 5. Трансляционная симметрия - тип симметрии, при которой свойства рассматриваемой системы не изменяются при сдвиге на определённый
- 6. [c] Кварц (SiO2) Кварцевое стекло и расплав Аморфный SiO2
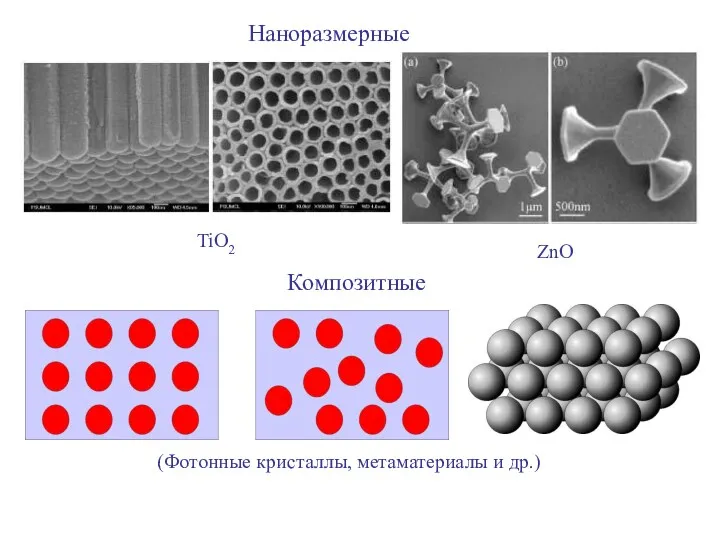
- 7. Композитные Наноразмерные TiO2 ZnO (Фотонные кристаллы, метаматериалы и др.)
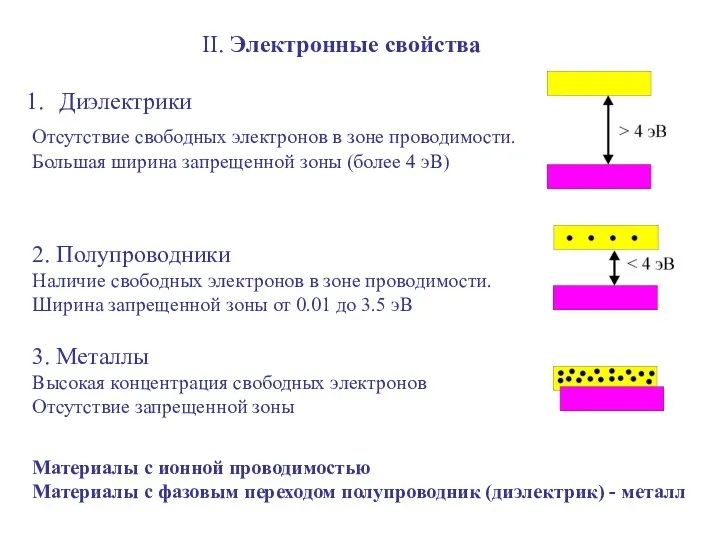
- 8. II. Электронные свойства Диэлектрики Отсутствие свободных электронов в зоне проводимости. Большая ширина запрещенной зоны (более 4
- 9. Зонная теория твёрдого тела — квантовомеханическая теория движения электронов в твёрдом теле. Свободные электроны могут иметь
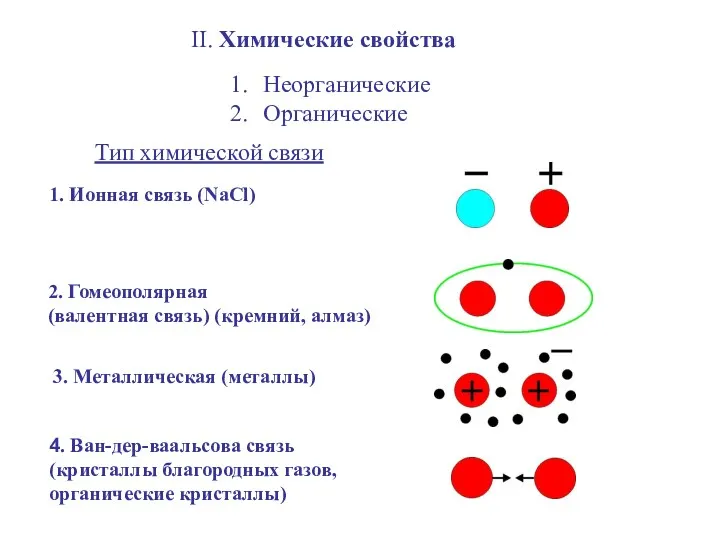
- 10. II. Химические свойства Неорганические Органические Тип химической связи 1. Ионная связь (NaCl) 2. Гомеополярная (валентная связь)
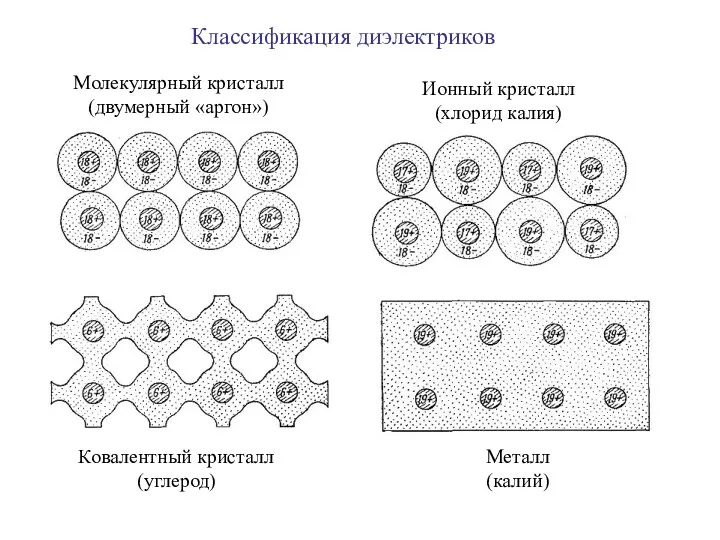
- 11. Молекулярный кристалл (двумерный «аргон») Ионный кристалл (хлорид калия) Ковалентный кристалл (углерод) Металл (калий) Классификация диэлектриков
- 13. Скачать презентацию


![[c] Кварц (SiO2) Кварцевое стекло и расплав Аморфный SiO2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/404759/slide-5.jpg)

 Ионно- диффузионные методы ХТО
Ионно- диффузионные методы ХТО Давление. Урок повторения и обобщения. 7 класс
Давление. Урок повторения и обобщения. 7 класс Цепные передачи
Цепные передачи Основы аэродинамики
Основы аэродинамики Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій
Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій Машины постоянного тока
Машины постоянного тока Машиноведение. Правила заправки верхней и нижней нитей швейной машины
Машиноведение. Правила заправки верхней и нижней нитей швейной машины Лазеры. Спонтанное и вынужденное излучение
Лазеры. Спонтанное и вынужденное излучение Парметры передачи оптических волокон. Оптическое волокно как диэлектрический волновод
Парметры передачи оптических волокон. Оптическое волокно как диэлектрический волновод Визначення модуля потужності гумми
Визначення модуля потужності гумми Энтропия в техносфере
Энтропия в техносфере Правило левой руки
Правило левой руки Zmena skupenstva látky
Zmena skupenstva látky Механические колебания и волны. Звук
Механические колебания и волны. Звук Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах
Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах Исполнительные механизмы и регулирующие органы
Исполнительные механизмы и регулирующие органы Физика – наука о наиболее общих формах движения материи и их взаимных превращениях. Лекция №1
Физика – наука о наиболее общих формах движения материи и их взаимных превращениях. Лекция №1 Изучение последовательного и параллельного соединения проводников. Лабораторная работа. 10класс
Изучение последовательного и параллельного соединения проводников. Лабораторная работа. 10класс Властивості поверхні рідини. Поверхневий натяг рідини
Властивості поверхні рідини. Поверхневий натяг рідини Викторина по физике
Викторина по физике Судовые двигатели
Судовые двигатели Автономные испытания компрессоров, камер сгорания и турбин авиационных ГТД
Автономные испытания компрессоров, камер сгорания и турбин авиационных ГТД Динамика поступательного движения
Динамика поступательного движения Урок-лаборатория Электризация тел, электрический заряд
Урок-лаборатория Электризация тел, электрический заряд Работа и мощность
Работа и мощность Жазық механизмдерді күштік талдау
Жазық механизмдерді күштік талдау Выпаривание и выпарные установки
Выпаривание и выпарные установки Техническая диагностика подвижного состава
Техническая диагностика подвижного состава