Основы термодинамики. Первое начало термодинамики. Работа газа при изменении объема. Теплоемкость идеального газа презентация
Содержание
- 2. Внутренняя энергия макросистемы U состоит из двух частей: 1) кинетической энергии хаотического движения молекул в системе
- 3. Разобьем макросистему на достаточно большие части. Поскольку межмолекулярные силы короткодействующие, то потенциальной энергией взаимодействия между частями
- 4. Внутренняя энергия U обладает еще одним свойством – она является функцией состояния. Это значит, что величина
- 5. Внутреннюю энергию макросистемы U можно изменить двумя способами 1) совершив над ней работу A′ 2) сообщив
- 6. При совершении работы A′ над макросистемой происходит перемещение внешних к ней тел. Например, при движении поршня
- 7. С другой стороны передача теплоты Q не связана с перемещением внешних тел. Передача теплоты происходит при
- 8. Теплота Q равна энергии, переданной системе внешними телами посредством таких микроскопических процессов. Из 3 - го
- 9. Из закона сохранения энергии следует, что изменение внутренней энергии системы ΔU при ее переходе из начального
- 10. Если ΔU > 0, то совершенная системой работа меньше полученного количества теплоты, то есть Q >
- 11. Пусть макросистема совершает процесс, в ходе которого она периодически возвращается в исходное состояние, тогда ее внутренняя
- 12. Теплота Q измеряется в тех же единицах, что энергия U и работа А , то есть
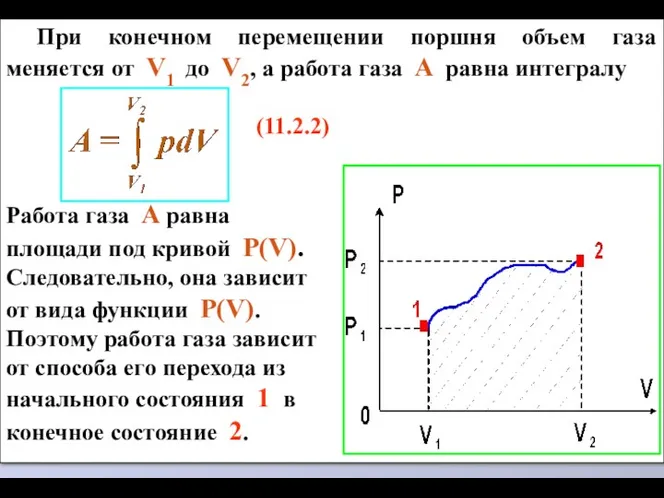
- 13. Пусть газ находится под поршнем цилиндрического сосуда. При своем расширении газ совершает работу A по перемещению
- 14. При конечном перемещении поршня объем газа меняется от V1 до V2, а работа газа A равна
- 15. Теплоемкость равна количеству теплоты, которое нужно передать телу, чтобы повысить его температуру на 1° К (11.3.1)
- 16. Молярная теплоемкость – количество теплоты, необходимое для нагревания 1 моля вещества на 1° К (11.3.3) где
- 17. Теплоемкость зависит от условий измерения. Различают молярную теплоемкость при постоянном объеме cV и постоянном давлении cP
- 18. Получим выражения для этих теплоемкостей, используя первый закон термодинамики (11.1.1) и формулу для работы газа d′A
- 19. Подставляя в выражения для теплоемкостей (11.3.4), (11.3.5) , получаем (11.3.6а) (11.3.6б)
- 20. Опыт показывает, что у газов, свойства которых близки к идеальному газу, теплоемкость сV практически не зависит
- 21. Найдем теплоемкость идеального газа. Для этого используем уравнение состояния идеального газа PV = νRT → PVm
- 23. Скачать презентацию



















 Основы расчета реакторов
Основы расчета реакторов Презентация к уроку физики в 7 классе по теме: Связь между силой тяжести и массой тела.
Презентация к уроку физики в 7 классе по теме: Связь между силой тяжести и массой тела. презентация урока в 7 классе Вес тела.Невесомость
презентация урока в 7 классе Вес тела.Невесомость Приводные характеристики машин и условия работы электроприводов в сельскохозяйственном производстве
Приводные характеристики машин и условия работы электроприводов в сельскохозяйственном производстве Повторительно - обобщающий урок по теме: Архимедова сила. Плавание. Воздухоплавание.
Повторительно - обобщающий урок по теме: Архимедова сила. Плавание. Воздухоплавание. Точность и погрешность измерений
Точность и погрешность измерений Мастер-класс Применение технологии интерактивного обучения на уроках физики
Мастер-класс Применение технологии интерактивного обучения на уроках физики Магнитное поле
Магнитное поле Электрооборудование автомобилей. Электростартеры. (Урок 4)
Электрооборудование автомобилей. Электростартеры. (Урок 4) Акустический шум и его воздействие на организм человека
Акустический шум и его воздействие на организм человека Аеродинамічні характеристики літака. Злітно-посадочна механізація. (Лекція 8.4.3)
Аеродинамічні характеристики літака. Злітно-посадочна механізація. (Лекція 8.4.3) Исследование структуры. Оптическая и электронная микроскопия
Исследование структуры. Оптическая и электронная микроскопия Нестационарная теплопроводность. Задачи
Нестационарная теплопроводность. Задачи Приемы работы на швейной машине. 5 класс
Приемы работы на швейной машине. 5 класс Вращательное движение твердого тела. Уравнение вращательного движения. Угловая скорость и угловое ускорение тела
Вращательное движение твердого тела. Уравнение вращательного движения. Угловая скорость и угловое ускорение тела Использование электронных образовательных ресурсов в преподавании физики
Использование электронных образовательных ресурсов в преподавании физики Физическая викторина 7-8 классы.
Физическая викторина 7-8 классы. Понятие о эпюрах гидростатического давления Понятие о центре давления. Эпюры гидростатического давления
Понятие о эпюрах гидростатического давления Понятие о центре давления. Эпюры гидростатического давления Гидропривод. Понятия и определения
Гидропривод. Понятия и определения Когда изобрели велосипед?
Когда изобрели велосипед? Вес воздуха. Атмосферное давление
Вес воздуха. Атмосферное давление Определение плотности хозяйственного мыла
Определение плотности хозяйственного мыла энергосберегающие источники света
энергосберегающие источники света Источники энергии для сварки
Источники энергии для сварки Зубчатые механизмы. Основные виды зубчатых передач. (Лекция 2)
Зубчатые механизмы. Основные виды зубчатых передач. (Лекция 2) Три состояния вещества
Три состояния вещества равновесие тел
равновесие тел Лекция № 1. Ядерный топливный цикл и обращение с радиоактивными отходами. Вводная лекция по курсу
Лекция № 1. Ядерный топливный цикл и обращение с радиоактивными отходами. Вводная лекция по курсу