Слайд 2

ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
Энергия в природе не возникает из ничего и не
исчезает: количество энергии неизменно, она только переходит из одной формы в другую.
Слайд 3
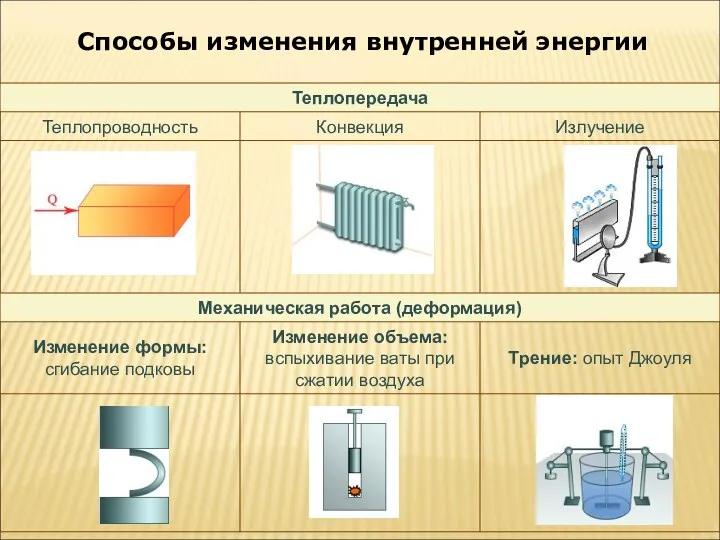
Способы изменения внутренней энергии
Слайд 4
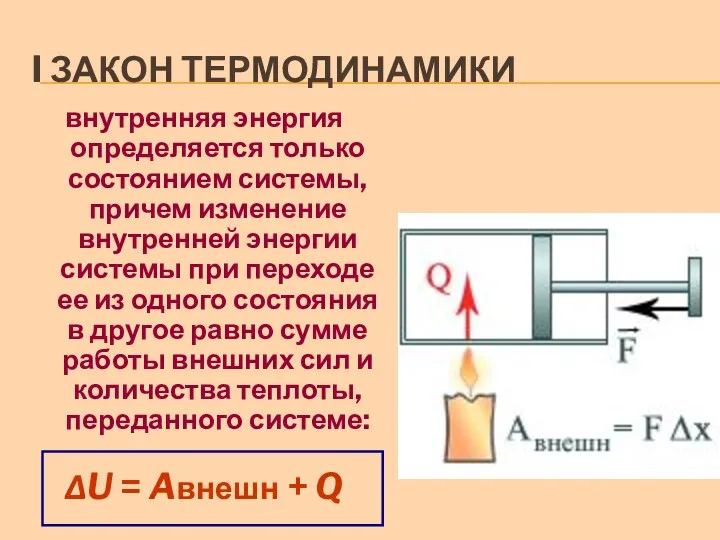
I ЗАКОН ТЕРМОДИНАМИКИ
внутренняя энергия определяется только состоянием системы, причем изменение внутренней
энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
ΔU = Aвнешн + Q
Слайд 5

ЕСЛИ ПРИ НАГРЕВАНИИ ГАЗ РАСШИРЯЕТСЯ И ПРИ ЭТОМ СОВЕРШАЕТ РАБОТУ A,
ТО ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ МОЖНО СФОРМУЛИРОВАТЬ ПО-ДРУГОМУ:
Q = ΔU + AI
Количество теплоты, переданное газу, равно сумме изменения его внутренней энергии и работы, совершенной газом.
Так как работа газа и работа внешних сил вследствие 3-го закона Ньютона равны по модулю и имеют противоположный знак:
Aвнешн = –AI
Слайд 6

I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫ
Слайд 7

I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫ
Слайд 8
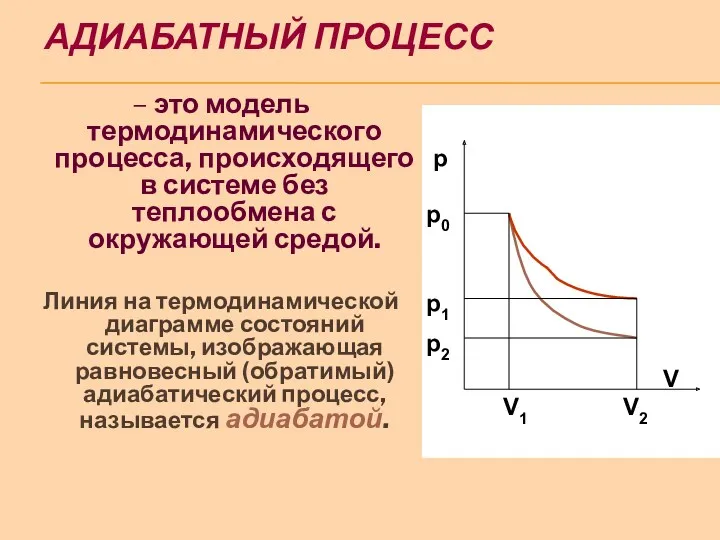
АДИАБАТНЫЙ ПРОЦЕСС
– это модель термодинамического процесса, происходящего в системе без теплообмена
с окружающей средой.
Линия на термодинамической диаграмме состояний системы, изображающая равновесный (обратимый) адиабатический процесс, называется адиабатой.
Слайд 9
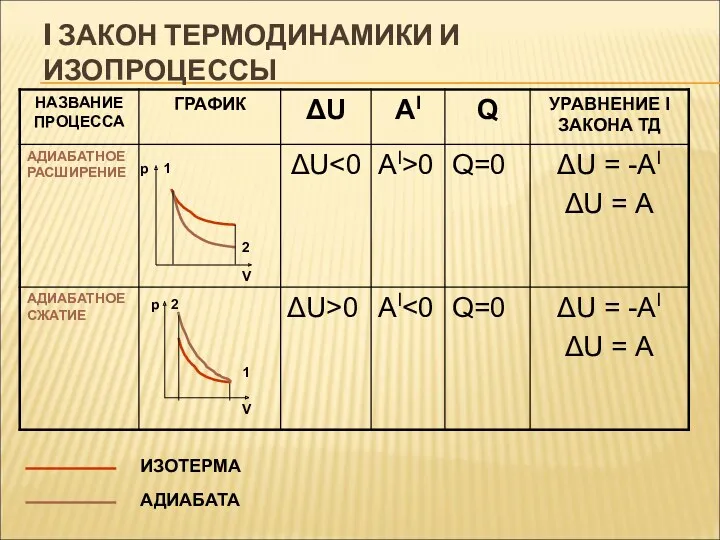
I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫ
V
р
1
2
ИЗОТЕРМА
АДИАБАТА
V
р
2
1








 презентация по физике Сила трения
презентация по физике Сила трения Закон Архимеда
Закон Архимеда Электростатика. Электр зарядтарының өзара әсерлесуі және сақталу заңы
Электростатика. Электр зарядтарының өзара әсерлесуі және сақталу заңы Выпаривание
Выпаривание Магнитное поле
Магнитное поле Измерение удельной теплоемкости твердого тела
Измерение удельной теплоемкости твердого тела Конденсатор, 9 класс
Конденсатор, 9 класс Ядерный реактор. Первые ядерные реакторы
Ядерный реактор. Первые ядерные реакторы Общие принципы работы двигателей
Общие принципы работы двигателей Сообщающие сосуды
Сообщающие сосуды Насыщенный пар
Насыщенный пар Молекулярно-кинетическая теория
Молекулярно-кинетическая теория Розв’язування задач із теми Взаємодія тіл (урок 43 - 44)
Розв’язування задач із теми Взаємодія тіл (урок 43 - 44) Технология ТО и ремонта. Ходовая часть
Технология ТО и ремонта. Ходовая часть Законы сохранения в классической механике
Законы сохранения в классической механике Гидравлика
Гидравлика Фазированные антенные решетки и их назначение. Надежность ФАР
Фазированные антенные решетки и их назначение. Надежность ФАР Виды телескопов
Виды телескопов Презентация к уроку физики в 7 классе на тему Измерение размеров малых тел
Презентация к уроку физики в 7 классе на тему Измерение размеров малых тел презентация
презентация Простые механизмы. Рычаг. Условие равновесия рычага
Простые механизмы. Рычаг. Условие равновесия рычага Обобщающий урок по физике 8 класс Тепловые явления.Агрегатные состояния вещества
Обобщающий урок по физике 8 класс Тепловые явления.Агрегатные состояния вещества Лекция №20. Трансформирование трёхфазного тока и схемы соединения обмоток трёхфазных трансформаторов
Лекция №20. Трансформирование трёхфазного тока и схемы соединения обмоток трёхфазных трансформаторов Методы исследования переключения в сегнетоэлектриках. Микроскопия
Методы исследования переключения в сегнетоэлектриках. Микроскопия Презентация Электрический ток. Сила тока
Презентация Электрический ток. Сила тока Организация мониторинга показателей качества электрической энергии
Организация мониторинга показателей качества электрической энергии Макросистема (термодинамическая система)
Макросистема (термодинамическая система) Устройство и принцип работы крана вспомогательного тормоза 254
Устройство и принцип работы крана вспомогательного тормоза 254