Содержание
- 2. Атом – найменша, електронейтральна, хімічно неподільна частинка речовини Атом складається з щільного ядра з позитивно заряджених
- 3. Стан електронів в атомі Електрон одночасно проявляє властивості і частинки, і хвилі – говорячи науковою мовою,
- 4. Електронна хмара Електронна хмара – модель руху електрона в атомі, графічне зображення області, де можливе перебування
- 5. Атомна орбіталь – це частина простору навколо ядра, ймовірність перебування електрона в якому дорівнює до 95%,
- 6. Рухаючись навколо ядра, електрон ще й обертається навколо своєї осі. Цей рух називається «спін». Спін електрона
- 7. Характеристака орбіталей Орбіталі, які утворюють електрони, відрізняються одна від одної: Розміром Формою Положенням у просторі Орбіталі
- 8. Характеристака орбіталей Орбіталі мають різні форми. Вони можуть бути кулястими, гантелеподібними, у формі чотирьох або шестипелюсткової
- 9. s-орбіталі мають форму сфери, а електрони з такою формою електронної хмари називаються s-електронами; S – орбіталь
- 10. Р-орбіталі мають форму об’ємної вісімки (гантелі), а електрони з такою формою електронної хмари називаються р-електронами. Р
- 11. d – орбіталі Електрони набувають ще більшого запасу енергії, складніших рухів, у результаті утворюються складні і
- 12. f – орбіталі Ще більшого запасу енергії і складніших рухів набувають f - електрони, у результаті
- 13. Характеристака орбіталей Орбіталі мають різні положення у просторі.
- 14. s-орбіталь має одне положення в просторі; p-орбіталь – 3 положення в просторі . d-орбіталь – 5
- 15. Атомні орбіталі
- 16. Закріплення набутих знань Електрон – це А. Позитивно заряджена частинка, що входить до складу ядра. Б.
- 17. 2. Як можна визначити кількість електронів у атомі: А. По номеру періоду, де розташований хімічний елемент.
- 18. 3. Виберіть правильне твердження: А. Електрон – це частинка, що одночасно проявляє властивості і частинки, і
- 19. 4. Орбіталь –це А. Траєкторія руху електрона навколо ядра. Б. Частина простору навколо ядра, ймовірність перебування
- 22. 7. Кількість S – орбіталей на одному енергетичному рівні: А. 1 Б. 2 В. 3 Г.
- 23. 8 . Кількість Р – орбіталей на одному енергетичному рівні: А. 1 Б. 2 В. 3
- 24. 9. Знайдіть відповідність:
- 26. Скачать презентацию























 Испарение и конденсация Урок в 8 классе
Испарение и конденсация Урок в 8 классе Фокусировка, свет. Эксплуатация вспомогательного фото-оборудования
Фокусировка, свет. Эксплуатация вспомогательного фото-оборудования внеклассное мероприятие по физике
внеклассное мероприятие по физике Кванттық механиканың математикалық аппараты
Кванттық механиканың математикалық аппараты Световые явления в живой и неживой природе
Световые явления в живой и неживой природе Технічні засоби виявлення зброї, наркотичних та вибухових речовин
Технічні засоби виявлення зброї, наркотичних та вибухових речовин Low-momentum K/π identification for τ/c factories
Low-momentum K/π identification for τ/c factories Поверхностное натяжение
Поверхностное натяжение Физика и лирика
Физика и лирика Электродинамика бөлімі бойынша оқу материалын қайталау, қорытындылау және жүйелеу
Электродинамика бөлімі бойынша оқу материалын қайталау, қорытындылау және жүйелеу Программа элективного курса История физики и развитие представлений о мире
Программа элективного курса История физики и развитие представлений о мире Тепломассообмен. Нестационарная теплопроводность
Тепломассообмен. Нестационарная теплопроводность Радиоактивность, как свидетельство сложного строения атомов. Альфа-, бета- и гамма-излучения
Радиоактивность, как свидетельство сложного строения атомов. Альфа-, бета- и гамма-излучения Ультразвук, источники ультразвука
Ультразвук, источники ультразвука Виды соединения проводников
Виды соединения проводников Влияния состава и размера зерна аустенита на температуру фазового превращения и физико-механические свойства сплавов
Влияния состава и размера зерна аустенита на температуру фазового превращения и физико-механические свойства сплавов Презентация по теме Архимедова сила
Презентация по теме Архимедова сила Электростатика
Электростатика Заземление
Заземление Газовые законы
Газовые законы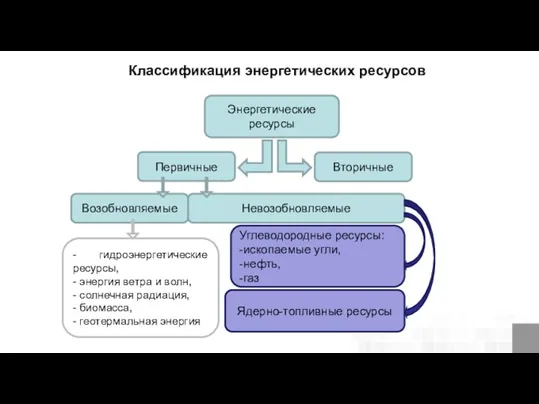 Классификация энергетических ресурсов
Классификация энергетических ресурсов Силы, действующие в магнитном поле: сила Ампера, сила Лоренца
Силы, действующие в магнитном поле: сила Ампера, сила Лоренца Инфракрасное излучение
Инфракрасное излучение Синусоидалы емес периодты сигналдарды Фурье қатарына жіктеу. Синусоидалы емес периодты сигналдардың әрекеттік орташа мәндері
Синусоидалы емес периодты сигналдарды Фурье қатарына жіктеу. Синусоидалы емес периодты сигналдардың әрекеттік орташа мәндері Масса и размеры молекул. Количество вещества
Масса и размеры молекул. Количество вещества Диагностика неисправностей системы нейтрализации выхлопных газов двигателя 2.7CTI
Диагностика неисправностей системы нейтрализации выхлопных газов двигателя 2.7CTI Основы кристаллографии
Основы кристаллографии Закон сохранения импульса
Закон сохранения импульса