Содержание
- 2. НЕКОТОРЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ ВЕРОЯТНОСТЕЙ В термодинамике состояние любого тела, образован- ного огромным числом молекул, задается
- 3. Пусть имеется некоторая макросистема. Возьмем конкретную характеристику микросостояния этой системы, например, число молекул в какой-то части
- 4. Обозначим ΣNi = N. (1) Набор из N результатов представляет собой весь статистический ансамбль. Отношение Ni
- 5. Вероятность получения результата xi либо xk равна Pi или k = (Ni + Nk)/N = Pi
- 6. Введенное нами понятие вероятности относилось к величинам, характеризуемым дискретными значениями. Распространим полученные результаты на случай, когда
- 7. Отобразим графически все величины ΔРх на одной диаграмме . Для этого отложим вверх от каждого интервала
- 8. Если теперь устремить величину интервала ε к нулю, то ступенчатая линия, ограничивающая гистограмму сверху, превратится в
- 9. Площадь, ограниченная всей кривой распределения вероятностей, так же как и площадь гистограммы, равна единице. То есть
- 10. Отношение этой суммы к общему числу N всех измерений даст среднюю величину х (6) Некоторые физические
- 11. Функция распределения молекул по скоростям – распределение Максвелла. В разных областях физики используют понятие фазового пространства,
- 12. Введем трехмерное пространство скоростей vx,vy,vz . Каждая молекула имеет скорость и отобразится в этом пространстве точкой.
- 13. В результате плотность распределения точек в пространстве скоростей в условиях равновесия газа во времени не изменяется
- 14. Графиком этой функции является, так называемая, кривая Гаусса. Определим число точек dNv , попадающих в интервал
- 15. Относительное число молекул, имеющих скорость в интервале от v до v + dv будет равно В
- 16. График этой функции распределения для различных температур имеет вид: Т2>T1 Площадь заштрихованной полоски равна вероятно- сти
- 17. Ход кривой распределеня по скоростям обусловлен конкуренцией двух сомножителей, входящих в функцию распределения: v2 и exp(-av2)
- 18. Итак, f(υ) – имеет смысл вероятности, то есть показывает, какова вероятность, что любая молекулы газа имеет
- 19. Из выражения (8) для функции распределения (8) следует: - вид распределения молекул газа по скоростям, для
- 20. Фактически, распределение Максвелла характеризует распределение молекул по значениям кинетической энергии молекул ε. Из распределения Максвелла можно
- 21. Имея в явном виде функцию распределения молекул по энергиям f(ε), мы можем вычислить среднюю кинетическую энергию
- 22. Характерные скорости молекул газа Наиболее вероятной называют такую скорость молекул Vвер , для которой функция распределения
- 23. Решение этого уравнения дает следующее значение наиболее вероятной скорости: Здесь М – масса моля. Для средней
- 24. Средней квадратичной скоростью молекул Vкв называется квадратный корень из среднего значения квадрата скорости, то есть Нахождении
- 26. Зависимость функции распределения Максвелла от массы молекул и температуры газа На рисунке изображены три кривые, которые
- 28. Скачать презентацию





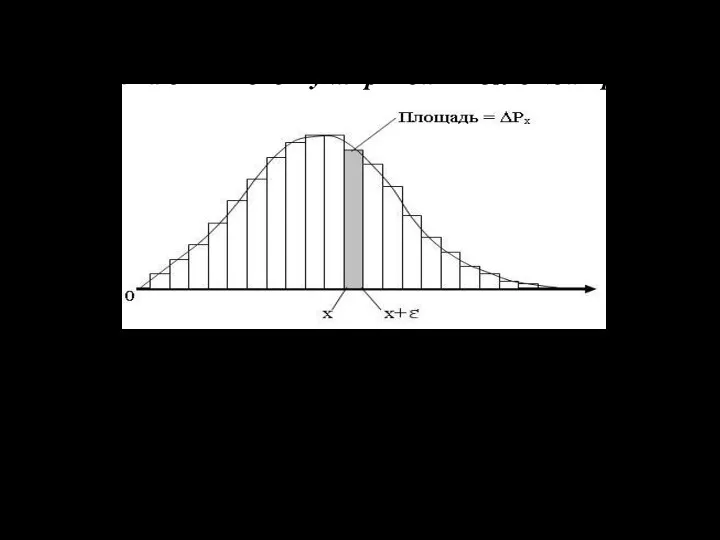
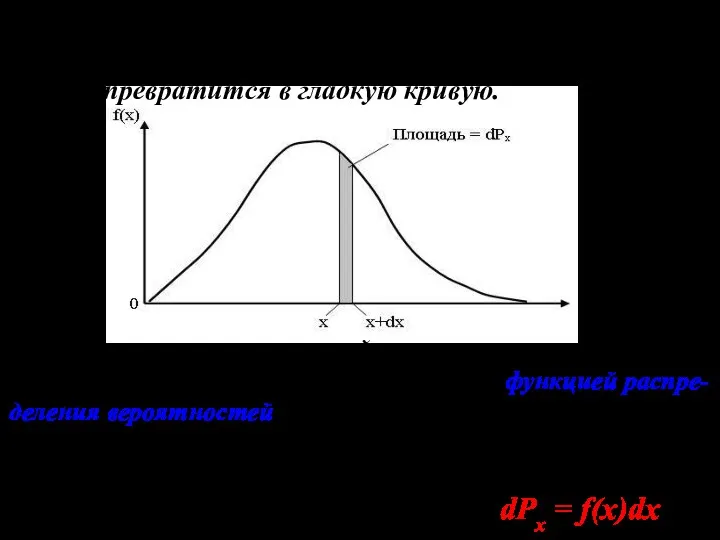



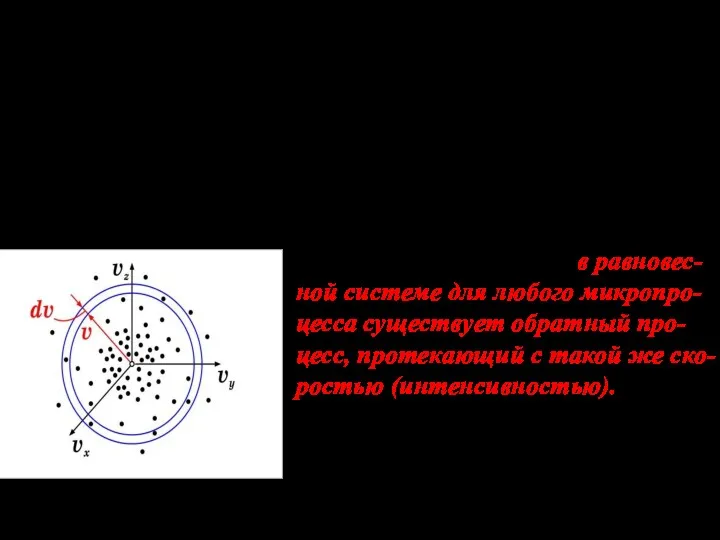

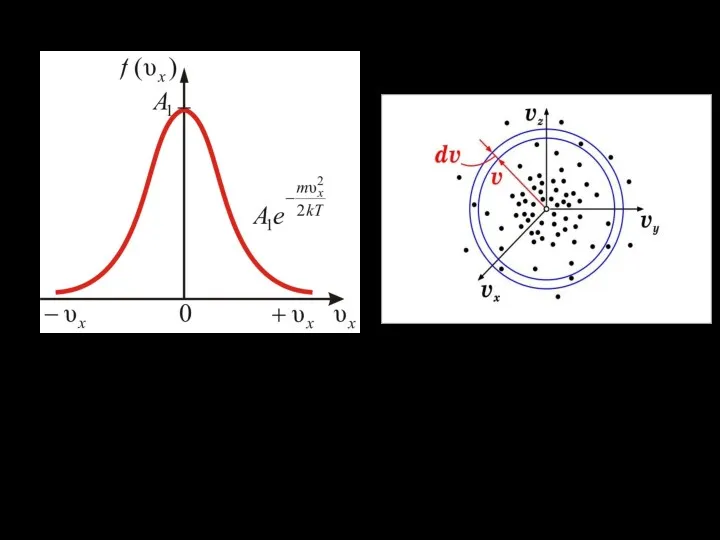

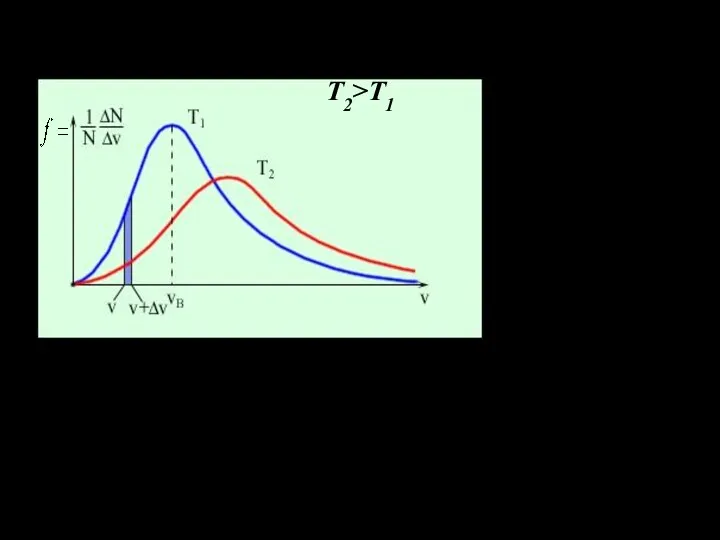
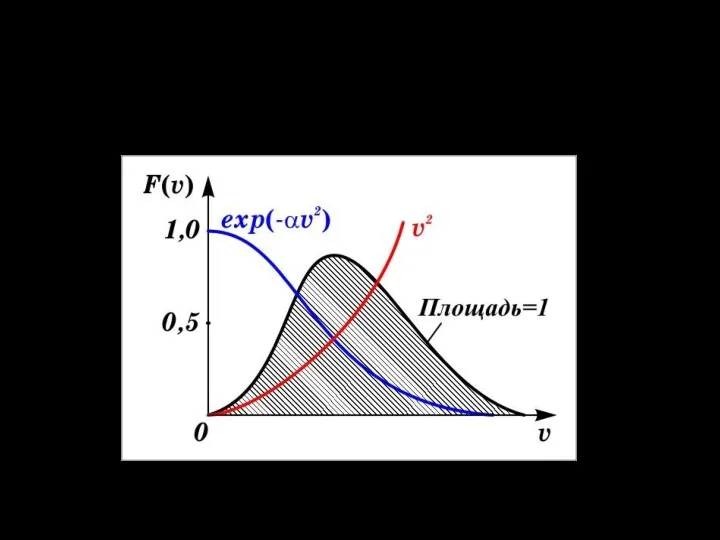




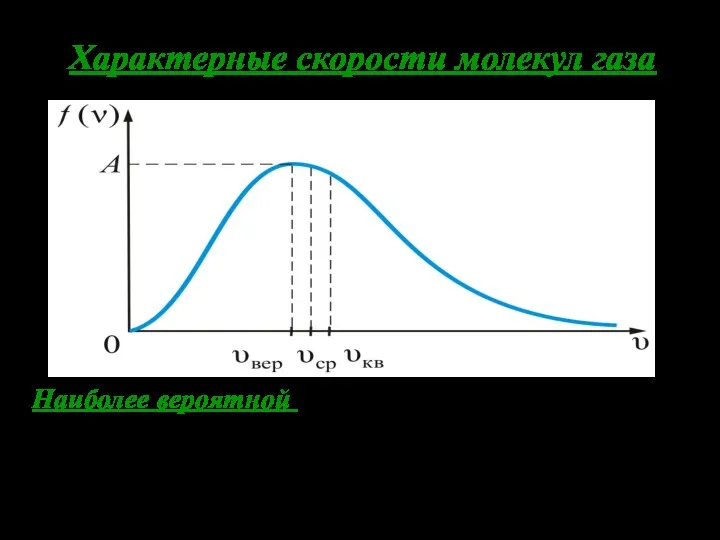


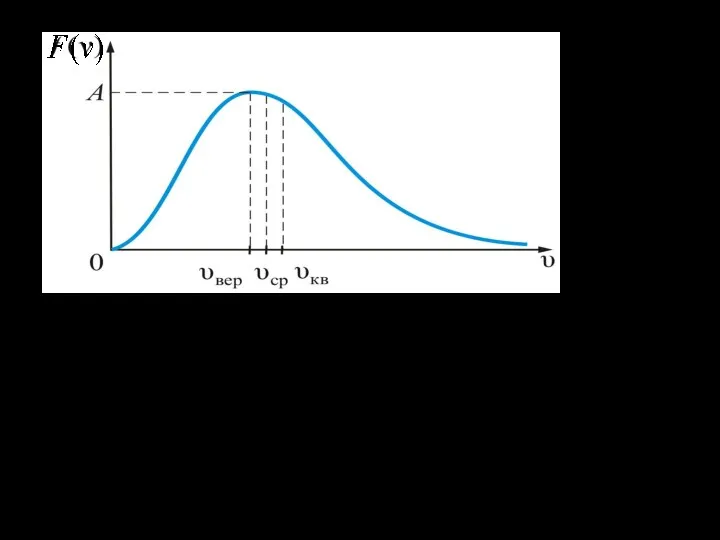
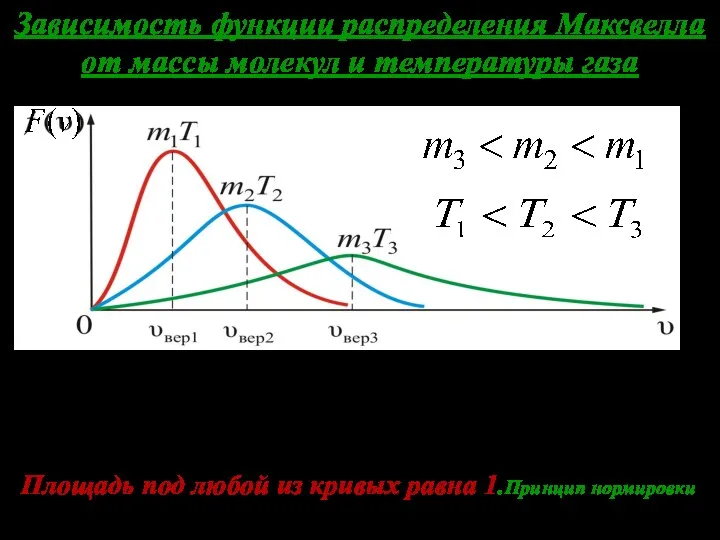
 Схема строения ракеты
Схема строения ракеты Физика, математика
Физика, математика Подготовка машин к эксплуатации
Подготовка машин к эксплуатации Представления об атоме в разных концепциях
Представления об атоме в разных концепциях ПРИМЕНЕНИЕ КОМИКСА ПРИ РАБОТЕ С УЧЕБНИКОМ
ПРИМЕНЕНИЕ КОМИКСА ПРИ РАБОТЕ С УЧЕБНИКОМ Скрипкин А., Филючков Д. Кривошипно-шатунный механизи
Скрипкин А., Филючков Д. Кривошипно-шатунный механизи Основные характеристики электротехнических материалов
Основные характеристики электротехнических материалов Электрический ток
Электрический ток Физико-химические методы анализа. Атомно эмиссионный спектральный анализ
Физико-химические методы анализа. Атомно эмиссионный спектральный анализ История зарождения квантовой физики
История зарождения квантовой физики Элементы кинетической теории газов. (Лекция 2)
Элементы кинетической теории газов. (Лекция 2) Химическая термодинамика и биоэнергетика. Второй закон термодинамики
Химическая термодинамика и биоэнергетика. Второй закон термодинамики Статика – раздел механики
Статика – раздел механики Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Quasi-optimal detectors for uwb signals
Quasi-optimal detectors for uwb signals Полупроводниковые приборы
Полупроводниковые приборы Презентация МАРИЯ СКЛОДОВСКАЯ-КЮРИ
Презентация МАРИЯ СКЛОДОВСКАЯ-КЮРИ Металл материалдардың механикалық қасиеттері: беріктік, қаттылық, майысқақтық, тұтқырлық, нәзіктік
Металл материалдардың механикалық қасиеттері: беріктік, қаттылық, майысқақтық, тұтқырлық, нәзіктік Amped 2021: How State Government is Supporting More Electric Vehicle Use in Pennsylvania
Amped 2021: How State Government is Supporting More Electric Vehicle Use in Pennsylvania Оптика. Развитие взглядов на природу света. Скорость света
Оптика. Развитие взглядов на природу света. Скорость света Экспериментальные исследования воспламенения древесины под воздействием динамического потока лучистой энергии
Экспериментальные исследования воспламенения древесины под воздействием динамического потока лучистой энергии ВКР: Організація відділення ТО і ПР кермового керування легкових автомобілів
ВКР: Організація відділення ТО і ПР кермового керування легкових автомобілів Синхронные машины
Синхронные машины Устройство и принцип действия холодильника
Устройство и принцип действия холодильника Тепломассообмен. Поперечное обтекание одиночных труб и трубных пучков
Тепломассообмен. Поперечное обтекание одиночных труб и трубных пучков Формирование навыков смыслового чтения и работы с текстом на уроках физики (Часть2)
Формирование навыков смыслового чтения и работы с текстом на уроках физики (Часть2) Передача и использование электрической энергии
Передача и использование электрической энергии Развитие систем тягового электроснабжения. Сравнение электрификации железных дорог России с другими странами
Развитие систем тягового электроснабжения. Сравнение электрификации железных дорог России с другими странами