Содержание
- 2. Цели урока: познакомиться с историей открытия нейтрона; выяснить как устроено ядро атома; познакомиться с новым видом
- 3. Подумай и ответь Вопросы 1. Какой заряд имеют α-частица, β-частица? A. α-частица - отрицательный, β-частица -
- 4. Подумай и ответь Вопросы 3. В результате β-распада новый элемент занял место в таблице Менделеева: A.
- 5. Вопросы Подумай и ответь 5. Какой прибор позволяет наблюдать следы заряженных частиц в виде полосы из
- 6. Вопросы Подумай и ответь 7. Какие частицы излучаются при указанном процессе распада A. ядро гелия. B.
- 7. Вопросы Подумай и ответь 9. β-излучение это ….. A. поток электронов. B. поток ядер атомов гелия.
- 8. Вопросы Подумай и ответь 11. В результате α - распада новый элемент занял место в таблице
- 9. Вопросы Подумай и ответь 13. Проактиний α – радиоактивен. Определите какой элемент получится в результате этого
- 10. Вопросы Подумай и ответь 15. Определите неизвестный продукт Х ядерной реакци A. B. C. 16. Определите
- 11. Вопросы Подумай и ответь 17. Определите неизвестный продукт Х ядерной реакци A. B. C. 18. Определите
- 12. Задачи Подумай и реши 19. Сколько по массе радиоактивного вещества останется по истечении шести суток, если
- 13. Открытие нейтрона Джеймсом Чедвиком в 1932 году Дж. Чедвик наблюдал в камере Вильсона треки ядер азота,
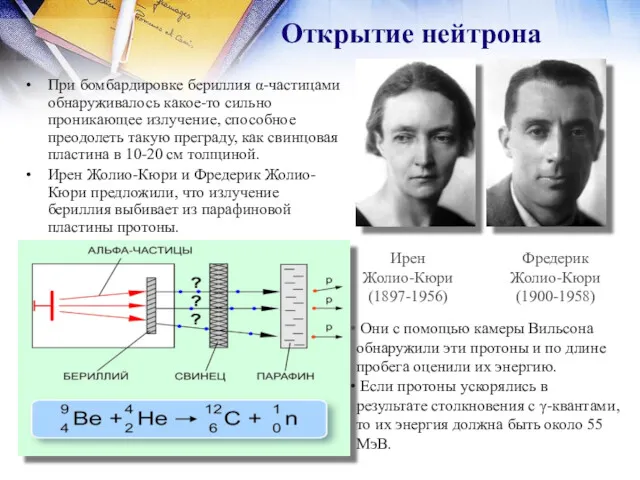
- 14. При бомбардировке бериллия α-частицами обнаруживалось какое-то сильно проникающее излучение, способное преодолеть такую преграду, как свинцовая пластина
- 15. Советский физик Д. Д. Иваненко и В. Гейзенберг предложили протонно-нейтронную модель ядра: ядра состоят из элементарных
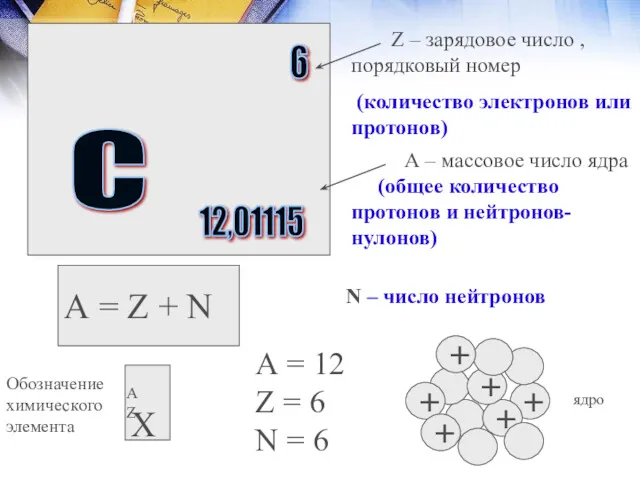
- 17. C 6 12,01115 Z – зарядовое число , порядковый номер (количество электронов или протонов) А –
- 18. Пример: Строение атома 7Li3 Электрон (е) – отрицательный заряд, вращается вокруг положительного ядра. Протон (р) –
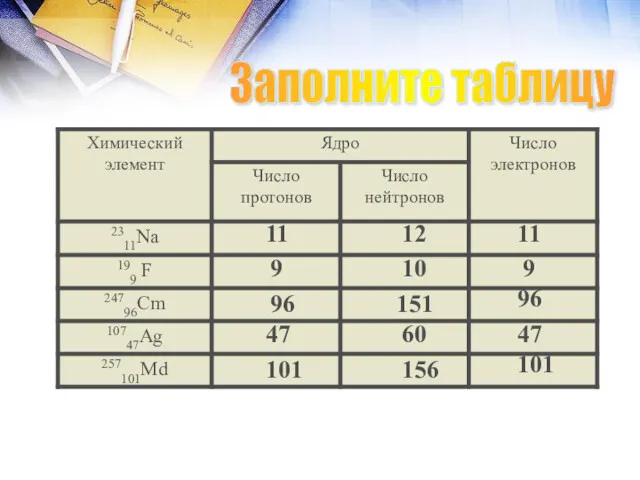
- 19. Заполните таблицу 11 12 11 9 10 9 96 151 96 47 60 47 101 156
- 20. Размеры атомных ядер Так как для ядер существенны квантовые законы поведения, то они не имеют четко
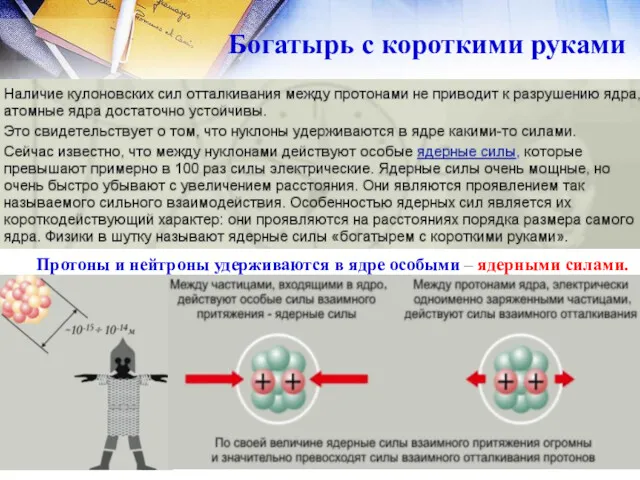
- 21. Богатырь с короткими руками Протоны и нейтроны удерживаются в ядре особыми – ядерными силами.
- 22. В 1911 г. Содди высказал предположение, что имея одинаковое строение электронных оболочек, изотопы обладают практически одинаковыми
- 23. Применение искусственных радиоактивных элементов Метод меченных атомов Применение их в металлургии, геологии, машиностроении, сельском хозяйстве, в
- 24. Применение естественных радиоактивных элементов Лечебное применение радия Применение изотопов в диагностике Определение возраста Земли
- 25. Изучив материал урока «Строение атомного ядра. Ядерные силы», проверьте свои знания, ответив на вопросы итогового тестирования.
- 26. Вопросы для закрепления Подумай и ответь 1. Нейтрон это? A. Нейтрон – это частица, которая не
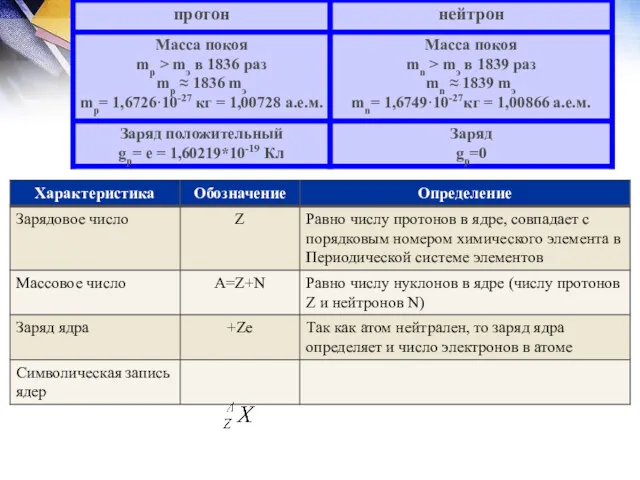
- 27. Вопросы для закрепления Подумай и ответь 3. Зарядовое число это? A. Зарядовое число – это порядковый
- 28. Вопросы для закрепления Подумай и ответь 5. Сколько нуклонов содержат ядра лития , меди , серебра
- 29. Вопросы для закрепления Подумай и ответь 7. Определите нуклонный состав ядра ? A. 8 протонов, 8
- 30. Вопросы для закрепления Подумай и ответь 9. Назовите химический элемент, в атомном ядре которого содержатся нуклоны:
- 31. Вопросы для закрепления Подумай и ответь 11. Назовите химический элемент, в атомном ядре которого содержатся нуклоны:
- 32. Домашнее задание: § 22.5 – 22.8, 22.22 с/р: подготовить сообщение об атомной энергетике
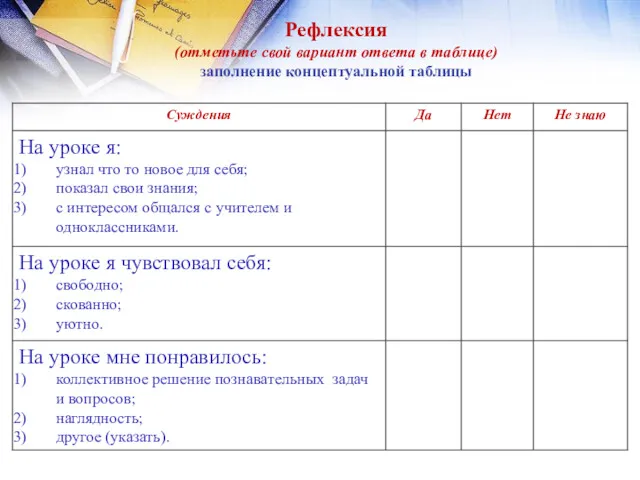
- 33. Рефлексия (отметьте свой вариант ответа в таблице) заполнение концептуальной таблицы
- 35. Скачать презентацию


























 Электростатическое поле в проводниках. Тема 4
Электростатическое поле в проводниках. Тема 4 Презентация к уроку по теме Способы изменения внутренней энергии(8 класс)
Презентация к уроку по теме Способы изменения внутренней энергии(8 класс) Применение простых механизмов
Применение простых механизмов Методы, основанные на использовании магнитного поля: спектроскопия ПМР
Методы, основанные на использовании магнитного поля: спектроскопия ПМР Что такое сила? Сила упругости
Что такое сила? Сила упругости Внеклассная работа: презентация КВН (7 класс)
Внеклассная работа: презентация КВН (7 класс) Исследовательская работа Посудомоечная машина
Исследовательская работа Посудомоечная машина Урок - исследование. Воздух и его свойства. Воздушная оболочка Земли
Урок - исследование. Воздух и его свойства. Воздушная оболочка Земли Строение атома, энергия связи атомных ядер, радиоактивность. Применение радиоактивных изотопов
Строение атома, энергия связи атомных ядер, радиоактивность. Применение радиоактивных изотопов Магнитные свойства вещества
Магнитные свойства вещества Кинематика. Виды движения
Кинематика. Виды движения Урок-лаборатория на тему Электризация. Два рода электрических зарядов Учитель физики Бейбулатова Е.А.
Урок-лаборатория на тему Электризация. Два рода электрических зарядов Учитель физики Бейбулатова Е.А. Фильтры. Направленные ответвители
Фильтры. Направленные ответвители Применение аккумуляторов
Применение аккумуляторов Теория возраста. энергия нейтрона до и после рассеяния
Теория возраста. энергия нейтрона до и после рассеяния Ходовая часть танка. Тема 13
Ходовая часть танка. Тема 13 Презентация.Реактивное движение
Презентация.Реактивное движение Проект по физике Турнир смекалистов
Проект по физике Турнир смекалистов Клиновые и шлифтовые соединения
Клиновые и шлифтовые соединения Нанотехнологии. Возникновение и развитие нанотехнологий
Нанотехнологии. Возникновение и развитие нанотехнологий Механические свойства твердых тел. Деформации. Практическое занятие 4
Механические свойства твердых тел. Деформации. Практическое занятие 4 Жартылай өткізгішті фотодиодтар
Жартылай өткізгішті фотодиодтар Физический диктант. Электромагнитные явления
Физический диктант. Электромагнитные явления Гидродинамика Солнца. (Лекция 6)
Гидродинамика Солнца. (Лекция 6) Электромагнитная индукция. Опыты Фарадея
Электромагнитная индукция. Опыты Фарадея Магнит өрісіндегі тогы бар контур
Магнит өрісіндегі тогы бар контур Ленталы конвейерлер. Ленталы конвейерлердің жалпы құрылымы
Ленталы конвейерлер. Ленталы конвейерлердің жалпы құрылымы Поршеньді компрессорларды жөндеу
Поршеньді компрессорларды жөндеу