Содержание
- 2. Вопросы к зачёту 13. Определение второго начала термодинамики. 14. Понятие замкнутой системы. 15. Понятие деградации энергии.
- 3. Вопросы к зачёту 19. Открытые системы и их свойства. 20. Понятие диссипативных структур. Примеры. 21. Понятие
- 4. Первое начало термодинамики или закон сохранения энергии ΔQ = ΔU + ΔA
- 5. Формулировка второго начала термодинамики Тепло само собой всегда переходит от более нагретого тела к более холодному
- 6. Замкнутая система Система не обменивающаяся с внешней средой ни энергией, ни веществом, ни информацией.
- 7. Формулировка второго начала термодинамики Второе начало термодинамики запрещает так называемые вечные двигатели второго родаВторое начало термодинамики
- 8. Формулировка второго начала термодинамики Постулат Клаузиуса: «Невозможен процесс, единственным результатом которого являлась бы передача тепла от
- 9. Необратимые процессы Необратимым называется процесс называется процесс, который нельзя провести в противоположном направлении через все те
- 10. Деградация энергии “Высококачественная” световая энергия превращается в энергию химических связей тканей растений, которая затем после гибели
- 11. Энтропия Энтропи́я (от греч. ἐντροπία — поворот, превращение) — мера беспорядка системы или мера хаотической составляющей
- 12. Принцип двойственности систем Все системы состоят из двух составляющих: хаотической и упорядоченной. Соотношение этих составляющих меняется
- 13. Энтропи́я Энтропи́я – мера деградации энергии, мера неупорядоченности, неопределённости, нестабильности.
- 14. Свойства замкнутой системы Энергия замкнутой системы остается постоянной. Энтропия замкнутой системы возрастает
- 15. Формула Больцмана S = k lnW Людвиг Больцман
- 16. Демон Максвелла Демон Максвелла — мысленный экспериментмысленный эксперимент 1867 года, а также его главный персонаж —
- 17. Суть парадокса Мысленный экспериментМысленный эксперимент состоит в следующем: предположим, сосуд с газомМысленный эксперимент состоит в следующем:
- 18. Суть парадокса Таким образом, получается, что демон Максвелла позволяет нагреть правую часть сосуда и охладить левую
- 19. Демон Максвелла и информация Получена она в 1928 г. американским инженером Р. Хартли. Процесс получения информации
- 20. Наименьшее количество информации 1бит – соответствует выбору одного из двух значений одной цифры при двоичной записи
- 21. Открытые системы Лекция 6
- 22. Открытые системы – системы, обменивающиеся с окружающей средой веществом, энергией и информацией. Энтропия открытой системы может
- 23. Автотрофы (др.-греч. αὐτός — сам и τροφή — пища) — живые организмы, синтезирующие органические соединения) —
- 24. Диссипативные структуры Диссипативная система (или диссипативная структура, от лат. dissipatio — «рассеиваю, разрушаю») — это открытая
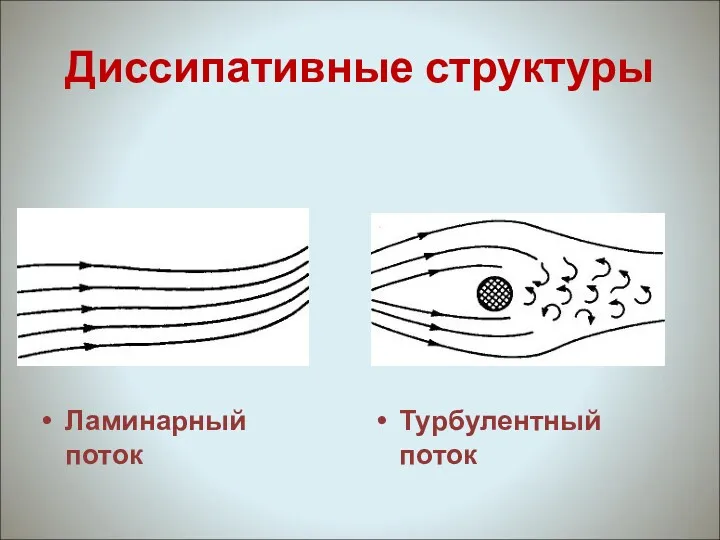
- 25. Диссипативные структуры Ламинарный поток Турбулентный поток
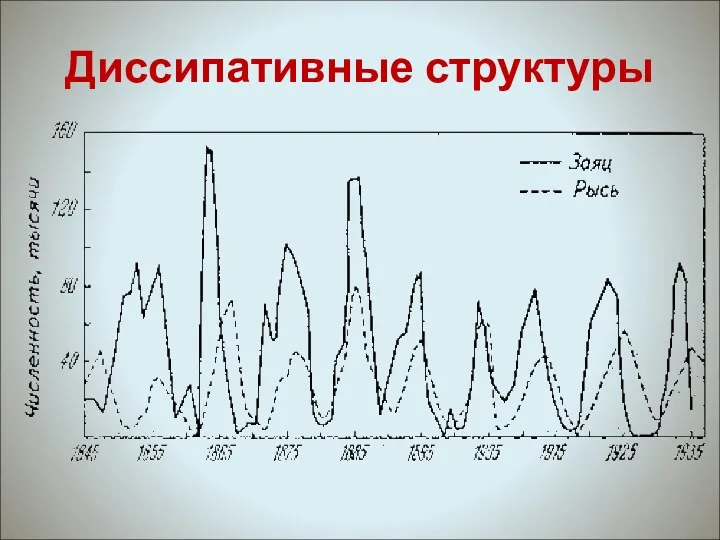
- 26. Диссипативные структуры Диссипативные структуры в экологии связаны в первую очередь с системами "хищник - жертва" или
- 27. Диссипативные структуры
- 28. Ячейки Бенара
- 29. Ячейки Бенара
- 30. Ячейки Бенара
- 31. Ячейки Бенара
- 32. Ячейки Бенара
- 33. Реакция Белоусова Жаботинского
- 34. Необходимые свойства самоорганизующихся систем Система должна быть открытой; Наличие управляющих параметров; Наличие внутрисистемных связей.
- 35. Схема процесса самоорганизации внешнее воздействие на систему; изменение управляющего параметра; изменение эффективности прежних или образование новых
- 36. Теория Дарвина и самоорганизация или от простого к сложному
- 37. Дарвин против Больцмана? Больцман против космоса?
- 38. Синергетика Синергетический подход означает эквивалентность рассмотрения процессов в различных открытых системах, из которых состоит наш мир
- 40. Скачать презентацию


































 Волновая оптика. Интерференция света
Волновая оптика. Интерференция света Магнитное поле в вакууме
Магнитное поле в вакууме Экспериментальные факты, лежащие в основе теории магнетизма
Экспериментальные факты, лежащие в основе теории магнетизма Техническое обучение по харвестерной головке Лог Макс 6000
Техническое обучение по харвестерной головке Лог Макс 6000 Плавление тел
Плавление тел Волновые свойства света: интерференция, дифракция
Волновые свойства света: интерференция, дифракция Машины для уборки и послеуборочной доработки картофеля. (Тема 13)
Машины для уборки и послеуборочной доработки картофеля. (Тема 13) Электромагнитные волны (ЭМВ)
Электромагнитные волны (ЭМВ) Микроскоп – знакомство, создание, опыты
Микроскоп – знакомство, создание, опыты Квантовая физика. Фотоэффект. Урок 29
Квантовая физика. Фотоэффект. Урок 29 Нахождение механической силы через силу и перемещение
Нахождение механической силы через силу и перемещение Кинематика твердого тела
Кинематика твердого тела Взаимозаменяемость шпоночных и шлицевых соединений
Взаимозаменяемость шпоночных и шлицевых соединений Методические рекомендации по организации экспериментальной работы на уроках физики и во внеурочное время
Методические рекомендации по организации экспериментальной работы на уроках физики и во внеурочное время использование энергии деления ядер
использование энергии деления ядер Ойын алаңы.Теориялық механика
Ойын алаңы.Теориялық механика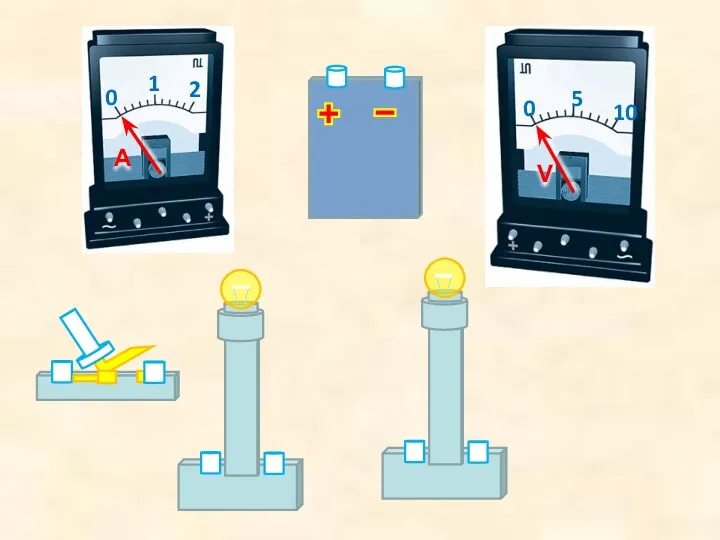 Тема урока Последовательное соединение
Тема урока Последовательное соединение Электрические источники света. Светодиодные, люминесцентные и индукционные лампы, их достоинства и недостатки
Электрические источники света. Светодиодные, люминесцентные и индукционные лампы, их достоинства и недостатки Сравнение вариантов монтажных кранов
Сравнение вариантов монтажных кранов Дефектация деталей и ремонт типовых сборочных единиц ДСМ
Дефектация деталей и ремонт типовых сборочных единиц ДСМ Кинематика. Основные понятия. Траектория. Средняя и мгновенная скорости. Ускорение. Закон равноускоренного движения
Кинематика. Основные понятия. Траектория. Средняя и мгновенная скорости. Ускорение. Закон равноускоренного движения Наноматеріали
Наноматеріали Електромагнітна індукція
Електромагнітна індукція Планирование наземной экспериментальной отработки и летных испытаний космических аппаратов
Планирование наземной экспериментальной отработки и летных испытаний космических аппаратов Техническое обслуживание и текущий ремонт двигателя, системы охлаждения и смазки
Техническое обслуживание и текущий ремонт двигателя, системы охлаждения и смазки Көміртекті нанотүтікше
Көміртекті нанотүтікше Звуковые волны
Звуковые волны Гальваническое покрытие
Гальваническое покрытие