Содержание
- 2. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА – раздел физической химии, использующий законы термодинамики для изучения энергетических эффектов, сопровождающих химические процессы,
- 3. Ответы на эти вопросы дают возможность: выбрать условия проведения реакции, при которых выход нужных продуктов был
- 4. Химические реакции, в результате которых теплота выделяется, называются экзотермическими например: процессы кристаллизации, конденсации, десублимации (газ в
- 5. Система – это совокупность находящихся во взаимодействии веществ или частиц, мысленно или фактически обособленная от окружающей
- 6. Отдельная часть системы, отделенная от других ее частей поверхностью раздела, называется фазой. Системы, состоящие из одной
- 7. Параметрами - называют переменные величины, определяющие состояние системы. (концентрация, температура, объем, давление, плотность и т.д). В
- 8. Существует два основных типа энергии – кинетическая (обусловленная движением тела) потенциальная (обусловленная положением тела или его
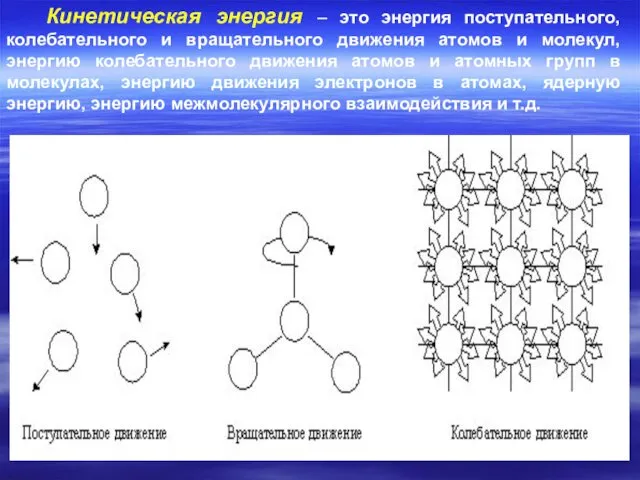
- 9. Кинетическая энергия – это энергия поступательного, колебательного и вращательного движения атомов и молекул, энергию колебательного движения
- 10. Внутренняя энергия вещества (или системы) – это полная энергия частиц, составляющих данное вещество. Она слагается из
- 11. Передача энергии, вызываемая разностью температур между системой и ее окружением или между одной системой и другой
- 12. Другой формой передачи энергии является работа - А (Дж). В химии работа чаще всего связана с
- 13. Тепловым эффектом реакции называется теплота, которая выделяется или поглощается при необратимом протекании химической реакции, причем продукты
- 14. 1. Тепловой эффект разложения какого-либо вещества равен по величине, но противоположен по знаку тепловому эффекту его
- 15. Если в результате протекания химической реакции система поглотила количество теплоты Q и совершила работу А, то
- 16. ∆Н, как и Q, называется тепловым эффектом реакции. Связь между ∆Н и Q выражается уравнением: ∆Н
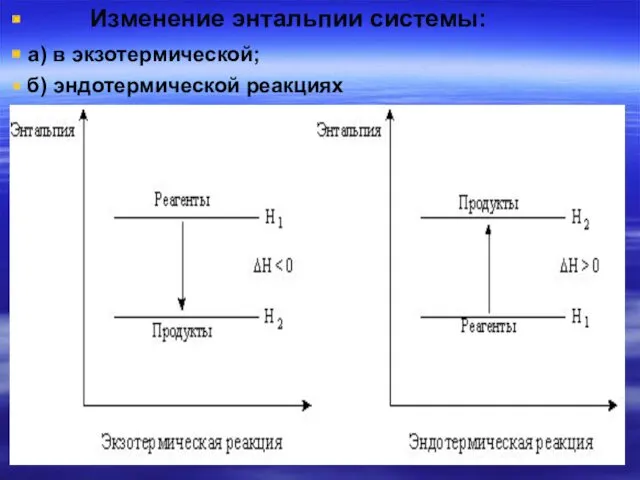
- 17. Изменение энтальпии системы: а) в экзотермической; б) эндотермической реакциях
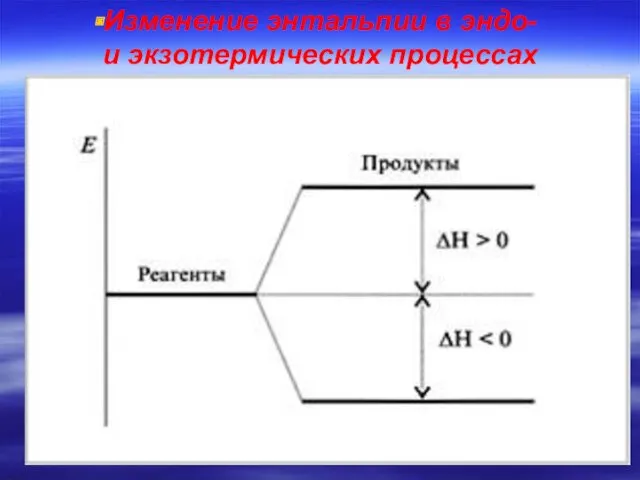
- 18. Изменение энтальпии в эндо- и экзотермических процессах
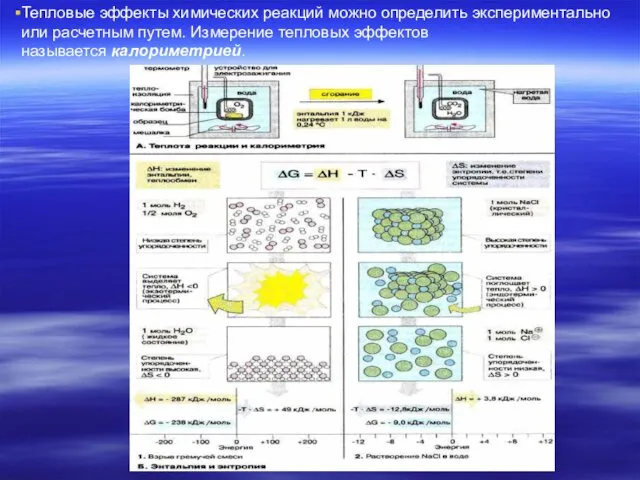
- 19. Тепловые эффекты химических реакций можно определить экспериментально или расчетным путем. Измерение тепловых эффектов называется калориметрией.
- 20. Закон Гесса Тепловой эффект реакции зависит от природы и состояния исходных веществ и конечных продуктов, но
- 21. 12 Проиллюстрируем закон на примере реакции сгорания метана: СН4 + 2О2 = СО2 + 2Н2О(Г) ∆
- 22. Экспериментально было установлено (закон Ломоносова - Лавуазье - Лапласа), что тепловые эффекты прямой и обратной реакций
- 23. 13 Следствие из закона Гесса: Изменение энтальпии системы (∆Н) в результате протекания реакции равно сумме энтальпий
- 24. Энтальпия (теплота) сгорания - это тепловой эффект сгорания 1 моль горючего вещества до продуктов предельного окисления
- 25. Стандартные энтальпии образования и стандартные энтальпии сгорания некоторых веществ
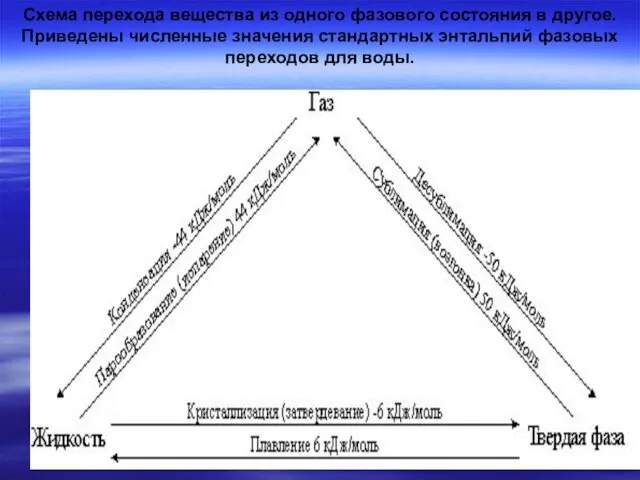
- 26. Схема перехода вещества из одного фазового состояния в другое. Приведены численные значения стандартных энтальпий фазовых переходов
- 27. Самопроизвольным называется процесс, который осуществляется без затраты работы (энергии) извне. Направление диффузии вещества от большей концентрации
- 28. - растворение хлорида калия в воде: KCl(т) н2о KCl(р) ; ∆H°(298 К) = 19 кДж/моль; -
- 29. 14 Мерой неупорядоченности системы служит термодинамическая функция – энтропия. Энтропи́я (от греч. εντροπία — поворот, превращение)
- 30. Способы распределения молекул по двум половинам сосуда S = k * lgW
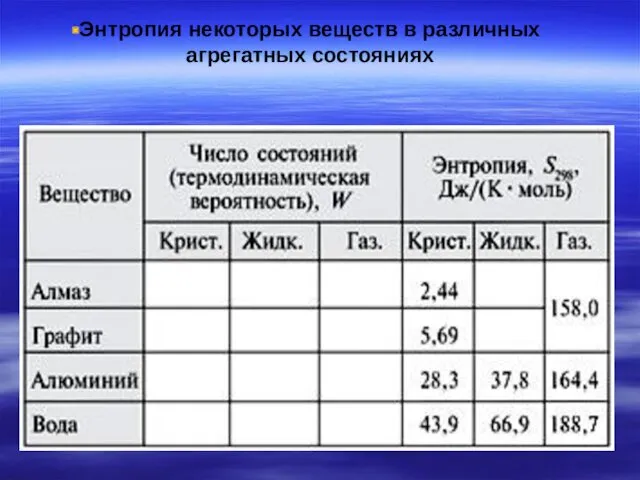
- 31. Энтропия некоторых веществ в различных агрегатных состояниях
- 32. Энтропия – экстенсивный параметр системы. Поэтому чем больше в ней вещества, тем больше ее энтропия. Чем
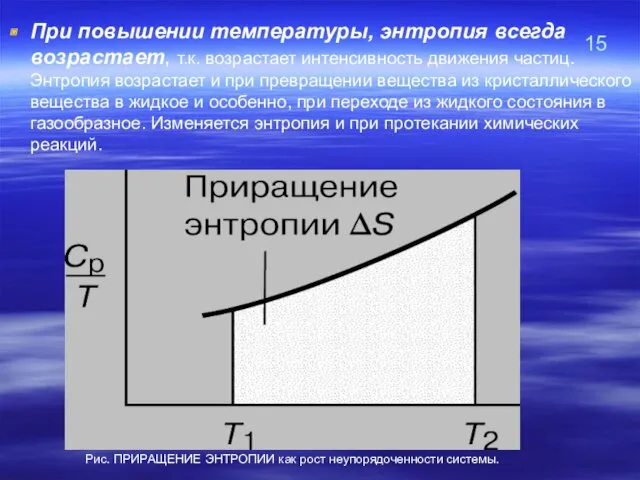
- 33. 15 При повышении температуры, энтропия всегда возрастает, т.к. возрастает интенсивность движения частиц. Энтропия возрастает и при
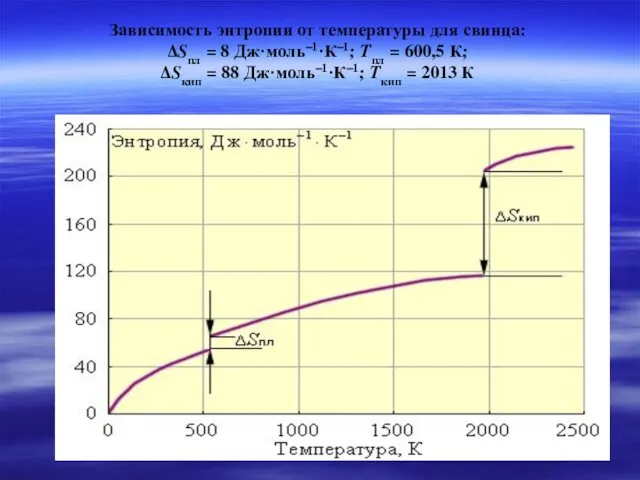
- 34. Зависимость энтропии от температуры для свинца: ΔSпл = 8 Дж·моль–1·К–1; Tпл = 600,5 К; ΔSкип =
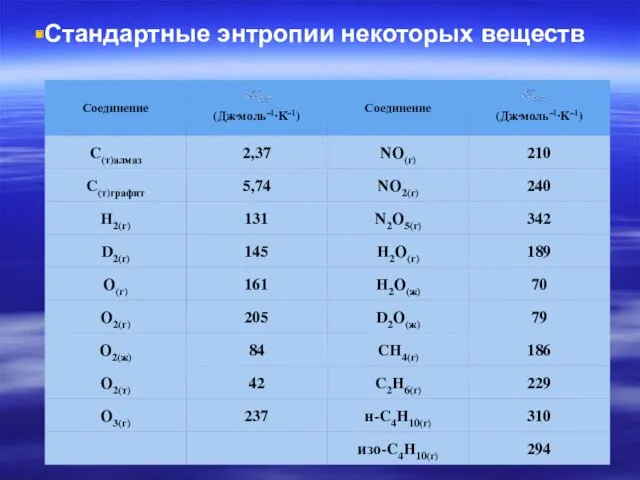
- 35. Стандартные энтропии некоторых веществ
- 36. -агрегатного состояния вещества, энтропия увеличивается при переходе от твердого к жидкому и особенно к газообразному состоянию
- 37. 16 Изменение энтропии системы (ΔS) в результате протекания химической реакции равно сумме энтропий продуктов реакции за
- 38. 17 Первый закон термодинамики утверждает, что энергия не может быть создана или уничтожена, а может лишь
- 39. Джозайя Вилард Гиббс родился 11 февраля 1839 г. в Нью-Гевене, штат Коннектикут, в семье профессора Гейльского
- 41. 18 Изобарно-изотермический потенциал (энергия Гиббса). ΔG = ∆Н - Т∆S F = U – TS или
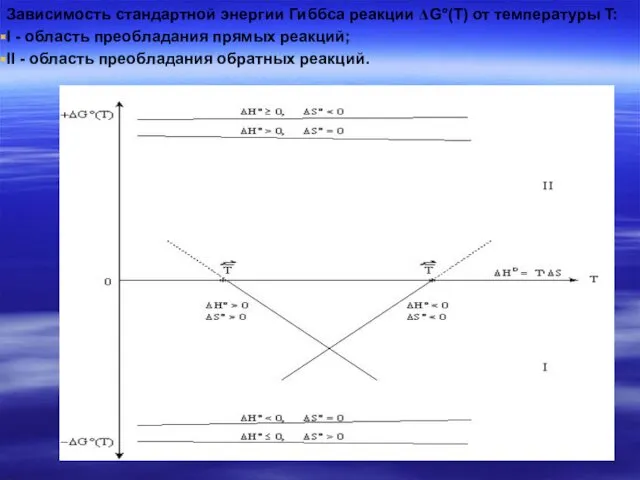
- 42. Зависимость стандартной энергии Гиббса реакции ΔG°(Т) от температуры T: I - область преобладания прямых реакций; II
- 43. Изобарно-изотермический потенциал (энергия Гиббса). ΔG = ∆Н - Т∆S
- 44. 19 При постоянстве температуры и давления химическая реакция принципиально возможна, если энергия Гиббса уменьшается: ΔG Химическая
- 45. ΔG = ∆Н - Т∆S
- 47. Скачать презентацию


































 Чистые вещества и смеси
Чистые вещества и смеси Вода-растворитель. Работа воды в природе
Вода-растворитель. Работа воды в природе Щелочные металлы
Щелочные металлы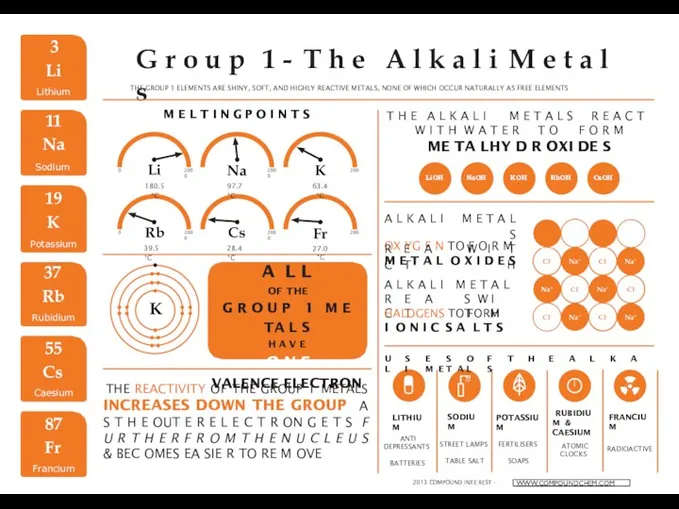 The alkali metals
The alkali metals Предмет органической химии
Предмет органической химии Приготування розчинів
Приготування розчинів Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Энергоресурсы и их использование
Энергоресурсы и их использование Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології
Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології Химические соединения в организме человека
Химические соединения в организме человека Углеводы. Моносахариды
Углеводы. Моносахариды Карбоновые кислоты. Нахождение в природе
Карбоновые кислоты. Нахождение в природе Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений
Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений Химические формулы
Химические формулы Задачі на визначення ступеню електролітичної дисоціації
Задачі на визначення ступеню електролітичної дисоціації Закон збереження маси речовини. Хімічні рівняння
Закон збереження маси речовини. Хімічні рівняння Методы составления уравнений окислительно-восстановительных реакций. Лекция №20
Методы составления уравнений окислительно-восстановительных реакций. Лекция №20 История мыловарения. Моющее действие мыла
История мыловарения. Моющее действие мыла Чистые вещества и смеси
Чистые вещества и смеси Подготовка к ГИА. В3. Степень окисления химических элементов. Окислительно-восстановительные реакции
Подготовка к ГИА. В3. Степень окисления химических элементов. Окислительно-восстановительные реакции Добування кисню
Добування кисню Основы теории смазывания и стандарты качества моторных масел
Основы теории смазывания и стандарты качества моторных масел Гидроксид аммония
Гидроксид аммония Structural revision of (+)-uprolide F diacetate confirmed by asymmetric total synthesis
Structural revision of (+)-uprolide F diacetate confirmed by asymmetric total synthesis Кислород O2
Кислород O2 Химия и живопись
Химия и живопись Кислородные соединения азота
Кислородные соединения азота Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату