Слайд 2

Водород самый распространенный элемент во вселенной
Слайд 3

История открытия
Впервые этот газ в чистом виде выделил 240 лет назад
английский химик Генри Кавендиш. Свойства полученного им газа были настолько удивительны, что ученый принял его за легендарный «флогистон», «теплород» — вещество, по канонам науки того времени определявшее температуру тел. Он прекрасно горел (а огонь считался почти чистым флогистоном), был необычайно легок, в 15 раз легче воздуха, хорошо впитывался металлами и так далее.
Слайд 4

Другой великий химик, француз Антуан-Лоран Лавуазье, уже в 1787 году доказал,
что полученное Кавендишем вещество — вполне обычный, хотя и очень интересный химический элемент. Свое название он получил оттого, что при горении давал не дым, сажу и копоть, а воду.
Слайд 5

Общая характеристика:
Водород занимает первое место в периодической системе (Z = 1).
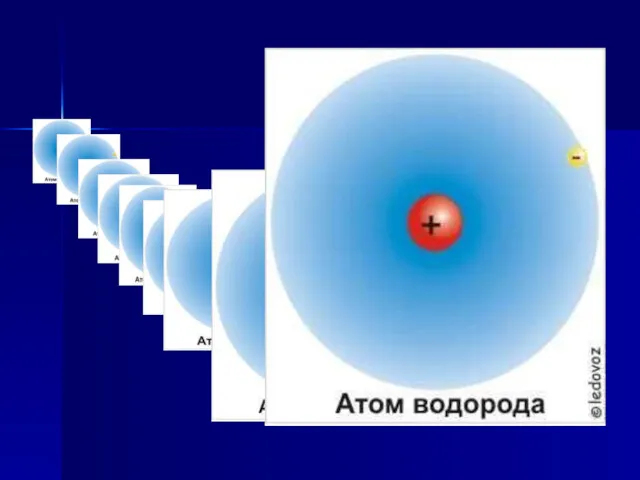
Он имеет простейшее строение атома: ядро атома окружено электронным облаком. Электронная конфигурация 1s1.
В одних условиях водород проявляет металлические свойства (отдает электрон), в других — неметаллические (принимает электрон). Однако по свойствам он более сходен с галогенами, чем со щелочными металлами. Поэтому водород помещают в VII группу периодической системы элементов Д.И. Менделеева, а в I группе символ водорода заключают в скобки.
Слайд 6
Слайд 7

Водород в природе:
Водород широко распространен в природе — содержится в воде,
во всех органических соединениях, в свободном виде — в некоторых природных газах. Содержание его в земной коре достигает 0,15% ее массы (с учетом гидросферы — 1%). Водород составляет половину массы Солнца.
Слайд 8

Каждую секунду Солнце излучает в космическое пространство энергию, эквивалентную примерно 4 млн т
массы. Эта энергия рождается в ходе слияния четырех ядер водорода, протонов, в ядро гелия;
Слайд 9
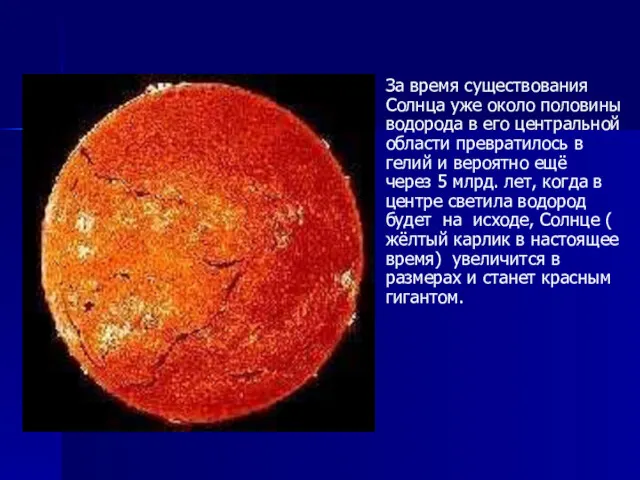
За время существования Солнца уже около половины водорода в его центральной
области превратилось в гелий и вероятно ещё через 5 млрд. лет, когда в центре светила водород будет на исходе, Солнце ( жёлтый карлик в настоящее время) увеличится в размерах и станет красным гигантом.
Слайд 10

Молекула водорода
Молекула водорода состоит из двух атомов. Возникновение связи между
ними объясняется образованием обобщенной пары электронов (или общего электронного облака):
Н:Н или Н2
Благодаря этому обобщению электронов молекула Н2 более энергетически устойчива, чем его отдельные атомы. Чтобы разорвать в 1 моль водорода молекулы на атомы, необходимо затратить энергию 436 кДж:
Н2 = 2Н, ∆H° = 436 кДж/моль
Этим объясняется сравнительно небольшая активность молекулярного водорода при обычной температуре.
Слайд 11

Физические свойства.
Водород — это самый легкий газ (он в 14,4 раза
легче воздуха), не имеет цвета, вкуса и запаха. Мало растворим в воде (в 1 л воды при 20°С растворяется 18 мл водорода). При температуре — 252,8°С и атмосферном давлении переходит в жидкое состояние. Жидкий водород бесцветен.
Кроме водорода с массовым числом 1 существуют изотопы с массовыми числами 2 и 3 — дейтерий D и тритий Т.
ГазообразныйГазообразный водород может существовать в двух формах (модификациях) — в виде ортоГазообразный водород может существовать в двух формах (модификациях) — в виде орто- и пара- водорода.
В молекуле ортоводорода (т. пл. -259,20 °С, т. кип. -252,76 °С) ядерные спины направлены одинаково (параллельны), а у параводорода (т. пл. -259,32 °С, т. кип. -252,89 °С) — противоположно друг другу (антипараллельны).
Слайд 12
Слайд 13
Получение:
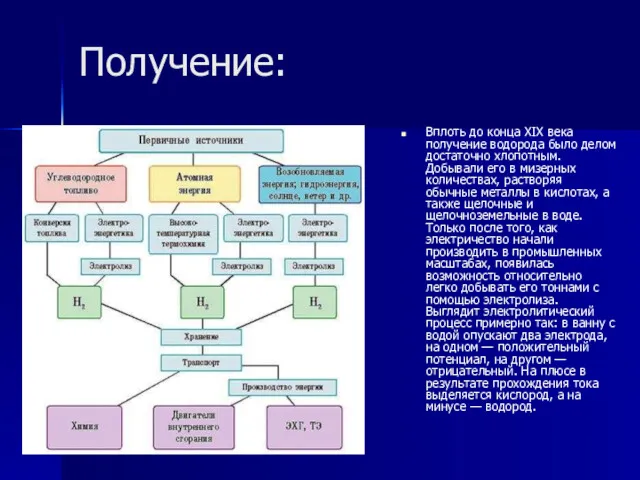
Вплоть до конца XIX века получение водорода было делом достаточно хлопотным.
Добывали его в мизерных количествах, растворяя обычные металлы в кислотах, а также щелочные и щелочноземельные в воде. Только после того, как электричество начали производить в промышленных масштабах, появилась возможность относительно легко добывать его тоннами с помощью электролиза. Выглядит электролитический процесс примерно так: в ванну с водой опускают два электрода, на одном — положительный потенциал, на другом — отрицательный. На плюсе в результате прохождения тока выделяется кислород, а на минусе — водород.
Слайд 14

Эксперимент по получению водорода из воды с помощью солнечной энергии
Слайд 15

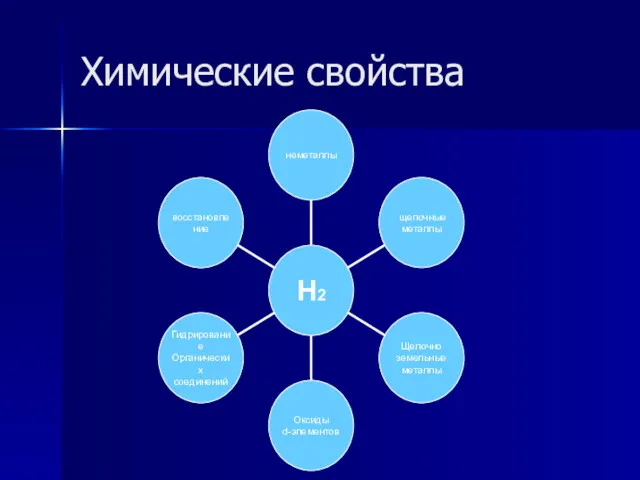
Применение:
Наработав в достаточном количестве этот легкий газ, люди сначала приспособили его
для воздушных полетов. В этом качестве первый элемент Таблицы Менделеева применяли вплоть до 1937 года, когда в воздухе сгорел крупнейший в мире, в два футбольных поля размером, заполненный водородом немецкий дирижабль «Гинденбург». Катастрофа унесла жизни 36 человек, и на таком использовании водорода был поставлен крест. С тех пор аэростаты заправляют исключительно гелием. Гелий — газ, увы, более плотный, но зато негорючий. .
Слайд 16

Водородная энергетика
В недалёком будущем основным источником получения энергии станет реакция горения
водорода, и водородная энергетикаВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (угольВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (уголь, нефтьВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (уголь, нефть и др.). При этом предполагалось, что для получения водорода в больших масштабах можно будет использовать электролиз воды.
Слайд 17

Водородные автомобили
В 1979 году компания BMW выпустила первый автомобиль, вполне успешно
ездивший на водороде, при этом не взрывавшийся и выпускавший из выхлопной трубы водяной пар. В эпоху усиливающейся борьбы с вредными выхлопами машина была воспринята как вызов консервативному автомобильному рынку. Вслед за BMW в экологическую сторону потянулись и другие производители. К концу века каждая уважающая себя автокомпания имела в запаснике хотя бы один концепт-кар, работающий на водородном топливе.
Слайд 18

Слайд 19

Водород и будущее
Слова «дейтерий» и «тритий» напоминают нам о том, что
сегодня человек располагает мощнейшим источником энергии, высвобождающейся при реакции:
21Н + 31Н → 42Не +10n + 17,6 МэВ.
Эта реакция начинается при 10 млн градусов и протекает за ничтожные доли секунды при взрыве термоядерной бомбы, причем выделяется гигантское по масштабам Земли количество энергии.
Водородные бомбы иногда сравнивают с Солнцем. Однако мы уже видели, что на Солнце идут медленные и стабильные термоядерные процессы. Солнце дарует нам жизнь, а водородная бомба – сулит смерть...
Слайд 20

Но когда-нибудь настанет время – и это время не за горами,
– когда мерилом ценности станет не золото, а энергия. И тогда изотопы водорода спасут человечество от надвигающегося энергетического голода: в управляемых термоядерных процессах каждый литр природной воды будет давать столько же энергии, сколько ее дают сейчас 300 л бензина. И человечество будет с недоумением вспоминать, что было время, когда люди угрожали друг другу животворным источником тепла и света...
Слайд 21

ДОМАШНЕЕ ЗАДАНИЕ:
прочитать § 40 Учебника, ответить на вопросы:
1. Чем различаются водородные
соединения металлов и неметаллов?
2. Какие закономерности наблюдлаются в изменении свойств летучих водородных соединений в периодах и группах?
3. Охарактеризуйте сущность изменения свойств.




















 Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Основные характеристи нефти и нефтеподуктов
Основные характеристи нефти и нефтеподуктов Задачи
Задачи Ненасыщенные (непредельные) алифатические углеводороды. Алкены
Ненасыщенные (непредельные) алифатические углеводороды. Алкены Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Электрохимические процессы. Лекция 7
Электрохимические процессы. Лекция 7 Современные положения теории А.М. Бутлерова
Современные положения теории А.М. Бутлерова Введение. Теория строения органических соединений А.М.Бутлерова. Лекция № 1
Введение. Теория строения органических соединений А.М.Бутлерова. Лекция № 1 Свойства минералов
Свойства минералов Минералы и горные породы
Минералы и горные породы Розчин і його компоненти
Розчин і його компоненти Химические процессы зоны гипергенеза
Химические процессы зоны гипергенеза Алициклді көмірсутекті қосылыстар
Алициклді көмірсутекті қосылыстар Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Изомерия. Типы изомерии
Изомерия. Типы изомерии Минералдар
Минералдар c0198e3edf1db804a5527004a7864ed1
c0198e3edf1db804a5527004a7864ed1 ФОСФОР и его соединения
ФОСФОР и его соединения Предельные углеводороды
Предельные углеводороды Мына қосылыстардағы элементтердің тотығу дәрежелерін анықтаңдар
Мына қосылыстардағы элементтердің тотығу дәрежелерін анықтаңдар Химические реакции. Классификация химических реакций
Химические реакции. Классификация химических реакций Водород
Водород Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Колоїдний захист
Колоїдний захист Предмет органической химии
Предмет органической химии Физические свойства металлов
Физические свойства металлов