Содержание
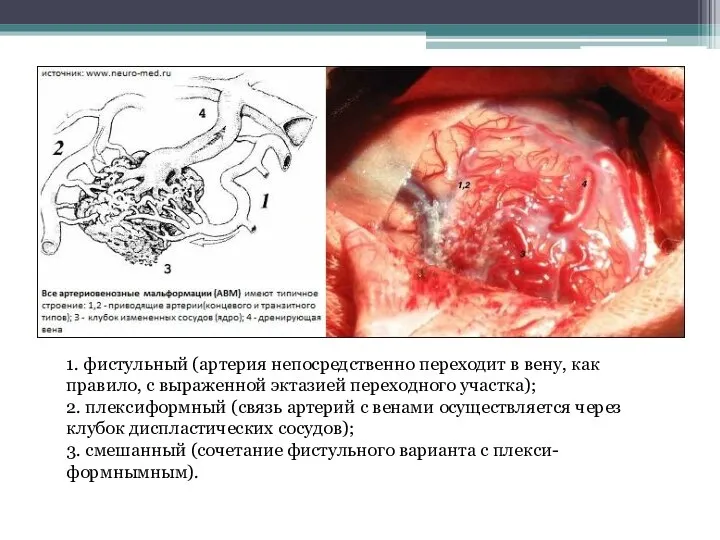
- 2. Артериовенозные мальформации (АВМ) представляют собой неправильное соединение артериальных и венозных сосудов, формирующих ядро, минуя капиллярную сеть.
- 3. 1. фистульный (артерия непосредственно переходит в вену, как правило, с выраженной эктазией переходного участка); 2. плексиформный
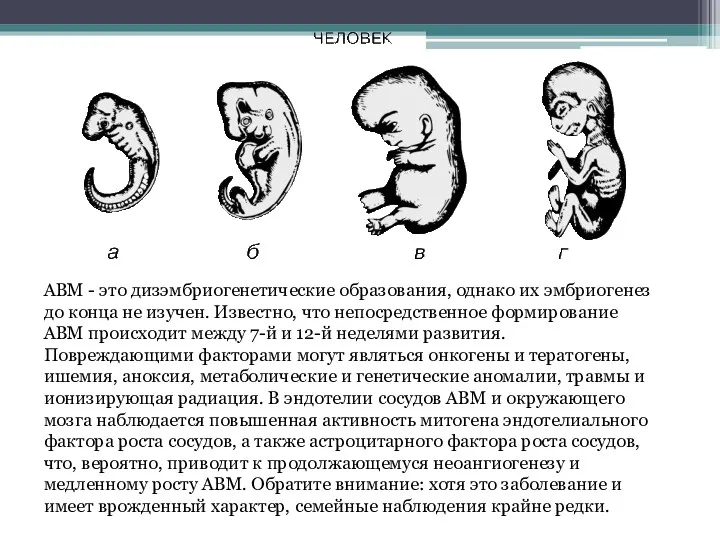
- 4. АВМ - это дизэмбриогенетические образования, однако их эмбриогенез до конца не изучен. Известно, что непосредственное формирование
- 5. АВМ могут обнаруживаться в любых отделах центральной нервной системы пропорционально объему мозговой ткани: От 70 до
- 6. АВМ представляют из себя клубки различного размера и формы, состоящие из порочно развитых сосудов различного диаметра.
- 7. Классификация По размерам АВМ подразделяются: микро ( малые (2 - 5 см3), средние (5 - 20
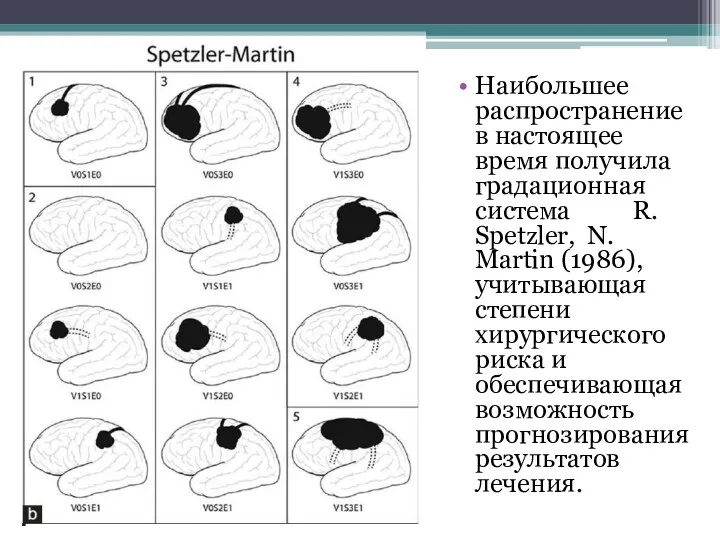
- 8. Наибольшее распространение в настоящее время получила градационная система R. Spetzler, N. Martin (1986), учитывающая степени хирургического
- 9. по размеру: менее 3 см в одном из размеров - 1 балл, 3 - 6 см
- 10. По данной градации АВМ разделяются на 5 типов: 1, 2 балла - АВМ низкого хирургического риска;
- 11. Клиника. Выделяют два варианта клинического течения АВМ: Торпидный (псевдотуморозный); Геморрагический;
- 12. Торпидный (псевдотуморозный): характеризуется дебютом судорожного синдрома, кластерных головных болей, симптоматики объемного поражения мозга или прогрессирующего неврологического
- 13. торпидный тип течения более характерен для крупных АВМ категории 4 и 5 по Spetzler-Martin - это
- 14. Крайне редко патогенез клинических проявлений в виде нарастающего неврологического дефицита связан с явлениями синдрома обкрадывания, который
- 15. Геморрагический: отмечается в 30 - 87% наблюдений всех АВМ, преимущественно характерен для категорий 1 - 3
- 16. Примерно в половине случаев этот тип течения АВМ осложняется развитием внутричерепных гематом на фоне субарахноидальных и(или)
- 17. К основным факторам риска кровотечения из АВМ относятся: ранее перенесенное кровоизлияние; единственная дренирующая вена; диффузное строение
- 18. В детском возрасте Клинически себя проявляют лишь 20 - 30% АВМ. Они служат причиной нетравматического субарахноидального
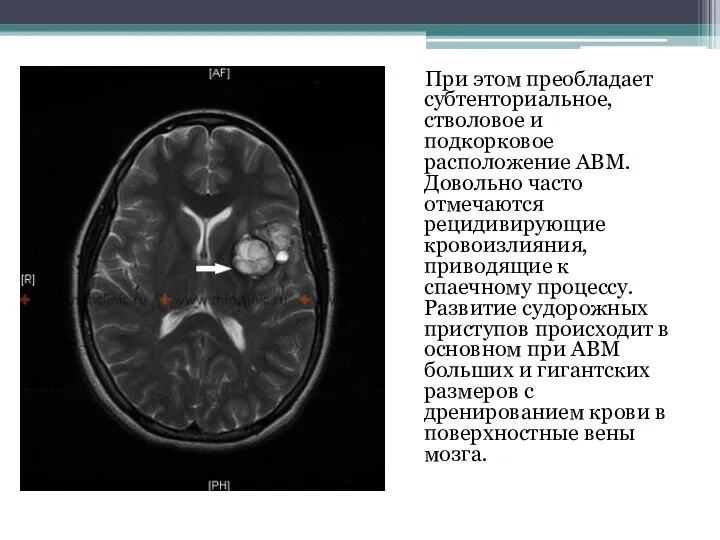
- 19. При этом преобладает субтенториальное, стволовое и подкорковое расположение АВМ. Довольно часто отмечаются рецидивирующие кровоизлияния, приводящие к
- 20. Характер приступов зависит от локализации АВМ. При расположении в передних отделах коры больших полушарий возникают преимущественно
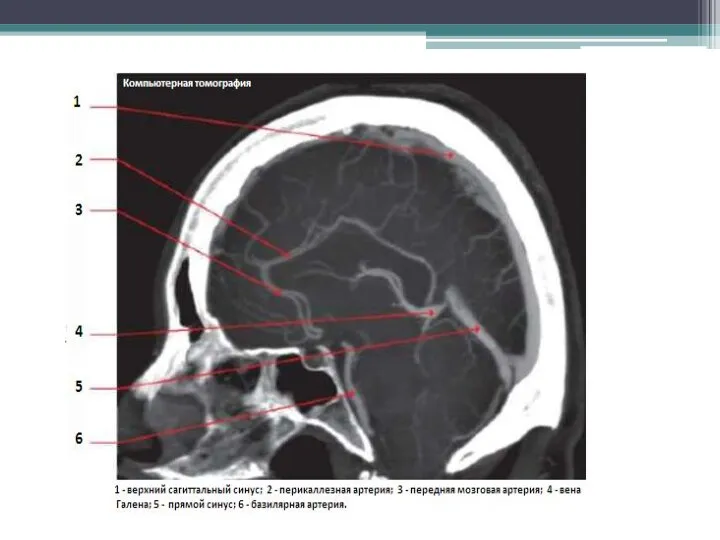
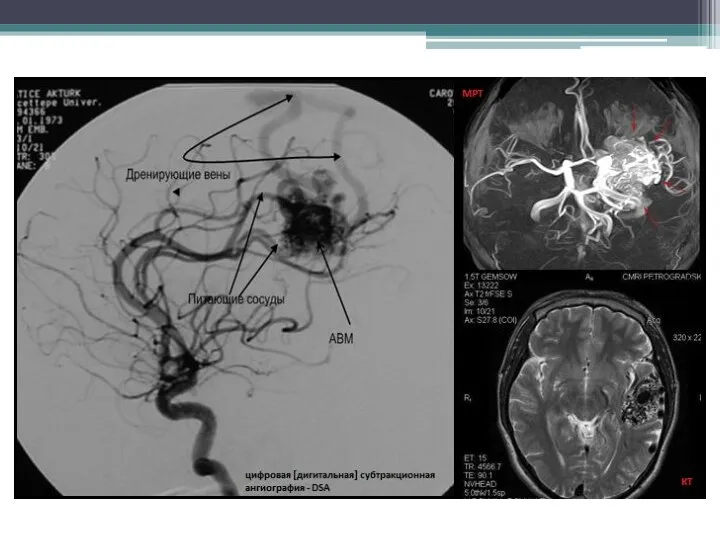
- 22. Диагностика: АВМ головного мозга проявляются характерными признаками по данным МРТ. МРТ характеризуется высокой чувствительностью в выявлении
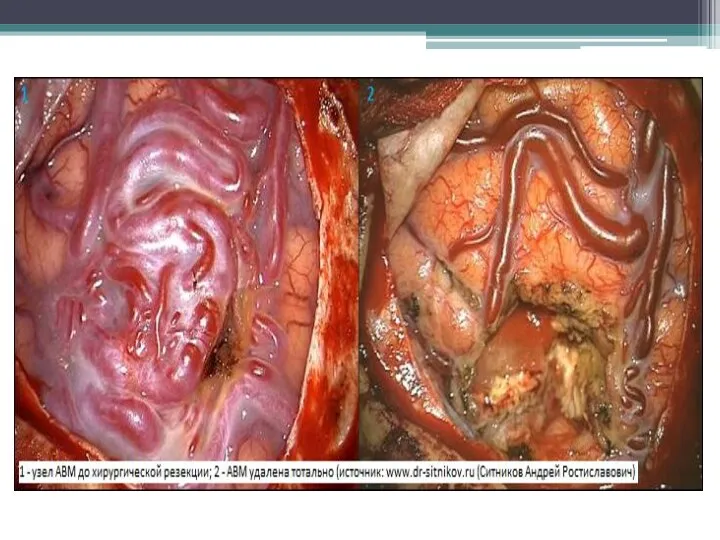
- 24. Лечение: Современные принципы лечения больных АВМ сводятся к комплексному использованию методов микронейрохирургии, эндоваскулярной хирургии и радиохирургии,
- 25. Основной задачей любого вида вмешательства является полное выключение патологической сосудистой сети мальформации для профилактики внутричерепных кровоизлияний
- 27. При формировании внутричерепной гематомы вследствие разрыва АВМ, когда тяжесть состояния больного прогрессивно нарастает (что обусловлено сдавлением,
- 29. Скачать презентацию


















 Паразитарные заболевания кожи
Паразитарные заболевания кожи Приобретенные (вторичные) иммунодефициты
Приобретенные (вторичные) иммунодефициты Этиология дизартрии
Этиология дизартрии Зарядка для глаз
Зарядка для глаз Вирусные кишечные инфекции
Вирусные кишечные инфекции Клиническая фармакология препаратов для лечения ЖКТ
Клиническая фармакология препаратов для лечения ЖКТ Помощь при обструкции дыхательных путей. Приём Хеймлиха
Помощь при обструкции дыхательных путей. Приём Хеймлиха Дискинезии желчевыводящих путей у детей
Дискинезии желчевыводящих путей у детей Алергозы. Этиология и патогенез
Алергозы. Этиология и патогенез Современный алгоритм диспансерного регламента для детей с врожденной патологией челюстно-лицевой области
Современный алгоритм диспансерного регламента для детей с врожденной патологией челюстно-лицевой области Наследственность. Генетика человека. Часть 2
Наследственность. Генетика человека. Часть 2 Психическое расстройство депрессия
Психическое расстройство депрессия Клиническая биохимия щитовидной железы
Клиническая биохимия щитовидной железы Инфузионная терапия в детской инфекционной патологии
Инфузионная терапия в детской инфекционной патологии Хирургическое лечение портальной гипертензии и её осложнений
Хирургическое лечение портальной гипертензии и её осложнений Повреждения наружных половых органов
Повреждения наружных половых органов Сухожильный шов
Сухожильный шов Бронхобструктивті синдром
Бронхобструктивті синдром Репродуктивное здоровье и профилактика репродуктивных нарушений
Репродуктивное здоровье и профилактика репродуктивных нарушений Aberration of normal development and involution (andi) of thebreast
Aberration of normal development and involution (andi) of thebreast Спектроскопия и оптическая биопсия в медицине. Аутофлуоресценция клеток
Спектроскопия и оптическая биопсия в медицине. Аутофлуоресценция клеток Сульфаниламидные средства
Сульфаниламидные средства Гепатит С
Гепатит С 7 советов о здоровом питании
7 советов о здоровом питании Вегетарианство
Вегетарианство Особенности работы медицинской сестры офтальмологического отделения
Особенности работы медицинской сестры офтальмологического отделения Пероральные лекарственные формы с модифицированным высвобождением
Пероральные лекарственные формы с модифицированным высвобождением Методы индивидуальной и коммунальной профилактики стом заболеваний у детей и взрослых
Методы индивидуальной и коммунальной профилактики стом заболеваний у детей и взрослых