Содержание
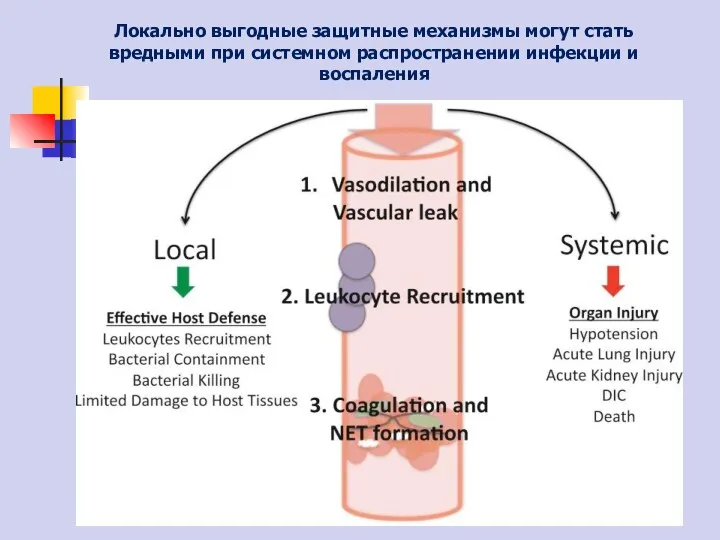
- 2. Локально выгодные защитные механизмы могут стать вредными при системном распространении инфекции и воспаления
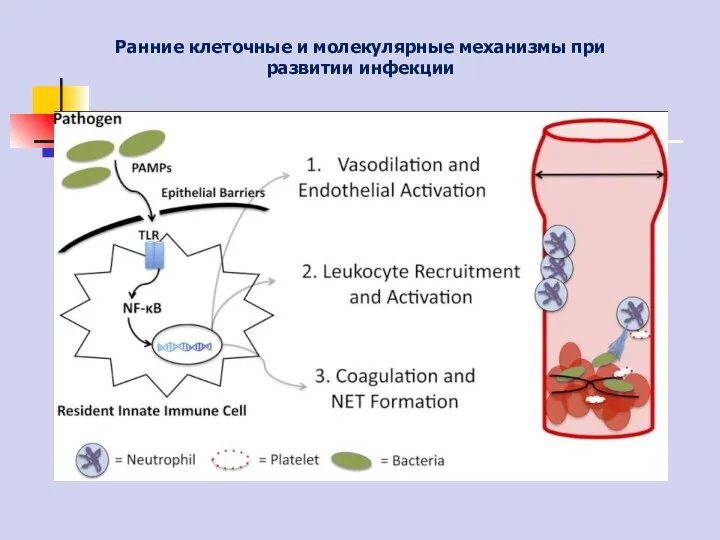
- 3. Ранние клеточные и молекулярные механизмы при развитии инфекции
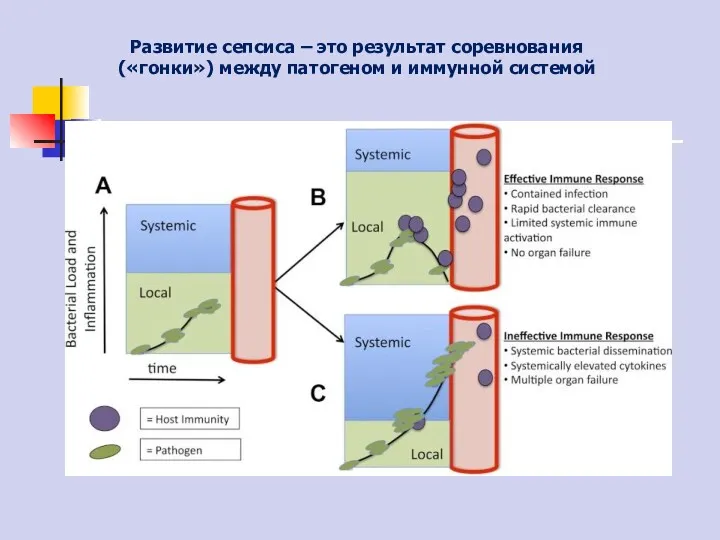
- 4. Развитие сепсиса – это результат соревнования («гонки») между патогеном и иммунной системой
- 5. «За исключением некоторых случаев, пациент скорее умирает от ответа организма на инфекцию, чем от самой инфекции»
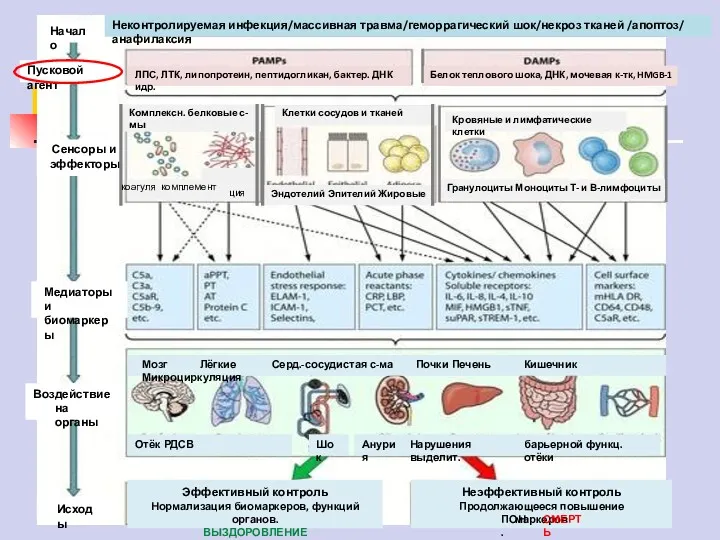
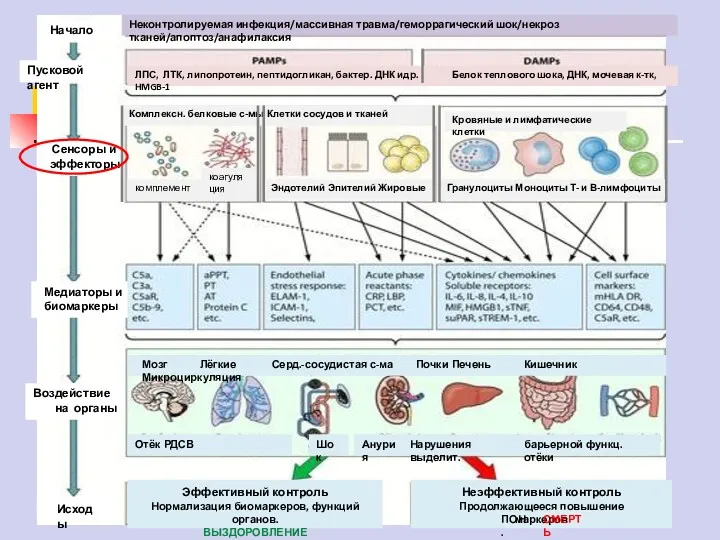
- 6. Неконтролируемая инфекция/массивная травма/геморрагический шок/некроз тканей /апоптоз/ анафилаксия ЛПС, ЛТК, липопротеин, пептидогликан, бактер. ДНК идр. Белок теплового
- 7. Неконтролируемая инфекция/массивная травма/геморрагический шок/некроз тканей/апоптоз/анафилаксия ЛПС, ЛТК, липопротеин, пептидогликан, бактер. ДНК идр. Белок теплового шока, ДНК,
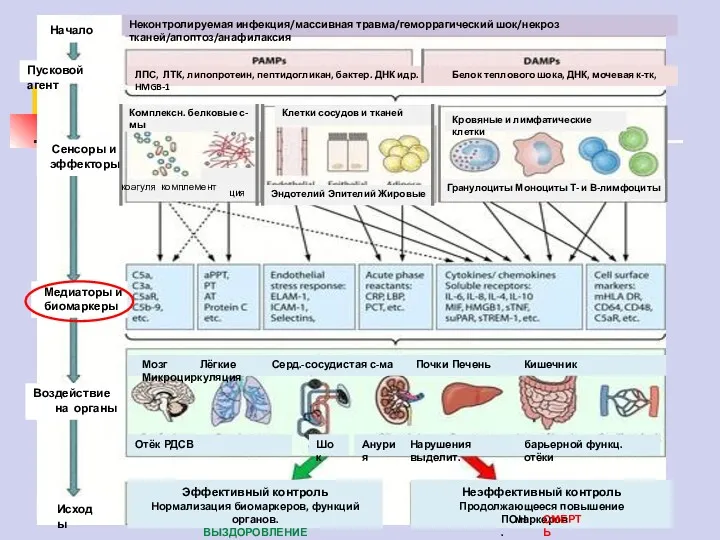
- 8. Неконтролируемая инфекция/массивная травма/геморрагический шок/некроз тканей/апоптоз/анафилаксия ЛПС, ЛТК, липопротеин, пептидогликан, бактер. ДНК идр. Белок теплового шока, ДНК,
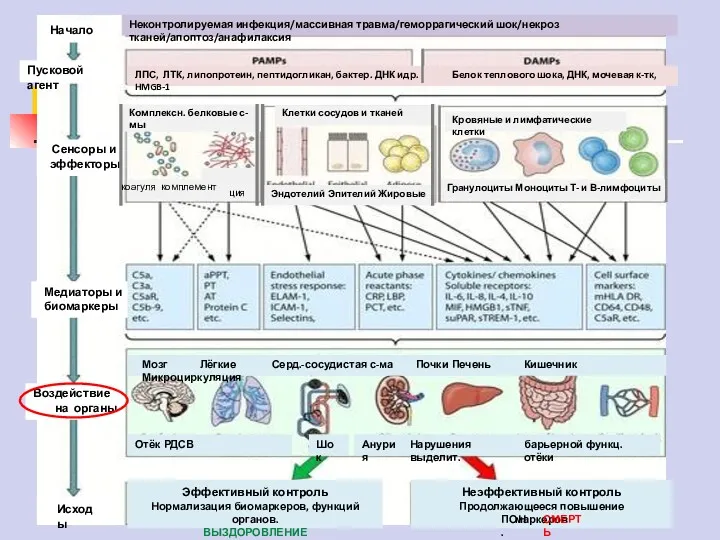
- 9. Неконтролируемая инфекция/массивная травма/геморрагический шок/некроз тканей/апоптоз/анафилаксия ЛПС, ЛТК, липопротеин, пептидогликан, бактер. ДНК идр. Белок теплового шока, ДНК,
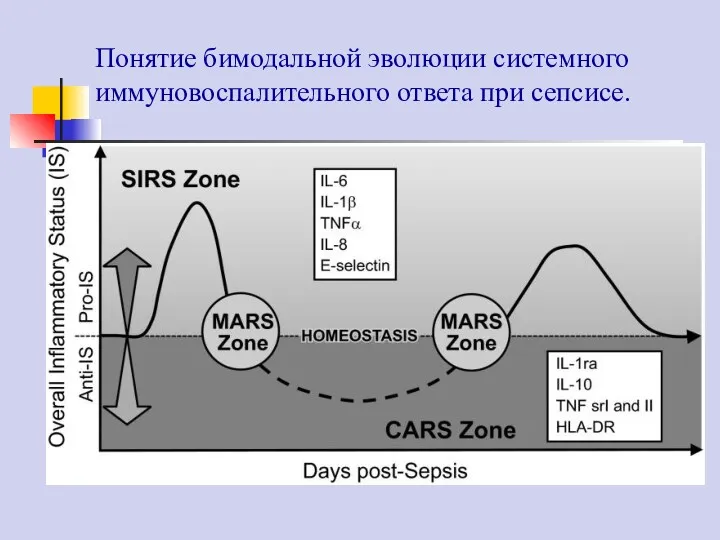
- 10. Понятие бимодальной эволюции системного иммуновоспалительного ответа при сепсисе.
- 11. практике имеется дефицит лабораторных показателей, В клинической объективных позволяющих точно определять этиологию системного воспалительного ответа и
- 12. Поиск дополнительных объективных лабораторных показателей, обеспечивающих раннюю диагностику развивающейся воспалительной реакции, отражающих степень тяжести данного процесса
- 13. Высокая чувствительность и специфичность Доступность Быстрый результат Воспроизводимость Корреляция с тяжестью и исходом Совпадение с клиническим
- 14. Лейкоцитоз C – реактивный белок Прокальцитонин Проадреномедуллин Интерлейкин-6 Эндотоксин Неоптерин Глюканы Маннан Бактериальная ДНК Бактериальный липопротеин
- 15. Классические маркеры активности воспаления Клинический анализ крови: лейкоцитоз, нейтрофильный гранулоцитоз, увеличение количества незрелых форм НГ, ускорение
- 16. Клинический анализ крови В норме содержание лейкоцитов в крови: от 4 до 9·109 /л Лейкоцитоз наблюдают
- 17. СОЭ Скорость оседания эритроцитов (СОЭ) - неспецифический лабораторный показатель крови, отражающий соотношение фракций белков плазмы; изменение
- 18. Оксидативный стресс Оксидативным стрессом называют процесс повреждения клетки в результате реакций окисления. У человека оксидативный стресс
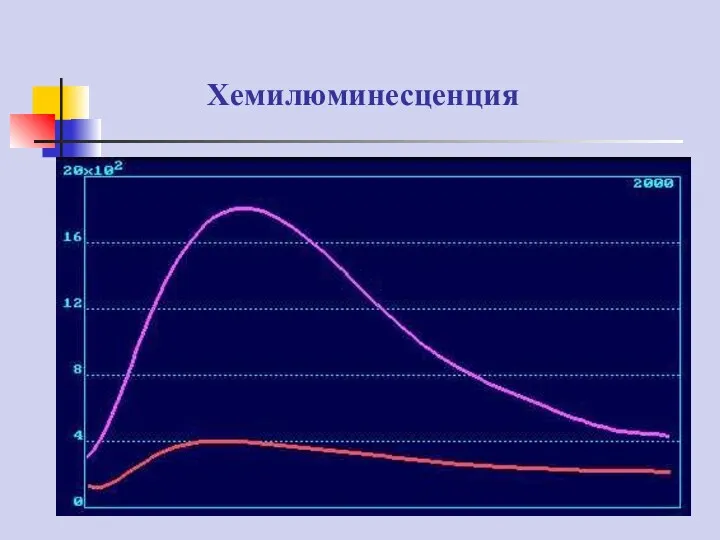
- 19. Хемилюминесценция
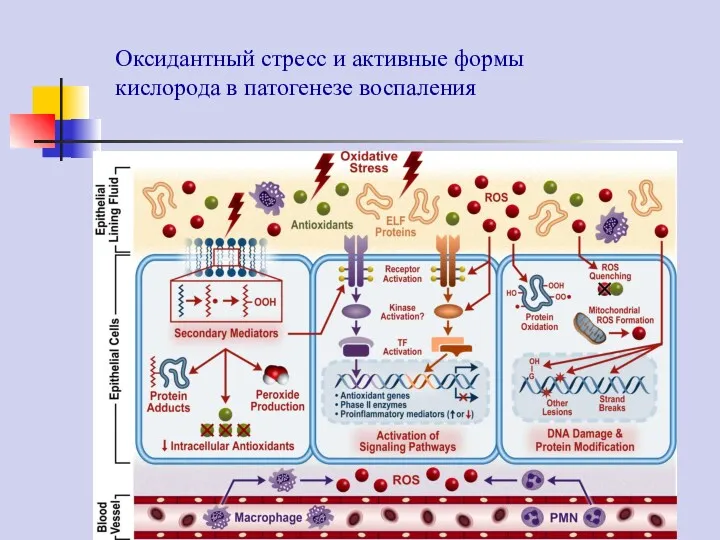
- 20. Оксидантный стресс и активные формы кислорода в патогенезе воспаления
- 21. Гуморальные факторы при системном воспалении
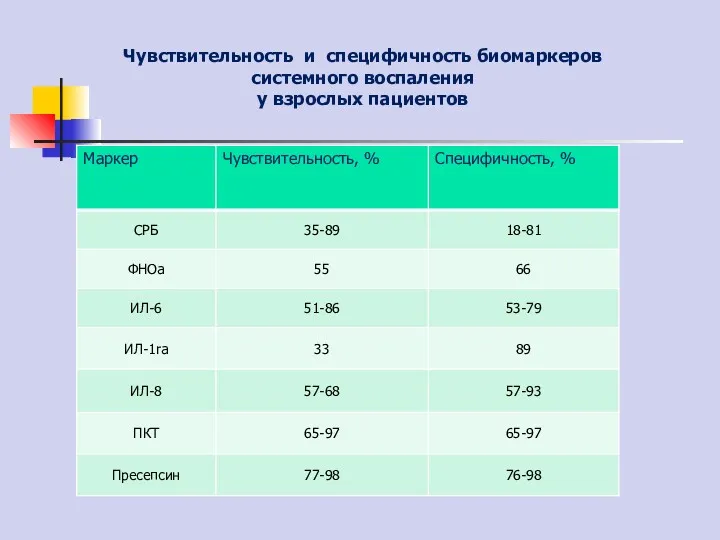
- 22. Чувствительность и специфичность биомаркеров системного воспаления у взрослых пациентов
- 23. Белки острой фазы воспаления Синтезируются преимущественно в печени. Концентрация существенно изменяется и зависит от массивности повреждения,
- 24. Белки острой фазы воспаления (БОФ) В зависимости от степени изменения их концентрации в крови выделяют: Главные
- 25. С-реактивный белок (СРБ, CRP) и сывороточный амилоид А (САА, SAA) СРБ и САА относятся к пентраксинам
- 26. С-реактивный белок Главный белок острой фазы. β-глобулин. Норма: менее 5 мг/л в плазме. Концентрация С-реактивного белка
- 27. Сывороточный амилоид А (САА) САА является нормальным белком сыворотки; предшественник фибриллярного тканевого белка АА. Относится к
- 28. Фибронектин (Fibronectin) - внеклеточный гликопротеин, участвующий в осуществлении защитных реакций организма. В плазме крови он усиливает
- 29. α1-антитрипсин (α1-АТ) α1-АТ – линейный гликопротеин, синтезирующийся преимущественно в печени, а также макрофагами, моноцитами и эпителиальными
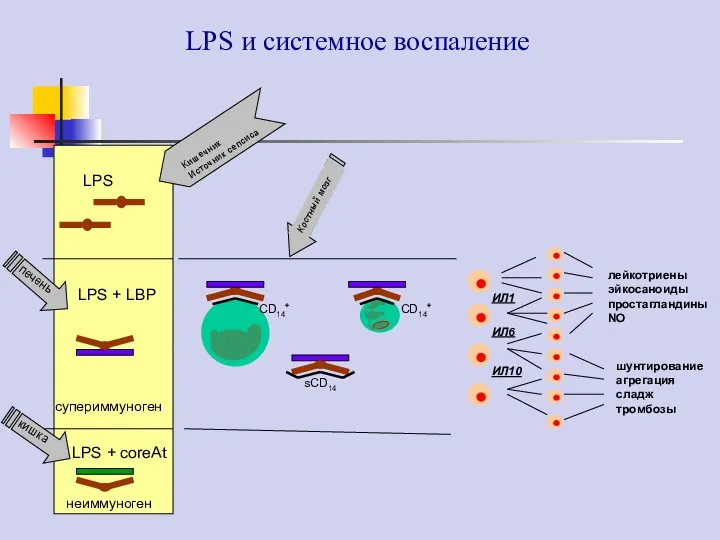
- 30. LPS LPS + LBP LPS + coreAt супериммуноген неиммуноген sCD14 CD14+ CD14+ лейкотриены эйкосаноиды простагландины NO
- 31. Липополисахарид-связывающий белок (LBP) LBP представляет собой БОФ с м.м. 58 кДа. Этот белок конститутивно синтезируется гепатоцитами
- 32. ЛПС-связывающий белок (LBP) Регуляция синтеза LBP в печени связана с пространственной близостью клеток Купфера и гепатоцитов.
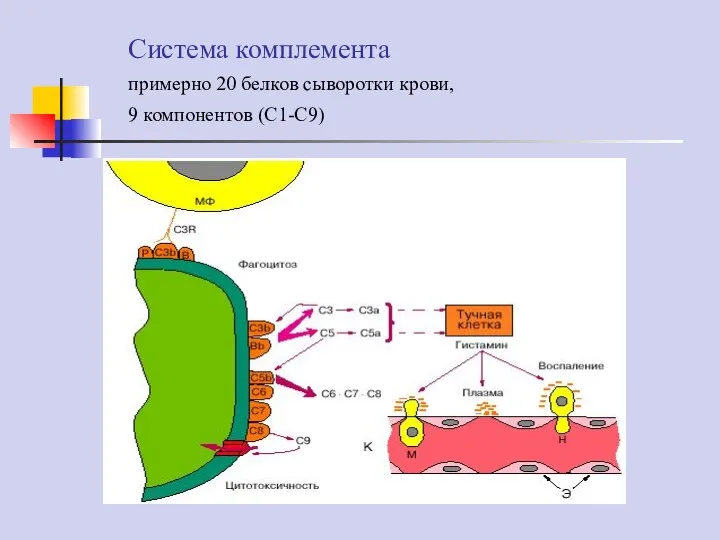
- 33. Система комплемента примерно 20 белков сыворотки крови, 9 компонентов (С1-С9)
- 34. Опсонизация микроорганизмов для поглощения фагоцитами (C3b) Непосредственное уничтожение микроорганизмов путем лизиса (С5b6789) Активация и хемотаксис лейкоцитов
- 35. Полезные: Содействие в уничтожении микроорганизмов Интенсивное удаление иммунных комплексов Индукция и усиление гуморального иммунного ответа Эффекты
- 36. Негативные: Генерализованная массированная активация (например при септицемии) Активация в очаге тканевого некроза (при ОИМ) Активация при
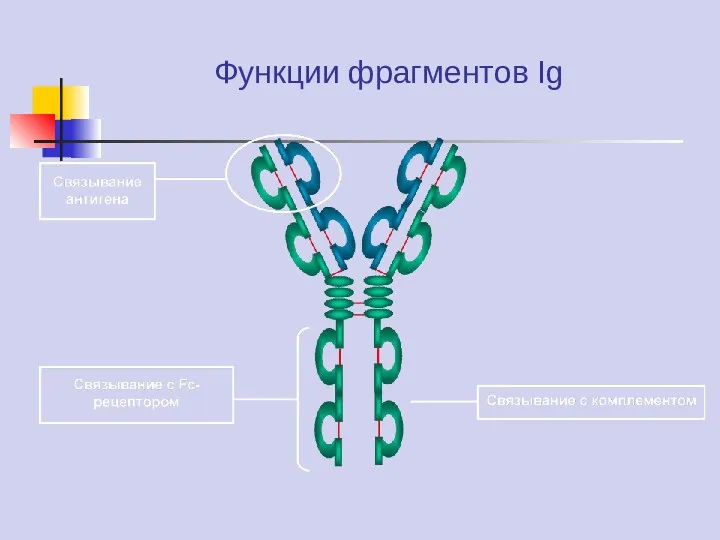
- 37. Иммуноглобулины – группа гликопротеинов, содержащихся в плазме крови и тканевой жидкости. Синтез Ig осуществляют В-клетки после
- 38. Функции фрагментов Ig
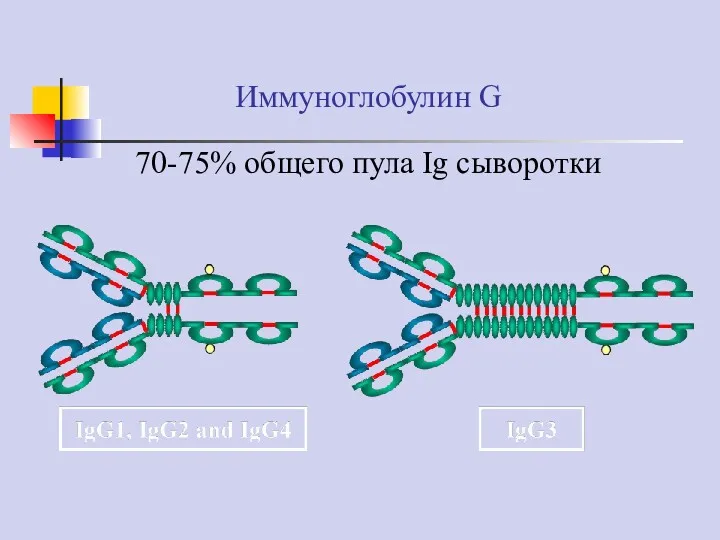
- 39. Иммуноглобулин G 70-75% общего пула Ig сыворотки
- 40. Иммуноглобулин G IgG3, IgG1 и IgG2 – активируют комплемент по классическому пути IgG4 способен активировать комплемент
- 41. IgG Повышение: - острые и хронические инфекции - аутоиммунные заболевания - миеломная болезнь - гаммапатии -
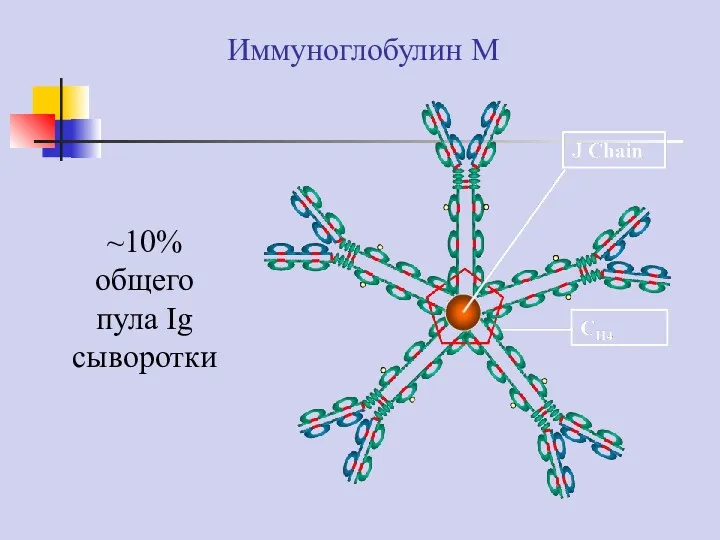
- 42. Иммуноглобулин M ~10% общего пула Ig сыворотки
- 43. Иммуноглобулин М Из всех типов антител IgM проявляют наибольшую способность к связыванию комплемента. IgM1 связывают комплемент,
- 44. IgМ Повышение: - острые инфекции - аутоиммунные заболевания - миеломная болезнь - гаммапатии - острый и
- 45. Иммуноглобулин A 15-20% общего пула Ig сыворотки, из них 80% в виде мономера
- 46. IgА Повышение: - острые и хронические инфекции - аутоиммунные заболевания - миеломная болезнь - гаммапатии -
- 47. Циркулирующие иммунные комплексы С1q (ЦИК-C1q) и С3d (ЦИК-C3d) ЦИК – комплексы, состоящие из антигена, антител и
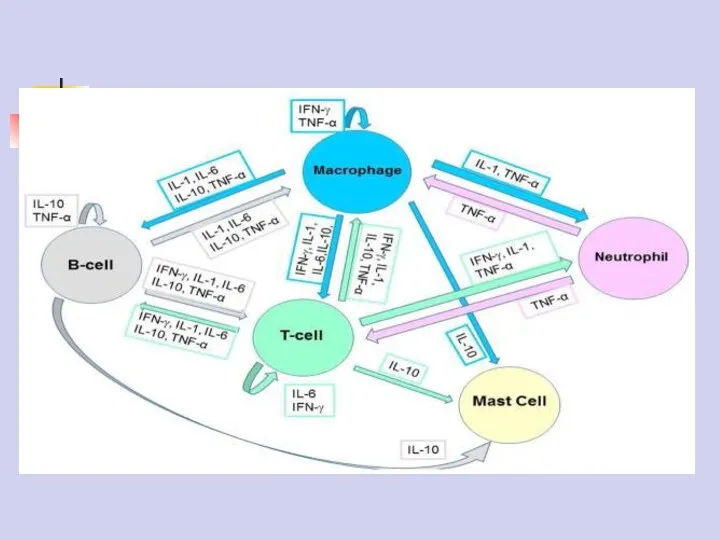
- 48. Цитокины Цитокины служат для межклеточной сигнализации при развитии воспалительного процесса. На начальной стадии местные тканевые клетки
- 50. Факторы некроза опухоли ФНОα - продуцируется макрофагами, а также тучными клетками и лимфоцитами. обусловливает развитие токсического
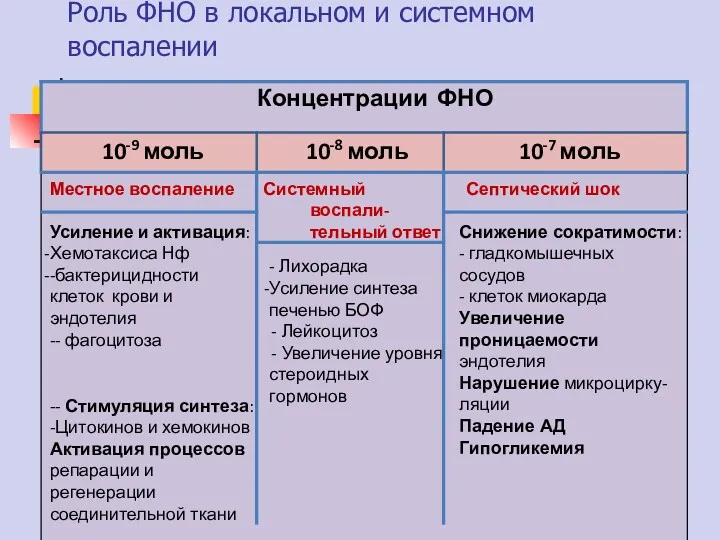
- 51. Роль ФНО в локальном и системном воспалении
- 52. Интерлейкины ИЛ-1 продуцируется гл. обр. макрофагами и в меньшей степени дендритными клетками, эндотелиоцитами, фибробластами, NK, кератиноцитами,
- 53. ИЛ-6 можно использовать для ежедневного мониторинга системного воспаления и прогноза развития бактериальной инфекции. Синтез и секреция
- 54. Интерлейкины ИЛ-8 синтезируется моноцитами, макрофагами, фибробластами. Вызывает миграцию нейтрофилов и базофилов в очаг воспаления и их
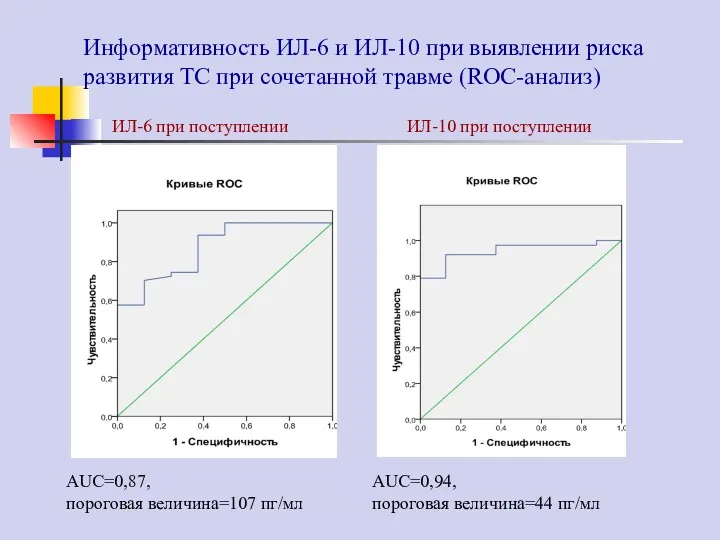
- 55. Информативность ИЛ-6 и ИЛ-10 при выявлении риска развития ТС при сочетанной травме (ROC-анализ) ИЛ-6 при поступлении
- 56. Интерфероны I типа ИНФ-α - продуцируется мононуклеарными фагоцитами (отсюда одно из названий - "лейкоцитарный ЛФН"), ИНФ-β
- 57. Интерфероны II типа ИФН-γ ("иммунный ИФН") продуцируется Т-лимфоцитами и NK. Стимулирует активность Т- и В-лимфоцитов, моноцитов/макрофагов
- 58. Колониестимулирующие факторы Гранулоцитарный КСФ (Г-КСФ) продуцируется в основном макрофагами, а также фибробластами. Стимулирует деление и дифференцировку
- 59. Хемокины У человека выделено около 40 отдельных подобных белков, их подразделили на альфа- и бета-хемокины. Альфа-хемокины
- 60. Факторы роста Трансформирующий фактор роста-β (ТФР-β) -вызывает неадгезивный рост фибробластов но, помимо этого, ингибирует активность некоторых
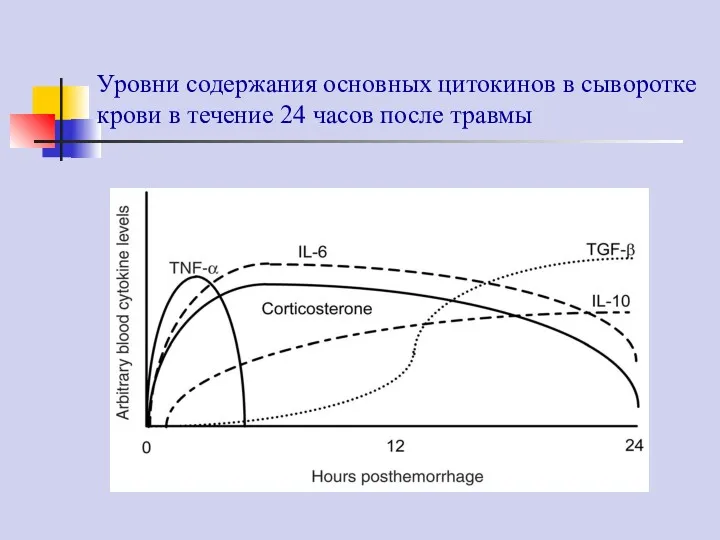
- 61. Уровни содержания основных цитокинов в сыворотке крови в течение 24 часов после травмы
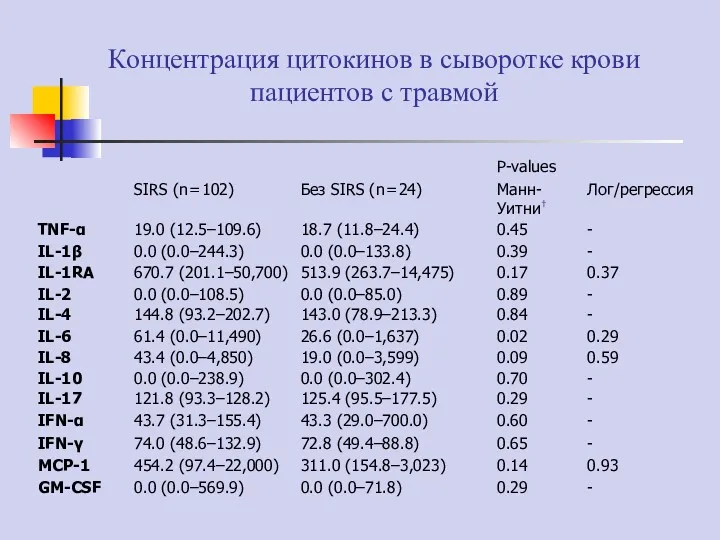
- 62. Концентрация цитокинов в сыворотке крови пациентов с травмой
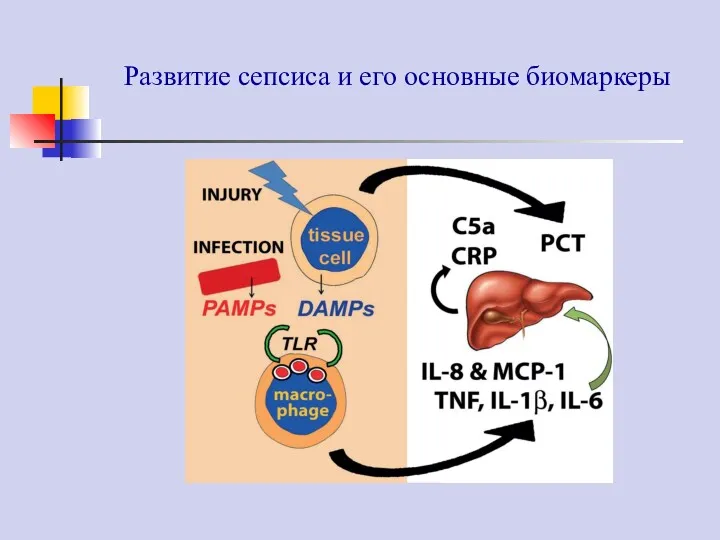
- 63. Развитие сепсиса и его основные биомаркеры
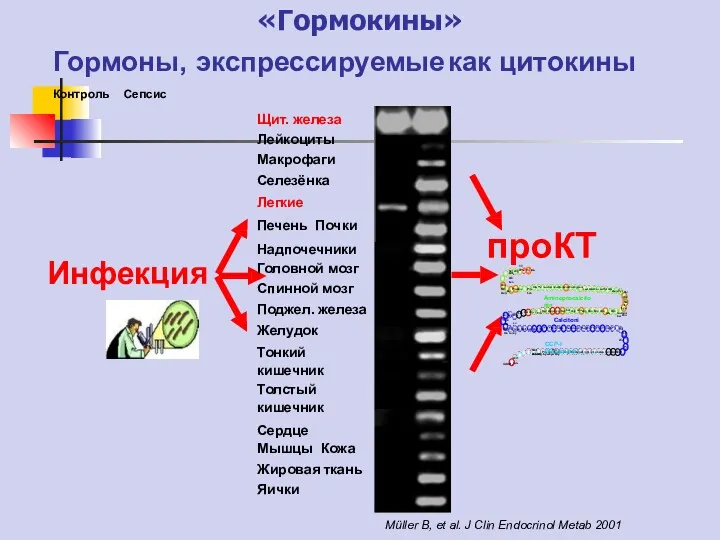
- 64. Инфекция проКТ Щит. железа Лейкоциты Макрофаги Селезёнка Легкие Печень Почки Надпочечники Головной мозг Спинной мозг Поджел.
- 65. Прокальцитонин представляет собой пептид с молекулярной массой 14,5 кДа. Является предшественником кальцитонина. В норме кальцитонин синтезируется
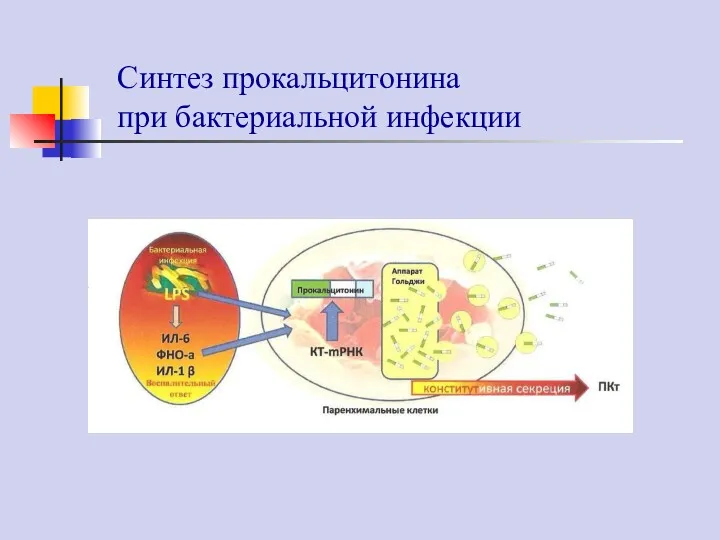
- 66. Синтез прокальцитонина при бактериальной инфекции
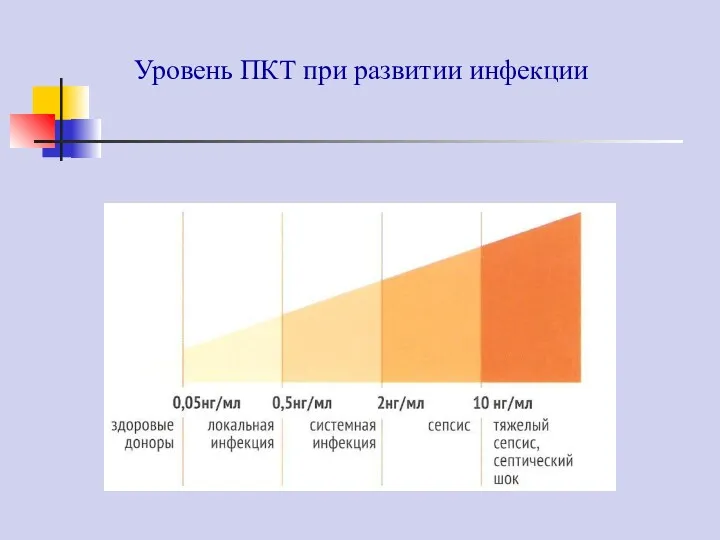
- 67. Уровень ПКТ при развитии инфекции
- 68. Проадреномедуллин (proADM ) Был выделен японскими учеными K. Kitamura и сотрудниками в 1993 г. из клеток
- 69. Отмечается повышение содержания в крови по мере нарастания тяжести инфекционного процесса В отличие от ПКТ зарегистрирована
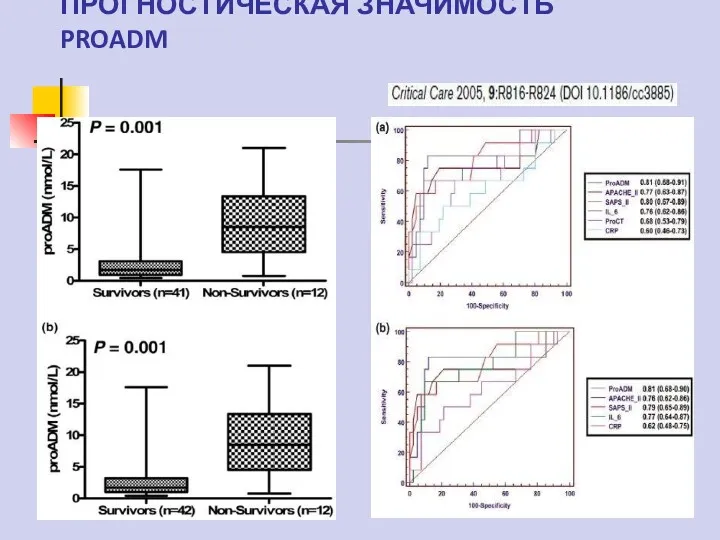
- 70. ПРОГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ PROADM
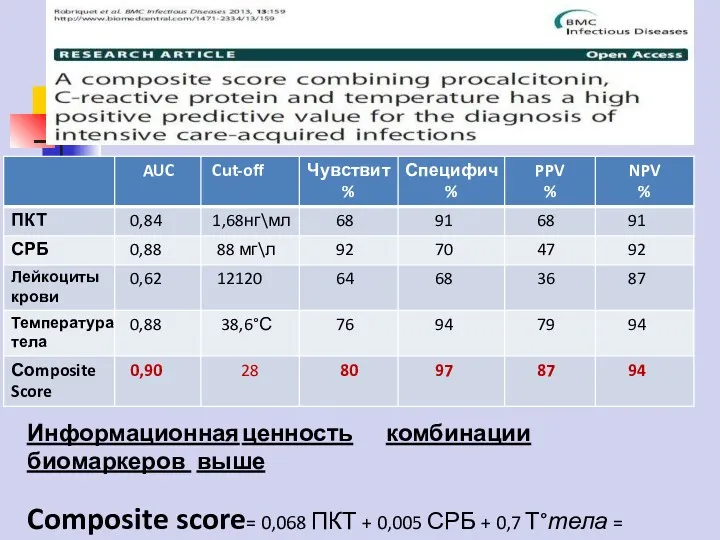
- 71. Информационная ценность комбинации биомаркеров выше Composite score= 0,068 ПКТ + 0,005 СРБ + 0,7 Т°тела =
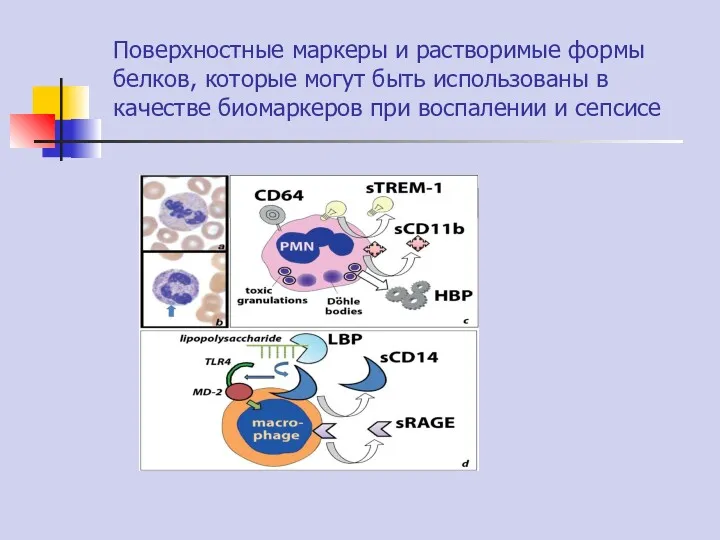
- 72. Поверхностные маркеры и растворимые формы белков, которые могут быть использованы в качестве биомаркеров при воспалении и
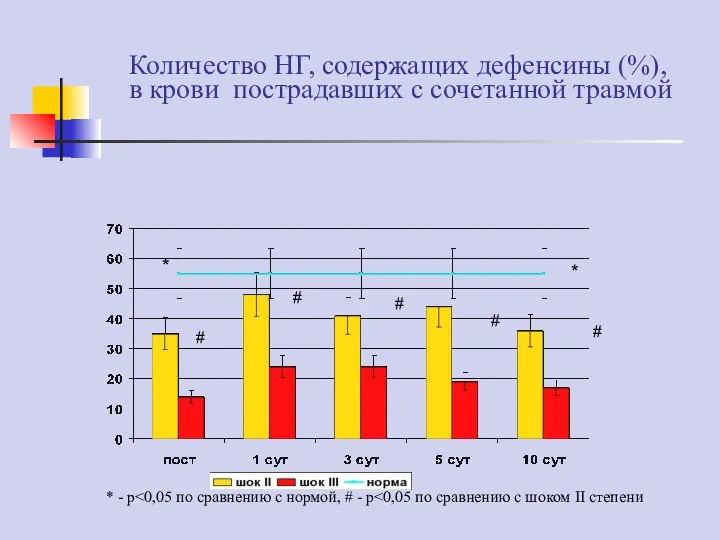
- 73. Количество НГ, содержащих дефенсины (%), в крови пострадавших с сочетанной травмой # # # # #
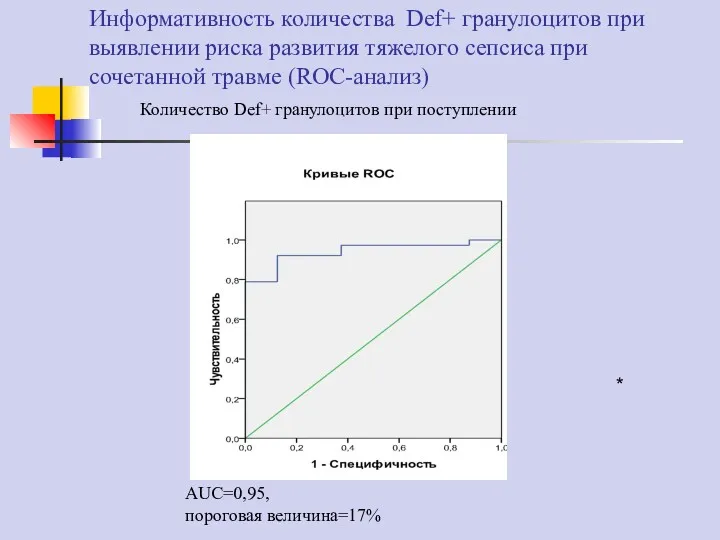
- 74. Информативность количества Def+ гранулоцитов при выявлении риска развития тяжелого сепсиса при сочетанной травме (ROC-анализ) * Количество
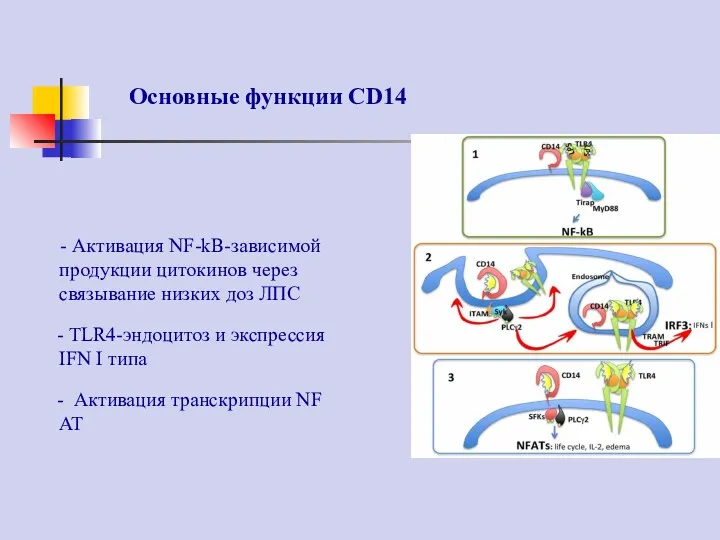
- 75. Основные функции CD14 - Активация NF-kB-зависимой продукции цитокинов через связывание низких доз ЛПС - TLR4-эндоцитоз и
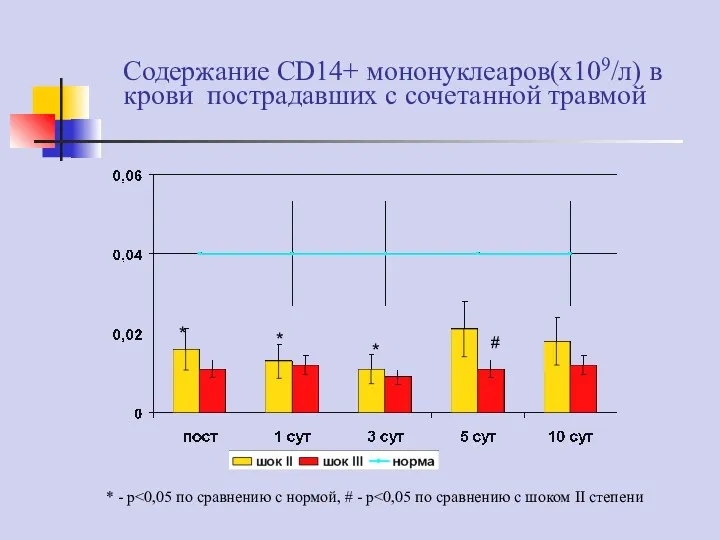
- 76. Содержание CD14+ мононуклеаров(х109/л) в крови пострадавших с сочетанной травмой # * * * * - p
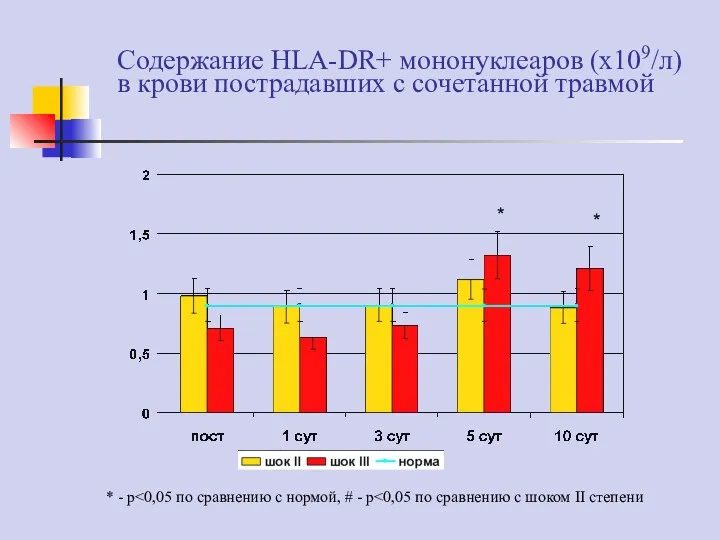
- 77. Содержание HLA-DR+ мононуклеаров (х109/л) в крови пострадавших с сочетанной травмой * * * - p
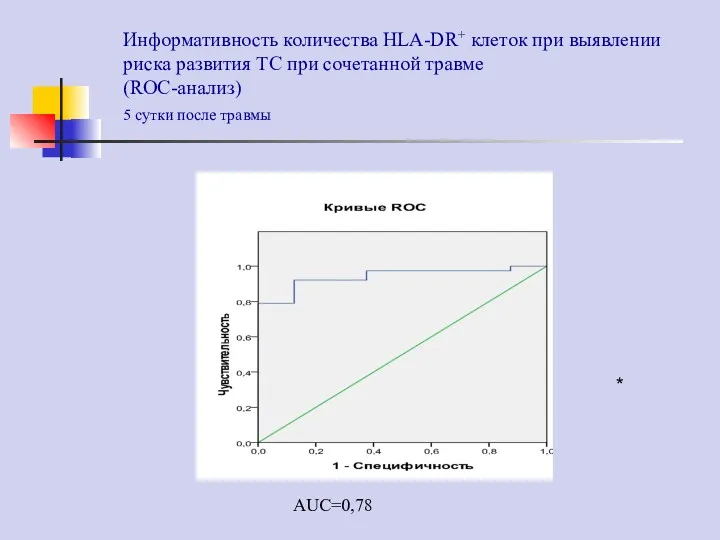
- 78. Информативность количества HLA-DR+ клеток при выявлении риска развития ТС при сочетанной травме (ROC-анализ) 5 сутки после
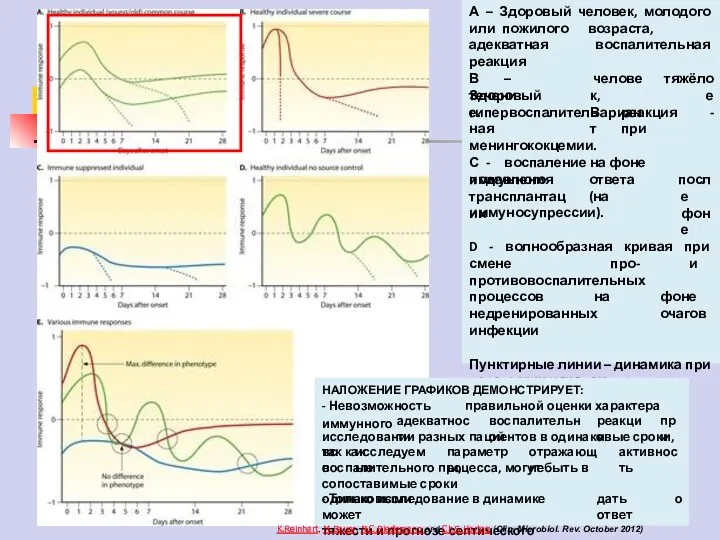
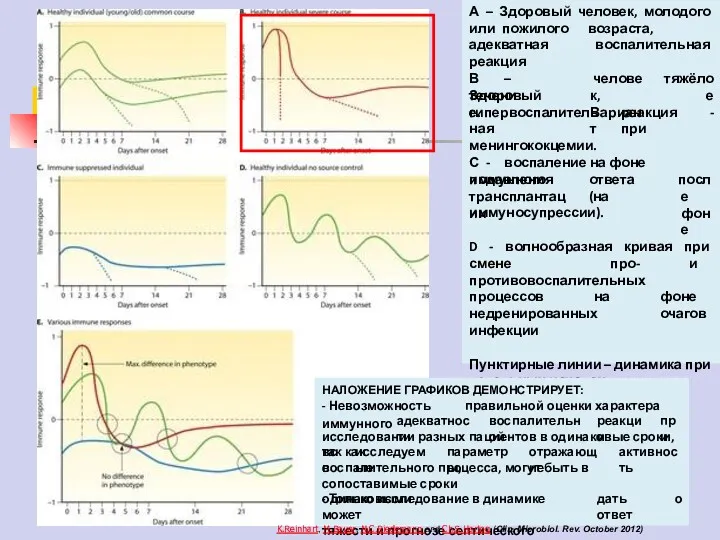
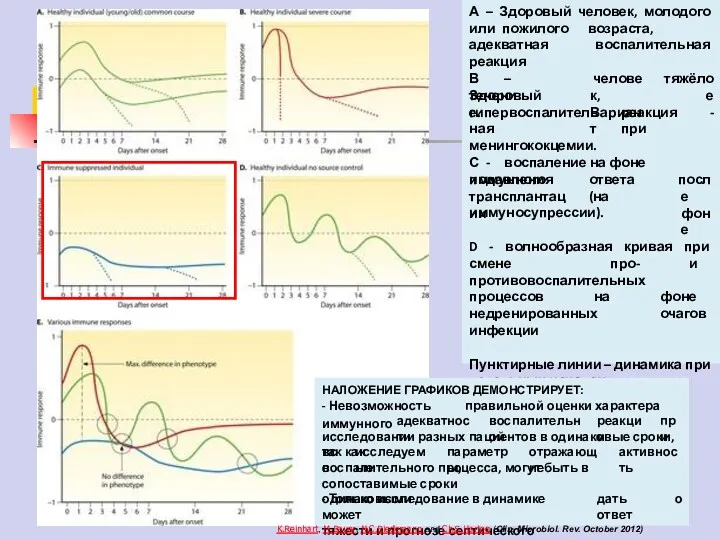
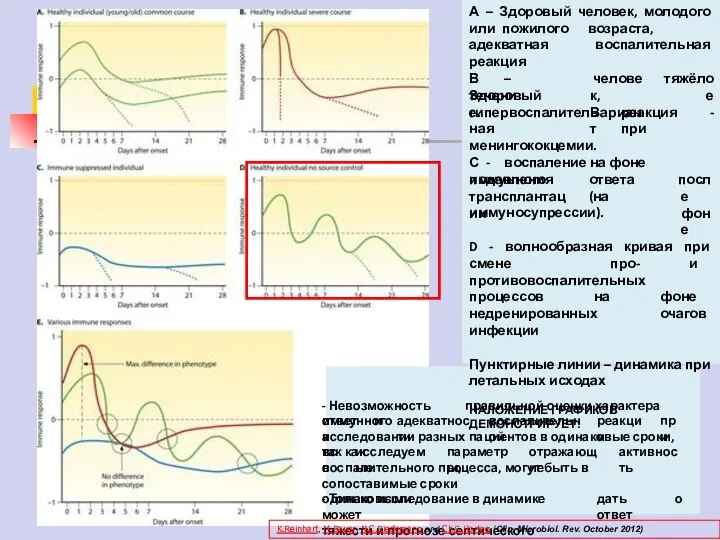
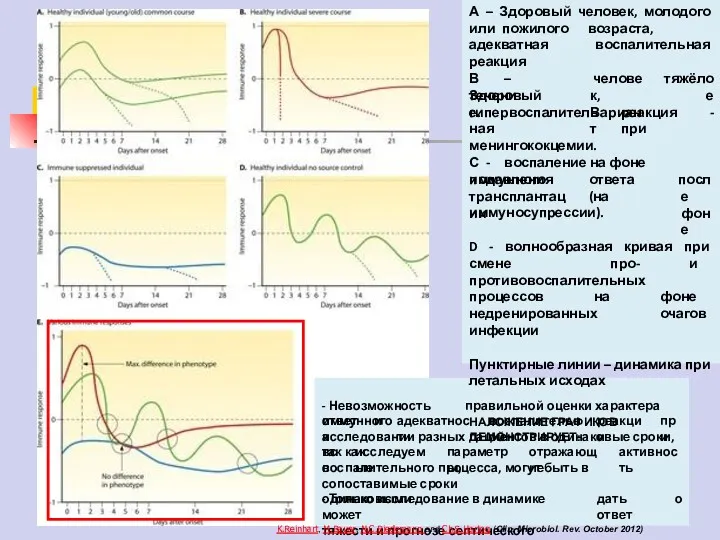
- 79. А – Здоровый человек, молодого или пожилого возраста, адекватная воспалительная реакция В – Здоровый течение. человек,
- 80. А – Здоровый человек, молодого или пожилого возраста, адекватная воспалительная реакция В – Здоровый течение. человек,
- 81. А – Здоровый человек, молодого или пожилого возраста, адекватная воспалительная реакция В – Здоровый течение. человек,
- 82. А – Здоровый человек, молодого или пожилого возраста, адекватная воспалительная реакция В – Здоровый течение. человек,
- 83. А – Здоровый человек, молодого или пожилого возраста, адекватная воспалительная реакция В – Здоровый течение. человек,
- 84. ИЛ-6 + ЛБП у 100 больных ежедневно в течение 17дн. 50 000 €/год (1,5% от общих
- 86. Скачать презентацию











































 Хронофармакология
Хронофармакология Мероприятия по снижению распространения злокачественных новообразований среди женщин в Свердловской области
Мероприятия по снижению распространения злокачественных новообразований среди женщин в Свердловской области Исследование дыхательной системы. Перкуссия и аускультация легких
Исследование дыхательной системы. Перкуссия и аускультация легких Сезімталдық және олардың бұзылыстары
Сезімталдық және олардың бұзылыстары Борьба организма с инфекцией
Борьба организма с инфекцией Коллекция адаптивной одежды для людей с ограниченными возможностями здоровья (ОВЗ)
Коллекция адаптивной одежды для людей с ограниченными возможностями здоровья (ОВЗ) Беременность и заболевания сердечно-сосудистой и дыхательной систем
Беременность и заболевания сердечно-сосудистой и дыхательной систем Пикфлоуметрия
Пикфлоуметрия Асқазан аурулары
Асқазан аурулары Дистрофии. Причины и классификация дистрофий
Дистрофии. Причины и классификация дистрофий Кодекс этики в фармацевтической деятельности
Кодекс этики в фармацевтической деятельности Мероприятия по снижению риска заражения и распространения новой коронавирусной инфекции 2019-nCoV
Мероприятия по снижению риска заражения и распространения новой коронавирусной инфекции 2019-nCoV Синдром поражения миокарда
Синдром поражения миокарда Средства, влияющие на агрегацию тромбоцитов, свертывание крови и фибринолиз
Средства, влияющие на агрегацию тромбоцитов, свертывание крови и фибринолиз Стандарты лучевой диагностики заболеваний легких и средостения
Стандарты лучевой диагностики заболеваний легких и средостения Лечебная гимнастика и массаж при вибрационной болезни
Лечебная гимнастика и массаж при вибрационной болезни СП при ревматизме
СП при ревматизме Курстық жұмыс. Сальмонеллез ауруының таралу мониторингі. Диагностикасы және емі
Курстық жұмыс. Сальмонеллез ауруының таралу мониторингі. Диагностикасы және емі Размножение и развитие человека
Размножение и развитие человека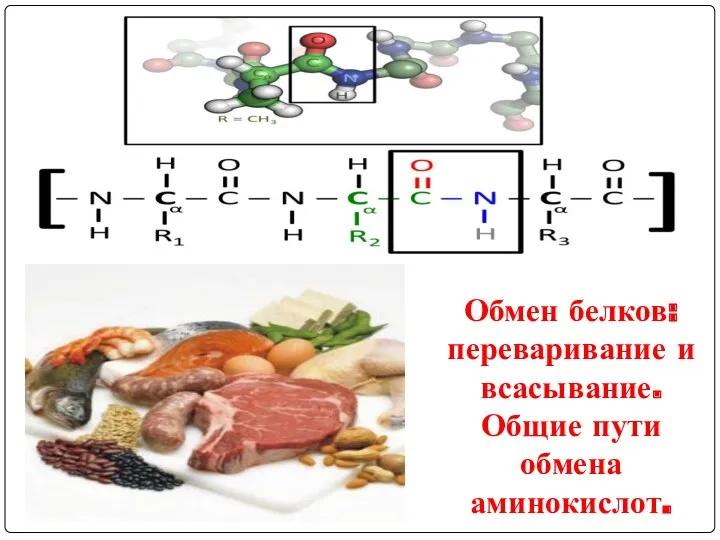 Обмен белков. Переваривание и всасывание. Общие пути обмена
Обмен белков. Переваривание и всасывание. Общие пути обмена Кисты яичника и беременность
Кисты яичника и беременность Классификация речевых нарушений
Классификация речевых нарушений Генитальді эндометриоз, этиологиясы, жіктелуі, емдеу принциптері
Генитальді эндометриоз, этиологиясы, жіктелуі, емдеу принциптері Заболевания толстой кишки
Заболевания толстой кишки Практическое занятие № 17.Травмы зубов у детей.Группировка острой травмы.Клиника,диагностика,лечение
Практическое занятие № 17.Травмы зубов у детей.Группировка острой травмы.Клиника,диагностика,лечение Инвалидность и реабилитация как медико-социальная проблема
Инвалидность и реабилитация как медико-социальная проблема Эпилепсия. Анықтамасы. Таралымы. Этиология. Классификация. Клиника. Диагностика. Емі
Эпилепсия. Анықтамасы. Таралымы. Этиология. Классификация. Клиника. Диагностика. Емі Моногибридті будандастыру. Гибридологиялық зерттеу әдісі
Моногибридті будандастыру. Гибридологиялық зерттеу әдісі