Содержание
- 2. Нормативные документы в сфере иммунопрофилактики КОДЕКС РЕСПУБЛИКИ КАЗАХСТАН «О ЗДОРОВЬЕ НАРОДА И СИСТЕМЕ ЗДРАВООХРАНЕНИЯ» от 18
- 3. Нормативные документы в сфере иммунопрофилактики (продолжение) Постановление Правительства Республики Казахстан от 30 декабря 2009 года №
- 4. Нормативные документы в сфере иммунопрофилактики (продолжение) Постановление Правительства Республики Казахстан № 1691 от 30 декабря 2011
- 6. Медицинские иммунобиологические препараты препараты для специфической профилактики, диагностики и лечения инфекционных и иммунных (включая аллергические) заболеваний,
- 7. Виды МИБП Анатоксины бактериофаги вакцины иммуноглобулины сыворотки;
- 8. Виды МИБП (продолжение) Анатоксин - медицинский препарат, приготовленный из токсина, не имеющий выраженных токсических свойств, но
- 9. Виды МИБП (продолжение) вакцина – медицинский препарат для специфической профилактики инфекционных заболеваний, оказывающий профилактический эффект через
- 10. Холодовая цепь бесперебойно функционирующая система, обеспечивающая оптимальный температурный режим хранения и транспортировки МИБП и ДП на
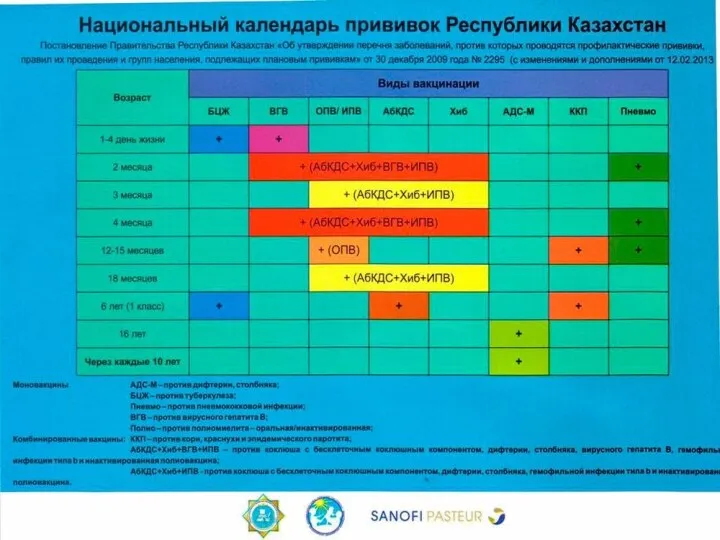
- 11. Группы населения, подлежащие плановым прививкам Плановым прививкам против инфекционных и паразитарных заболеваний подлежат следующие группы населения:
- 12. Группы населения, подлежащие плановым прививкам (продолжение) 5) дети детских домов, домов ребенка, контингент домов престарелых (грипп);
- 13. Перед применением ИБП необходимо изучить приложенную к ней инструкцию, проверить маркировку и целостность ампулы (флакона), соответствие
- 14. 5) ИБП с нарушением целостности ампул (флаконов); 6) ИБП с неясной или отсутствующей маркировкой на ампуле
- 15. Оформление допуска к проведению профилактических прививок Перед проведением профилактических прививок в обязательном порядке проводится осмотр прививаемого
- 16. Интервалы между прививками Допускается совмещение различных видов профилактических прививок в один день, за исключением прививки против
- 17. Общие постоянные противопоказания для всех видов вакцин: 1) сильная реакция, развившаяся в течение 48 часов после
- 18. Постоянные противопоказания для использования живых вакцин: 1) стабильные иммунодефицитные состояния; 2) симптоматическая форма ВИЧ-инфекции; 3) злокачественные
- 19. Временные противопоказания, общие для всех видов вакцин: 1) острые инфекционные и неинфекционные заболевания вне зависимости от
- 20. Дополнительные противопоказания к отдельным видам вакцин 1) к вакцинам, содержащим столбнячный анатоксин (АДС, АДС-М, АС): не
- 21. Политика использования «открытых» флаконов вакцины «открытый флакон» вакцины – флакон вакцины, вводимой инъекционным способом, из которого
- 22. Политика использования «открытых» флаконов вакцины (продолжение) «Открытые флаконы» АКДС-содержащей вакцины, АДС, АДС-М, АД-М, АС, вакцины против
- 23. Учетные формы медицинских документов по иммунопрофилактике Все проведенные профилактические прививки подлежат учету медицинским работником и должны
- 24. Наблюдение за состоянием привитого в поствакцинальном периоде После получения прививки привитые лица в течение 30 минут
- 25. Учет и расследование поствакцинальных осложнений Медицинский работник, получивший вызов к привитому лицу, немедленно обслуживает данный вызов,
- 26. Прививочный кабинет обеспечивается лекарственными препаратами противошоковой терапии: 0,1 процентный (далее - %) раствор адреналина, 1 %
- 27. Вакцинация против вирусного гепатита В лиц старше 15 лет Вакцинация лиц старше 15 лет проводится после
- 28. Контингенты, подлежащие вакцинации против ВГВ: 1) новорожденные с целью предупреждения перинатальной передачи в первые двенадцать часов
- 29. Контингенты, подлежащие вакцинации против ВГВ (продолжение) 6) впервые выявленные ВИЧ-инфицированные 7) впервые выявленные лица, подлежащие гемодиализу
- 30. Лица подлежащие вакцинации в очагах дифтерии. Сроки наблюдения за контактными В очагах больных дифтерией проводится иммунизация:
- 31. В очаге дифтерии контактные лица наблюдаются в течение 7 дней с момента последнего контакта с больным.
- 32. Лица подлежащие вакцинации в очагах кори, краснухи, паротита. Сроки наблюдения за контактными. Для иммунизации населения против
- 33. При регистрации случаев эпидемического паротита в организованном коллективе проводится однократная иммунизация детей до 18 лет, привитых
- 34. Санитарно-эпидемиологические требования к уничтожению неиспользованных остатков иммунобиологических препаратов Ампулы и флаконы, содержащие неиспользованные остатки ИБП, обеззараживаются
- 36. Скачать презентацию
































 Патология терморегуляции. Лекция № 8
Патология терморегуляции. Лекция № 8 Шетелдегі инклюзивті білім беру
Шетелдегі инклюзивті білім беру Планирование научного исследования в медицине
Планирование научного исследования в медицине Спинальная мышечная атрофия тип lll. Болезнь Кугельберга-Веландера
Спинальная мышечная атрофия тип lll. Болезнь Кугельберга-Веландера Prezentatsia_po_biologii_na_temu_Znachenie_pischi_i_eyo_sostav__8_klass
Prezentatsia_po_biologii_na_temu_Znachenie_pischi_i_eyo_sostav__8_klass Анемія. Етіологія і патогенез
Анемія. Етіологія і патогенез Борьба с вирусными заболеваниями (СПИД и другие)
Борьба с вирусными заболеваниями (СПИД и другие) Заманауи гепатопротекторлы заттар
Заманауи гепатопротекторлы заттар Ортопедиялық стоматология
Ортопедиялық стоматология Комплексная программа организации летнего отдыха и оздоровления детей и подростков Беломорская волна
Комплексная программа организации летнего отдыха и оздоровления детей и подростков Беломорская волна Дети с особыми образовательными потребностями
Дети с особыми образовательными потребностями Непрерывное медицинское образование. Периодическая аккредитация
Непрерывное медицинское образование. Периодическая аккредитация Гравидограмма интерпритациясы
Гравидограмма интерпритациясы Экстрагенитальная патология и беременность
Экстрагенитальная патология и беременность Фізіологічні механізми та закономірності формування рухових навичок
Фізіологічні механізми та закономірності формування рухових навичок Физиология плода. Физиология беременности
Физиология плода. Физиология беременности Асфиксии новорождённых
Асфиксии новорождённых Герпетическая инфекция
Герпетическая инфекция Риккетсии. Хламидии
Риккетсии. Хламидии Общая и специальная подготовка полости рта перед протезированием
Общая и специальная подготовка полости рта перед протезированием Босанғаннан кейінгі ерте кезеңдегі қан кетудің себептері: травма,тромбин
Босанғаннан кейінгі ерте кезеңдегі қан кетудің себептері: травма,тромбин Антибиотики и химиотерапия. Химиотерапевтические препараты
Антибиотики и химиотерапия. Химиотерапевтические препараты Первая помощь при синдроме длительного сдавления (СДС) или тяжелая компрессионная травма
Первая помощь при синдроме длительного сдавления (СДС) или тяжелая компрессионная травма Мышцы верхних и нижних конечностей человека
Мышцы верхних и нижних конечностей человека Синдром диабетической стопы
Синдром диабетической стопы Острый аппендицит. История учения об аппендиците. Анатомо-физиологические особенности
Острый аппендицит. История учения об аппендиците. Анатомо-физиологические особенности Холера
Холера Острые респираторные вирусные инфекции
Острые респираторные вирусные инфекции