Содержание
- 2. Послеоперационный период - время, прошедшее от момента окончания оперативного вмешательства до выздоровления больного. фазы послеоперационного периода:
- 3. Обезболивание в послеоперационном периоде: Опиаты и опиоиды (наркотические анальгетики). Нестероидные противовоспалительные средства Местные анестетики Ингибиторы протеаз
- 4. • расчет суточного объема инфузий, их коллоидно-осмотического состава; • стабилизация гемодинамики, кислотно-основного состояния, метаболизма; • коррекция
- 6. Во время проведения плановых операций восполнение жидкости производится обычно из расчета 1 л/час. В течение суток
- 7. Рекомендуемый стартовый объем инфузий составляет 25–30 мл/кг/сут. (обычно на время от окончания операции до начала следующего
- 8. Очень важна роль электролита калия– главного катиона клетки: участвует в обменах, передаче нервного импульса, особенно в
- 9. Итак, соотношение коллоиды/кристаллоиды в суточном рационе рекомендуют в 1 сутки – 1:1, 1:2; вторые сутки после
- 10. Магний – второй по содержанию после калия катион клетки (вне клетки – 1–2% от всего). Суточная
- 11. Считается оправданным начинать парентеральное питание со 2-х суток (по стабилизации гемодинамики и газо-обмена – можно раньше).
- 12. Для уменьшения катаболических процессов, гипоксии, улучшения микроциркуляции, реологических свойств крови показано парентеральное введение пентоксифиллина (до 7
- 13. Для предупреждения развития после операции пареза кишечника, рвоты, прежде всего, необходимо не допускать гипоксии, гиповолемии, гипокалиемии,
- 14. Парентеральное введение миолитика НО-ШПА (папаверина гидрохлорид) – 2% раствора по 2 мл каждые 6 часов в
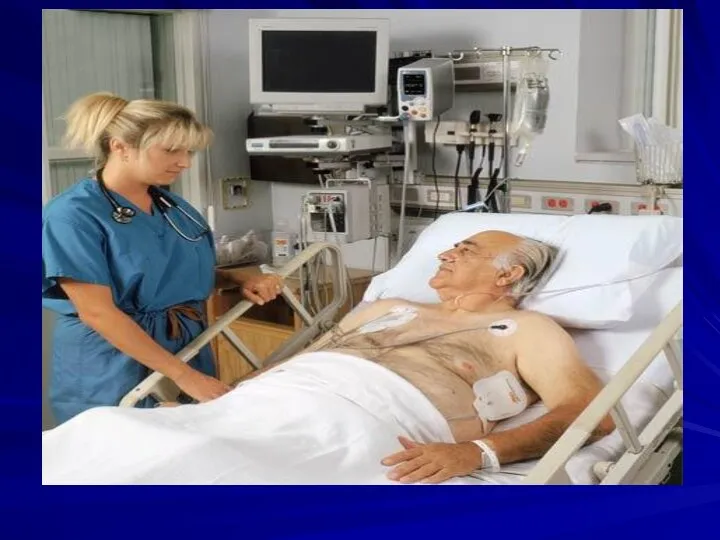
- 15. Кормление можно начинать через 6–12 часов после неосложненной операции. К этому времени восстанавливается всасывающая и моторная
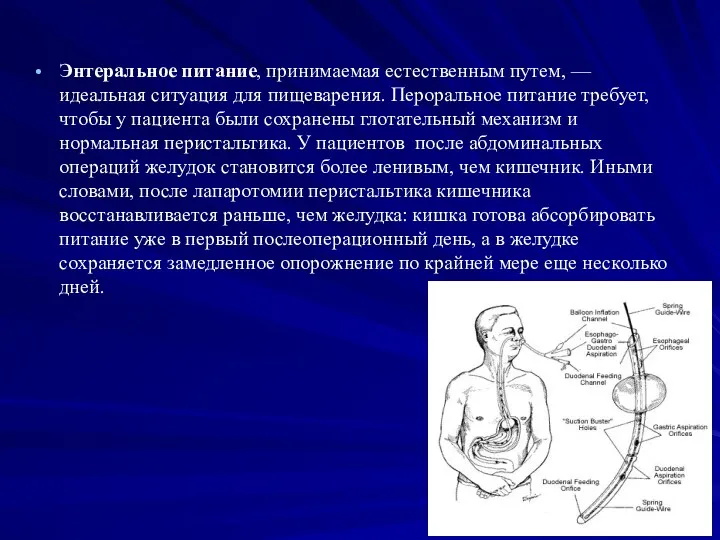
- 16. Энтеральное питание, принимаемая естественным путем, — идеальная ситуация для пищеварения. Пероральное питание требует, чтобы у пациента
- 17. Пути энтерального питания Когда питание через рот недоступно, остаются следующие возможности для энтерального питания: • Назогастральный
- 19. Скачать презентацию













 Воспалительные заболевания височно-нижнечелюстного сустава
Воспалительные заболевания височно-нижнечелюстного сустава Эндометриоз. Биологические характеристики эндометриоза
Эндометриоз. Биологические характеристики эндометриоза Влияние здорового образа жизни на долголетие
Влияние здорового образа жизни на долголетие Заболевания кишечника
Заболевания кишечника Общие физико-математические закономерности движения крови по сосудам
Общие физико-математические закономерности движения крови по сосудам Эндокринные заболевания и беременность
Эндокринные заболевания и беременность Жас нәрестеге үйіне патронажға бару, есептік амбулаторлық картасын толтыру
Жас нәрестеге үйіне патронажға бару, есептік амбулаторлық картасын толтыру Жұқпалы үрдіс патогенезінің жалпы тізбектері: қызба, қабыну, гипоксия, метаболизм бұзылыстары
Жұқпалы үрдіс патогенезінің жалпы тізбектері: қызба, қабыну, гипоксия, метаболизм бұзылыстары Балалардағы пародонт аурулары
Балалардағы пародонт аурулары Здоровье на всю жизнь. Международное предприятие Tiens. Система продукции Тяньши
Здоровье на всю жизнь. Международное предприятие Tiens. Система продукции Тяньши Остеоартроз. Классификация
Остеоартроз. Классификация Нейросифилис
Нейросифилис Основы мануально-мышечного тестирования
Основы мануально-мышечного тестирования Чума - инфекционное заболевание группы карантинных инфекций
Чума - инфекционное заболевание группы карантинных инфекций Корь. Эпидемиология, клиника, диагностика, профилактика
Корь. Эпидемиология, клиника, диагностика, профилактика Міри радіобіологічних ефектів
Міри радіобіологічних ефектів Илік заттар (немесе тұтқыр заттар), тітіркендіруші заттар.қаптаушы заттар, адсорбциялаушы заттар
Илік заттар (немесе тұтқыр заттар), тітіркендіруші заттар.қаптаушы заттар, адсорбциялаушы заттар Мягкие лекарственные формы. Мази, пасты, гели, кремы, линименты
Мягкие лекарственные формы. Мази, пасты, гели, кремы, линименты Как сохранить и преумножить женское здоровье с Витамакс
Как сохранить и преумножить женское здоровье с Витамакс Респираторная поддержка новорожденных с дыхательными расстройствами
Респираторная поддержка новорожденных с дыхательными расстройствами Введение в вакцинологию: виды вакцинных препаратов
Введение в вакцинологию: виды вакцинных препаратов Сухожильный шов
Сухожильный шов Витамин B1
Витамин B1 Гепатолиенальный синдром
Гепатолиенальный синдром Кишечные инфекции: брюшной тиф, дизентерия, сальмонеллез
Кишечные инфекции: брюшной тиф, дизентерия, сальмонеллез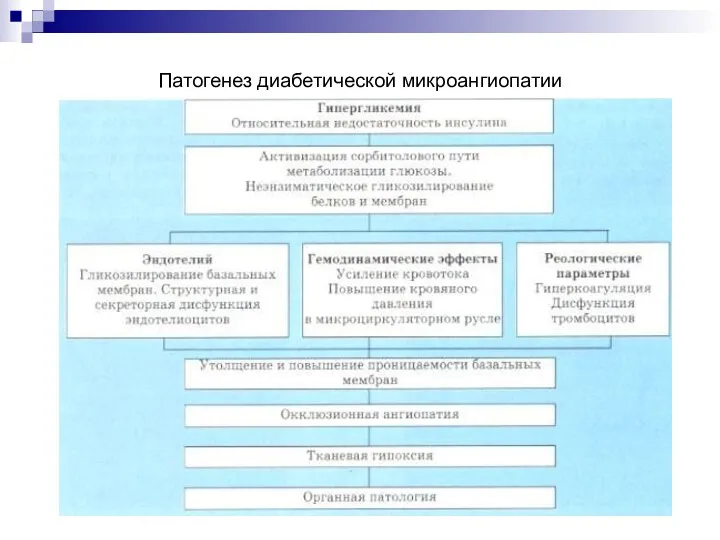 Патогенез диабетической микроангиопатии
Патогенез диабетической микроангиопатии Қазіргі қоғамдағы аномальды балаларға деген көзқарас
Қазіргі қоғамдағы аномальды балаларға деген көзқарас Топографическая анатомия и операции на голове. (Лекция 1)
Топографическая анатомия и операции на голове. (Лекция 1)