Содержание
- 2. Электродный потенциал Электрохимия устанавливает механизмы процессов и явлений, протекающих на границе раздела фаз с участием заряженных
- 3. Электродным потенциалом (E) называют максимальную разность потенциалов, возникающую на границе твердая фаза – раствор в момент
- 4. Электродный потенциал Механизмы возникновения электродного потенциала При погружении металла в раствор его одноименной соли, в системе
- 5. Электродный потенциал Возможны 2 случая возникновения потенциала в данных условиях: 1) При погружении активного металла (Zn)
- 6. На электроде протекает процесс: Zn0 – 2e- ↔ Zn2+ При этом часть ионов цинка с поверхности
- 7. Электродный потенциал 2) При погружении неактивного металла (Cu) в раствор его соли (CuSO4) равновесие электродной реакции
- 8. Поэтому часть ионов меди переходит из раствора на пластинку, заряжая ее положительно, раствор при этом заряжается
- 9. Электродный потенциал Существуют и другие механизмы возникновения ДЭС, например, процесс адсорбции адсорбата на поверхности адсорбента. При
- 10. Таким образом, ДЭС может формироваться за счет различных механизмов, в основе которых лежат реакции осаждения, ионизации,
- 11. Электродный потенциал Схему электрода изображают в виде вертикальной черты, которая разделяет твердую и жидкую фазы. Например,
- 12. Строение ДЭС. Термодинамика ДЭС ДЭС можно сравнить с конденсатором, одна обкладка которого – металл, другая –
- 13. Подвижную часть ДЭС можно разделить на две части: 1) Адсорбционный слой – состоит из противоионов, расположенных
- 14. Строение ДЭС. Термодинамика ДЭС Схема ДЭС для пластинки с «-» зарядом имеет вид: - + -
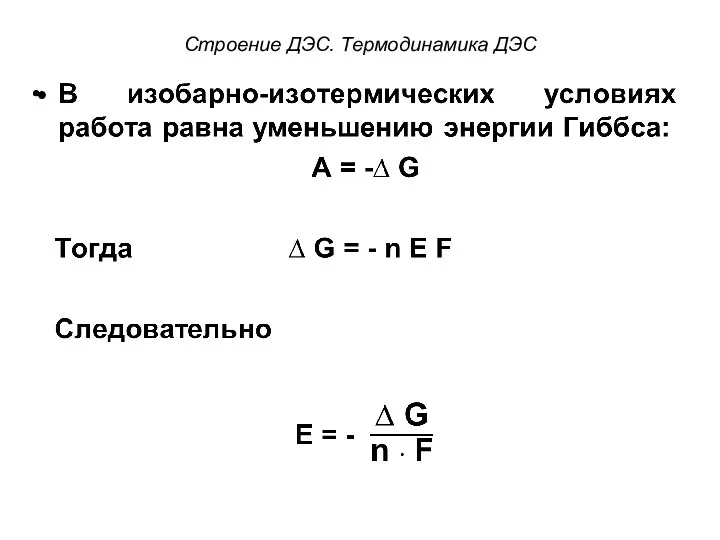
- 15. Строение ДЭС. Термодинамика ДЭС От величины электродного потенциала зависит величина работы, которая совершается системой при образовании
- 16. Строение ДЭС. Термодинамика ДЭС
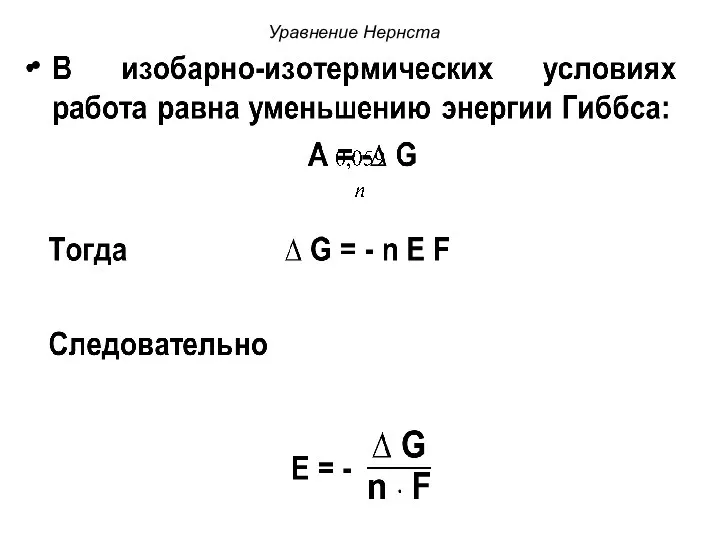
- 17. Уравнение Нернста Величину электродного потенциала можно рассчитать по уравнению Нернста: E = E0 ± ln aкатион,
- 18. Если потенциалопределяющими ионами являются катионы, то в уравнении Нернста ставится знак «+», если анионы – знак
- 19. Уравнение Нернста
- 20. При 180 С (291K) уравнение Нернста имеет вид: E = E0 ± lg aкат./анион. Величина E0
- 21. Измерение величины электродных потенциалов. Гальванические цепи. Электродный потенциал нельзя измерить непосредственно. Можно измерять только разность потенциалов
- 22. Для определения стандартных элек-тродных потенциалов металлов собирают гальваническую цепь из металлического электрода и стан-дартного (нормального) водородного
- 23. Измерение величины электродных потенциалов. Гальванические цепи Нормальный водородный электрод состоит из черненой платиновой пластинки, насыщенной газообразным
- 24. Измерение величины электродных потенциалов. Гальванические цепи Его электродная реакция: H+ + 1e- ↔ 1/2 H20 Уравнение
- 25. Для измерения стандартных электродных потенциалов металлов собирают гальваническую цепь, состоящую из исследуемого электрода и стандартного водородного
- 26. Измерение величины электродных потенциалов. Гальванические цепи Схему гальванической цепи записывают следующим образом: тв1 ж1 ж2 тв2
- 27. ЭДС всегда величина положи-тельная, т.е. при ее расчете необхо-димо из более положительного значения электродного потенциала вычитать
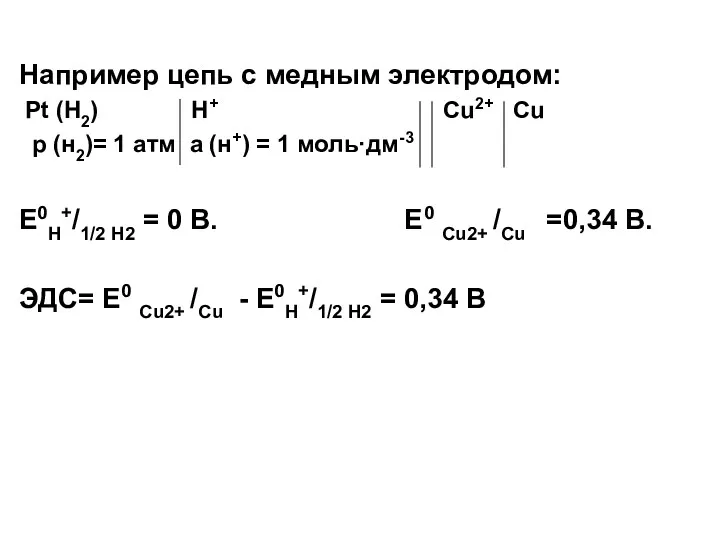
- 28. Например цепь с медным электродом: Pt (H2) H+ Cu2+ Cu p (н2)= 1 атм a (н+)
- 29. Водородный электрод сложен по конструкции и его потенциал зависит от трудно контролируемых факторов. Поэтому на практике
- 30. Хлорсеребряный электрод (ХСЭ) сравнения представляет собой серебряную проволоку, покрытую слоем хлорида серебра и опущенную в насыщенный
- 31. Зависимость электродного потенциала от активности хлорид-ионов описывается уравнением Нернста: Eх.с. = E0х.с. - ln a (Cl-)
- 32. Электроды определения (мембранные электроды) В электрохимических измерениях наряду с электродами сравнения широко используются электроды определения или
- 33. Наиболее распространенным электродом определения является стеклянный электрод. Он состоит из стеклянной трубки, заканчивающейся шариком из специального
- 34. Стеклянный электрод перед использованием вымачивают не менее суток в дистиллированной воде или слабом растворе НСI. Набухшая
- 35. При помещении стеклянного электрода в раствор в поверхностный слой стекла из раствора интенсивно проникают ионы водорода,
- 36. Ионоселективные электроды В последние годы ионоселективные электроды приобретают особо важное значение для медицины. Это электроды, проявляющие
- 37. . В настоящее время число ионоселективных электродов с четко выраженной селективностью к определенным ионам составляет более
- 38. Окислительно-восстановительные электроды Раствор, содержащий одновременно окисленную и восстановленную формы вещества, называют окислительно-восстановительной системой (red–ox) системой. Инертный
- 39. Окислительно-восстановительные электроды Инертный металл выполняет роль посредника в осуществлении переноса электронов между окисленной и восстановленной формами
- 40. Окислительно-восстановительные электроды Например: [Fe (CN)6]3- Pt [Fe (CN)6]4- Электродная реакция: [Fe (CN)6]3- + 1e- [Fe (CN)6]4-
- 41. Окислительно-восстановительные электроды В осуществлении электродной реакции в сложных электродах помимо окисленной и восстановленной форм принимают участие
- 42. Окислительно-восстановительные электроды Таким образом, в уравнение Нернста-Петерса для сложного red–ox электрода, помимо концентраций окисленной и восстановленной
- 43. Направление окислительно-восстановительных процессов Окислительно-восстановительный процесс будет протекать в нужном направлении при условии, что разность электродных потенциалов
- 44. Направление окислительно-восстановительных процессов Таким образом, первая система является системой восстановителя. На этом электроде будет протекать процесс
- 46. Скачать презентацию



































![Окислительно-восстановительные электроды Например: [Fe (CN)6]3- Pt [Fe (CN)6]4- Электродная реакция:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/443103/slide-39.jpg)




 Аномалии развития пищевода
Аномалии развития пищевода Искусственная вентиляция легких
Искусственная вентиляция легких Методы исследования в акушерстве и гинекологии
Методы исследования в акушерстве и гинекологии Технология изготовления мостовидного протеза из пластмассы
Технология изготовления мостовидного протеза из пластмассы Анатомия глазного яблока
Анатомия глазного яблока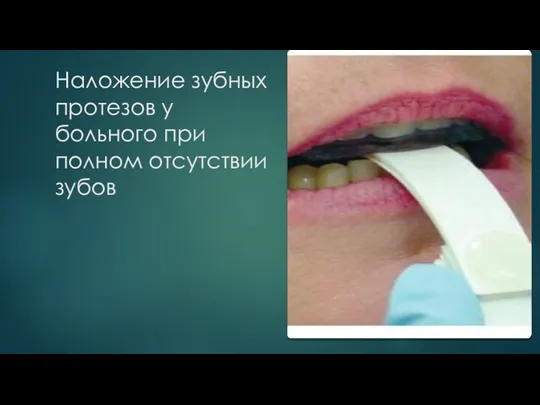 Наложение зубных протезов у больного при полном отсутствии зубов
Наложение зубных протезов у больного при полном отсутствии зубов Стандартизация паразитологических методов в лабораторной диагностике
Стандартизация паразитологических методов в лабораторной диагностике Жас балаларда көмірсу алмасуының маңызы. Оның бұзылыстарының семиотикасы
Жас балаларда көмірсу алмасуының маңызы. Оның бұзылыстарының семиотикасы Балалардағы субүйрек
Балалардағы субүйрек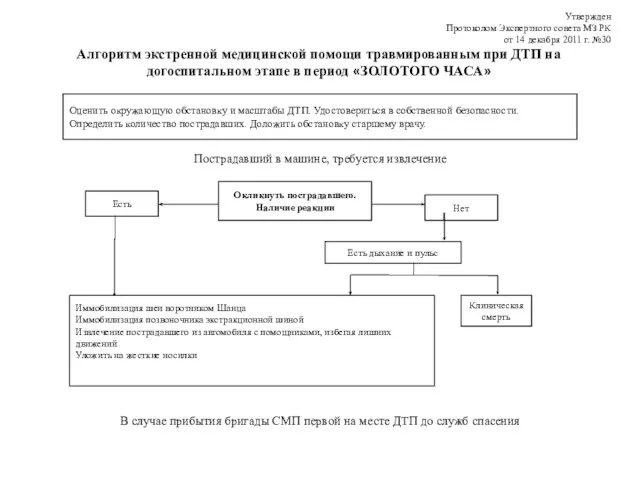 Алгоритм экстренной медицинской помощи травмированным при ДТП на догоспитальном этапе в период золотого часа
Алгоритм экстренной медицинской помощи травмированным при ДТП на догоспитальном этапе в период золотого часа Саркома матки
Саркома матки Аномалии конституции
Аномалии конституции Применение плазмафареза и внутривенного иммуноглобулина при лечении синдрома Гийена-Барре
Применение плазмафареза и внутривенного иммуноглобулина при лечении синдрома Гийена-Барре Жүрек-тамыр жүйесі зақымдануларындағы өмірге қауіп кезін анықтау мен жедел жәрдем көрсету
Жүрек-тамыр жүйесі зақымдануларындағы өмірге қауіп кезін анықтау мен жедел жәрдем көрсету Неотложная помощь при вывихе
Неотложная помощь при вывихе Вирустар және фагтар
Вирустар және фагтар Геморрагические заболевания у новорожденных
Геморрагические заболевания у новорожденных Билиарлы жүйенің және өт шығару жолдарының дисфункциясы
Билиарлы жүйенің және өт шығару жолдарының дисфункциясы Операции на сосудах. Сосудистый шов, виды, инструменты для операций на сосудах
Операции на сосудах. Сосудистый шов, виды, инструменты для операций на сосудах Гемостаз және гемокоагуляцияның клиникалық физиологиясы және биохимиясы. Гематологиядағы интенсивті терапия
Гемостаз және гемокоагуляцияның клиникалық физиологиясы және биохимиясы. Гематологиядағы интенсивті терапия Жедел перитонит
Жедел перитонит Перемещение пациента
Перемещение пациента Миастения - вопросы дифференциального диагноза и лечения
Миастения - вопросы дифференциального диагноза и лечения ЛФ упруго-вязко-пластичной консистенций. Мази
ЛФ упруго-вязко-пластичной консистенций. Мази Государственный материальный резерв медицинского и санитарнохозяйственного имущества
Государственный материальный резерв медицинского и санитарнохозяйственного имущества Оптическая система глаза. Лекция № 5
Оптическая система глаза. Лекция № 5 Балалардағы бет – жақ аймағындағы ауытқуларды емдеуде миогимнастикасы
Балалардағы бет – жақ аймағындағы ауытқуларды емдеуде миогимнастикасы Преждевременные роды
Преждевременные роды