Содержание
- 2. СТРУКТУРА УЧЕБНОГО СОДЕРЖАНИЯ Определение Магнитные свойства Методы получения магнитных наночастиц 3.1. Химические методы синтеза магнитных наночастиц
- 3. ОПРЕДЕЛЕНИЕ
- 4. Определение Магнитные наночастицы (МНЧ) – наночастицы, имеющие постоянный или наведенный магнитный момент. Магнитные наночастицы могут состоять
- 5. МАГНИТНЫЕ СВОЙСТВА
- 6. Магнитные свойства Вещества проявляют магнитные свойства вследствие внутренних движений электрических зарядов, так называемых круговых токов. Источниками
- 7. Магнитно-упорядоченные вещества К магнитно-упорядоченным веществам относят ферромагнетики, антиферромагнетики и ферримагнетики. Ферромагнетики – это вещества, обладающие большой,
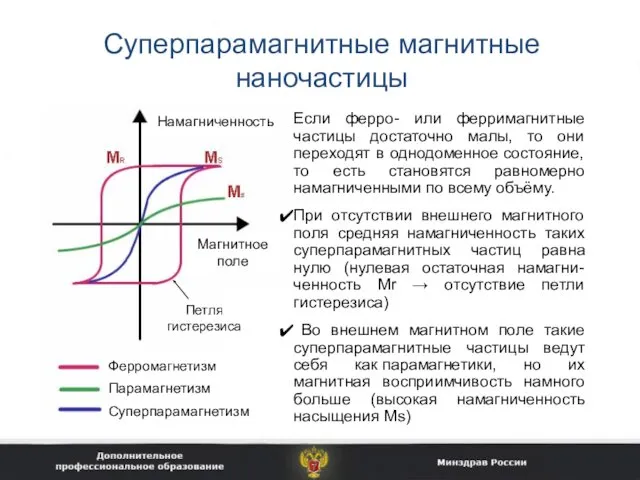
- 8. Суперпарамагнитные магнитные наночастицы Если ферро- или ферримагнитные частицы достаточно малы, то они переходят в однодоменное состояние,
- 9. МЕТОДЫ ПОЛУЧЕНИЯ МАГНИТНЫХ НАНОЧАСТИЦ
- 10. Классификация Физические методы (из компактного материала путем диспергирования различными методами) Химические методы Направленный синтез (из химических
- 11. Особенности синтеза магнитных наночастиц В ходе синтеза наночастиц любой природы (в том числе и магнитных наночастиц)
- 12. Физические методы получения магнитных наночастиц Механохимический синтез (измельчение с помощью шаровых, вибрационных, планетарных и других мельниц)
- 13. 1. Химические методы получения магнитных наночастиц
- 14. Химические методы получения магнитных наночастиц Метод соосаждения и осаждения (соосаждение / осаждение солей из водных растворов
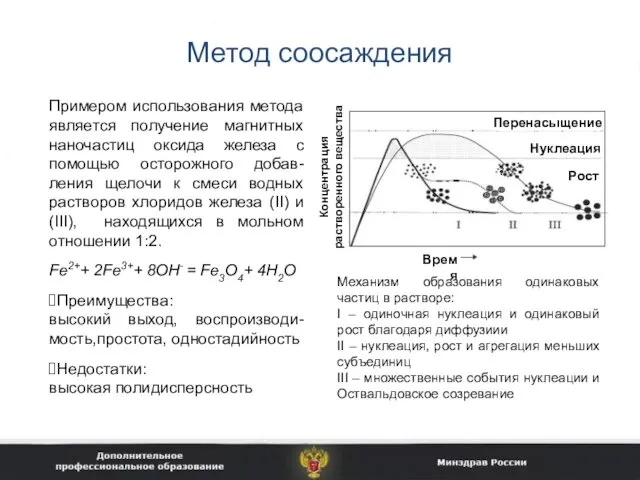
- 15. Метод соосаждения Механизм образования одинаковых частиц в растворе: I – одиночная нуклеация и одинаковый рост благодаря
- 16. Синтез в обратных мицеллах Мицеллы – термодинамически стабильные коллоиды, образованные двумя несмешивающимися жидкостя-ми за счет стабилизации
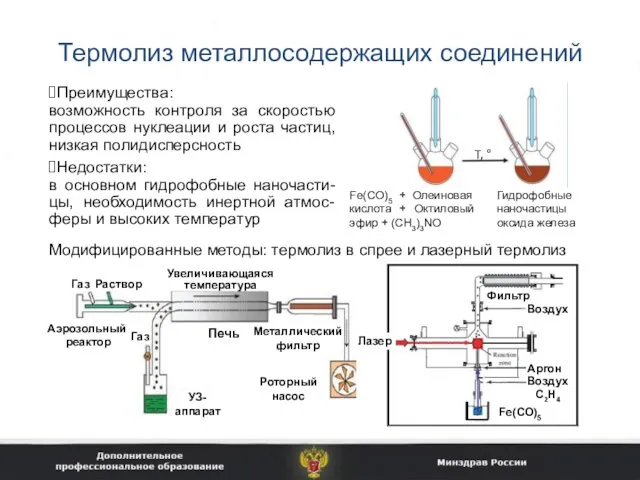
- 17. Термолиз металлосодержащих соединений Преимущества: возможность контроля за скоростью процессов нуклеации и роста частиц, низкая полидисперсность Недостатки:
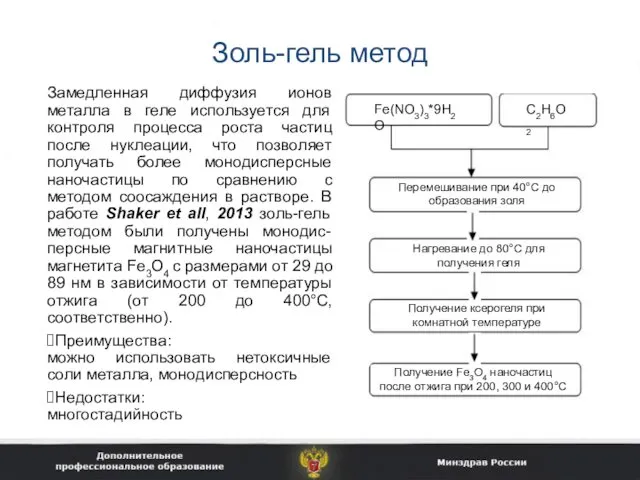
- 18. Золь-гель метод Замедленная диффузия ионов металла в геле используется для контроля процесса роста частиц после нуклеации,
- 19. Микробиологические методы получения магнитных наночастиц Живые организмы могут быть использованы как прямой источник ультрадисперсных материалов, свойства
- 20. Сравнение методов получения магнитных наночастиц Физические методы синтеза (возможно получать магнитные наночастицы с высоким уровнем поверхностной
- 21. СТАБИЛИЗАЦИЯ МАГНИТНЫХ НАНОЧАСТИЦ
- 22. Стабилизация магнитных наночастиц Для биомедицинских применений магнитных наночастиц оксида железа необходимым шагом является осуществление их покрытия
- 23. Функции покрытий для магнитных наночастиц снижение агрегации (увеличение стабильности в водном растворе) увеличение времени циркуляции в
- 24. Требования к покрытиям для магнитных наночастиц Для осуществления направленной доставки лекарственных препаратов и визуализирующих агентов, а
- 25. Виды покрытий магнитных наночастиц органические синтетические полимеры (хитозан, декстран, полиэтиленгликоль - ПЭГ, поли-D,L-лактид-ко-гликолид – PLGA, поливинилпироллидон
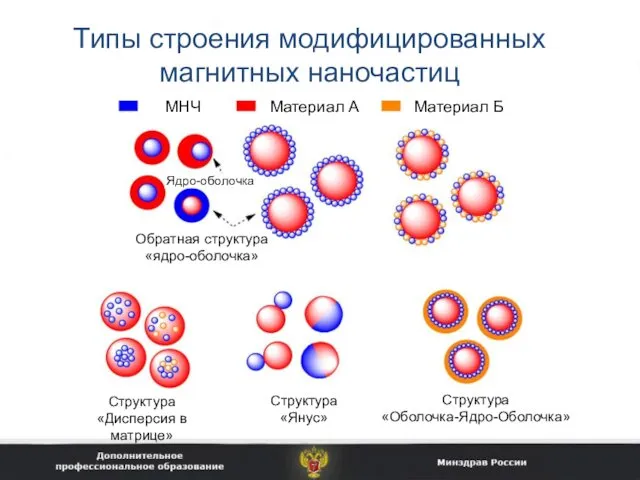
- 26. Типы строения модифицированных магнитных наночастиц
- 27. ОБЛАСТИ ПРИМЕНЕНИЯ МАГНИТНЫХ НАНОЧАСТИЦ
- 28. Области применения магнитных наночастиц Магнитно-резонансная томография (МРТ) Магнитная сепарация Магнитная гипертермия Магнитная визуализация частиц Магнитная биодетекция
- 29. 1. Применение магнитных наночастиц в МРТ
- 30. Применение магнитных наночастиц в МРТ Взаимодействие радиочастотного поля с магнитными ядрами, находящимися во внешнем магнитном поле,
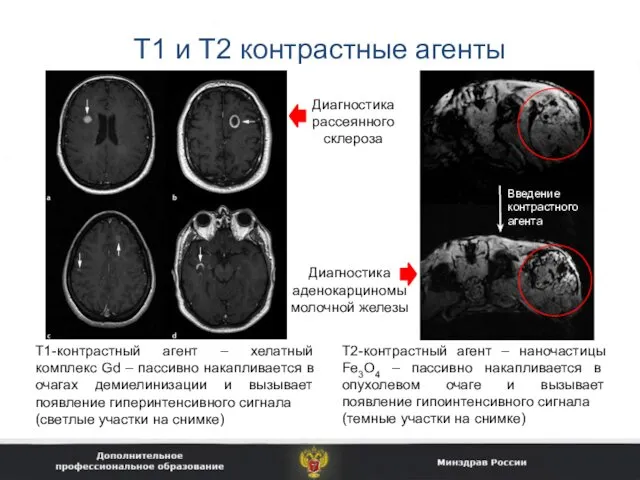
- 31. Т1 и Т2 контрастные агенты Т1-контрастный агент – хелатный комплекс Gd – пассивно накапливается в очагах
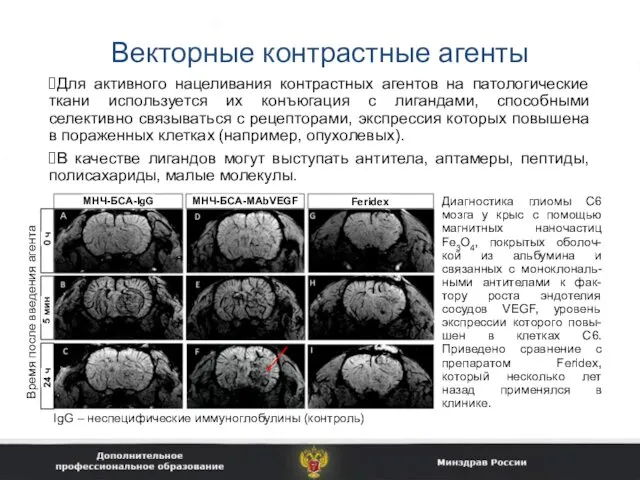
- 32. Векторные контрастные агенты Для активного нацеливания контрастных агентов на патологические ткани используется их конъюгация с лигандами,
- 33. 2. Магнитные наночастицы в тераностике
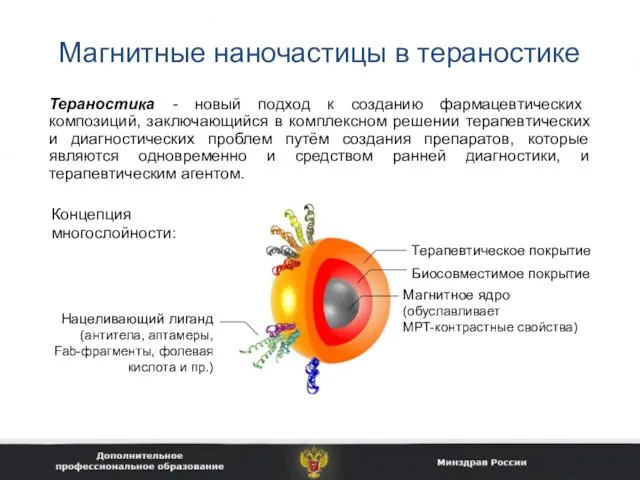
- 34. Магнитные наночастицы в тераностике Тераностика - новый подход к созданию фармацевтических композиций, заключающийся в комплексном решении
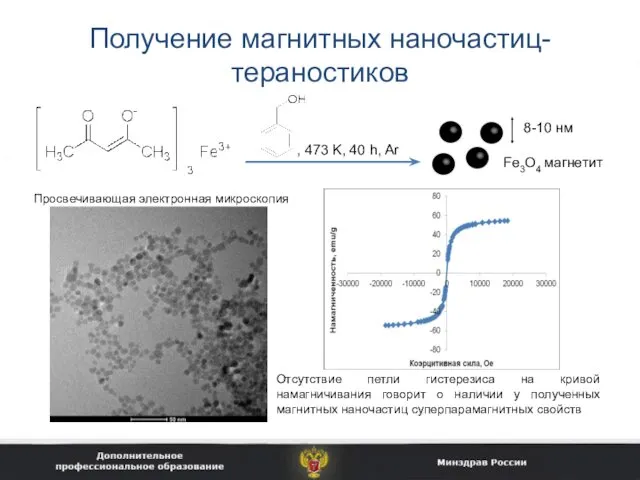
- 35. Получение магнитных наночастиц-тераностиков Просвечивающая электронная микроскопия Отсутствие петли гистерезиса на кривой намагничивания говорит о наличии у
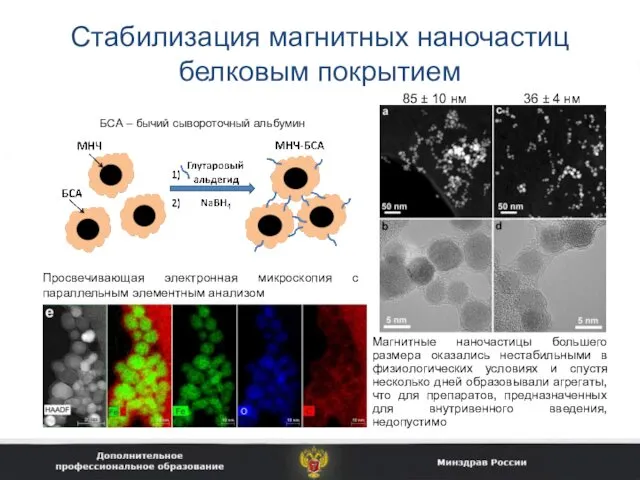
- 36. Стабилизация магнитных наночастиц белковым покрытием 85 ± 10 нм 36 ± 4 нм Просвечивающая электронная микроскопия
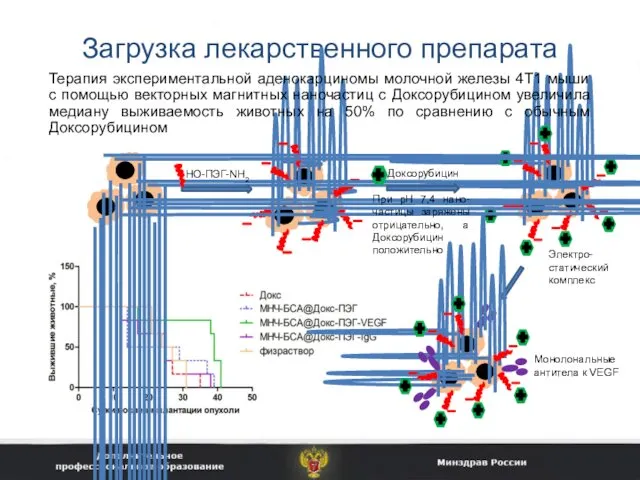
- 37. Загрузка лекарственного препарата Монолональные антитела к VEGF Терапия экспериментальной аденокарциномы молочной железы 4T1 мыши с помощью
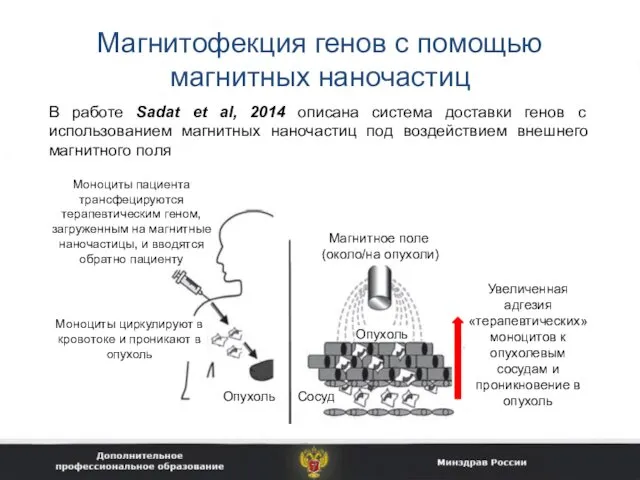
- 38. Магнитофекция генов с помощью магнитных наночастиц В работе Sadat et al, 2014 описана система доставки генов
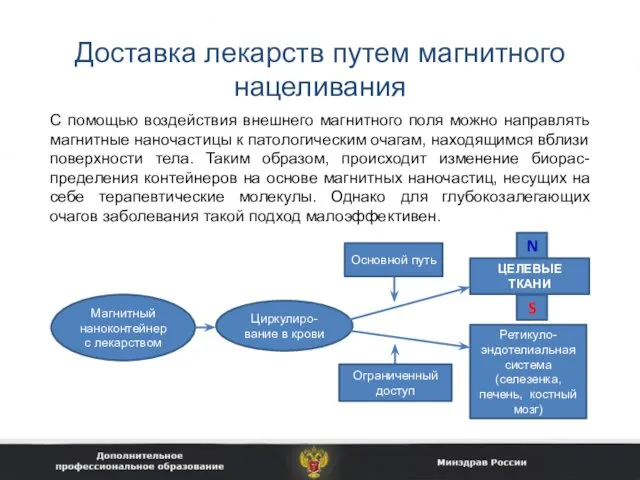
- 39. Доставка лекарств путем магнитного нацеливания С помощью воздействия внешнего магнитного поля можно направлять магнитные наночастицы к
- 40. Магнитная гипертермия Механизм действия магнитной гипертермии основан на повышенной чувствительности опухолевых клеток к воздействию высокой температуры
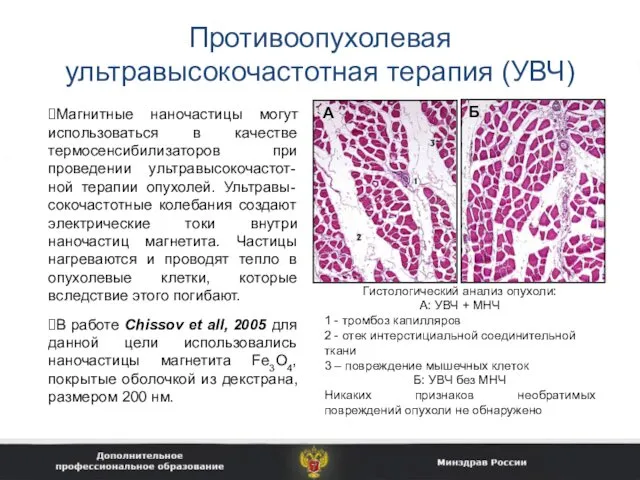
- 41. Противоопухолевая ультравысокочастотная терапия (УВЧ) Магнитные наночастицы могут использоваться в качестве термосенсибилизаторов при проведении ультравысокочастот-ной терапии опухолей.
- 43. Скачать презентацию


























 Анемии
Анемии Бальнеологические курорты Сибири
Бальнеологические курорты Сибири Осложнения сахарного диабета
Осложнения сахарного диабета Мед процес в дермат
Мед процес в дермат Биохимия крови-3. Водно-электролитный обмен
Биохимия крови-3. Водно-электролитный обмен Неотложная медицинская помощь и лечение при астматическом статусе
Неотложная медицинская помощь и лечение при астматическом статусе Кавернозный и фиброзно-кавернозный туберкулез легких. Патогенез каверны. Цирротический туберкулез легких
Кавернозный и фиброзно-кавернозный туберкулез легких. Патогенез каверны. Цирротический туберкулез легких Энтеровирусы. Классификация рода энтеровирусы
Энтеровирусы. Классификация рода энтеровирусы Меланома. Методы диагностики меланомы
Меланома. Методы диагностики меланомы Здоровый образ жизни
Здоровый образ жизни Искусственное вскармливание детей первого года жизни
Искусственное вскармливание детей первого года жизни Ішкі жұқпалы емес аурулар клиникалық диагностикамен. Ветеринариялық зоогигиена, хирургия
Ішкі жұқпалы емес аурулар клиникалық диагностикамен. Ветеринариялық зоогигиена, хирургия Средства, влияющие на эфферентную нервную систему: Адренергические ЛС
Средства, влияющие на эфферентную нервную систему: Адренергические ЛС Қант диабеті кезіндегі лабораториялық зерттеулер
Қант диабеті кезіндегі лабораториялық зерттеулер Клиническая фармакология антипсихотических препаратов
Клиническая фармакология антипсихотических препаратов Физическое развитие детей
Физическое развитие детей Основы кардиохирургии. Введение
Основы кардиохирургии. Введение Травматизм в хореографии
Травматизм в хореографии Жанұя денсаулығы. Бала денсаулығы
Жанұя денсаулығы. Бала денсаулығы Предсказание магнитных свойств наночастиц для биомедицинских применений. Сбор данных
Предсказание магнитных свойств наночастиц для биомедицинских применений. Сбор данных Классификация лекарственных средств М.Д.Машковского
Классификация лекарственных средств М.Д.Машковского Жүкті әйелдердегі және балалардағы тыныс алу патологиясының визуальді диагностикасы
Жүкті әйелдердегі және балалардағы тыныс алу патологиясының визуальді диагностикасы В здором теле - здоровый дух
В здором теле - здоровый дух Роль физической культуры и спорта в профилактике заболеваний и укреплении здоровья
Роль физической культуры и спорта в профилактике заболеваний и укреплении здоровья Заболевания нижних дыхательных путей. Клиническая анатомия гортани
Заболевания нижних дыхательных путей. Клиническая анатомия гортани Гипердинамическое расстройство детства или синдром дефицита внимания, импульсивности и гиперактивности подготовила клинический
Гипердинамическое расстройство детства или синдром дефицита внимания, импульсивности и гиперактивности подготовила клинический Сахарный диабет у кошек и собак
Сахарный диабет у кошек и собак Радионуклеидные методы исследования органов желудочнокишечного тракта
Радионуклеидные методы исследования органов желудочнокишечного тракта