Содержание
- 2. Раннее энтеральное питание – один из методов, имеющий доказанное влияние на снижение осложнений. [Doig GS, Heighes
- 3. Концепция раннего энтерального питания обладает рядом преимуществ: — предотвращает атрофию слизистой оболочки кишечника и поддерживает целостность
- 4. Классификация смесей для энтерального питания. 1. Стандартные смеси 1.1 Изокалорийные стандартные смеси 1.2 Изокалорийные стандартные смеси
- 5. Метаболически направленные смеси. 3.1 Смеси предназначенные для больных с сахарным диабетом и стрессорной гипергликемией (типа «Диабет»)
- 6. Алгоритм проведения раннего энтерального питания: — энтеральное питание следует проводить так рано, как это только возможно;
- 7. Метоклопрамид – прокинетик первого поколения, обладает ярко выраженным свойством усиливать моторику желудка и кишечника. Вводится внутривенно
- 8. противопоказания к энтеральному питанию, которые выделяет целевая группа ЕSPEN: — паралитический илеус; — обструктивная кишечная непроходимость;
- 9. Побочные эффекты неадекватной нутритивной поддержки «Недостаточное питание»: - нарушение заживления п/о ран - увеличение риска инфекционных
- 10. Когда?
- 11. Противопоказаниями к проведению тотального парентерального питания : острая фаза немедленно после хирургического вмешательства, шок любой этиологии,
- 12. Необходимым условием для старта раннего энтерального питания является восстановление всасывательной и моторной функций кишечника в пределах
- 13. СТЕПЕНИ ОСТРОГО ГАСТРОИНТЕСТИНАЛЬНОГО ПОВРЕЖДЕНИЯ (ОГИП) 1-я степень ОГИП (риск гастроинтестинальной недостаточности – risk of developing gastrointestinal
- 14. Шкала гастроинтестинального повреждения (A.Reintam) Представленные рекомендации и шкала ОГИП создают базу для адекватной оценки проводимой интенсивной
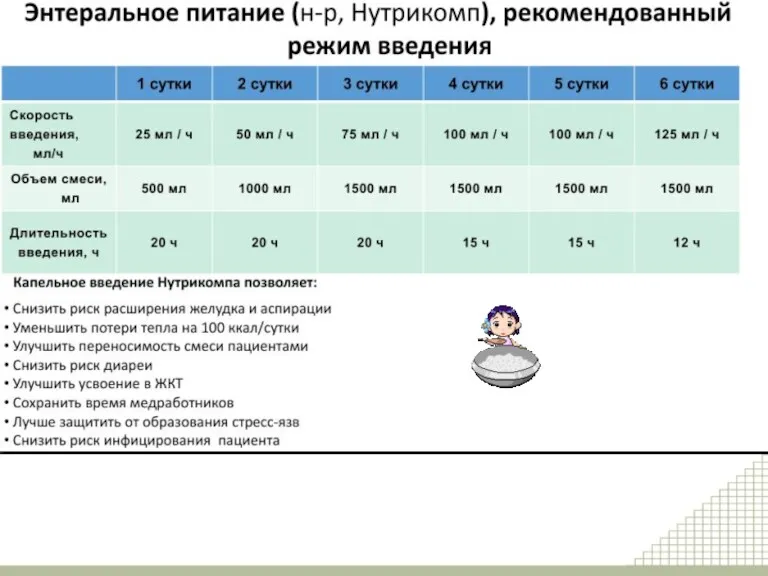
- 15. Толерантность к ранней энтеральной поддержке определяется на основании регистрации времени восстановления всасывательной функции кишечника, оценки резидуального
- 16. Практически всем пациентам с 8-12 часа после операции лаваж начинают с введения глюкозо-электролитного раствора непрерывным капельным
- 17. При применении Стерофундина происходит восстановление и поддержание осмотического баланса, как вне клетки, так и внутриклеточно. Малат
- 18. Энергетическая ценность смеси для питания в стандартной концентрации - 1 ккал/мл готовой смеси. При этом осмоляльность
- 19. Согласно новых акцентов конгресса ESPEN [http://www.espen.org/education/espen-guidelines] удовлетворение белковых и энергетических потребностей при использовании только энтерального питания
- 20. СКОЛЬКО ? •С ЧЕГО НАЧИНАТЬ ?
- 22. уравнения Харриса — Бенедикта: для мужчин: ОО = 88,362 + (13,397 х вес, кг) + (4,799
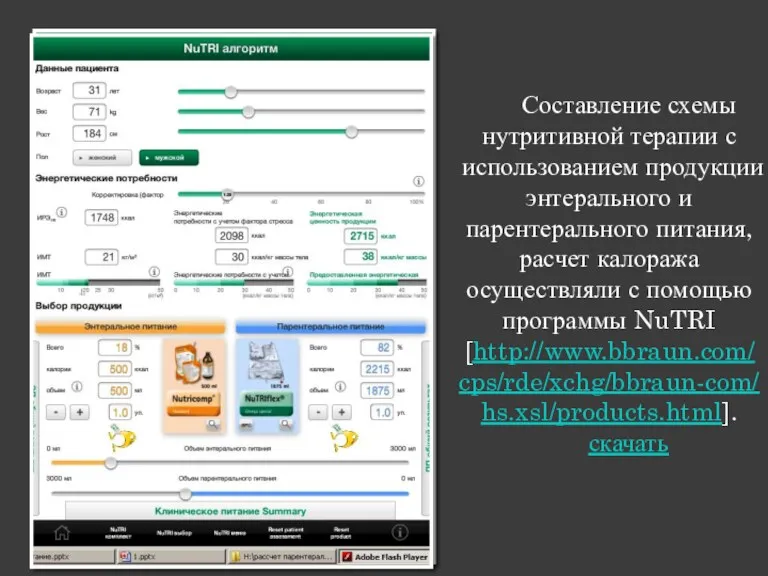
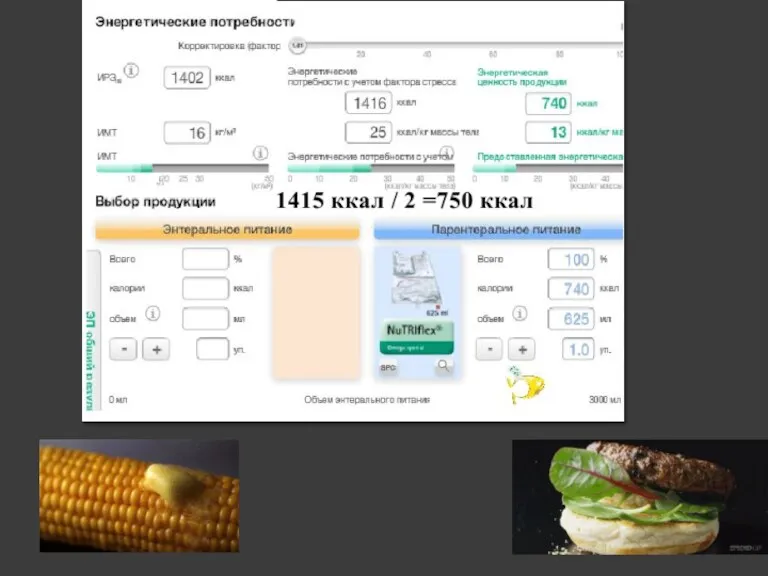
- 23. Составление схемы нутритивной терапии с использованием продукции энтерального и парентерального питания, расчет калоража осуществляли с помощью
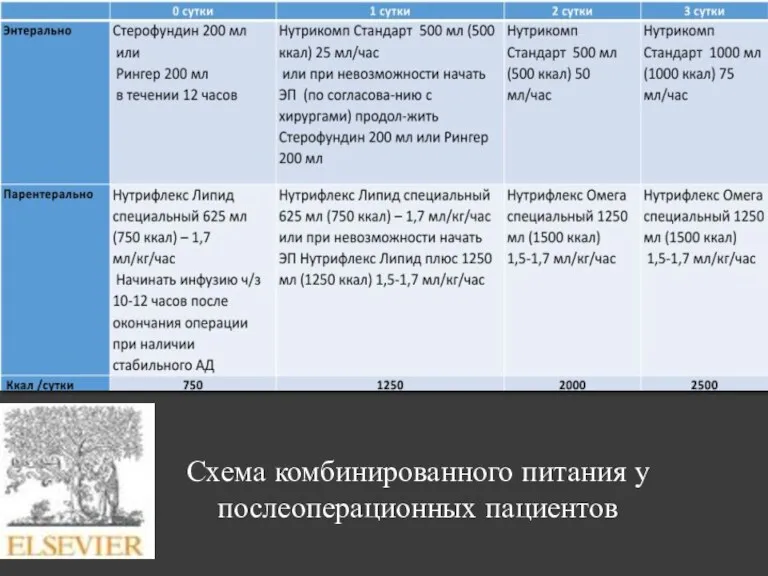
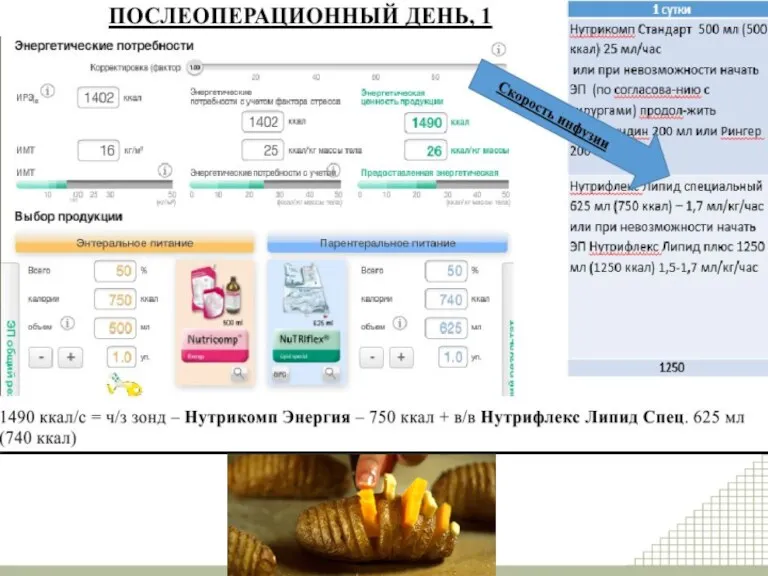
- 26. Схема комбинированного питания у послеоперационных пациентов
- 29. ПОСЛЕОПЕРАЦИОННЫЙ ДЕНЬ, 2 ПОСЛЕОПЕРАЦИОННЫЙ ДЕНЬ, 3 ПОСЛЕОПЕРАЦИОННЫЙ ДЕНЬ, 4
- 30. Эффективность рестриктивной инфузионной терапии оценивалась по достижению целевых значений целенаправленной терапии травмы : центрального венозного давления
- 31. Особое значение придавали показателям, характеризующим адекватность питания – белкового (азот мочевины, альбумин сыворотки и протромбиновое время),
- 32. ПАЦИЕНТАМ С ОРДС рекомендуется низкоуглеводная/высоколипидная формула. Уровень глюкозы выше 5 мг/кг/мин может увеличить дыхательный коэффициент более
- 33. ОЖОГИ Белки: потребность в белках у обожженных выше, чем у других категорий больных, и должна удовлетворяться
- 34. НУТРИТИВНАЯ ТЕРАПИЯ ПРИ ТЯЖЕЛОМ СЕПСИСЕ И СЕПТИЧЕСКОМ ШОКЕ 1. Проводить пероральное или энтеральное питание (ЭП) в
- 35. НУТРИТИВНАЯ ТЕРАПИЯ ПРИ ОСТРОМ ПАНКРЕАТИТЕ 1. Пероральное питание при средне- и тяжелом остром панкреатите может возобновляться,
- 36. НУТРИТИВНАЯ ТЕРАПИЯ У ОНКОХИРУРГИЧЕСКИХ БОЛЬНЫХ Показания к назначению клинического питания: снижение массы тела — 5 %
- 37. пребиотики - субстрат обладающих способностью избирательного усваивания различными микроорганизмами. Перспективным в этом плане может оказаться лактулоза,
- 39. Скачать презентацию

















![Согласно новых акцентов конгресса ESPEN [http://www.espen.org/education/espen-guidelines] удовлетворение белковых и энергетических](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/440508/slide-18.jpg)












 Блефариты. Клиника, диагностика, лечение
Блефариты. Клиника, диагностика, лечение Вакцинопрофилактика. Национальный календарь прививок
Вакцинопрофилактика. Национальный календарь прививок Концепция минимальной интервенции в ортопедической стоматологии
Концепция минимальной интервенции в ортопедической стоматологии Гимназиялар мен лицейлерді жоспарлау мен құрылыс жүргізуде қойылатын гигиеналық талаптар. (Дәріс 16)
Гимназиялар мен лицейлерді жоспарлау мен құрылыс жүргізуде қойылатын гигиеналық талаптар. (Дәріс 16) Корь: этиология, патогенез, клиника, лечение и профилактика
Корь: этиология, патогенез, клиника, лечение и профилактика Хирургоялық науқастарды тексерудің қосымша тексеру әдістері
Хирургоялық науқастарды тексерудің қосымша тексеру әдістері Системная красная волчанка
Системная красная волчанка Синдром поликистозных яичников
Синдром поликистозных яичников Листериоз. Возбудитель. Классификация. Лабораторная диагностика
Листериоз. Возбудитель. Классификация. Лабораторная диагностика Гемофилия В
Гемофилия В Синдром длительного сдавления
Синдром длительного сдавления Гельминтоздар. Кіріспе
Гельминтоздар. Кіріспе Внутрибольничная инфекция
Внутрибольничная инфекция Синдром задержки развития плода
Синдром задержки развития плода Вакуум терапия
Вакуум терапия Динамикалық қатар. Медициналық ұйымдардағы динамикалық көрсеткіштерін сараптау және есептеу
Динамикалық қатар. Медициналық ұйымдардағы динамикалық көрсеткіштерін сараптау және есептеу Жүректің жүрекше мен қарынша гипертрофиясының визуальды диагностикалау әдістері
Жүректің жүрекше мен қарынша гипертрофиясының визуальды диагностикалау әдістері ВРТ в лечении мужского бесплодия
ВРТ в лечении мужского бесплодия Вакцинопрофилактика коклюша. Часть 2
Вакцинопрофилактика коклюша. Часть 2 Микробиология. Иммунодиагностические реакции и методы
Микробиология. Иммунодиагностические реакции и методы Современные подходы к лечению дегенеративнодистрофических заболеваний суставов и позвоночника
Современные подходы к лечению дегенеративнодистрофических заболеваний суставов и позвоночника Гастроэзофагальді рефлюкстік синдром
Гастроэзофагальді рефлюкстік синдром Кандидоз слизистой оболочки полости рта
Кандидоз слизистой оболочки полости рта ВИЧ-положительная женщина на приеме у педиатра
ВИЧ-положительная женщина на приеме у педиатра Микробиологическая диагностика ВИЧ-инфекции и СПИД -ассоциированных заболеваний
Микробиологическая диагностика ВИЧ-инфекции и СПИД -ассоциированных заболеваний Растения, которые нас лечат. Фитотерапия
Растения, которые нас лечат. Фитотерапия Неотложная хирургия заболеваний ободочной кишки
Неотложная хирургия заболеваний ободочной кишки Профилактика остеопороза
Профилактика остеопороза