Содержание
- 2. ОРГАНИЗАЦИЯ ДОКЛИНИЧЕСКИХ ИСПЫТАНИЙ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ И ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
- 3. ДОКЛИНИЧЕСКИЕ ИСПЫТАНИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ И ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ЯВЛЯЮТСЯ ОДНОЙ ИЗ ОСНОВНЫХ,ЕСЛИ НЕ ОСНОВНОЙ СФЕРОЙ ДЕЯТЕЛЬНОСТИ
- 4. Основные этапы создания медицинского продукта любого вида и назначения Ответственность разработчика Проработка по аналогам Синтез молекул
- 5. Ответственность контрольно-разрешительных инстанций (Департамент госконтроля качества, эффективности и безопасности лекарственных ср-в, Научный центр экспертизы и госконтроля
- 6. Биоэквивалентность означает, что активный ингредиент воспроизведенного препарата всасывается в организм с аналогичной скоростью и в том
- 7. ТЕ ЖЕ ЭТАПЫ ПРОХОДЯТ ИЗДЕЛИЯ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ . Особенностью является контроль механических, химических свойств материалов и
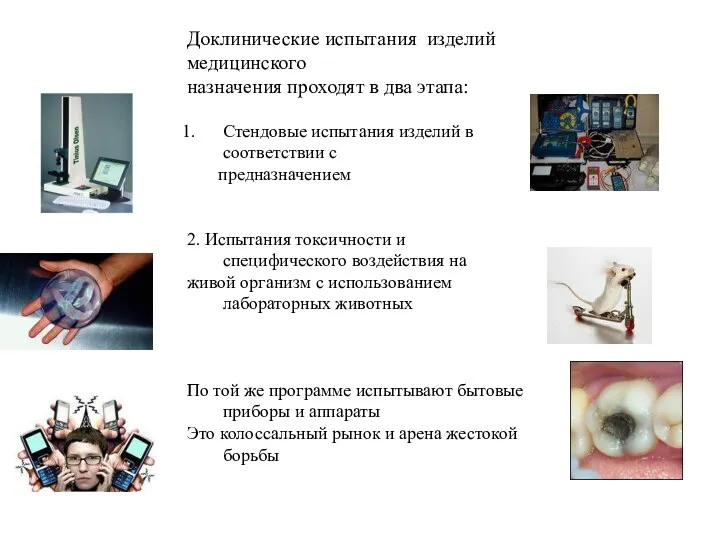
- 8. Доклинические испытания изделий медицинского назначения проходят в два этапа: Стендовые испытания изделий в соответствии с предназначением
- 10. Контроль за соблюдением правовых и этических норм использования животных при проведении доклинических исследований лекарственных средств осуществляется
- 11. Статья 11 2. Доклиническое исследование лекарственного средства для медицинского применения проводится в соответствии с правилами надлежащей
- 12. ТАКИМ ОБРАЗОМ, В ОСНОВУ ПРОВЕДЕНИЯ ДОКЛИНИЧЕСКИХ ИСПЫТАНИЙ ПОЛОЖЕНЫ ПРИНЦИПЫ НАДЛЕЖАЩЕЙ ЛАБОРАТОРНОЙ ПРАКТИКИ GLP КОНКРЕТНЫЕ МЕТОДИКИ И
- 13. ОЧЕНЬ ВАЖНЫМ МОМЕНТОМ ДЛЯ ПРОВЕДЕНИЯ ГРАМОТНОГО ПОЛНОЦЕННОГО ДОКЛИНИЧЕСКОГО ИСПЫТАНИЯ , ДА И ДЛЯ ПРОВЕДЕНИЯ ЛЮБОГО МЕДИКО-БИОЛОГИЧЕСКОГО
- 14. Доклинические исследования безопасности стандартны и складываются из следующих разделов: Изучение общетоксического действия Оценка аллергизирующих свойств Оценка
- 17. ИССЛЕДОВАНИЕ КАК ОСТРОЙ, ТАК И ХРОНИЧЕСКОЙ ТОКСИЧНОСТИ ПОДРАЗУМЕВАЕТ ИСПОЛЬЗОВАНИЕ НЕ МЕНЕЕ ДВУХ ВИДОВ ЖИВОТНЫХ СЛЕДУЕТ ИСПОЛЬЗОВАТЬ
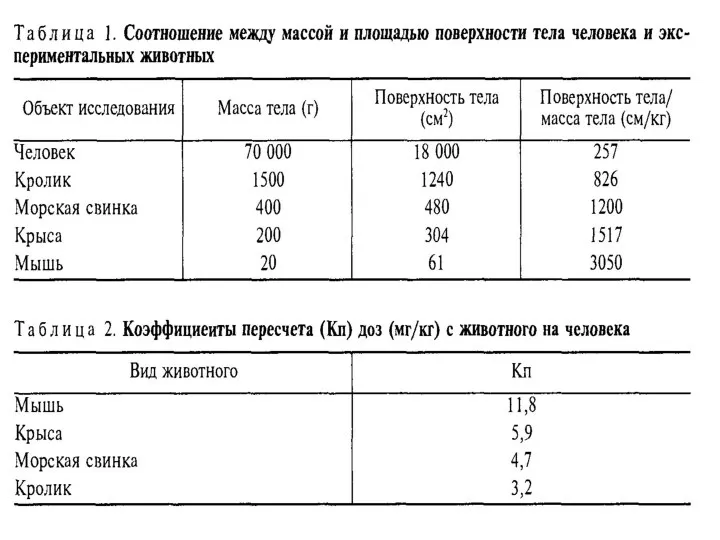
- 19. ЛЕКАРСТВЕННАЯ ФОРМА ИСПЫТЫВАЕМОГО ВЕЩЕСТВА ДОЛЖНА СООТВЕТСТВОВАТЬ ФОРМЕ, ПРИМЕНЯЕМОЙ В КЛИНИКЕ ДОЗА ВЕЩЕСТВА ПЕРЕСЧИТЫВАЕТСЯ НА КИЛОГРАММ (
- 20. АЛЛЕРГИЗИРУЮЩИЕ СВОЙСТВА, АЛЛЕРГЕННОСТЬ
- 22. АЛЛЕРГИЗАЦИЮ ОРГАНИЗМА ИММУНОТОКСИЧЕСКОЕ ДЕЙСТВИЕ
- 24. РЕПРОДУКТИВНАЯ ТОКСИЧНОСТЬ
- 25. МУТАГЕННОСТЬ ПОДРАЗУМЕВАЕТ ОЦЕНКУ ВЛИЯНИЯ ПРЕПАРАТА НА ГЕНЕТИЧЕСКИЙ АППАРАТ БОЛЬНОГО ПОЭТОМУ НАИБОЛЕЕ АКТУАЛЬНО ЕЕ ИССЛЕДОВАНИЕ В ТЕХ
- 26. КАНЦЕРОГЕННОСТЬ
- 27. ДЛЯ ОЦЕНКИ КАНЦЕРОГЕННОГО ДЕЙСТВИЯ ИСПЫТУЕМОГО ВЕЩЕСТВА ОНО ВВОДИТСЯ МЫШАМ В ТЕЧЕНИЕ 18 МЕСЯЦЕВ А КРЫСАМ В
- 28. ТОКСИЧЕСКОЕ ДЕЙСТВИЕ ПРОТИВООПУХОЕВЫХ ПРЕПАРАТОВ ОЦЕНИВАЮТ БОЛЕЕ ТЩАТЕЛЬНО И ВСЕСТОРОННЕ, ЧЕМ ОБЫЧНЫЕ ПРЕПАРАТЫ В СИЛУ ИХ ЗАВЕДОМОЙ
- 29. БИОТЕХНОЛОГИЧЕСКИЕ НЕОРИГИНАЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА (BIOSIMILAR) GUIDELINES ON EVALUATION OF SIMILAR BIOTHERAPEUTIC PRODUCTS (SBPs). WHO, Expert Committee
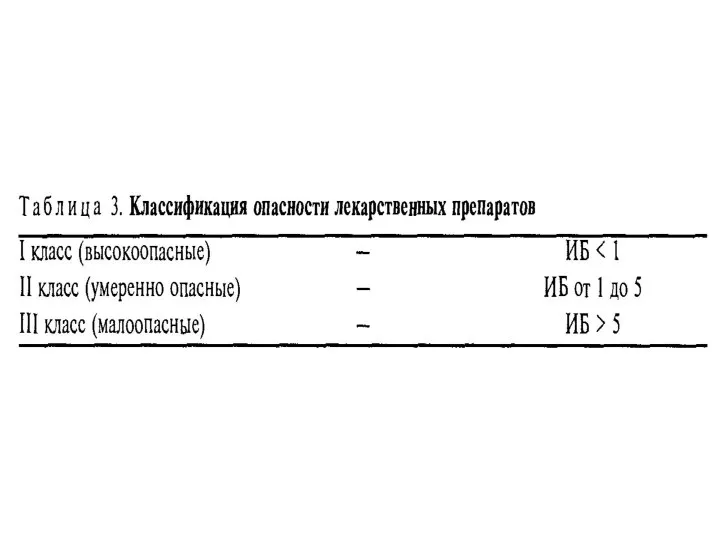
- 30. Оценка безопасности фармакологических веществ на стадии доклинического изучения является неотъемлемой частью комплекса исследований, необходимых для передачи
- 33. При пересчете
- 36. ТРЕБОВАНИЯ К ДОКЛИНИЧЕСКИМ ИССЛЕДОВАНИЯМ (РЕГИСТРАЦИОННОЕ ДОСЬЕ) Общий технический документ (CTD) является международным правилом оформления регистрационного досье.
- 37. ФАРМАКОЛОГИЧЕСКИЙ КОМИТЕТ: ЕГО ФУНКЦИИ И ЗАДАЧИ К основным функциям касательно данных доклинических работ относятся (из Положения
- 38. КЛИНИЧЕСКИЕ ИСПЫТАНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
- 39. Основным регламентирующим документом является
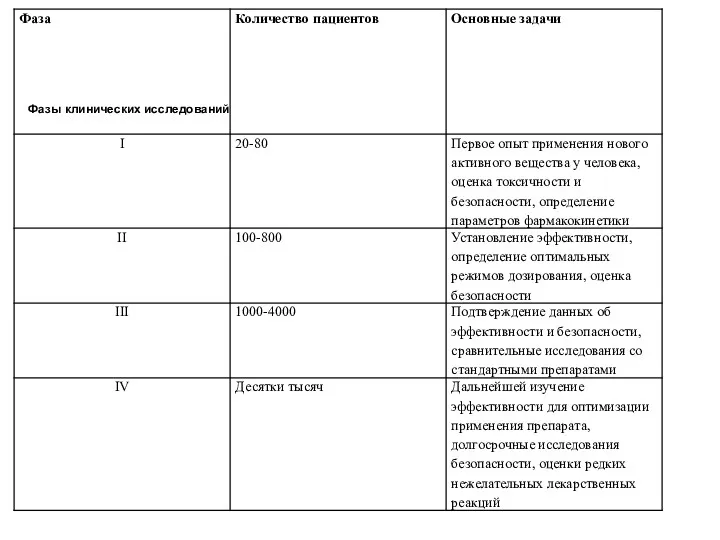
- 40. Фаза I. Первый опыт применения нового активного вещества у человека. Чаще всего исследования проводятся на добровольцах
- 41. Иногда невозможно провести исследования I фазы у здоровых добровольцев из-за токсичности данного препарата (лечение онкологических заболеваний,
- 42. Исследования биоэквивалентности на добровольцах Комиссией по клинической фармакологии и этическим аспектам Фармакологического государственного комитета (ФГК) РФ
- 43. Фаза II. Обычно это первый опыт применения у пациентов с заболеванием, для лечения которого предполагается использовать
- 44. Фаза III. Многоцентровые испытания с участием больших (и, по возможности, разнообразных) групп пациентов (в среднем, 1000-3000
- 45. Фаза IV. Исследования проводятся после начала продажи препарата с целью получить более подробную информацию о длительном
- 46. Фазы клинических исследований
- 47. МОНОЦЕНТРОВЫЕ МУЛЬТИЦЕНТРОВЫЕ
- 48. ИНФОРМИРОВАННОЕ СОГЛАСИЕ Основополагающим документом, определяющим этические принципы проведения биомедицинских исследований с участием людей, является Хельсинкская Декларация
- 49. Правильно составленное ИС должно содержать в себе следующие разделы: положение о том, что предполагается проведение научного
- 50. Клинические исследования, имеющие целью определение безопасности лекарственных средств или иных субстанций или изделий, контактирующих прямо или
- 51. В ретроспективных исследованиях оцениваются события, которые уже произошли. Иногда исследование включает только изучение существующих официальных или
- 52. В несравнительных клинических исследованиях исследуемое лечение ни с чем не сравнивается. Обычно анализируется динамика какого-либо показателя
- 53. Контролируемые исследования. Исследование является контролируемым, когда исследуемый препарат сравнивают с группой сравнения (контрольной группой). Группой сравнения
- 54. РАНДОМИЗИРОВАННЫЕ ИССЛЕДОВАНИЯ Происходит от английского слова RANDOM – CЛУЧАЙНЫЙ При этом исследовании никто до последнего момента
- 55. Плацебо в клинических исследованиях лекарственных средств. Причины, по которым в исследования включают группу, получающую плацебо: Контроль
- 56. разъяснения к статье 29 декларации всемирной медицинской ассоциации гласят: «Настоящим ВМА подтверждает свою позицию в отношении
- 57. Некоторые виды исследований поведения человека включают только наблюдение за людьми в общественных местах (например, наблюдение за
- 58. Исследования при помощи опросов, анкетирования и интервью. Опросы анкетирования и интервью обычно применяются в таких общественных
- 59. Исследования на студентах и служащих. Студенты. Если ожидается участие студентов в исследовании, ЭК должен рассмотреть возможность
- 60. Исследования на людях с нарушениями психики и органов чувств Исследования с привлечением субъектов с психическими нарушениями
- 61. Исследования на пожилых людях В соответствии с общим мнением, пожилые люди представляют собой разнородную по характеру
- 62. Исследования на военнослужащих Действующий в России закон «О лекарственных средствах» запретил проведение клинических испытаний лекарственных средств
- 63. Проблемы клинических исследований стволовых клеток. Проблемы связаны с получением СК, источником которых может быть кровь из
- 65. Скачать презентацию

























































 Еркін қозғалыс жүйесі. Қозғалыс анализаторының анатомо-физиологиялық ерекшеліктері. Орталық және шеткі салдану белгілері
Еркін қозғалыс жүйесі. Қозғалыс анализаторының анатомо-физиологиялық ерекшеліктері. Орталық және шеткі салдану белгілері Принципы рационального питания. Лечебно-профилактическое питание, болезни связанные с характером питания
Принципы рационального питания. Лечебно-профилактическое питание, болезни связанные с характером питания Экстракорпоральные методы детоксикации
Экстракорпоральные методы детоксикации Балаларда Helicobacter pylori – инфекциясымен шақырылған асқорыту жолының жоғары бөлігін емдеу схемасы
Балаларда Helicobacter pylori – инфекциясымен шақырылған асқорыту жолының жоғары бөлігін емдеу схемасы Безсмертник
Безсмертник Онкология сегодня
Онкология сегодня Пороки развития головного мозга. Синдром Веста
Пороки развития головного мозга. Синдром Веста Дистрофии. Механизмы развития дистрофий
Дистрофии. Механизмы развития дистрофий Filling’s material: permanent & temporary
Filling’s material: permanent & temporary Гигиена зрения. Предупреждение глазных болезней
Гигиена зрения. Предупреждение глазных болезней Жүктіліктің УД зерттеу әдісі
Жүктіліктің УД зерттеу әдісі Сифилис. Лепра. Склерома. Сап. Карантинные инфекции
Сифилис. Лепра. Склерома. Сап. Карантинные инфекции Педикулез: симптомы, клиника, диагностика, лечение
Педикулез: симптомы, клиника, диагностика, лечение Описание локального статуса хирургического больного
Описание локального статуса хирургического больного Венерические заболевания
Венерические заболевания Первая медицинская помощь при неотложных состояниях
Первая медицинская помощь при неотложных состояниях Мукополисахаридоз типа I-Н (синдром Гурлер)
Мукополисахаридоз типа I-Н (синдром Гурлер) Организация акушерско-гинекологической помощи
Организация акушерско-гинекологической помощи Электромагниттердің адам өміріне зияны
Электромагниттердің адам өміріне зияны Транквилизаторы. Болеутоляющие средства. Седативные средства
Транквилизаторы. Болеутоляющие средства. Седативные средства Медикаментозная терапия при лихорадке
Медикаментозная терапия при лихорадке Понятия о ВИЧ-инфекции и СПИДе
Понятия о ВИЧ-инфекции и СПИДе Общественное здоровье и здравоохранение. Введение. (Лекция 1)
Общественное здоровье и здравоохранение. Введение. (Лекция 1) Семейства Гречишные (Polygonaceae), Буковые (Fagaceae), Берёзовые (Betulaceae)
Семейства Гречишные (Polygonaceae), Буковые (Fagaceae), Берёзовые (Betulaceae) Кардиопротективные свойства магния в комплексной терапии ишемической болезни сердца
Кардиопротективные свойства магния в комплексной терапии ишемической болезни сердца Государственное учреждение здравоохранения Севастополя Городская больница №5 – Центр охраны здоровья матери и ребенка
Государственное учреждение здравоохранения Севастополя Городская больница №5 – Центр охраны здоровья матери и ребенка Нарушение осанки и плоскостопие
Нарушение осанки и плоскостопие Дистоция плечиков
Дистоция плечиков