Содержание
- 2. Медико-биологическое значение темы Абсорбция Метаболизм Экскреция Распреде-ление Усвоение питательных и лекарственных веществ
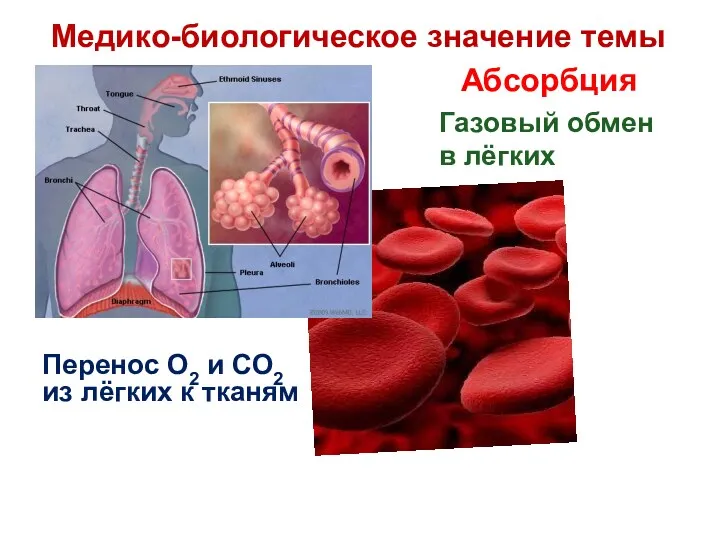
- 3. Абсорбция Перенос О2 и СО2 из лёгких к тканям Газовый обмен в лёгких Медико-биологическое значение темы
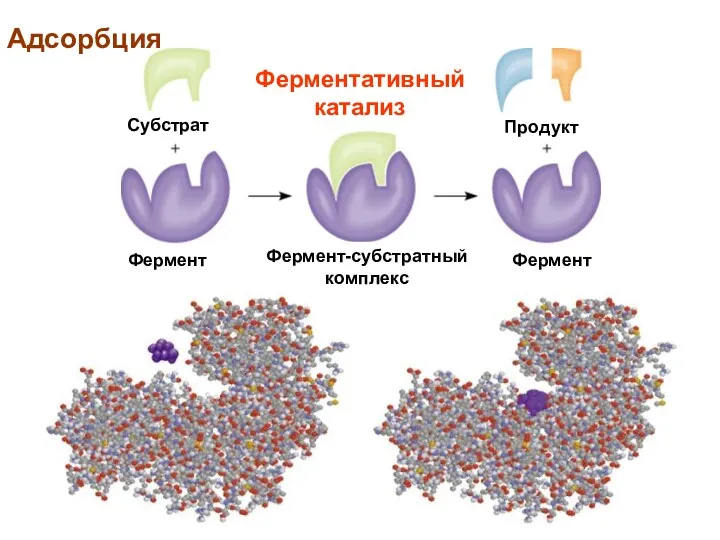
- 4. Ферментативный катализ Адсорбция Субстрат Фермент Фермент-субстратный комплекс Фермент Продукт
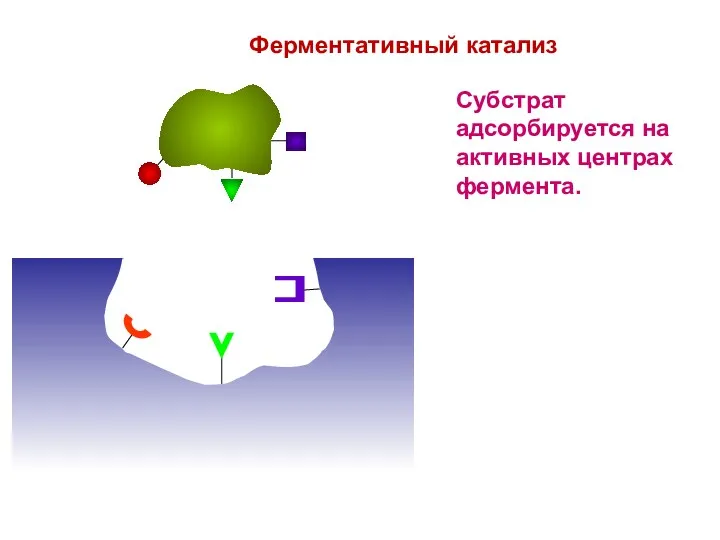
- 5. Ферментативный катализ Субстрат адсорбируется на активных центрах фермента.
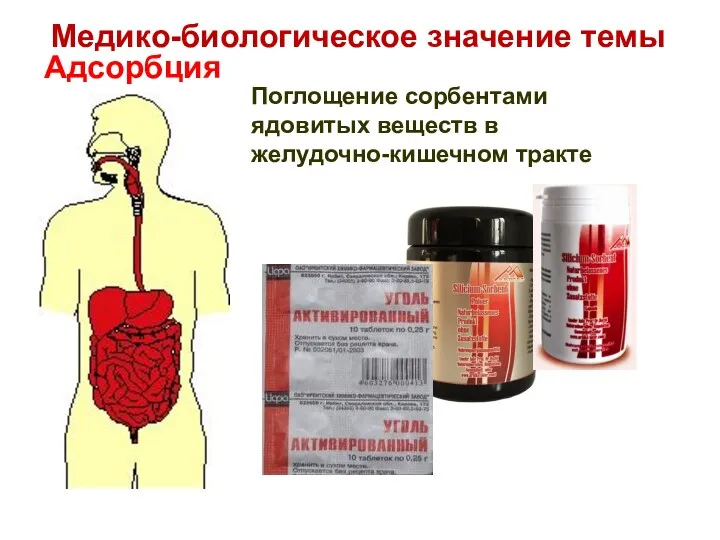
- 6. Адсорбция Поглощение сорбентами ядовитых веществ в желудочно-кишечном тракте Медико-биологическое значение темы
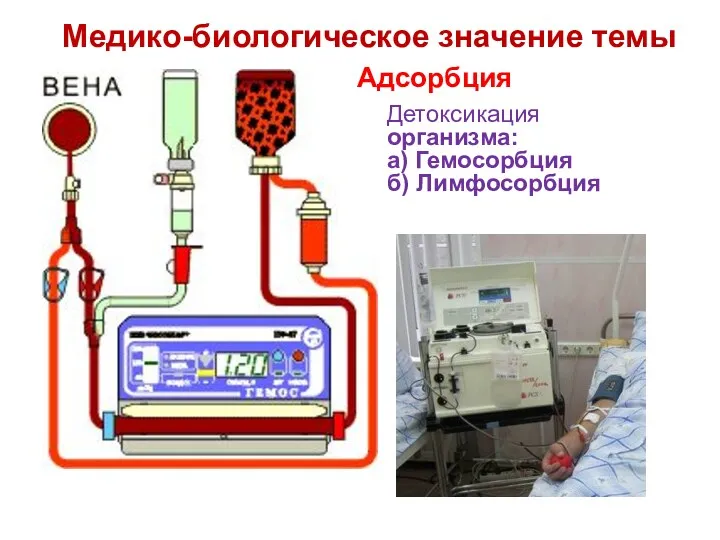
- 7. Детоксикация организма: а) Гемосорбция б) Лимфосорбция Адсорбция Медико-биологическое значение темы
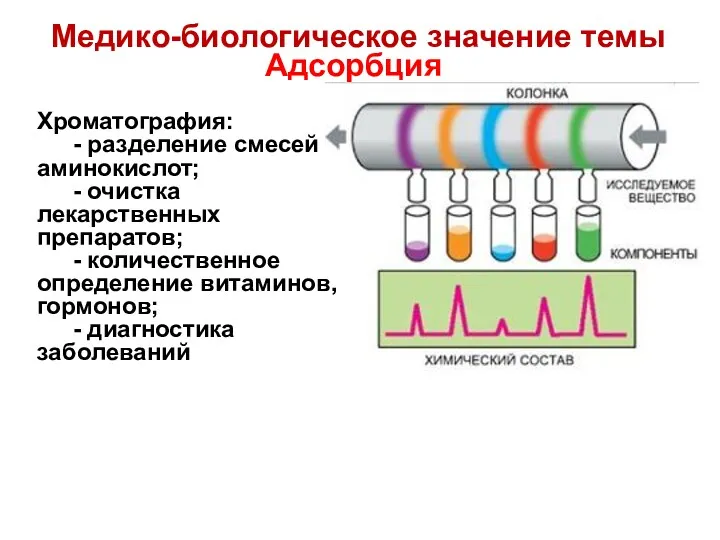
- 8. Хроматография: - разделение смесей аминокислот; - очистка лекарственных препаратов; - количественное определение витаминов, гормонов; - диагностика
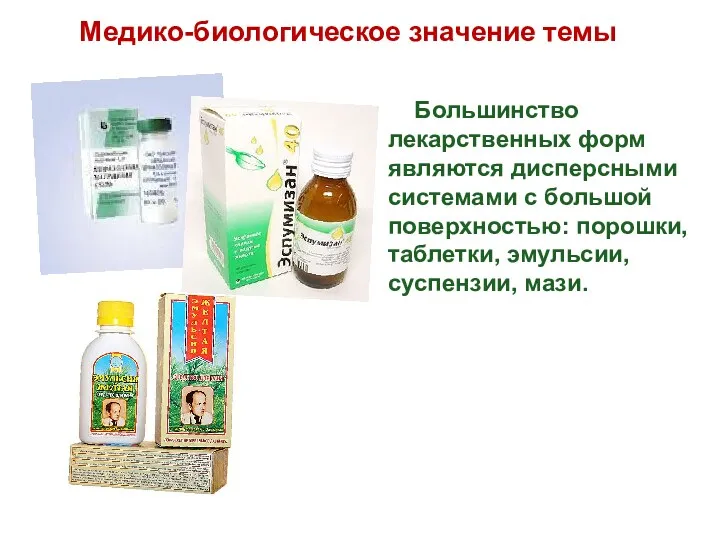
- 9. Медико-биологическое значение темы Большинство лекарственных форм являются дисперсными системами с большой поверхностью: порошки, таблетки, эмульсии, суспензии,
- 10. Многие процессы фарм. технологии - испарение, сублимация и конденсация, адсорбция, гетерогенный катализ и химические реакции протекают
- 11. Медико-биологическое значение темы Вопросы рациональной технологии, стабилизации, хранения, повышения эффективности терапевтического действия лекарств неразрывно связаны исследованиями
- 12. Поверхностные явления. Основные понятия На границе раздела фаз протекают процессы, обусловленные особенностями состава и строения поверхностей.
- 13. Поверхностные явления. Основные понятия Поверхность раздела фаз - слой от одного до нескольких молекулярных диаметров, возникающий
- 14. Поверхностные явления. Основные понятия Sуд = S / V или Sуд = S / m [м2/м3
- 15. Поверхностная энергия Всякая поверхность характеризуется запасом так называемой поверхностной энергии (GS или F). В эту энергию
- 16. Поверхностная энергия Поверхностная энергия (GS) зависит от величины поверхностного натяжения (σ) и площади поверхности (S). Эта
- 17. Поверхностное натяжение В свою очередь, величина поверхностного натяжения определяется изменением энергии Гиббса (∆GS), приходящейся на единицу
- 18. Поверхностные явления. Основные понятия Поверхностная энергия подчиняется основным законам ТД: Согласно первому закону ТД, поверхностная энергия
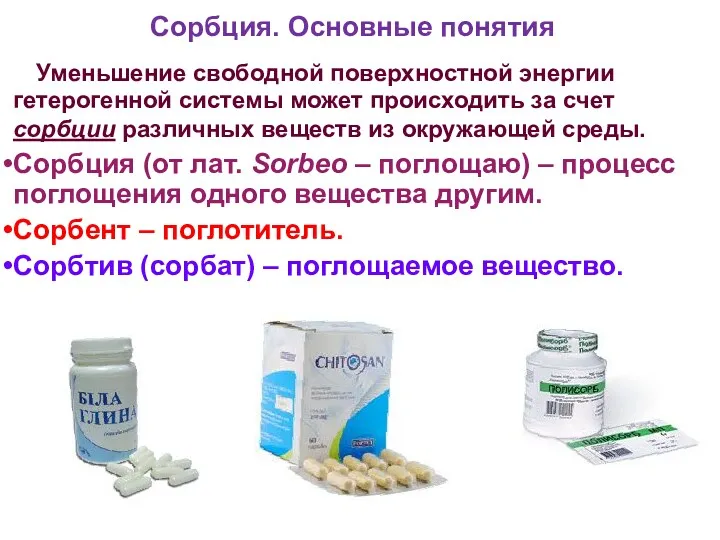
- 19. Сорбция. Основные понятия Уменьшение свободной поверхностной энергии гетерогенной системы может происходить за счет сорбции различных веществ
- 20. Адсорбция – поглощение поверхностью сорбента. Абсорбция – поглощение всем сорбентом. Сорбция. Основные понятия Адсорбция Абсорбция
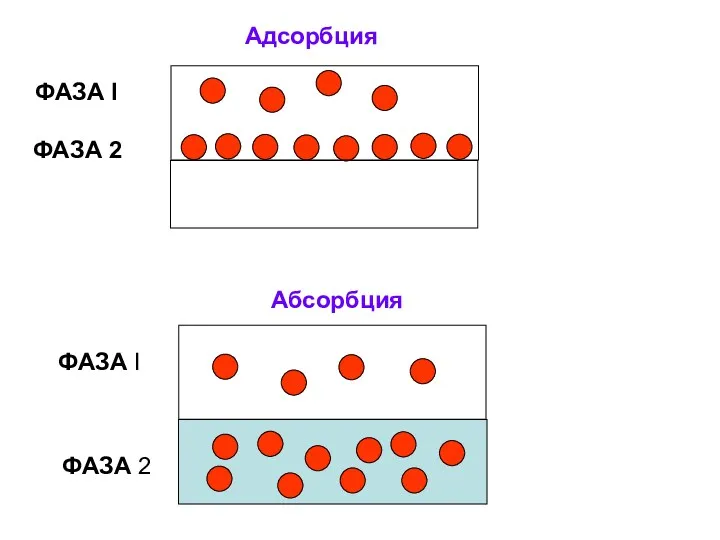
- 21. Адсорбция Абсорбция ФАЗА I ФАЗА 2 ФАЗА I ФАЗА 2
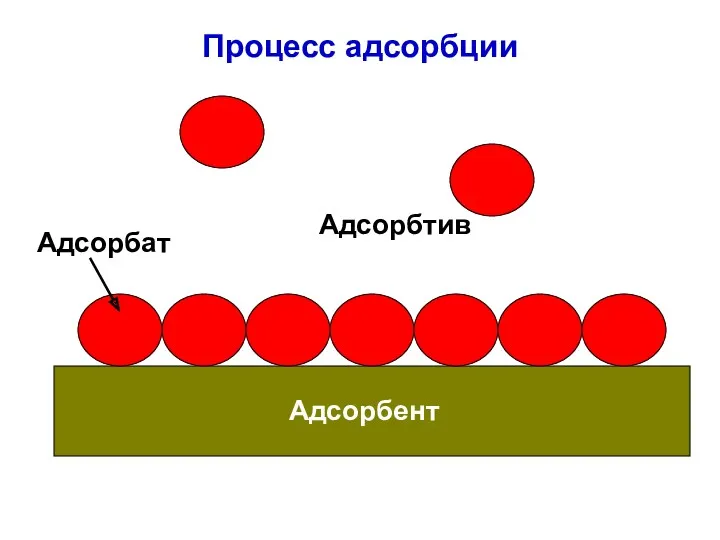
- 22. Процесс адсорбции Адсорбент
- 23. Адсорбция Адсорбция характеризуется обратимостью и высокой скоростью. Процесс обратный адсорбции называется десорбцией. В зависимости от характера
- 24. Адсорбция на жидких адсорбентах Об адсорбционной способности жидких адсорбентов судят либо по величине поверхностного натяжения, либо
- 25. Адсорбция на жидких адсорбентах а = (Со – С) V/S, где а – величина адсорбции (удельная
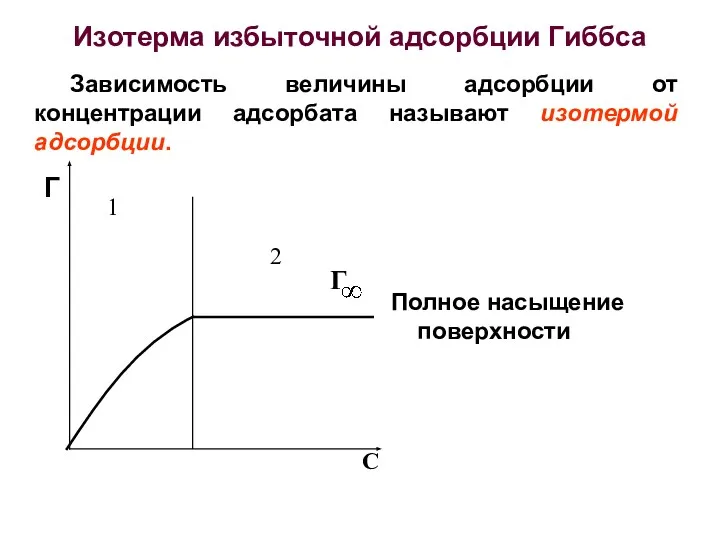
- 26. Изотерма избыточной адсорбции Гиббса 1 2 Г С Г Зависимость величины адсорбции от концентрации адсорбата называют
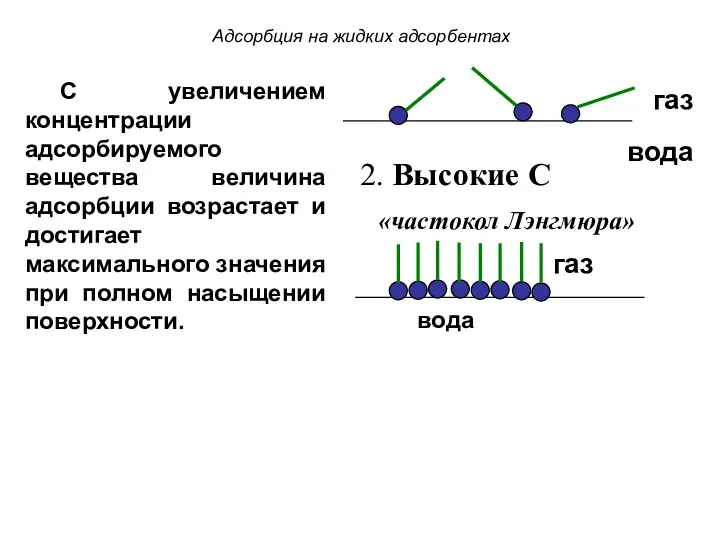
- 27. Адсорбция на жидких адсорбентах газ вода 2. Высокие С газ вода «частокол Лэнгмюра» С увеличением концентрации
- 28. Уравнение Гиббса Математически эта взаимосвязь характеризуется уравнением Гиббса: [ммоль м-2], где Г - количество адсорбированного вещества
- 29. Поверхностная активность Мера поверхностной активности (g) - способность растворенного вещества изменять поверхностное натяжение. По знаку величины
- 30. Адсорбция на жидких адсорбентах Поверхностно-активные вещества (ПАВ) обладают низким поверхностным натяжением . Поэтому из уравнения Гиббса
- 31. Строение молекулы ПАВ: Молекула ПАВ состоит из: неполярной гидрофобной углеводородной группы (“хвост”) полярной гидрофильной группы (“голова”):
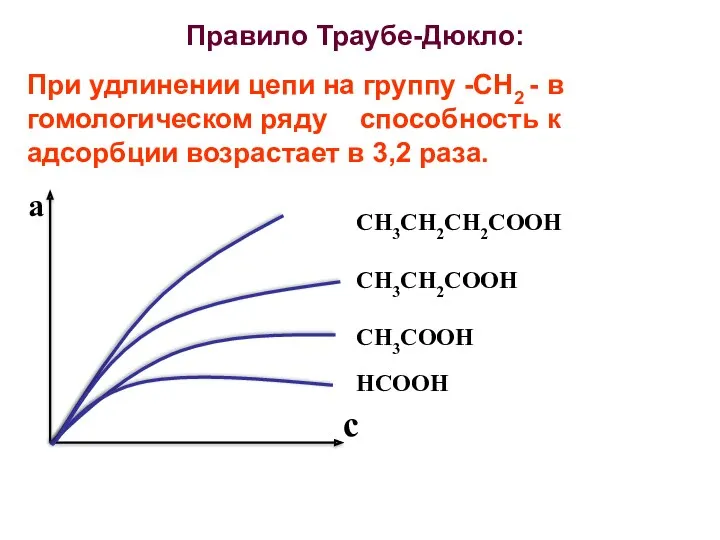
- 32. Правило Траубе-Дюкло: При удлинении цепи на группу -СН2 - в гомологическом ряду способность к адсорбции возрастает
- 33. Правило Ребиндера газ вода В адсорбционном слое молекулы ПАВ располагаются упорядоченно в соответствии с правилом Ребиндера:
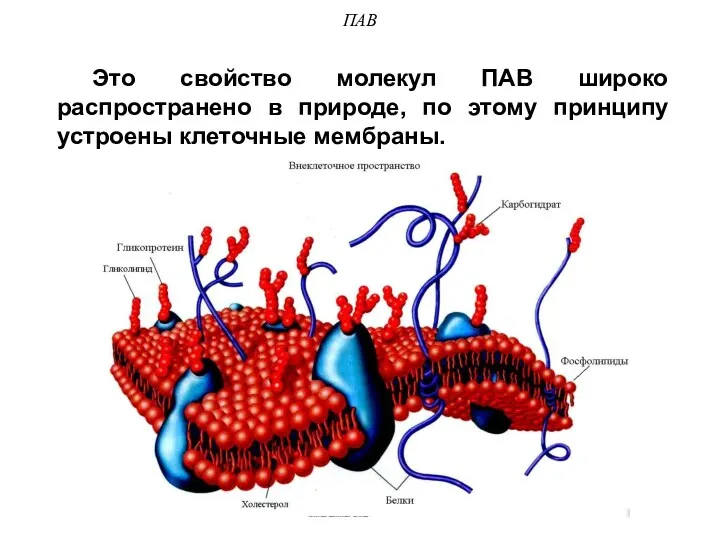
- 34. ПАВ Это свойство молекул ПАВ широко распространено в природе, по этому принципу устроены клеточные мембраны.
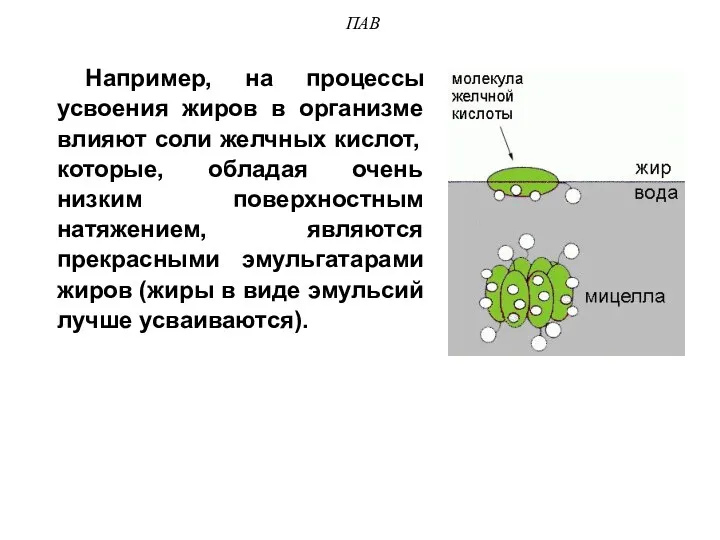
- 35. ПАВ Например, на процессы усвоения жиров в организме влияют соли желчных кислот, которые, обладая очень низким
- 36. ПАВ ПАВ широко используются в фармации в качестве основы для приготовления мазей, свечей, эмульсий, а также
- 37. Адсорбция на жидких адсорбентах Поверхностно-инактивные вещества (ПИВ) обладают высоким поверхностным натяжением . Следовательно, Г Эти вещества
- 38. ПАВ, ПИВ, ПНВ Поверхностно-неактивные вещества (ПНВ): не изменяют поверхностное натяжение растворителя. ПНВ: сахароза.
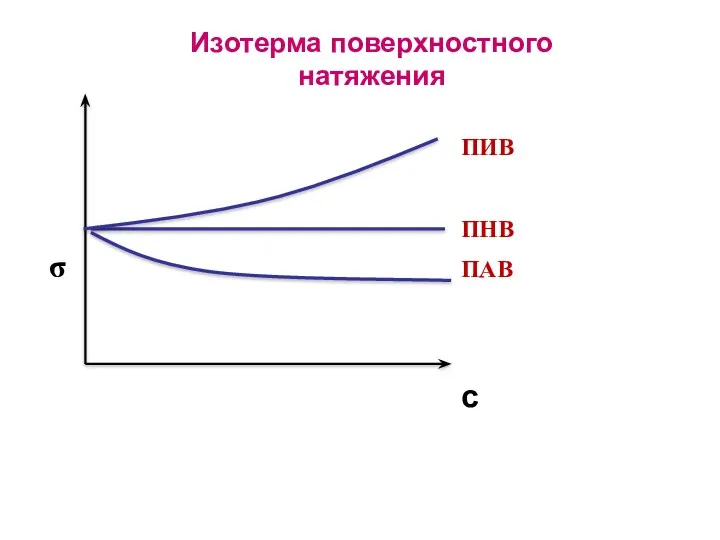
- 39. Изотерма поверхностного натяжения ПИВ ПНВ ПАВ σ с
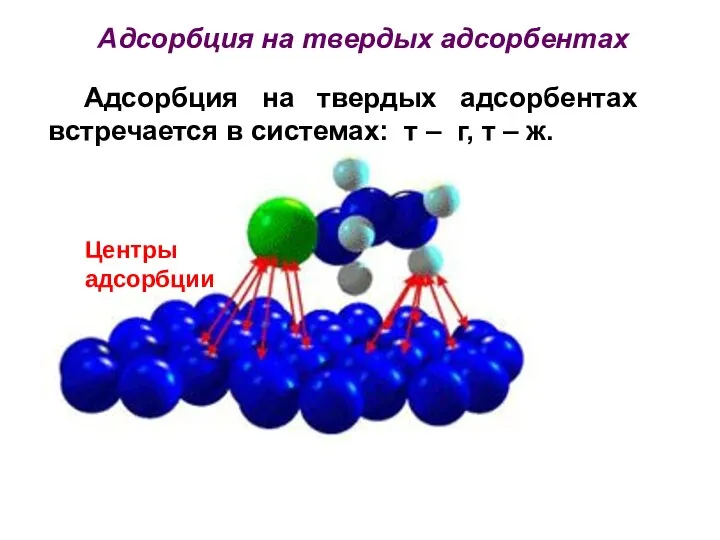
- 40. Центры адсорбции Адсорбция на твердых адсорбентах встречается в системах: т – г, т – ж. Адсорбция
- 41. Адсорбция на твердых адсорбентах Величина адсорбции для твердых сорбентов рассчитывается по формуле: a = (Со –
- 42. Адсорбция на твердых адсорбентах Величина адсорбции зависит от: Размера поверхности адсорбента (↑ S ↑ Г). 2.
- 43. Адсорбция на твердых адсорбентах Твердые сорбенты делят на гидрофильные (глины, силикагели) и гидрофобные (угли, графит, тальк,
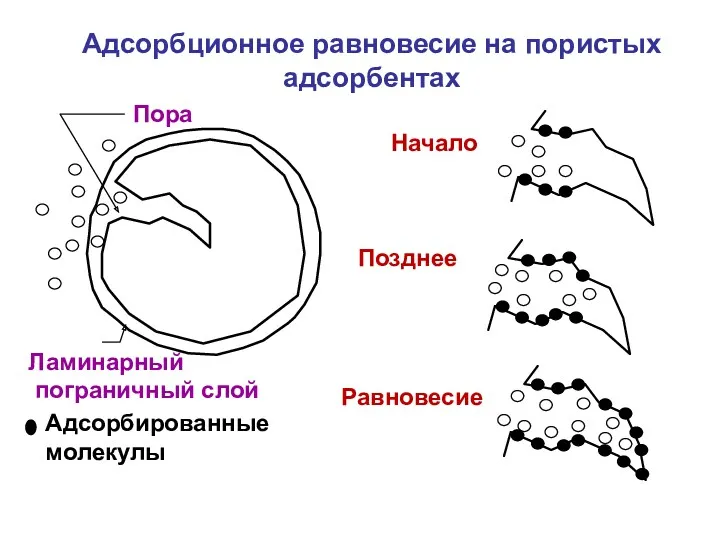
- 44. Адсорбционное равновесие на пористых адсорбентах Адсорбированные молекулы Равновесие Пора Начало Позднее Ламинарный пограничный слой
- 45. Электролитная адсорбция Электролитная (ионная) адсорбция – это избирательная адсорбция ионов (катионов или анионов) из раствора электролита
- 46. Электролитная адсорбция Избирательный характер адсорбции описывается следующими правилами: I. Правилом Панета-Фаянса: на поверхности кристалла преимущественно адсорбируются
- 47. Электролитная адсорбция Какой ион преимущественно адсорбируются на хлориде серебра? Ответ: хлорид-анион. Адсорбент – AgCl, адсорбаты: Cl-,
- 48. Электролитная адсорбция II. Правило изоморфизма: На полярном адсорбенте из раствора электролита преимущественно адсорбируются ионы, близкие по
- 49. Электролитная адсорбция Какой ион преимущественно адсорбируются на хлориде серебра? Ответ: бромид-анион. Адсорбент – AgCl, адсорбаты: Br-,
- 50. Электролитная адсорбция III. Если ионы-адсорбаты имеют одинаковые по знаку и разные по величине степени окисления, то
- 51. IV. Если ионы-адсорбаты имеют одинаковые по величине и знаку степени окисления, то в первую очередь адсорбируются
- 52. Электролитная адсорбция Различают необратимую и обратимую электролитную адсорбцию. При необратимой адсорбции адсорбат и адсорбент образуют нерастворимое
- 53. Ионообменная адсорбция Ионообменная адсорбция - это процесс, при котором твердый адсорбент (ионит) обменивает эквивалентное количество своих
- 54. Классификация ионитов По происхождению: природные (кристаллические силикаты, апатиты, гуминовые кислоты) и синтетические (в качестве каркаса используют,
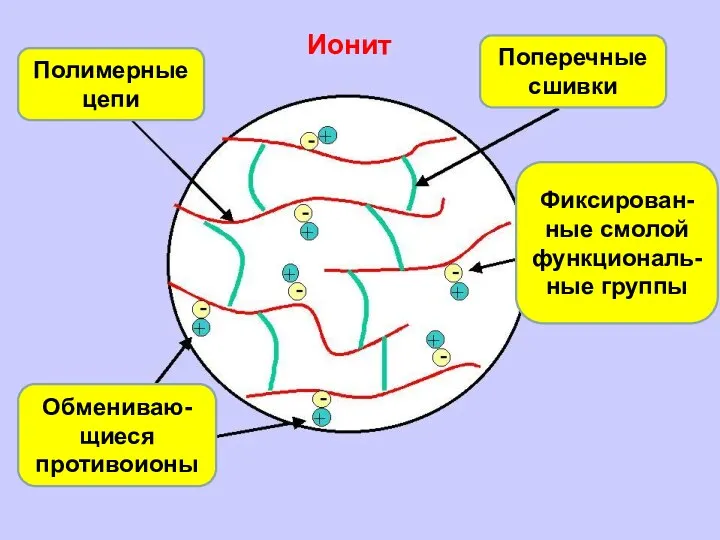
- 55. Ионообменная адсорбция Основой любого ионита является матрица (R), не участвующая в ионообменной адсорбции. На ней закреплены
- 56. Полимерные цепи Обмениваю-щиеся противоионы Фиксирован-ные смолой функциональ-ные группы Поперечные сшивки Ионит
- 57. Ионообменная адсорбция Микрофотографии гранул ионитов
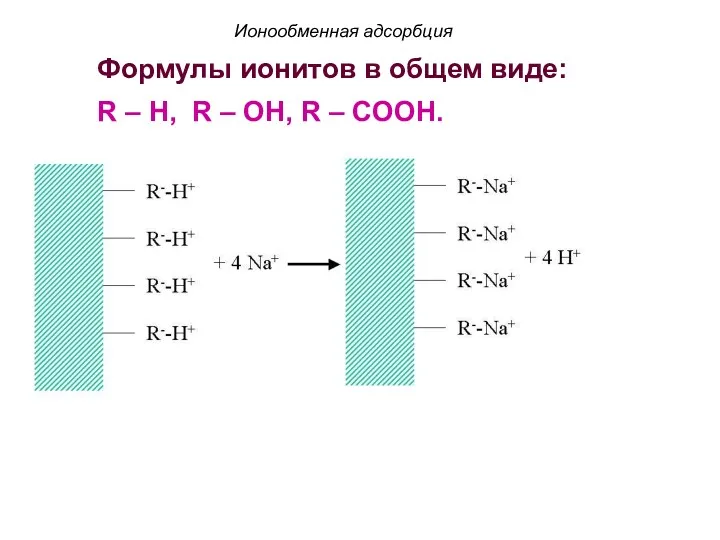
- 58. Ионообменная адсорбция Формулы ионитов в общем виде: R – H, R – OH, R – COOH.
- 59. Ионообменная адсорбция В зависимости от природы обменивающихся ионов, различают: катиониты; аниониты; амфолиты.
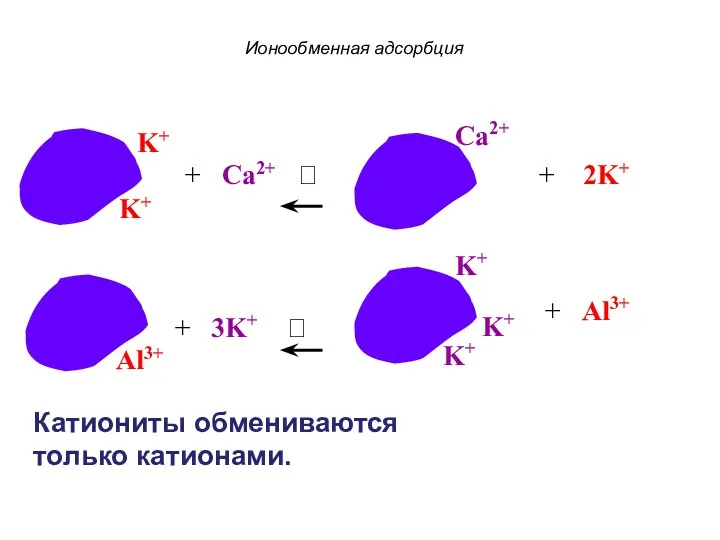
- 60. Ионообменная адсорбция + Ca2+ ? Катиониты обмениваются только катионами.
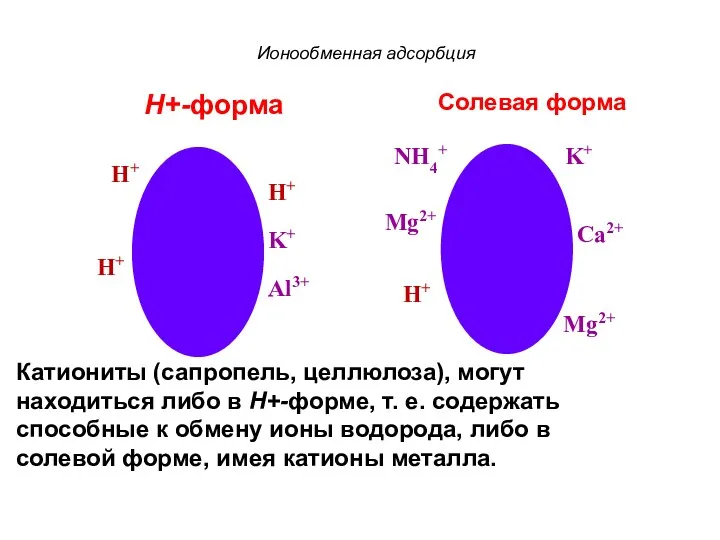
- 61. Ионообменная адсорбция Н+-форма Солевая форма Катиониты (сапропель, целлюлоза), могут находиться либо в Н+-форме, т. е. содержать
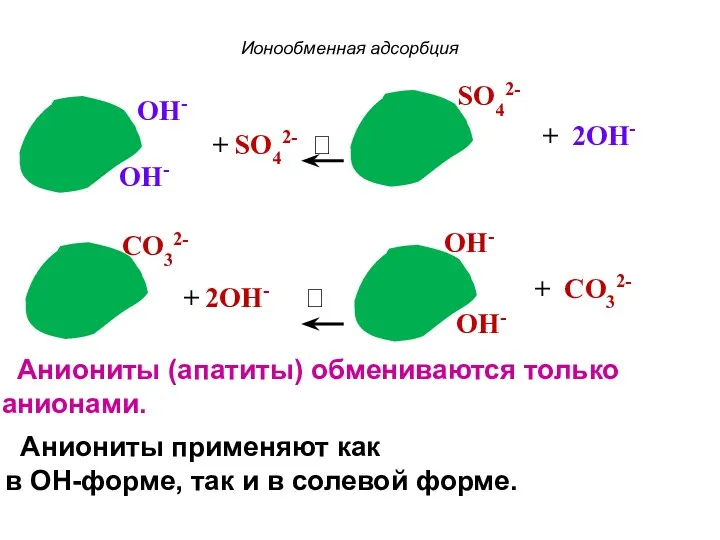
- 62. Ионообменная адсорбция + SO42- ? Аниониты (апатиты) обмениваются только анионами. Аниониты применяют как в ОН-форме, так
- 63. Ионообменная адсорбция Амфолиты (гуминовые кислоты) обмениваются и катионами и анионами. Ионообменная адсорбция подчиняется: закону эквивалентов, всем
- 64. Использование ионитов в фармации и медицине В санитарно-гигиенической практике иониты используются для очистки воды, выделения и
- 65. Использование ионитов в фармации и медицине: для декальцинирования крови с целью ее консервации;
- 66. Использование ионитов в фармации и медицине для осуществления гемодиализа крови (используется ионит - алюмогель); беззондовой диагностики
- 67. Использование ионитов в фармации и медицине детоксикации организма при различных отравлениях. Аниониты - антацидные средства, катиониты
- 68. Использование ионитов в фармации и медицине в фарм. технологии для получения и очистки лекарственных и биологически
- 70. Скачать презентацию













![Уравнение Гиббса Математически эта взаимосвязь характеризуется уравнением Гиббса: [ммоль м-2],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/401240/slide-27.jpg)




























 Лечение пациентов инфекционного профиля. Дизентерия
Лечение пациентов инфекционного профиля. Дизентерия Предмет и задачи психофизиологии
Предмет и задачи психофизиологии Основы организации лечебно-профилактической помощи населению. Амбулаторно-поликлиническая помощь, современные проблемы
Основы организации лечебно-профилактической помощи населению. Амбулаторно-поликлиническая помощь, современные проблемы Система противотуберкулезной помощи в РФ
Система противотуберкулезной помощи в РФ Формирование первичного эндодонтического доступа. Рабочая длина канала зуба, методы определения
Формирование первичного эндодонтического доступа. Рабочая длина канала зуба, методы определения Оборотные средства аптечной организации. (Тема 21)
Оборотные средства аптечной организации. (Тема 21) Гуморальная регуляция висцеральных функций. Роль эндокринных желез в регуляции роста и развития, гомеостаза и адаптации
Гуморальная регуляция висцеральных функций. Роль эндокринных желез в регуляции роста и развития, гомеостаза и адаптации Вред, причиняемый алкоголем. Тест
Вред, причиняемый алкоголем. Тест Острые пневмонии у детей. (Лекция 3)
Острые пневмонии у детей. (Лекция 3) Окклюзионные заболевания артерий нижних конечностей
Окклюзионные заболевания артерий нижних конечностей Advanced Life Support Algorithm. Алгоритм ALS. Лікування дефібриляційних, недефібриляційних ритмів
Advanced Life Support Algorithm. Алгоритм ALS. Лікування дефібриляційних, недефібриляційних ритмів Особливості системи крові у дітей різних вікових груп. Клініко - гематологічна семіотика основних синдромів
Особливості системи крові у дітей різних вікових груп. Клініко - гематологічна семіотика основних синдромів Ассортимент выпускаемой продукции фирмы ООО Альтфарм
Ассортимент выпускаемой продукции фирмы ООО Альтфарм Вскармливание детей грудного возраста
Вскармливание детей грудного возраста Психические болезни в предстарческом и старческом возрасте
Психические болезни в предстарческом и старческом возрасте Ауруханаішілік инфекциялар. Диагностикасы және алдын алу
Ауруханаішілік инфекциялар. Диагностикасы және алдын алу Допинг и антидопинговая политика
Допинг и антидопинговая политика Эвтаназия: история проблемы
Эвтаназия: история проблемы Хронический гнойный средний отит
Хронический гнойный средний отит Анаэробная инфекция и столбняк
Анаэробная инфекция и столбняк Блефариты. Клиника, диагностика, лечение
Блефариты. Клиника, диагностика, лечение Домедична допомога в умовах бойових дій (тактична медицина). Тема №3.8
Домедична допомога в умовах бойових дій (тактична медицина). Тема №3.8 Инфекционный эндокардит
Инфекционный эндокардит Отек Квинке
Отек Квинке Дезинфекция, дезинсекция, дератизация
Дезинфекция, дезинсекция, дератизация Группы крови. Переливание крови
Группы крови. Переливание крови Последовательность оказания первой помощи пострадавшему при ДТП
Последовательность оказания первой помощи пострадавшему при ДТП Тырысқақ
Тырысқақ