Содержание
- 2. ТЕРМІНИ Реєстрація/перереєстрація ГЛЗ - процедура, яка включає ряд етапів експертиз ЛЗ і відповідної НТД, які проводяться
- 3. РЕЄСТРАЦІЙНЕ досьє – комплект документів, які стосуються матеріалів доклінічного вивчення, клінічних випробувань лікарського засобу та їх
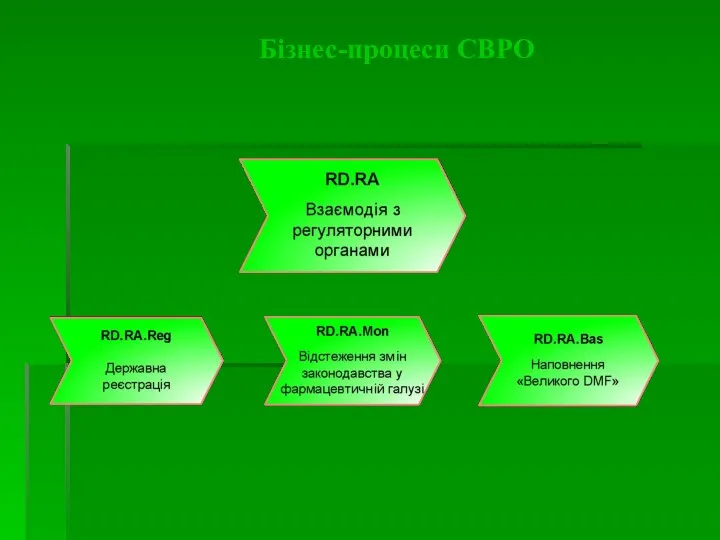
- 4. Бізнес-процеси СВРО
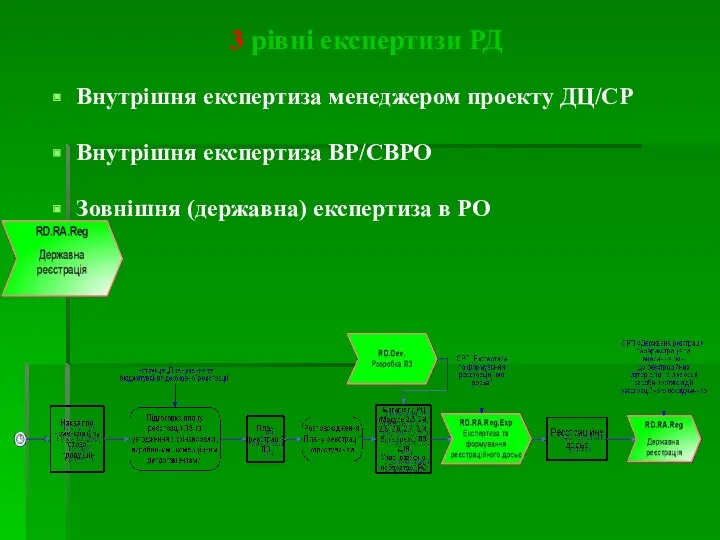
- 5. 3 рівні експертизи РД Внутрішня експертиза менеджером проекту ДЦ/СР Внутрішня експертиза ВР/СВРО Зовнішня (державна) експертиза в
- 6. Внутрішня експертиза РД (1) Експертна функція ВР (критична оцінка даних досьє на відповідність останнім фармакопейним та
- 7. Передача документів з ДЦ у ВР При реєстрації: Модуль 2 (розділ 2.3) і Модуль 3. При
- 8. Технічні вимоги до реєстраційного досьє Переплетення не повинно закривати інформацію. Текст і таблиці повинні бути з
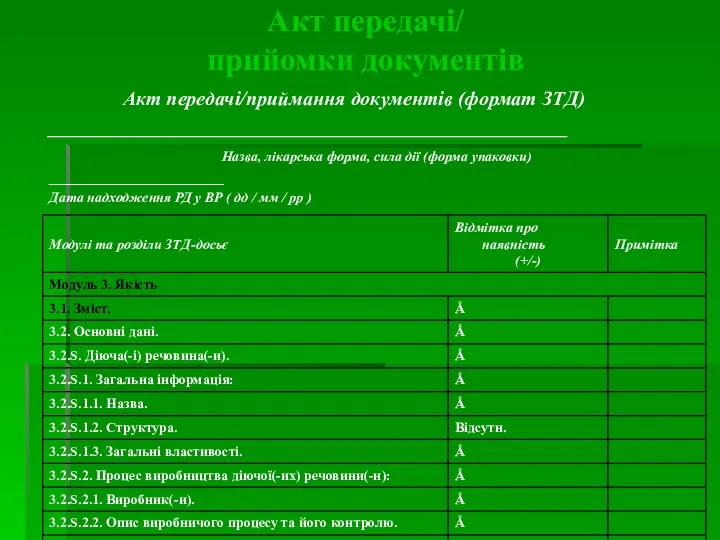
- 9. Акт передачі/ прийомки документів
- 10. Тривалість експертизи у ВР: - при реєстрації - 5 днів, - при перереєстрації - 3 дні,
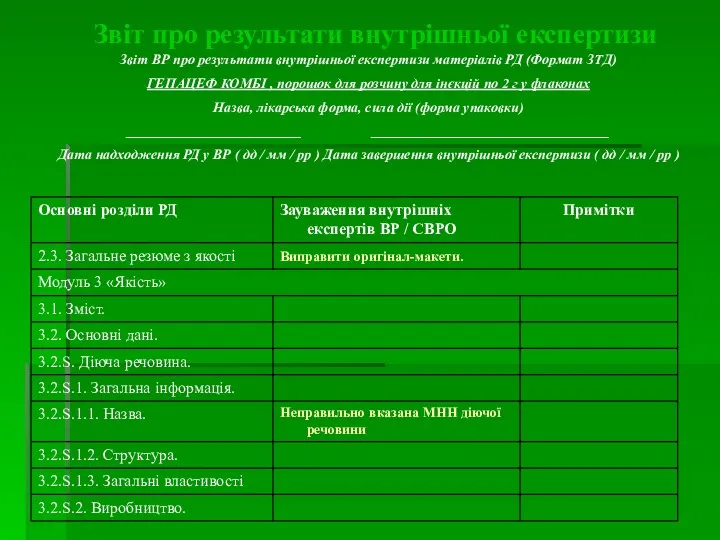
- 11. Звіт про результати внутрішньої експертизи Звіт ВР про результати внутрішньої експертизи матеріалів РД (Формат ЗТД) ГЕПАЦЕФ
- 12. Формування РД Порядок формування реєстраційного досьє у ВР. Матеріали, передані з ДЦ і СР, доповнюються :
- 13. ТЕРМІНИ ЕКСПЕРТИЗИ РД в регуляторних органах ТЕРМІНИ ЕКСПЕРТИЗИ (згідно Наказу №426) При реєстрації не більше 210
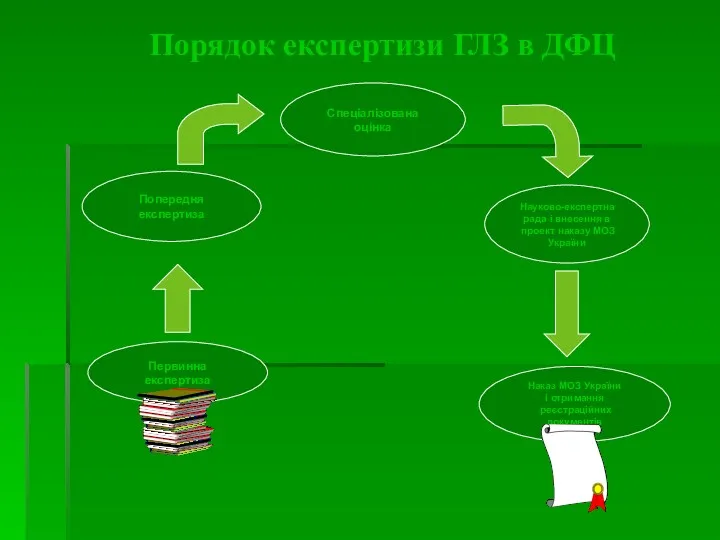
- 14. Порядок експертизи ГЛЗ в ДФЦ
- 15. Мета і терміни експертизи РД в регуляторних органах (1) Первинна експертиза заявки на предмет винесення мотивованого
- 16. Спеціалізована експертиза РО мають право : прийняти рішення про проведення додаткової експертизи даних, наведених у реєстраційних
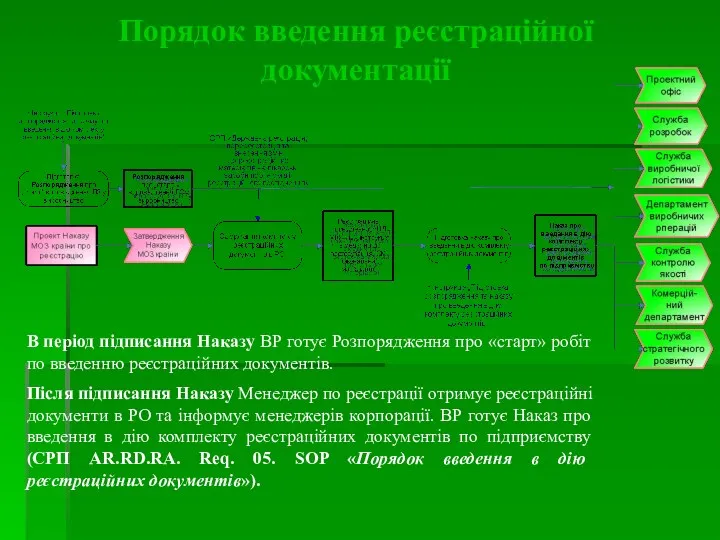
- 17. В період підписання Наказу ВР готує Розпорядження про «старт» робіт по введенню реєстраційних документів. Після підписання
- 18. Склад реєстраційного досьє у форматі CTD (Модуль 3 Якість/Фармацевтична розробка)
- 19. 1. Note for Guidance on Pharmaceutical Development. – EMEA/СHМР/167068/2004 – ICH (ICH Topic Q8). – May
- 20. Thomas J. DiFeo. Drug Product Development. A Technical Review of Chemistry, Manufacturing, and Control Information (…).
- 21. Мета: 1) Розглянути методологічний підхід до фармрозробки (ICH Q8) лікарських засобів у взаємозв'язку з структурними елементами
- 22. Складові сучасної фармацевтичної розробки Розробка лікарських препаратів повинна базуватись на декількох складових: на загальному методологічному підході
- 23. Головні структурні елементи Керівництва ICH Q8 «Pharmaceutical Development» 1. Компоненти лікарського препарату 1.1. Лікарська речовина 1.2.
- 24. ЗТД-МОДУЛЬ 3. Якість* СTD-Module 3. Quality 3.2.S. Діюча речовина 3.2.S.1. Загальна інформація 3.2.S.2. Виробництво 3.2.S.3. Характеристики
- 25. CTD 3.2.Р.2 Фармацевтична розробка (1) Pharmaceutical Development Розділ досьє «Фармацевтичня розробка» повинен містити інформацію, яка б
- 26. CTD 3.2.Р.2.2 Лікарська форма Розробка складу (CTD 3.2.Р.2.2.1) - резюме по розробці складу і вибору лікарської
- 27. Мета фармацевтичної розробки Мета фармацевтичної розробки – розробити продукт відповідної якості + такий процес його виробництва,
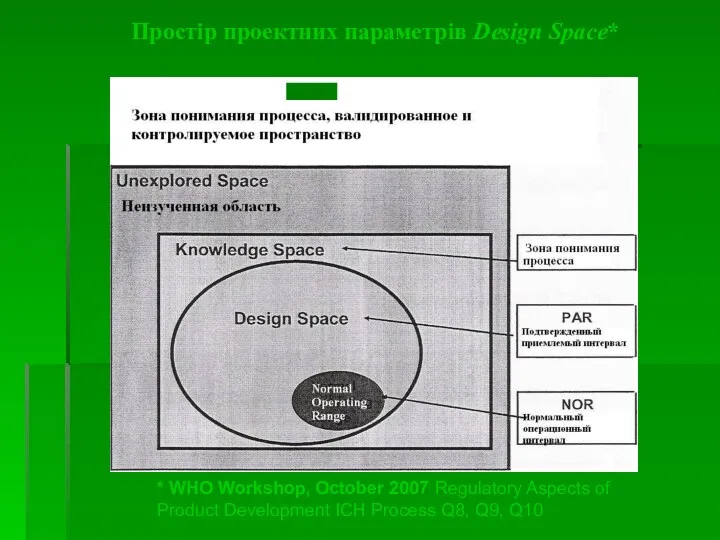
- 28. Важливі поняття* Простір проектних параметрів (design space) – це багатофакторна комбінація і взаємодія вхідних змінних, а
- 29. Простір проектних параметрів Design Space* * WHO Workshop, October 2007 Regulatory Aspects of Product Development ICH
- 30. Гнучкість сучасних регуляторних підходів • Вдосконалення виробничого процесу в межах схваленого простору дизайну, описаного в досьє,
- 31. Порядок вдосконалення процесів/якості Фармацевтична система якості потребує неперервного вдосконалення процесів і якості продукції: Для покращення процесів
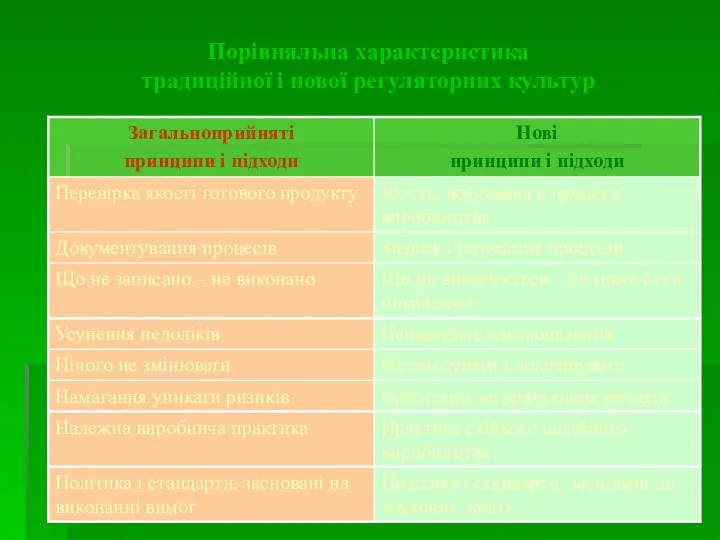
- 32. Порівняльна характеристика традиційної і нової регуляторних культур
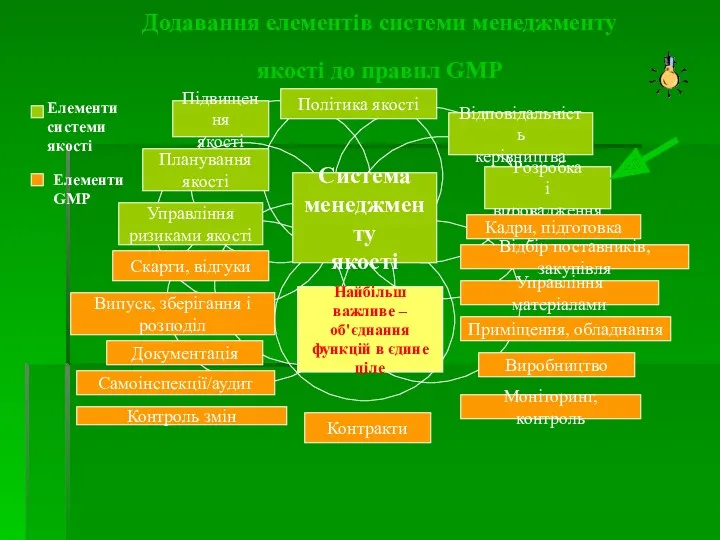
- 33. Додавання елементів системи менеджменту якості до правил GMP Система менеджменту якості Політика якості Підвищення якості Відповідальність
- 35. Скачать презентацию























 Кислотно-основное состояние крови
Кислотно-основное состояние крови Микозы. Общие сведения об эпидемиологии и этиологии микозов
Микозы. Общие сведения об эпидемиологии и этиологии микозов Тубулоінтерстиціальний нефрит
Тубулоінтерстиціальний нефрит Гестозы второй половины беременности
Гестозы второй половины беременности Маскүнемдік туралы жалпы түсінік, нашақорлық
Маскүнемдік туралы жалпы түсінік, нашақорлық Система крови
Система крови Расстройство микроциркуляции и местного кровообращения
Расстройство микроциркуляции и местного кровообращения Муковисцидоз. Этиология и патогенез
Муковисцидоз. Этиология и патогенез Вакцины. Виды вакцин
Вакцины. Виды вакцин Изменения регионарного кровообращения и микроциркуляции. Общие типовые патологические процессы. (Тема 5.10)
Изменения регионарного кровообращения и микроциркуляции. Общие типовые патологические процессы. (Тема 5.10) Пальмовое масло и его влияние на организм человека
Пальмовое масло и его влияние на организм человека Ведение физиологических родов и методы наблюдения во время родов
Ведение физиологических родов и методы наблюдения во время родов Внутренние незаразные болезни животных
Внутренние незаразные болезни животных Нәрестелердің асфиксиясы
Нәрестелердің асфиксиясы Побочные эффекты лекарственных средств. Взаимодействие лекарственных средств
Побочные эффекты лекарственных средств. Взаимодействие лекарственных средств Педагогический совет Роль здорового питания в формировании здорового образа жизни дошкольников
Педагогический совет Роль здорового питания в формировании здорового образа жизни дошкольников Лфк и массаж при операциях на органах грудной клетки
Лфк и массаж при операциях на органах грудной клетки Жүре пайда болған (ЖИТС, СПИД ағылш. AIDS) иммундық дефицитiнiң синдромы - Вич
Жүре пайда болған (ЖИТС, СПИД ағылш. AIDS) иммундық дефицитiнiң синдромы - Вич Основы рационального питания
Основы рационального питания Тісті тікелей қалпына келтіру.Қолданылатын материалдар
Тісті тікелей қалпына келтіру.Қолданылатын материалдар Коррекция дефицита магния в практике врача
Коррекция дефицита магния в практике врача Целиакия у детей
Целиакия у детей Патогенні мікобактерії. Туберкульоз. Лепра
Патогенні мікобактерії. Туберкульоз. Лепра Кондиционирования и осложнение после ТКМ
Кондиционирования и осложнение после ТКМ Острый холецистит
Острый холецистит Профилактическая инсектоакаритизация
Профилактическая инсектоакаритизация Причины и предрасполагающие факторы к возникновению рахита
Причины и предрасполагающие факторы к возникновению рахита Phẫu thuật bằng dao mổ điện
Phẫu thuật bằng dao mổ điện