Содержание
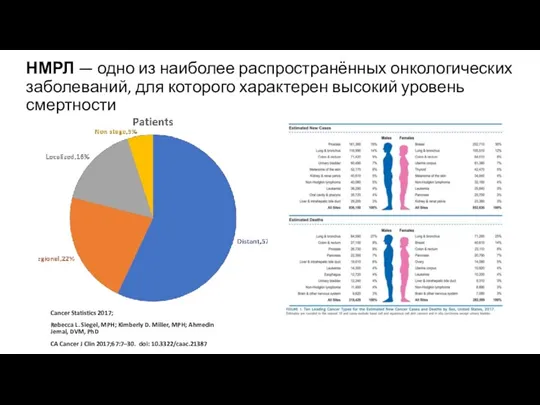
- 2. НМРЛ — одно из наиболее распространённых онкологических заболеваний, для которого характерен высокий уровень смертности Cancer Statistics
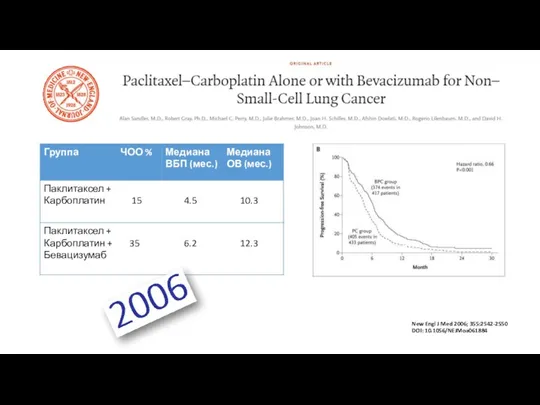
- 3. New Engl J Med 2006; 355:2542-2550 DOI: 10.1056/NEJMoa061884
- 4. Таргетная терапия https://www.celgene.com/getting-personal/aml-targeted-therapy/
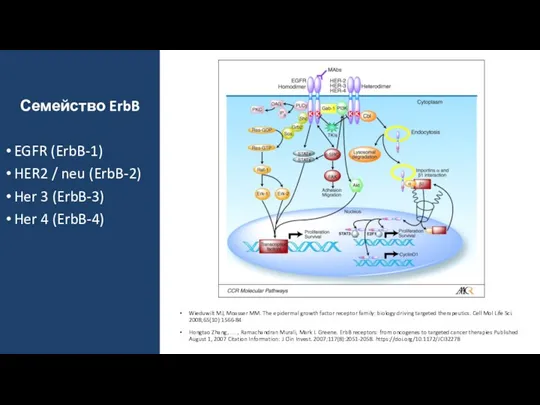
- 6. Семейство ErbB EGFR (ErbB-1) HER2 / neu (ErbB-2) Her 3 (ErbB-3) Her 4 (ErbB-4) Wieduwilt MJ,
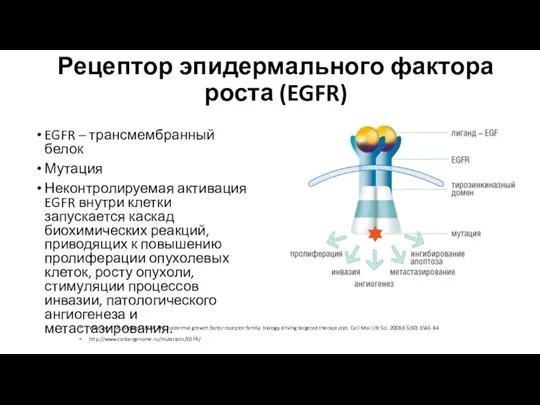
- 7. Рецептор эпидермального фактора роста (EGFR) Wieduwilt MJ, Moasser MM. The epidermal growth factor receptor family: biology
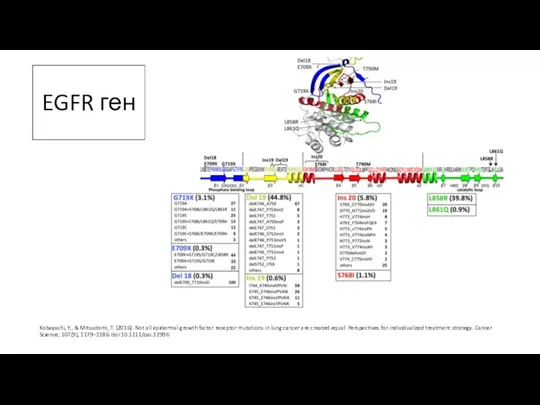
- 8. EGFR ген Kobayashi, Y., & Mitsudomi, T. (2016). Not all epidermal growth factor receptor mutations in
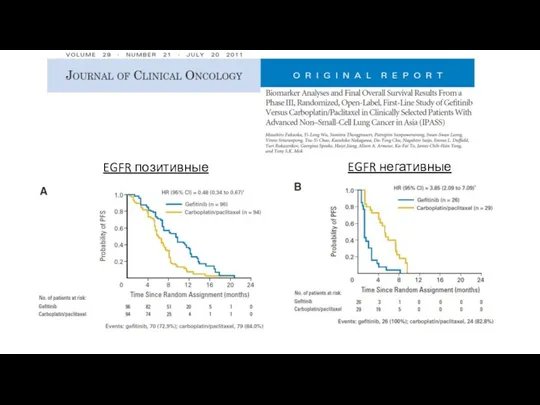
- 9. EGFR позитивные EGFR негативные
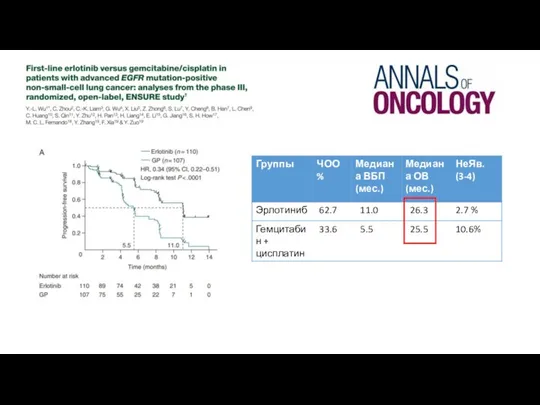
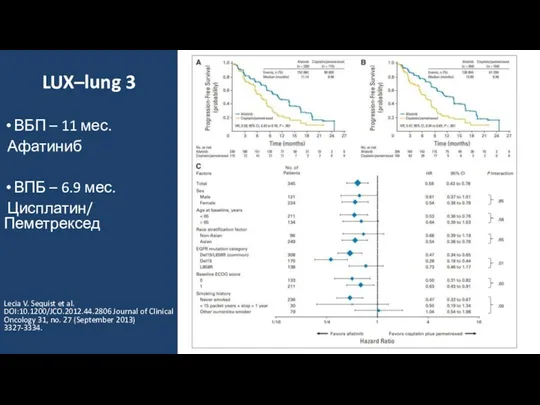
- 11. LUX–lung 3 ВБП – 11 мес. Афатиниб ВПБ – 6.9 мес. Цисплатин/ Пеметрексед Lecia V. Sequist
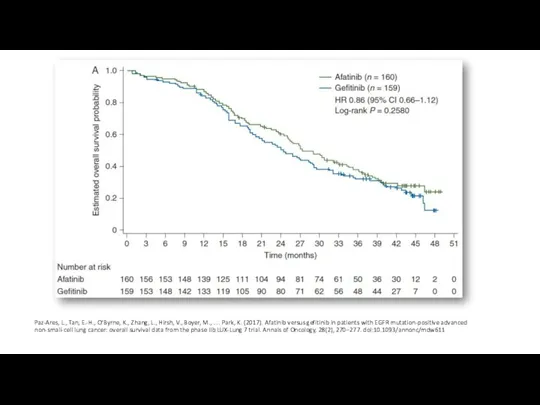
- 12. Афатиниб против гефитиниба Afatinib versus gefitinib in patients with EGFR mutation-positive advanced non-small-cell lung cancer: overall
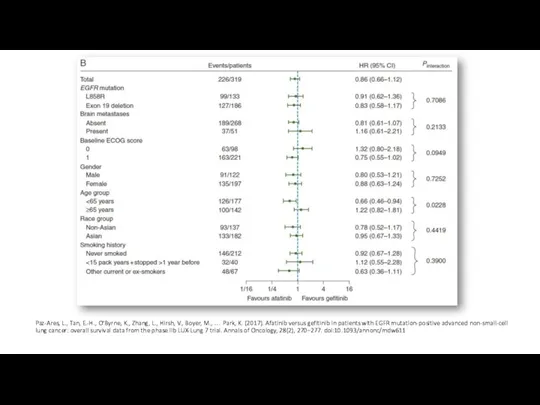
- 13. Paz-Ares, L., Tan, E.-H., O’Byrne, K., Zhang, L., Hirsh, V., Boyer, M., … Park, K. (2017).
- 14. Paz-Ares, L., Tan, E.-H., O’Byrne, K., Zhang, L., Hirsh, V., Boyer, M., … Park, K. (2017).
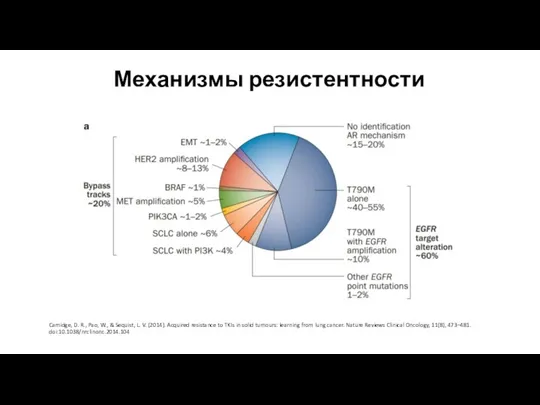
- 15. Механизмы резистентности Camidge, D. R., Pao, W., & Sequist, L. V. (2014). Acquired resistance to TKIs
- 16. Мутация T 790 m – около 60 % случаев Происходит изменение конфигурации рецептора EGFR Ингибиторы тирозинкиназы
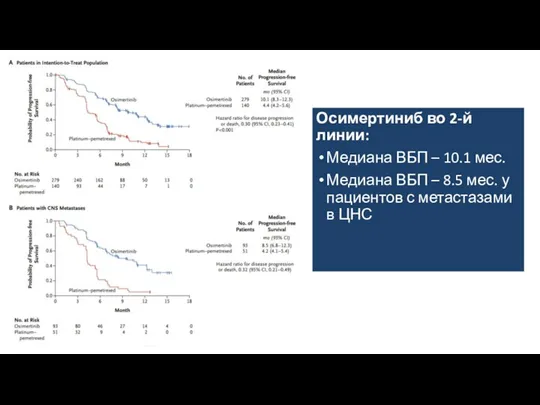
- 17. Осимертиниб vs Химиотерапия (2 линия) Mok, T. S., Wu, Y.-L., Ahn, M.-J., Garassino, M. C., Kim,
- 18. Осимертиниб во 2-й линии: Медиана ВБП – 10.1 мес. Медиана ВБП – 8.5 мес. у пациентов
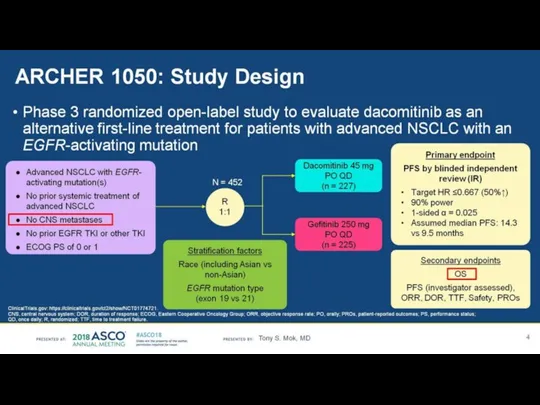
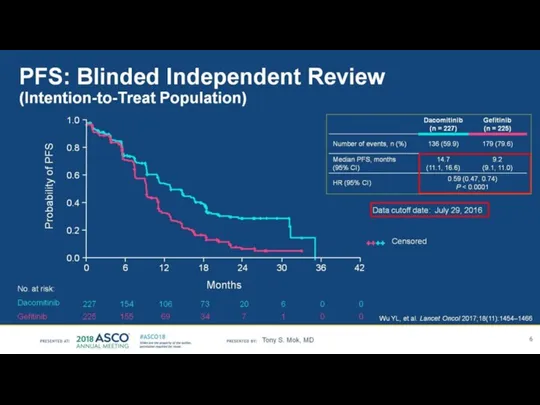
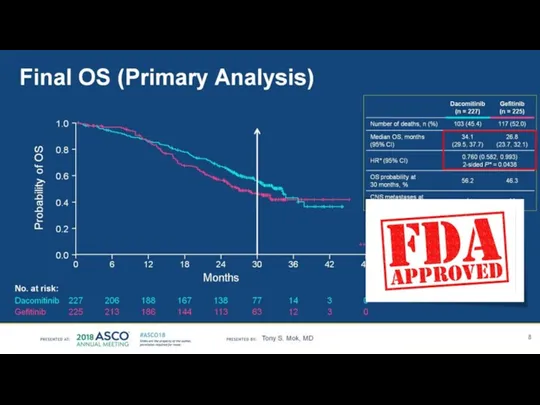
- 19. Рандомизированное двойное слепое исследование 3 фазы FLAURA (Osimertinib в 1-й линии) 556 пациентов EGFR + (делеция
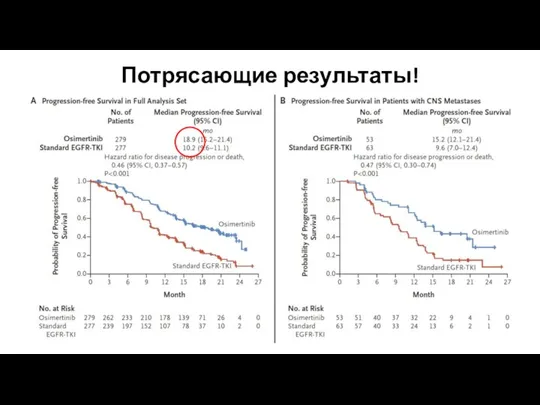
- 20. Потрясающие результаты!
- 21. Сложный выбор Park, K., Tan, E.-H., O’Byrne, K., Zhang, L., Boyer, M., Mok, T., … Paz-Ares,
- 25. ALK и другие…
- 26. 343 пациента с ALK +, местнораспространённый или метастатический НМРЛ, ECOG 0-2 Рандомизация 1:1 Кризотиниб vs Пеметрексед
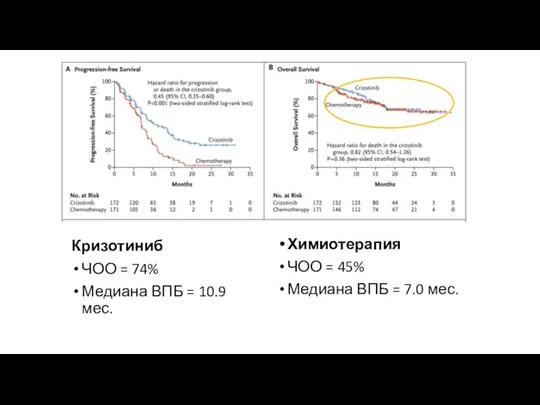
- 27. Кризотиниб ЧОО = 74% Медиана ВПБ = 10.9 мес. Химиотерапия ЧОО = 45% Медиана ВПБ =
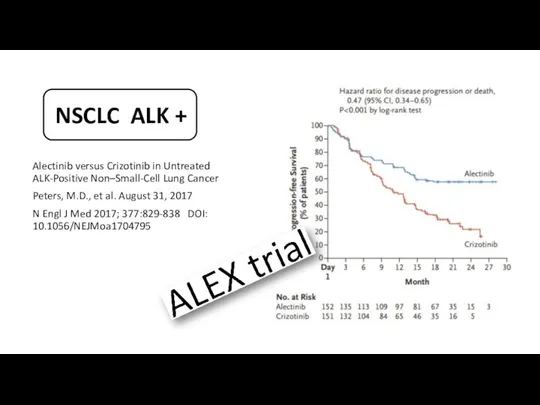
- 28. NSCLC ALK + Alectinib versus Crizotinib in Untreated ALK-Positive Non–Small-Cell Lung Cancer Peters, M.D., et al.
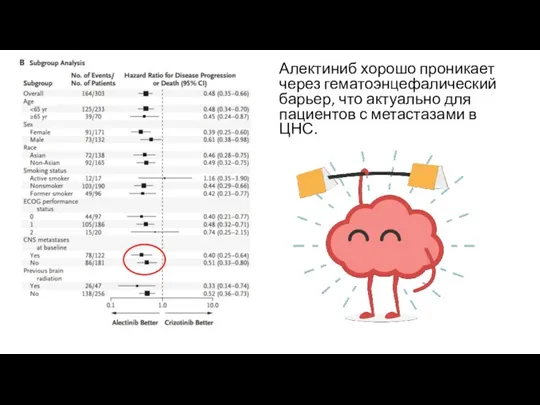
- 29. Алектиниб хорошо проникает через гематоэнцефалический барьер, что актуально для пациентов с метастазами в ЦНС.
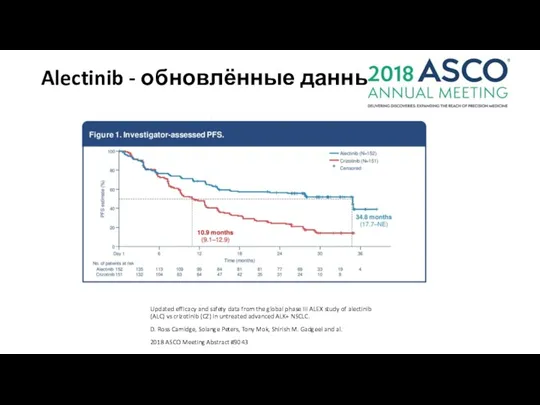
- 30. Alectinib - обновлённые данные Updated efficacy and safety data from the global phase III ALEX study
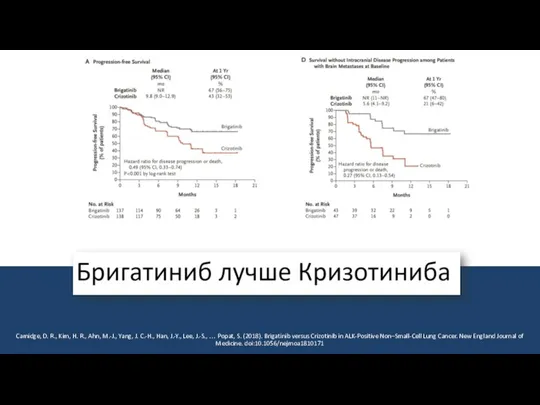
- 31. ALTA-1L первые результаты Camidge, D. R., Kim, H. R., Ahn, M.-J., Yang, J. C.-H., Han, J.-Y.,
- 32. Camidge, D. R., Kim, H. R., Ahn, M.-J., Yang, J. C.-H., Han, J.-Y., Lee, J.-S., …
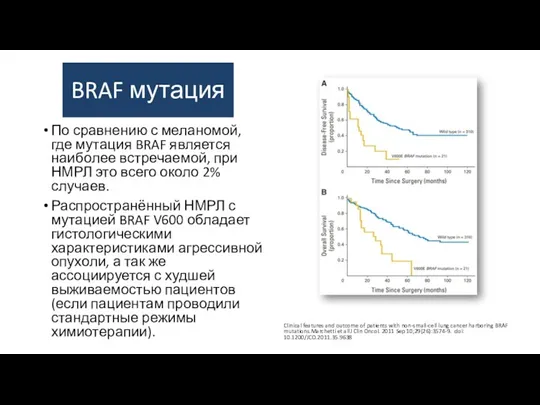
- 33. BRAF мутация По сравнению с меланомой, где мутация BRAF является наиболее встречаемой, при НМРЛ это всего
- 34. Дабрафениб + траметиниб В исследование включились пациенты c IV стадией НМРЛ, наличием мутации BRAF V600Е, общее
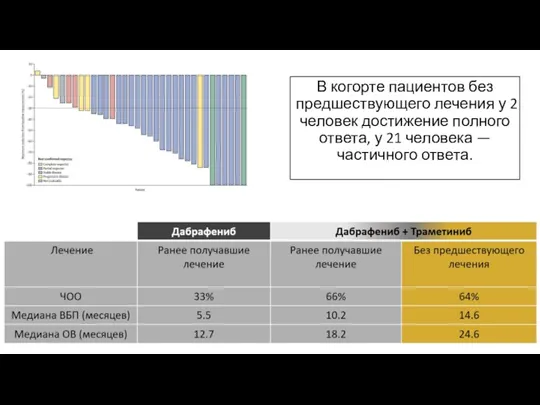
- 35. В когорте пациентов без предшествующего лечения у 2 человек достижение полного ответа, у 21 человека —
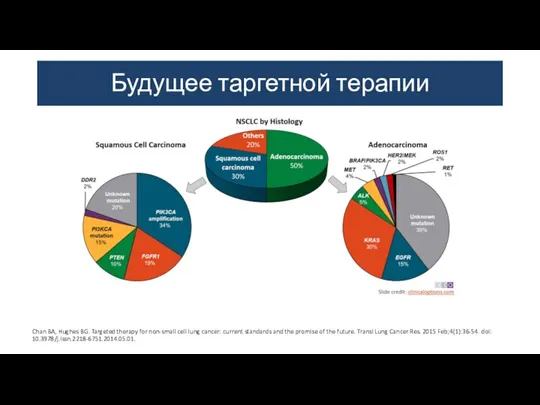
- 36. Будущее таргетной терапии Chan BA, Hughes BG. Targeted therapy for non-small cell lung cancer: current standards
- 37. Скоро… Ado-Trastuzumab Emtansine Tepotinib (MET amplification) Entrectinib (ROS1+) Lorlatinib (ALK +) LOXO-292 (RET+) Li BT, Shen
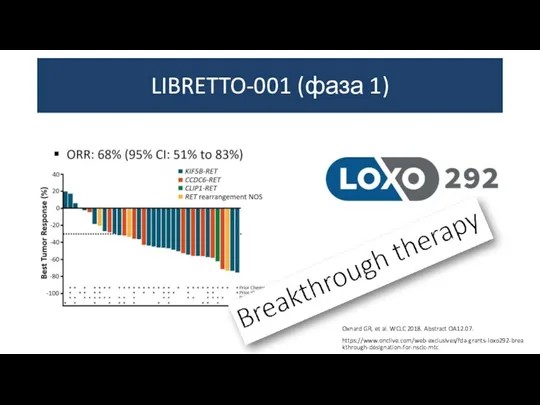
- 38. LIBRETTO-001 (фаза 1) Oxnard GR, et al. WCLC 2018. Abstract OA12.07. https://www.onclive.com/web-exclusives/fda-grants-loxo292-breakthrough-designation-for-nsclc-mtc
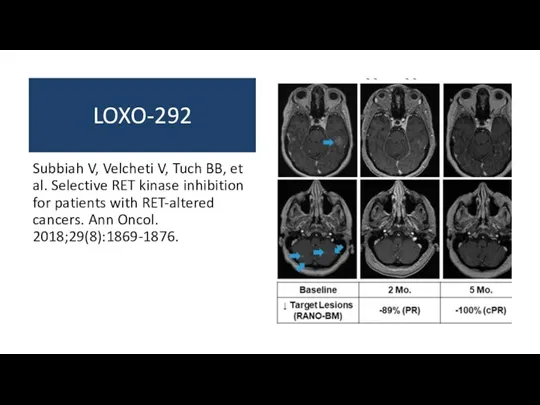
- 39. LOXO-292 Subbiah V, Velcheti V, Tuch BB, et al. Selective RET kinase inhibition for patients with
- 40. EGFR +, PD-L1 >50%
- 41. Пациенты с EGFR +, PD-L1 >50% без предшествующего лечения получали Pembrolizumab Исследование прекратилось из-за отсутствия эффективности
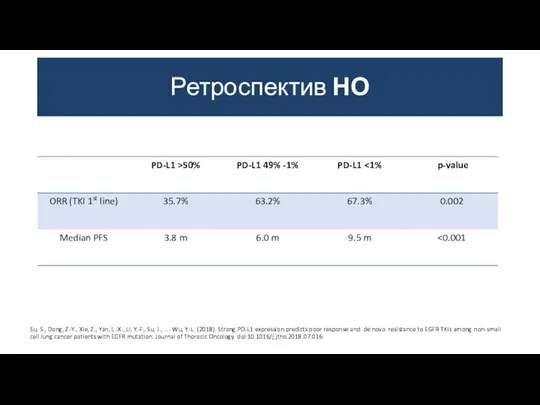
- 42. Ретроспектив НО Su, S., Dong, Z.-Y., Xie, Z., Yan, L.-X., Li, Y.-F., Su, J., … Wu,
- 44. Адъювантная и неоадъювантная терапия W-Z Zhong, et al. CTONG 1103: Erlotinib versus gemcitabine plus cisplatin as
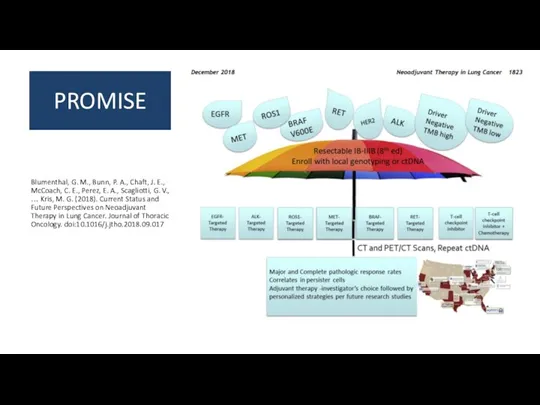
- 45. PROMISE Blumenthal, G. M., Bunn, P. A., Chaft, J. E., McCoach, C. E., Perez, E. A.,
- 46. Выводы Разделение пациентов на группы, в основе которого лежат молекулярно-генетические тесты, позволяет добиваться гораздо лучших результатов
- 49. Скачать презентацию

















 Острая дыхательная недостаточность
Острая дыхательная недостаточность Рациональная антимикробная терапия при инфекционных заболеваниях у детей
Рациональная антимикробная терапия при инфекционных заболеваниях у детей Дизентерия. Источник инфекции
Дизентерия. Источник инфекции Sistem nervos - generalitati
Sistem nervos - generalitati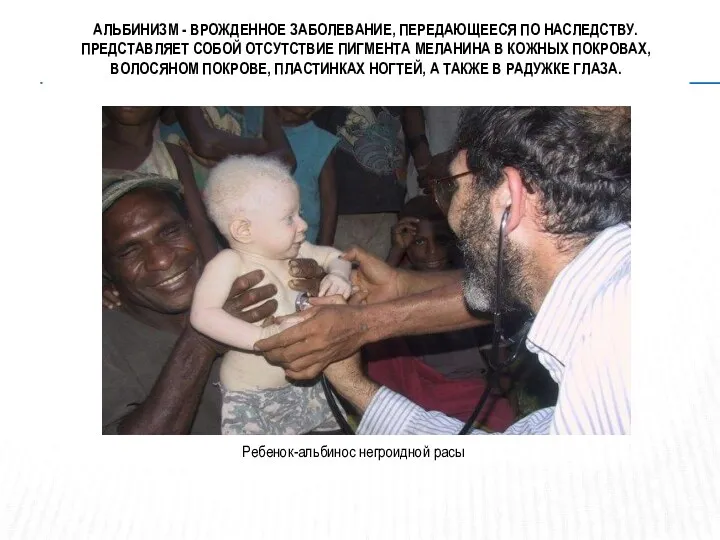 Альбинизм. Классификация альбинизма
Альбинизм. Классификация альбинизма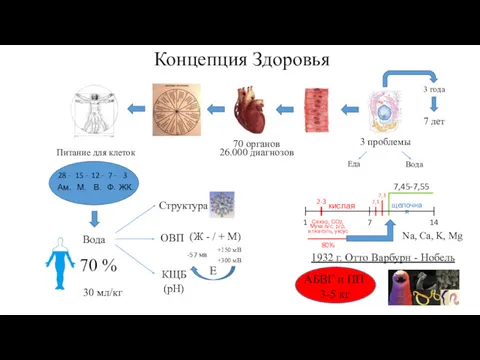 Концепция здоровья. Программы по очищению организма
Концепция здоровья. Программы по очищению организма ЛРС мочегонного действия
ЛРС мочегонного действия Симтоматология гастритов, язвенной болезни желудка и двенадцатиперстной кишки. Заболевания тонкого и толстого кишечника
Симтоматология гастритов, язвенной болезни желудка и двенадцатиперстной кишки. Заболевания тонкого и толстого кишечника Актуальные проблемы охраны репродуктивного здоровья детей и подростков в современных условиях
Актуальные проблемы охраны репродуктивного здоровья детей и подростков в современных условиях Сепсис. Современный взгляд на проблему
Сепсис. Современный взгляд на проблему Оценка транспланта и криоконсервирование стволовых гемопоэтических клеток
Оценка транспланта и криоконсервирование стволовых гемопоэтических клеток Родовые травмы новорожденных. Повреждение мягких тканей, костей и суставов
Родовые травмы новорожденных. Повреждение мягких тканей, костей и суставов Семіотика основних захворювань нервової системи у дітей
Семіотика основних захворювань нервової системи у дітей Перфоративная язва
Перфоративная язва Сердечно-легочная реанимация в рекомендациях Европейского реанимационного совета по реанимации
Сердечно-легочная реанимация в рекомендациях Европейского реанимационного совета по реанимации Нарушения теплового баланса организма
Нарушения теплового баланса организма Общественное здоровье. Статистика заболеваемости. Источники получения информации
Общественное здоровье. Статистика заболеваемости. Источники получения информации Гастрит, асқазан ойық жарасы
Гастрит, асқазан ойық жарасы Доғалы протездердің бекіткіш элементтерінің түрлері
Доғалы протездердің бекіткіш элементтерінің түрлері Гастроэзофагальная рефлюксная болезнь (ГЭРБ)
Гастроэзофагальная рефлюксная болезнь (ГЭРБ) Тканевая теория канцерогенеза
Тканевая теория канцерогенеза Современные репродуктивные технологии в лечении женского бесплодия
Современные репродуктивные технологии в лечении женского бесплодия Геморрагическая лихорадка с почечным синдромом (ГЛПС)
Геморрагическая лихорадка с почечным синдромом (ГЛПС) Наблюдение беременной в женской консультации при физиологической беременности
Наблюдение беременной в женской консультации при физиологической беременности Проявления на слизистой полости рта специфических инфекций
Проявления на слизистой полости рта специфических инфекций Иммунная система организма. Антигены. Антитела. Гуморальный иммунный ответ
Иммунная система организма. Антигены. Антитела. Гуморальный иммунный ответ Пороки развития гонад – дисгенезия гонад
Пороки развития гонад – дисгенезия гонад Терминальные состояния
Терминальные состояния