Содержание
- 2. Лимфома Ходжкина Первичное опухолевое заболевание лимфатической системы Патогномонично наличие гигантских многоядерных клеток Рид-Березовского-Штернберга и одноядерных клеток
- 3. Лимфома Ходжкина Нодулярная форма с лимфоидным преобладанием (5%) Классическая (95%) Вариант, богатый лимфоцитами Лимфоидное истощение Смешанно-клеточная
- 4. Эпидемиология Россия: 2,1 случая на 100000 населения в год Европа: 2,2 случая на 100000 населения в
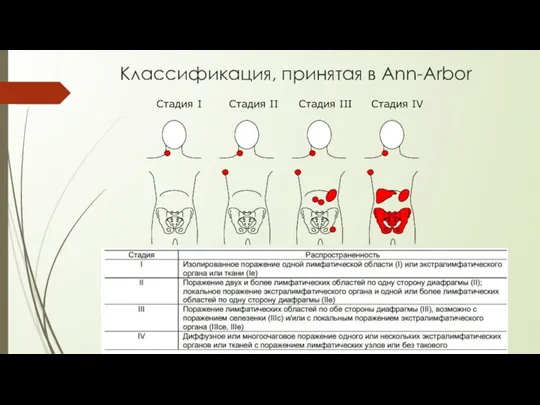
- 5. Классификация, принятая в Ann-Arbor
- 6. GHSG – German Hodgkin’s Lymphoma Study Group EORTC/GELA – European Organization for Research and Treatment of
- 7. Лечение классической лимфомы Ходжкина, I линия терапии a. Ранние стадии, благоприятный прогноз 2-4 цикла полихимиотерапии по
- 8. ABVD Доксорубицин 25 мг/м2 в/в, дни1 и15 Блеомицин 10 мг/м2 в/в, дни 1 и15 Винбластин 6
- 9. c. Распространённые стадии МПИ 0-2 - лечение 6 циклами ABVD при достижении полной ремиссии после 4-х
- 10. 2. Лечение рецидивов и резистентных форм Высокодозная химиотерапия с последующей трансплантацией аутологичных стволовых гемопоэтических клеток индукционная
- 11. ОСНОВЫ МЕТОДА ВЫСОКОДОЗОВОЙ ХТ (ВДХТ) И ТРАНСПЛАНТАЦИИ КЛЕТОК-ПРЕДШЕСТВЕННИКОВ ГЕМОПОЭЗА British National Lymphoma Investigation – 1993 –
- 12. GHSG и Lymphoma Working Party в составе EBMT Сравнение ВДХТ с кондиционированием по схеме ВЕАМ (кармустин/этопозид/цитарабин/мелфалан)
- 13. Техника аутотрансплантации Мобилизация (ХТ + Г-КСФ, ГМ-КСФ, плериксафор) Аферез мононуклеарной фракции клеток крови с помощью клеточных
- 14. Для улучшения результатов ауто ТГСК: • Качественный трансплантат • Улучшение собственно salvage – терапии, а именно
- 15. Требования к трансплантату Костный мозг должен быть без видимой примеси опухолевых клеток Клеточность трансплантата – не
- 16. Факторы риска недостаточного сбора ПСКК Пожилой возраст пациентов Распространённые стадии лимфомы Ходжкина Предшествующее лечение (большое количество
- 17. Предикторы эффективности ауто ТГСК: Поздний рецидив (>12 месяцев после достижения ремиссии) Отсутствие В-симптомов и экстранодальных поражений
- 18. Применение плериксафора для мобилизации гемопоэтических стволовых клеток Важную роль в фиксации гемопоэтических стволовых клеток (ГСК) к
- 19. Терапия при прогрессии заболевания после проведения аутоТГСК Немиелоаблативное кондиционирование с последующей аллогенной трансплантацией ГСК Паллиативная ХТ
- 20. Техника аллотрансплантации Подбор донора по HLA-антигенам 1 класса А, В и С, HLA-антигенам 2 класса DR,DQ
- 21. РОЛЬ АЛЛО-ТГСК ПРИ ЛХ В проспективное исследование ЕВМТ вошли 78 больных с немиелоаблативной аллоТСКК на основе
- 22. Брентуксимаб ведотин Брентуксимаб ведотин – это Antibody Drug Conjugate, состоящий из МКА к рецептору CD30 и
- 23. N Engl J Med. 2010 Nov 4;363(19):1812-21. doi: 10.1056/NEJMoa1002965. Brentuximab vedotin (SGN-35) for relapsed CD30-positive lymphomas.
- 25. Скачать презентацию





















 Социальное медицинское страхование в Республике Казахстан
Социальное медицинское страхование в Республике Казахстан Балалар мен жасөспірімдердің дене тәрбиесі мен шынығуының физикалық-гигиеналық негіздері
Балалар мен жасөспірімдердің дене тәрбиесі мен шынығуының физикалық-гигиеналық негіздері Метаболикалық синдромның биохимиясы
Метаболикалық синдромның биохимиясы ppt
ppt District sales manager, Novo Nordisk
District sales manager, Novo Nordisk 3D принтер в медицине
3D принтер в медицине Методы определения подлинности лекарственного растительного сырья. Занятие №2
Методы определения подлинности лекарственного растительного сырья. Занятие №2 Ампутация в хирургической практике
Ампутация в хирургической практике Лямблиоз. Клиника
Лямблиоз. Клиника Ғалымдар қоршаған ортадан келетін токсиндер ағзаның қартаюының жеделдетілуінің негізгі себептерінің бірі екенін анықтады
Ғалымдар қоршаған ортадан келетін токсиндер ағзаның қартаюының жеделдетілуінің негізгі себептерінің бірі екенін анықтады Инструментальные методы исследования сердца
Инструментальные методы исследования сердца Патронаж здорового новорожденного на дому с оформлением учебной амбулаторной карты
Патронаж здорового новорожденного на дому с оформлением учебной амбулаторной карты Аритмии сердца: ЭКГ-диагностика
Аритмии сердца: ЭКГ-диагностика Эстрогендерді қабылдау мен әйелдерде эдометрийдің қатерлі ісігінің дамуы арасындағы байланыс
Эстрогендерді қабылдау мен әйелдерде эдометрийдің қатерлі ісігінің дамуы арасындағы байланыс Точечный массаж
Точечный массаж Microscopic colitis
Microscopic colitis Интенсивная терапия осложненных форм СД, основы КЩС
Интенсивная терапия осложненных форм СД, основы КЩС Қазақстан республикасындағы психиатриялық көмекті ұйымдастыру
Қазақстан республикасындағы психиатриялық көмекті ұйымдастыру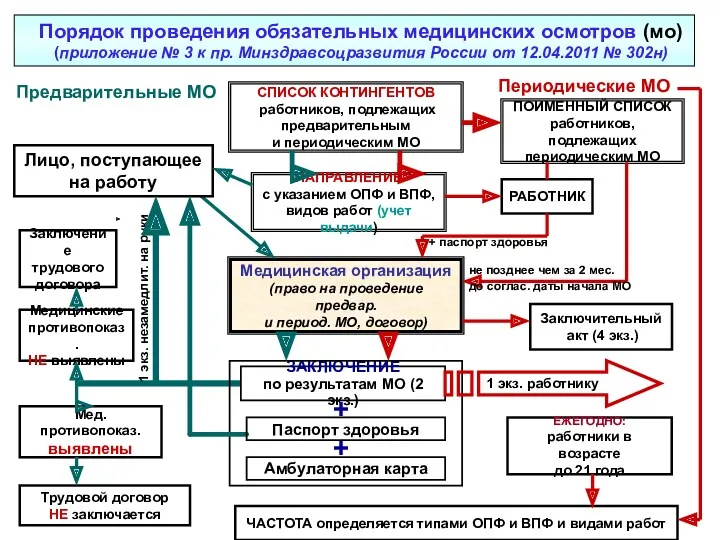 Порядок проведения обязательных медицинских осмотров
Порядок проведения обязательных медицинских осмотров Пренатальное развитие ребёнка
Пренатальное развитие ребёнка Шылым шегу
Шылым шегу Догляд за хворими із захворюваннями та ушкодженнями органів черевної порожнини
Догляд за хворими із захворюваннями та ушкодженнями органів черевної порожнини Синдром слабости синусового узла
Синдром слабости синусового узла Цереброваскулярные заболевания. Причины роста сосудистых заболеваний
Цереброваскулярные заболевания. Причины роста сосудистых заболеваний Балалардың физикалық критерийлер анықтау
Балалардың физикалық критерийлер анықтау Клеточные факторы врождённого иммунитета. Фагоцитоз и его стадии
Клеточные факторы врождённого иммунитета. Фагоцитоз и его стадии Тік ішектің және анустың атрезиясы
Тік ішектің және анустың атрезиясы Конусно-лучевая компьютерная томография в терапевтической стоматологии
Конусно-лучевая компьютерная томография в терапевтической стоматологии