Законодательство России и стран мира в области молекулярных и цитогенетических исследований презентация
Содержание
- 2. Клиническая лабораторная диагностика в практической медицине Деятельность клинико-диагностических лабораторий рассматривается в качестве важнейшей интегральной составляющей оказания
- 3. Направленность на профилактику и раннюю диагностику Внедрение эффективных методов, имеющих прогностическую значимость Должна базироваться на принципах
- 4. Основные направления развития лабораторий ЦКБ с Поликлиникой Обеспечение и контроль качества исследований на всех этапах Совместная
- 6. Основа взаимоотношений между клиникой и лабораторией
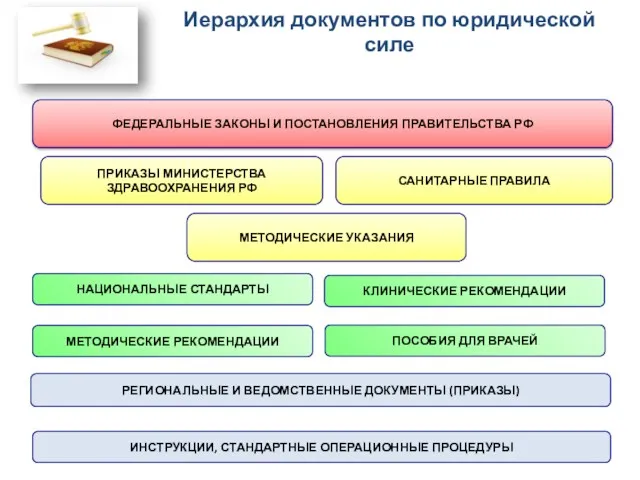
- 7. Иерархия документов по юридической силе ФЕДЕРАЛЬНЫЕ ЗАКОНЫ И ПОСТАНОВЛЕНИЯ ПРАВИТЕЛЬСТВА РФ ПРИКАЗЫ МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РФ САНИТАРНЫЕ
- 8. ФЕДЕРАЛЬНЫЙ ЗАКОН ОБ ОСНОВАХ ОХРАНЫ ЗДОРОВЬЯ ГРАЖДАН В РОССИЙСКОЙ ФЕДЕРАЦИИ Глава 1. ОБЩИЕ ПОЛОЖЕНИЯ Статья 2.
- 9. Статья 37. Порядки оказания медицинской помощи и стандарты медицинской помощи Медицинская помощь организуется и оказывается в
- 10. ФЕДЕРАЛЬНЫЙ ЗАКОН от 21.11.11 №323-ФЗ «ОБ ОСНОВАХ ОХРАНЫ ЗДОРОВЬЯ ГРАЖДАН Определение «Качество медицинской помощи» - совокупность
- 11. Организуем работу с документами КОНТРОЛЬ КАЧЕСТВА И БЕЗОПАСНОСТИ МЕДИЦИНСКОЙ ДЕЯТЕЛЬНОСТИ Ст. 85 – контроль в сфере
- 12. Организуем работу с документами КОНТРОЛЬ КАЧЕСТВА И БЕЗОПАСНОСТИ МЕДИЦИНСКОЙ ДЕЯТЕЛЬНОСТИ Ст. 87 – контроль качества и
- 13. УЧАСТНИКИ ПРОЦЕССА КОНТРОЛЯ КМП РОСЗДРАВНАДЗОР МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РФ МЕДИЦИНСКАЯ ОРГАНИЗАЦИЯ МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕГИОНА ФФОМС ТФОМС СМО
- 14. ПРИКАЗ МЗ РФ ОТ 21.12.12 № 1340н «Порядок организации и проведения ведомственного контроля качества и безопасности
- 15. УПРАВЛЕНИЕ КАЧЕСТВОМ МЕДИЦИНСКОЙ ПОМОЩИ Приказ МЗ РФ от 7 июля 2015 №422 ан - отменен Приказ
- 16. КЛЮЧЕВЫЕ РАЗДЕЛЫ ПРИКАЗА III. Критерии качества по группам заболеваний (состояний) (специализированная медицинская помощь) Критерии качества при
- 17. Приказ Минздрава России от 01.11.2012 N 572н (ред. от 11.06.2015) "Об утверждении Порядка оказания медицинской помощи
- 18. Приказ Минздрава России от 01.11.2012 N 572н (ред. от 12.01.2016) "Об утверждении Порядка оказания медицинской помощи
- 19. Постановление Правительства РФ от 08.12.2017 N 1492 (ред. от 21.04.2018) "О Программе государственных гарантий бесплатного оказания
- 20. Приложение N 6.1 к Тарифному соглашению на 2018 год от 29 декабря 2017 года «Тарифы на
- 21. 4. На территории Российской Федерации разрешается обращение медицинских изделий, зарегистрированных в порядке, установленном Правительством Российской Федерации,
- 22. Распоряжение Правительства РФ от 05.05.2018 N 870-р
- 23. ПЛАН МЕРОПРИЯТИЙ ("дорожная карта") "Хелснет" Национальной технологической инициативы П А С П О Р Т 69.
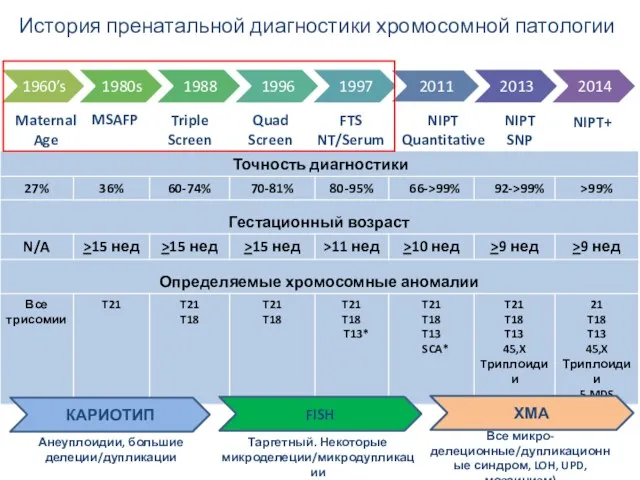
- 24. Maternal Age MSAFP Triple Screen Quad Screen FTS NT/Serum NIPT Quantitative NIPT SNP NIPT+ КАРИОТИП FISH
- 25. Программное обеспечение для оценки рисков патологии плода Программное обеспечение серии «PRISCA» РУ ФС № 2006/1569 (дата
- 26. Приказ Министерства здравоохранения РФ от 7 июля 2015 г. №422ан "Об утверждении Критериев оценки качества медицинской
- 27. Следственный комитет России 4 октября 2017 года следователи СК выступили инициативой – ввести в УК специальную
- 28. Основные этапы лабораторного анализа
- 29. Стандартные операционные процедуры (СОПы) ´ Стандартные операционные процедуры (СОП) представляют собой подробные описания условий, средств и
- 30. ´ СОП должна содержать ответ на следующие вопросы: КТО? (участвует в реализации СОП) КАК? (отражаются действия
- 31. ВИДЫ СОПов СОПы Преаналитического этапа за пределами лаборатории (анализируются и утверждаются руководители учреждения здравоохранения совместно с
- 32. Федеральная Система Внешней Оценки Качества лабораторных исследований (ФСВОК) Три цикла оценки правильности и внутрисерийной воспроизводимости определения
- 33. Акт проверки инспекцией ФАС России № 213 от 30.12.2014 в отношении Федеральной службы по надзору в
- 35. Maternal Screening External Quality Assessment The RIQAS Maternal Screening EQA programme – скрининг 1-го и 2-го
- 36. В 2018 году нет в программе внешней оценки.
- 37. UK NEQAS Clinical Cytogenetics (Англия) Неинвазивный пренатальный тест для диагностики анеуплоидий (пилотный проект) (совместно с UK
- 38. 19. Genetics and Molecular Pathology (США) Genetics and Molecular Pathology Cytogenetics Biochemical and Molecular Genetics Next-Generation
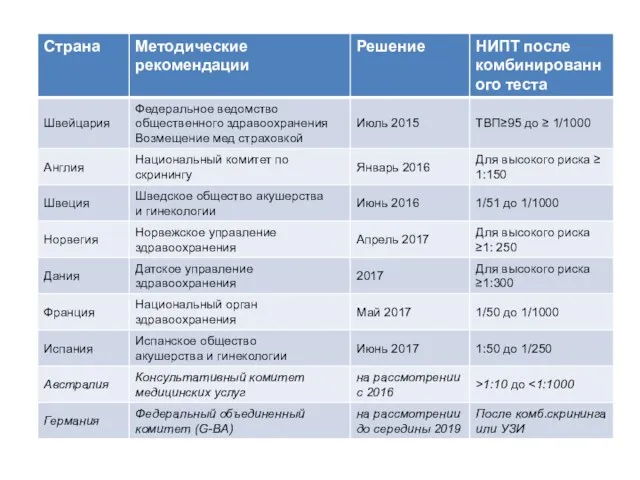
- 39. Рекомендации Международной федерации акушеров-гинекологов (FIGO) 2015 года Неинвазивный пренатальный скрининг Скрининг I триместра — комбинированный, в
- 40. Рекомендации Шведского общества акушерства и гинекологии (2016) По результатам комбинированного скрининга: ≥1 / 50 риск инвазивный
- 42. Приказ Минздрава России от 13.10.2017 N 804н "Об утверждении номенклатуры медицинских услуг» Класс раздела "A" 27
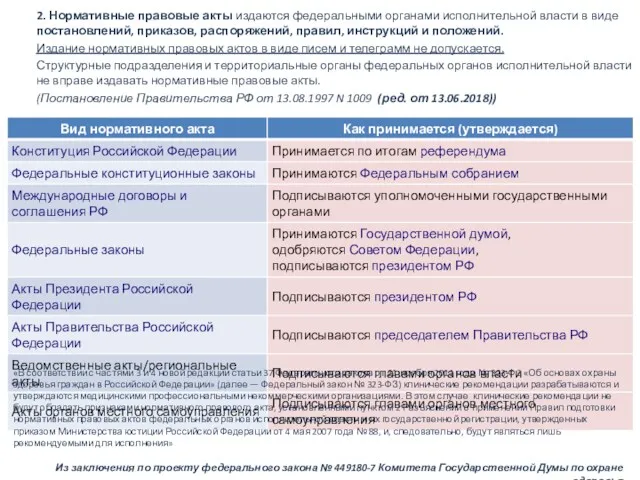
- 43. 2. Нормативные правовые акты издаются федеральными органами исполнительной власти в виде постановлений, приказов, распоряжений, правил, инструкций
- 44. Врач сегодня - не только специалист — профессионал, он настоящий солдат на фронте борьбы за здоровую,
- 46. Скачать презентацию







































 Здоровое питание – активное долголетие
Здоровое питание – активное долголетие Современные лабораторные маркеры аутоиммунных заболеваний. Аутоимунный гепатит, аутоимунный тиреоидит
Современные лабораторные маркеры аутоиммунных заболеваний. Аутоимунный гепатит, аутоимунный тиреоидит Акушерские кровотечения во время беременности
Акушерские кровотечения во время беременности Анатомо - физиологические особенности сердечно - сосудистой системы детей
Анатомо - физиологические особенности сердечно - сосудистой системы детей Робот Da Vinci
Робот Da Vinci Заключительная лекция по аллергии и иммунопатологии
Заключительная лекция по аллергии и иммунопатологии Эндокринная система
Эндокринная система Принципи будови та функції нервової системи. Безумовні рефлекси. Система довільних рухів
Принципи будови та функції нервової системи. Безумовні рефлекси. Система довільних рухів Беременность и рак молочной железы
Беременность и рак молочной железы Гастриты. Классификация острых гастритов
Гастриты. Классификация острых гастритов БДСҰ ұсынысы бойынша ана сүтімен тамақтануға дайындау,жанұяны жоспарлау,контрацепция,аналық сүт безі обыры
БДСҰ ұсынысы бойынша ана сүтімен тамақтануға дайындау,жанұяны жоспарлау,контрацепция,аналық сүт безі обыры Туберкулез және жүктілік
Туберкулез және жүктілік Микола Михайлович Амосов
Микола Михайлович Амосов Проблема бессонницы в структуре соматических заболеваний
Проблема бессонницы в структуре соматических заболеваний Проблемы регулирования цен на лекарственные препараты в Российской Федерации и возможные пути их решения
Проблемы регулирования цен на лекарственные препараты в Российской Федерации и возможные пути их решения Цирроз печени
Цирроз печени Обследование гинекологических больных
Обследование гинекологических больных Косметика. Косметология
Косметика. Косметология Холецистэктомия. Травма печени
Холецистэктомия. Травма печени Анафилактический шок. Неотложная помощь. Интенсивная терапия
Анафилактический шок. Неотложная помощь. Интенсивная терапия Здоровый образ жизни
Здоровый образ жизни Развитие в онтогенезе. Младенческий возраст
Развитие в онтогенезе. Младенческий возраст Косметический массаж. (Тема 4.5)
Косметический массаж. (Тема 4.5) Синдром дефицита внимания и гиперактивности
Синдром дефицита внимания и гиперактивности Лабораторная диагностика заболеваний спинномозговой жидкости
Лабораторная диагностика заболеваний спинномозговой жидкости Ерте босану немесе мерзімінен бұрын босану
Ерте босану немесе мерзімінен бұрын босану Гиподинамия. Причины гиподинамии
Гиподинамия. Причины гиподинамии Использование УЗИ при катетеризации центральных вен
Использование УЗИ при катетеризации центральных вен