Содержание
- 2. Учебные вопросы: Тепловая теория прекращения горения. Способы прекращения горения при различных материалах и режимах горения. Виды
- 3. Тепловая теория прекращения горения Согласно тепловой теории задача прекращения пламенного горения сводится к снижению температуры в
- 4. Зависимость интенсивности тепловыделения q+ от вида горючего, состава горючей смеси и температуры описывается уравнением: где Qн
- 5. Интенсивность процесса теплоотвода q - от фронта пламени описывается уравнением: где α - коэффициент теплопередачи; -
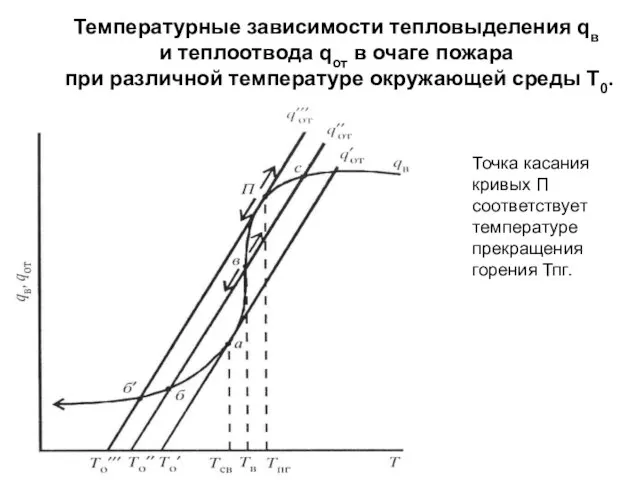
- 6. Температурные зависимости тепловыделения qв и теплоотвода qот в очаге пожара при различной температуре окружающей среды Т0.
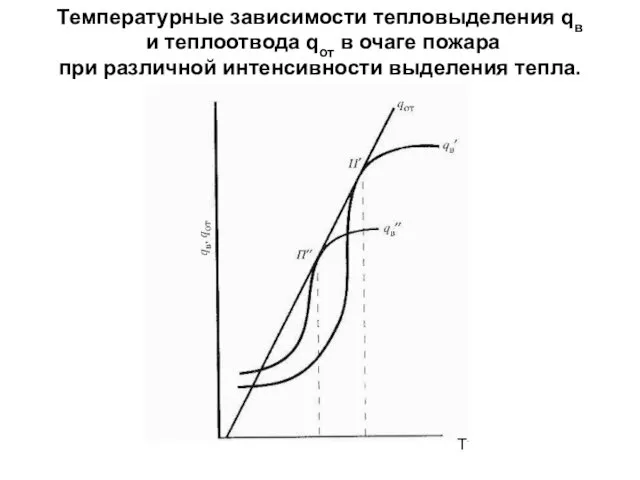
- 7. Температурные зависимости тепловыделения qв и теплоотвода qот в очаге пожара при различной интенсивности выделения тепла. Т
- 8. Критические граничные условия прекращения горения имеют вид:
- 9. 2. Способы прекращения горения при различных материалах и режимах горения. Виды огнетушащих веществ 3. Повышение Еа
- 10. Повышающие интенсивность теплоотвода из зоны горения q- Повышение излучательной способности пламени (ﻉ) за счёт специальных добавок;
- 11. Пожаротушение обеспечивают: 1. Изоляцией очага горения от воздуха или снижением концентрации кислорода в воздухе; 2. Охлаждением
- 12. Огнетушащими называют вещества , обладающие физико-химическими свойствами, позволяющими прекратить горение. Огнетушащие вещества (ОВ), классифицируют по агрегатному
- 13. По воздействию на процесс горения огнетушащие вещества подразделяются на: - охлаждающие (вода, подаваемая в очаг пожара
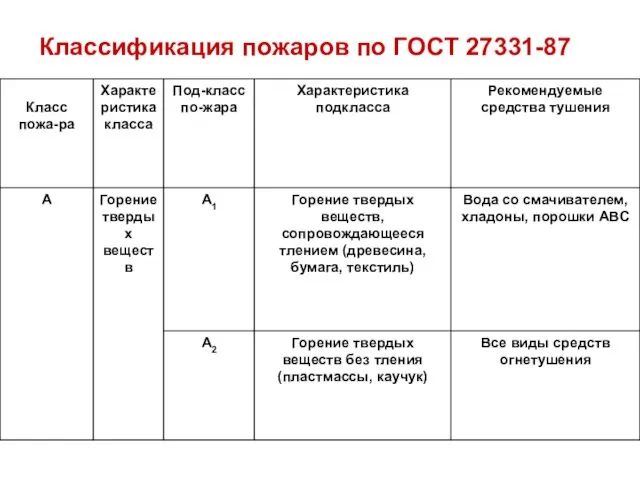
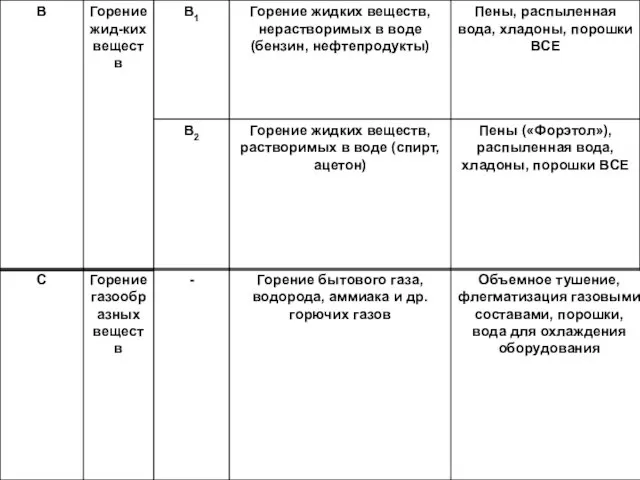
- 14. Классификация пожаров по ГОСТ 27331-87
- 17. Все способы пожаротушения подразделяют на 2 группы: 1) способы поверхностного тушения; 2) способы объемного тушения. Нормативные
- 18. Параметры огнетушения связаны между собой: G = I·τ где G – удельное количество средств, необходимое для
- 19. 3. Виды огнетушащих веществ. 1. Вода Недостатки: высокая температура замерзания; недостаточная смачивающая способность; высокая электропроводность; химическая
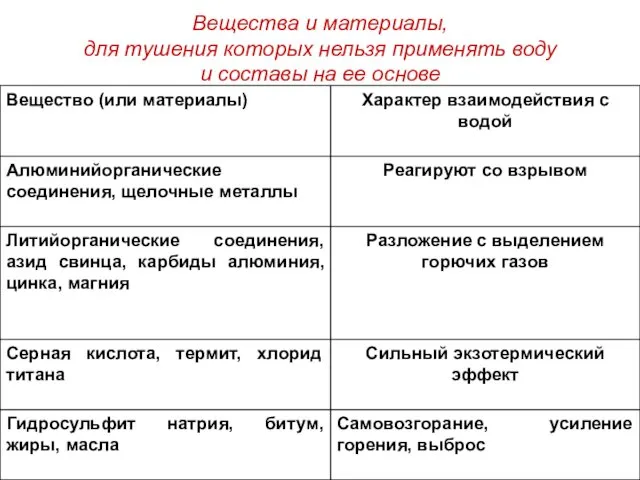
- 20. Вещества и материалы, для тушения которых нельзя применять воду и составы на ее основе
- 21. 2. Пены Пены – коллоидные системы, получают добавлением к воде пенообразователей (ПО) и порошков, в качестве
- 23. Важной характеристикой пены является ее кратность: Vпены Кратность = --------- Vжидкой фазы Воздушно-механические пены подразделяются на:
- 24. Максимальная кратность пены, получаемой из раствора ПАВ с концентрацией С0: где r – средний радиус пузырьков;
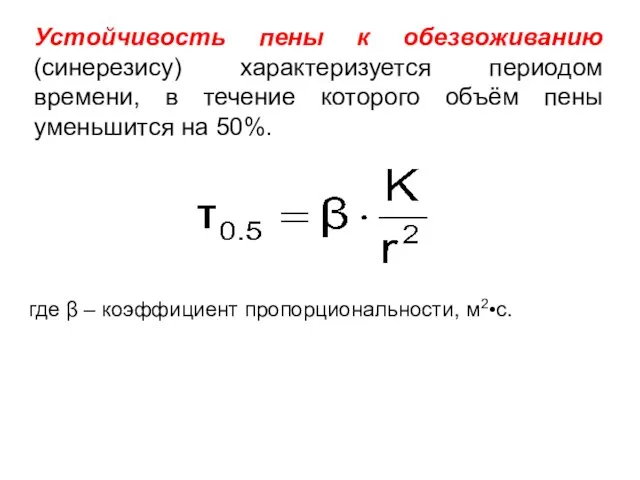
- 25. Устойчивость пены к обезвоживанию (синерезису) характеризуется периодом времени, в течение которого объём пены уменьшится на 50%.
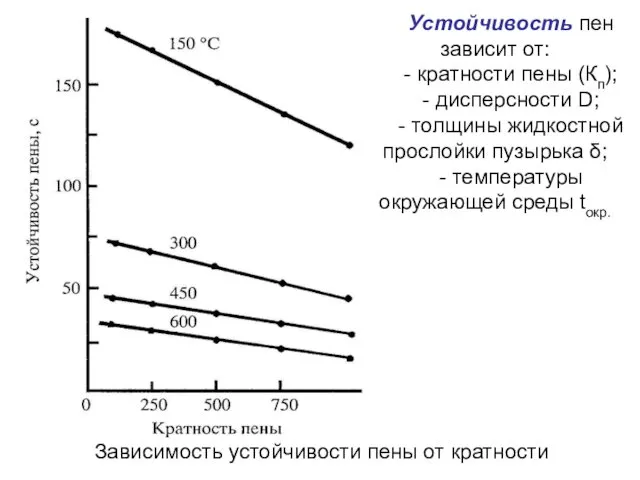
- 26. Устойчивость пен (S) зависит от: - кратности пены (Кп); - дисперсности D; - толщины жидкостной прослойки
- 27. Зависимость устойчивости пены от кратности Устойчивость пен зависит от: - кратности пены (Кп); - дисперсности D;
- 28. Тушение пожара пеной осуществляется при формировании на горящей поверхности критической толщины слоя (Hкр.), через который горючие
- 29. Нормативная интенсивность подачи пены при тушении жидких горючих веществ в резервуарах: Критическая толщина слоя (Hкр.) определяет
- 30. 3.3. Инертные разбавители В качестве инертных разбавителей используют: азот, аргон, дымовые газы, диоксид углерода, водяной пар,
- 31. Добавление инертного компонента , не способного вступать в реакцию с окислителем, снижает объемную концентрацию горючего. При
- 32. Требуемый для стационарных установок объемного тушения запас диоксида углерода m (в кг): m = 1,1 ⋅
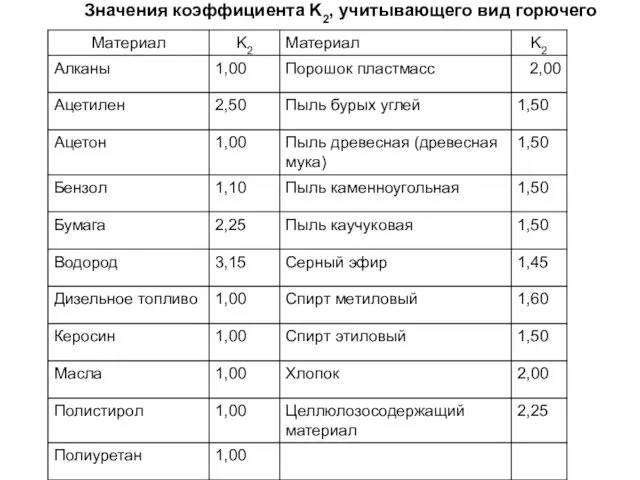
- 33. Значения коэффициента K2, учитывающего вид горючего
- 34. Время подачи CO2 по нормам принимают от 60 до 120 с. Недостатки CO2 : опасность отравления
- 35. 4. Хладоны СF3Br, СF2ClBr, С2F4Br2, СF2Br2. Огнетушащая эффективность хладонов повышается при замещении в них водорода галогенами
- 36. Хладоны являются ингибиторами горения. Механизм огнетушащего действия хладонов заключается в торможении цепного процесса, происходящего при горении,
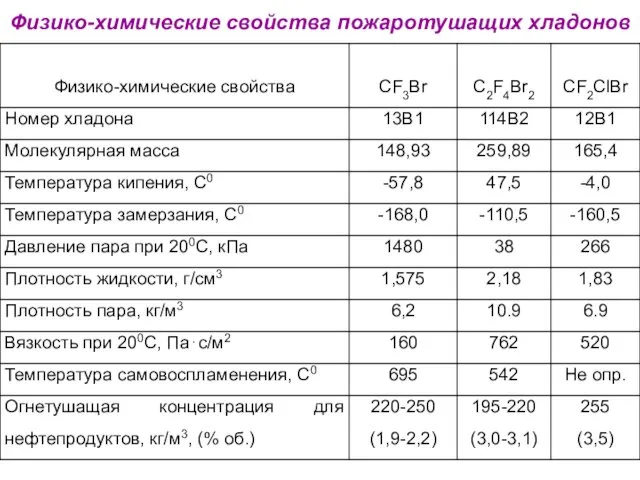
- 37. Физико-химические свойства пожаротушащих хладонов
- 38. Достоинства хладонов: наиболее эффективно тормозят горение органических веществ (нефтепродуктов, растворителей и др.) их можно применять при
- 39. 5. Порошки (ПОС) Огнетушащие порошки -мелкоизмельченные минеральные соли с различными добавками, препятствующими слеживанию. Наибольшее применение имеют
- 40. В качестве основы для порошков используют: фосфорноаммонийные соли (моно-, диаммоний фосфаты, аммофос), карбонат и бикарбонат натрия,
- 41. Эффект тушения с помощью ПОС является комбинированным и включает: − изоляцию горящей поверхности от доступа окислителя;
- 42. ГЛАВНЫЙ МЕХАНИЗМ огнетушащего действия порошков - это ингибирование горения в результате связывания активных центров цепных реакций,
- 43. По огнетушащей способности используемые в составе ПОС соли располагаются в ряд: K2С2O4⋅H2O > NaCl > Na2СO3
- 44. Основные преимущества ПОС : высокая огнетушащая способность, превышающая свойства таких сильных ингибиторов горения, как хладоны; универсальность
- 45. Основной недостаток ПОС заключается в их склонности к слеживанию и комкованию. Для его исключения влажность порошков
- 46. Аэрозольное пожаротушение заключается в заполнении защищаемого объёма сильнодиспергированным огнетушащим составом, образующимся при сжигании твёрдотопливной композиции. Огнетушащий
- 47. Комбинированные составы Комбинированные составы сочетают свойства различных огнетушащих средств. Наиболее эффективные из них представляют собой комбинации
- 49. Скачать презентацию





































 Единая государственная система предупреждения и ликвидации чрезвычайных ситуаций (РСЧС)
Единая государственная система предупреждения и ликвидации чрезвычайных ситуаций (РСЧС) Интерактивный тест Образцовый пешеход
Интерактивный тест Образцовый пешеход Деятельность отдела охраны труда, техники безопасности и окружающей среды ТОО Казахтуркмунай
Деятельность отдела охраны труда, техники безопасности и окружающей среды ТОО Казахтуркмунай Принципы организации медицины катастроф
Принципы организации медицины катастроф Превентивная защита от возгорания на транспортных средствах
Превентивная защита от возгорания на транспортных средствах Обеспечение личной безопасности на воздушном транспорте
Обеспечение личной безопасности на воздушном транспорте Презентация по безопасному движению.Создана для воспитанников старшей группы ГБДОУ №82
Презентация по безопасному движению.Создана для воспитанников старшей группы ГБДОУ №82 Защита технологического оборудования и коммуникаций от распространения пожаров
Защита технологического оборудования и коммуникаций от распространения пожаров Фаст-фудтың адам өміріне зияндылығы
Фаст-фудтың адам өміріне зияндылығы Здоровый образ жизни и его составляющие
Здоровый образ жизни и его составляющие Образ жизни и здоровье
Образ жизни и здоровье Причины дорожно-транспортных происшествий и травматизма людей. 8 класс
Причины дорожно-транспортных происшествий и травматизма людей. 8 класс Викторина по противопожарной безопасности для учащихся 2-6 классов
Викторина по противопожарной безопасности для учащихся 2-6 классов Вызов экстренных служб
Вызов экстренных служб Ұялы телефонды адам денсаулығына зияны
Ұялы телефонды адам денсаулығына зияны Домашняя аптечка
Домашняя аптечка Областной конкурс по профилактике детского дорожно - транспортного травматизма на 2018-2020гг
Областной конкурс по профилактике детского дорожно - транспортного травматизма на 2018-2020гг Секреты здорового питания (мероприятие для учеников начальных классов)
Секреты здорового питания (мероприятие для учеников начальных классов) India Taukebay Olzhas
India Taukebay Olzhas Мы выбираем жизнь!!! Жизнь без наркотиков!
Мы выбираем жизнь!!! Жизнь без наркотиков! Безопасность жизнедеятельности. Безопасность на транспорте. Вопрос № 5
Безопасность жизнедеятельности. Безопасность на транспорте. Вопрос № 5 Интегрированные уроки по основам безопасности жизнедеятельности как средство формирования универсальных учебных действий
Интегрированные уроки по основам безопасности жизнедеятельности как средство формирования универсальных учебных действий Основы безопасности и правила поведения на железной дороге
Основы безопасности и правила поведения на железной дороге Оптимизация труда человека - оператора ЭВМ
Оптимизация труда человека - оператора ЭВМ Профессия пожарный
Профессия пожарный Выпускная квалификационная работа: Совершенствование системы управления промышленной безопасностью и охраной труда
Выпускная квалификационная работа: Совершенствование системы управления промышленной безопасностью и охраной труда Опасные места. (Окружающий мир. 3 класс)
Опасные места. (Окружающий мир. 3 класс) Техногенная катастрофа
Техногенная катастрофа