Слайд 2

Сорбция – поглощение каким-либо веществом других веществ.
Адсорбция – процесс сорбции, идущий
на поверхности, который представляет собой увеличение концентрации на границе раздела фаз.
Абсорбция – процесс сорбции, при котором поглощаемое вещество диффундирует в глубь поглотителя и распределяется по объему.
Слайд 3

Хемосорбция – поглощение, сопровождающееся химическим взаимодействием поглощаемого вещества с веществом-поглотителем.
Капиллярная конденсация
– поглощение и конденсация твердыми пористыми адсорбентами газов и паров.
Адсорбент – вещество, на поверхности которого идет адсорбция.
Адсорбат – вещество, которое адсорбируется.
Слайд 4

1) A = X / S, где
A – адсорбция,
X –
адсорбат,
S – единица площади поверхности адсорбента, кмоль/м2.
2) A = X / m (если адсорбент твердое пористое тело и его поверхность определить невозможно), где
m – единица массы адсорбента, кмоль/кг
Слайд 5

Десорбция – процесс обратный адсорбции, который характеризуется удалением адсорбционных молекул с
поверхности адсорбента.
Скорость адсорбции с течением времени уменьшается, а скорость десорбции увеличивается. Эти изменения происходят до тех пор, пока их скорости не станут одинаковыми, т. е. наступает адсорбционное равновесие:
Адсорбция ‹-› Десорбция
Т. к. химическая адсорбция обусловлена образованием связей, близких к химическим, десорбция протекает с большим трудом.
Адсорбция носит избирательный характер.
Пр: активированный уголь хорошо поглощает хлор, но не адсорбирует угарный газ(со),адсорбционная способность активированного угля по отношению к йоду хорошая, т. к. уголь поглощает запах и цвет йода, а раствор становится прозрачным.




 Восстание под руководством Емельяна Пугачёва (1773 – 1775 гг.)
Восстание под руководством Емельяна Пугачёва (1773 – 1775 гг.) ПРЕЗЕНТАЦИЯ К МЕРОПРИЯТИЮ ДЛЯ ДЕТЕЙ ПОДГОТОВИТЕЛЬНОЙ ГРУППЫ Я — ПЕРВОКЛАССНИК Диск
ПРЕЗЕНТАЦИЯ К МЕРОПРИЯТИЮ ДЛЯ ДЕТЕЙ ПОДГОТОВИТЕЛЬНОЙ ГРУППЫ Я — ПЕРВОКЛАССНИК Диск Washington is the capital of the United States of America
Washington is the capital of the United States of America ВВЭР (водо-водяной энергетический реактор)
ВВЭР (водо-водяной энергетический реактор) Презентация Парад Победы
Презентация Парад Победы Организация свадебного торжества
Организация свадебного торжества Християнська етика. Щедрість і захланність
Християнська етика. Щедрість і захланність Современные средства поражения
Современные средства поражения prezetantsia
prezetantsia Презентация Проектная технология в начальной школе
Презентация Проектная технология в начальной школе Коротковой Юлии, юс1-11
Коротковой Юлии, юс1-11 past simple
past simple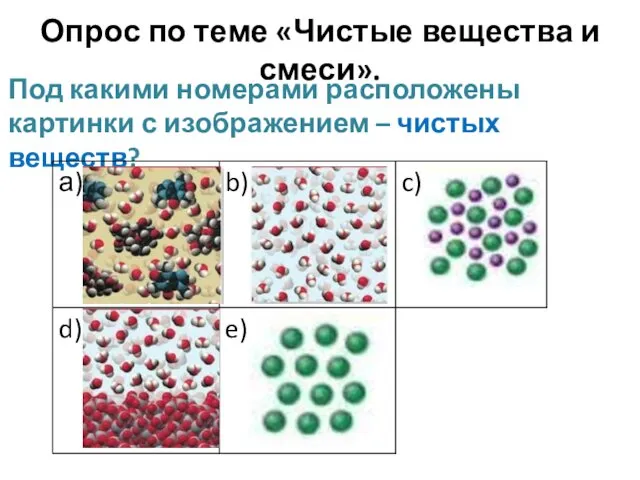 Классификация веществ. Приготовление растворов. Расчёт массовой доли растворённого вещества
Классификация веществ. Приготовление растворов. Расчёт массовой доли растворённого вещества Пізня зрілість (Е. Еріксон)
Пізня зрілість (Е. Еріксон) Проект Вместе лучше. Концепция воспитательной работы в классе.
Проект Вместе лучше. Концепция воспитательной работы в классе. Информационные технологии. Структура технологической системы
Информационные технологии. Структура технологической системы Детская игровая комната
Детская игровая комната Эпоха Просвещения
Эпоха Просвещения Реконструкция и реновация особняков России
Реконструкция и реновация особняков России Presentation Zilubag for customers
Presentation Zilubag for customers Асфиксия – жизнеугрожающее состояние, связанное с нарушением газообмена
Асфиксия – жизнеугрожающее состояние, связанное с нарушением газообмена Предмет органической химии
Предмет органической химии Автозаправочные станции
Автозаправочные станции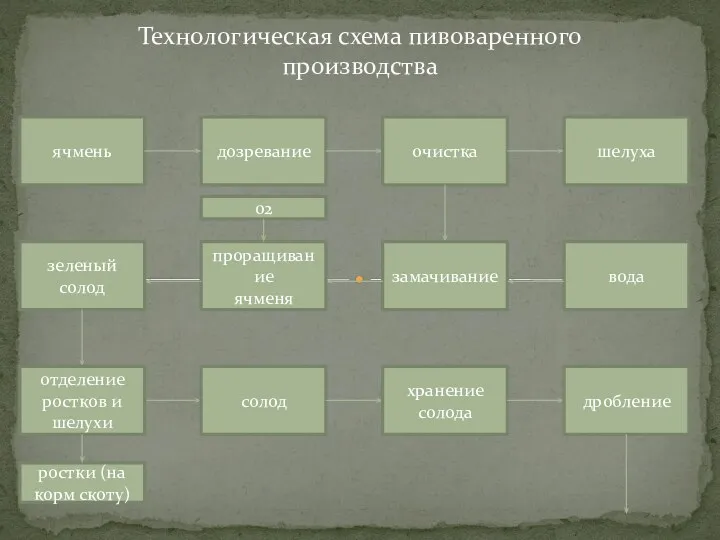 Технология производства пива
Технология производства пива Артикли в английском языке
Артикли в английском языке Сушка
Сушка урок по технологии обработки древесины на деревообрабатывающих станках
урок по технологии обработки древесины на деревообрабатывающих станках Овощи (большой - маленький). Уроки логопеда
Овощи (большой - маленький). Уроки логопеда