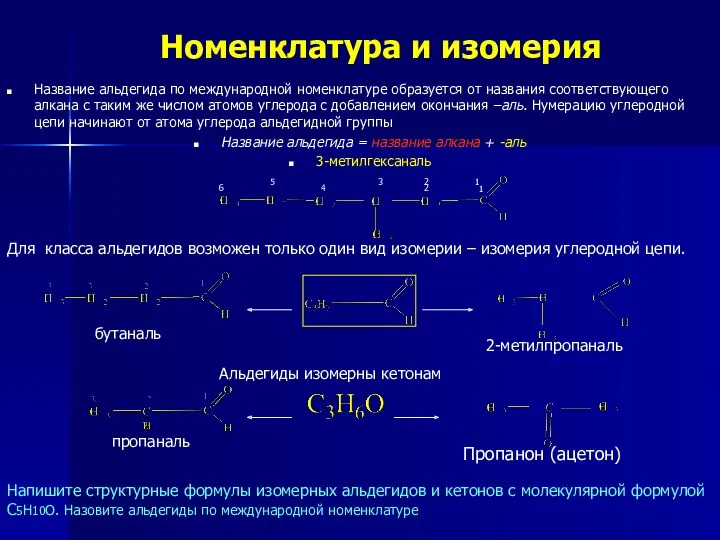
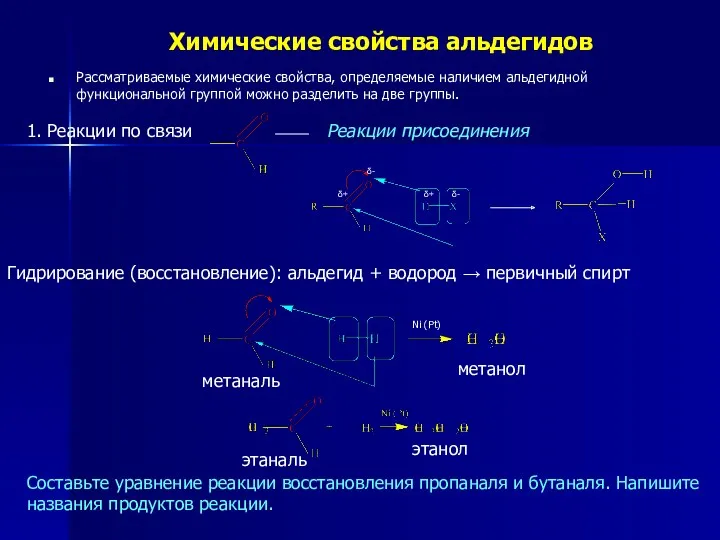
Электронное строение
δ
δ+
δ-
Атом углерода альдегидной группы находится в состоянии sp2-гибридизации, поэтому атомы,
которые непосредственно связаны с ним (атомы «О», «Н», «С») находятся в одной плоскости.
Атом углерода соединен с атомом кислорода двойной связью, которая состоит из σ- и π-связи. Электроны π-связи смещены в сторону более электроотрицательного атома кислорода. В результате атом «О» имеет δ-, а атом «С» - δ+.
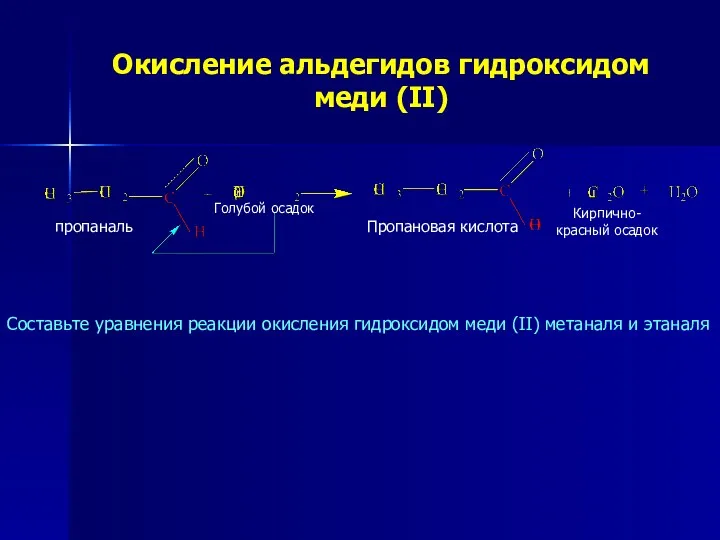
Физические свойства
газ
жидкости
Твердые вещества
Низшие альдегиды имеют резкий запах, высшие альдегиды, содержащие 8-12 атомов «С» - душистые вещества. Альдегиды с 1-3 атомами «С» хорошо растворяются в воде; с увеличением числа атомов «С» растворимость уменьшается.
Альдегиды раздражают слизистые оболочки глаз и верхних дыхательных путей, вредно влияют на нервную систему.





 Конспект классного часа
Конспект классного часа Инновационная педагогика Л.Н. Толстого
Инновационная педагогика Л.Н. Толстого Тепломассообмен. Расчёт теплообменных аппаратов. (Лекция 14)
Тепломассообмен. Расчёт теплообменных аппаратов. (Лекция 14) Здоровое питание.
Здоровое питание. Теплообменные аппараты холодильных машин и вспомогательное оборудование
Теплообменные аппараты холодильных машин и вспомогательное оборудование Правила пользования руководством 4Р
Правила пользования руководством 4Р Социальные взаимодействия
Социальные взаимодействия Неправильная парковка
Неправильная парковка Русская народная кукла
Русская народная кукла Лечение гриппа
Лечение гриппа Истечение жидкости через водосливы с тонкой стенкой и с широким порогом
Истечение жидкости через водосливы с тонкой стенкой и с широким порогом Основы спорта
Основы спорта Презентация 8 марта
Презентация 8 марта Российский стандарт профессиональной деятельности архитектора. Кодекс профессиональной этики архитектора. (Лекция 10)
Российский стандарт профессиональной деятельности архитектора. Кодекс профессиональной этики архитектора. (Лекция 10) Гидравлические и пневматические силовые установки
Гидравлические и пневматические силовые установки ДП Львівський бронетанковий завод
ДП Львівський бронетанковий завод Авиационные двигатели и их системы управления. Основы устройства силовых установок и их конструкция
Авиационные двигатели и их системы управления. Основы устройства силовых установок и их конструкция Рельеф Смоленской области
Рельеф Смоленской области Управление ИТ-услугами и его качество
Управление ИТ-услугами и его качество Равномерное прямолинейное движение
Равномерное прямолинейное движение Подвиг без национальности
Подвиг без национальности Математика 1 класс. УМК Перспектива. Урок №2. Тема Разговор о величине
Математика 1 класс. УМК Перспектива. Урок №2. Тема Разговор о величине Деректер қоры
Деректер қоры Феохромоцитома. Определение
Феохромоцитома. Определение Машины для земляных работ. Общие понятие и классификация
Машины для земляных работ. Общие понятие и классификация ГИА по математике: проблемы и пути решения
ГИА по математике: проблемы и пути решения How to assemble a wardrobe. Tools and fixing for assembling
How to assemble a wardrobe. Tools and fixing for assembling Жалобы пациентов с патологией дыхательной системы
Жалобы пациентов с патологией дыхательной системы