Содержание
- 2. Понятие об аминах Амины — производные аммиака, в молекулах которых один или несколько атомов водорода замещены
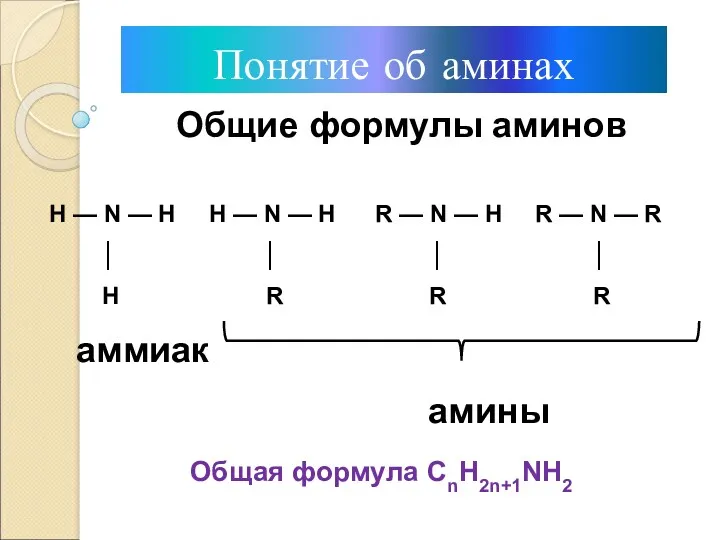
- 3. Понятие об аминах Общие формулы аминов Н — N — H Н — N — H
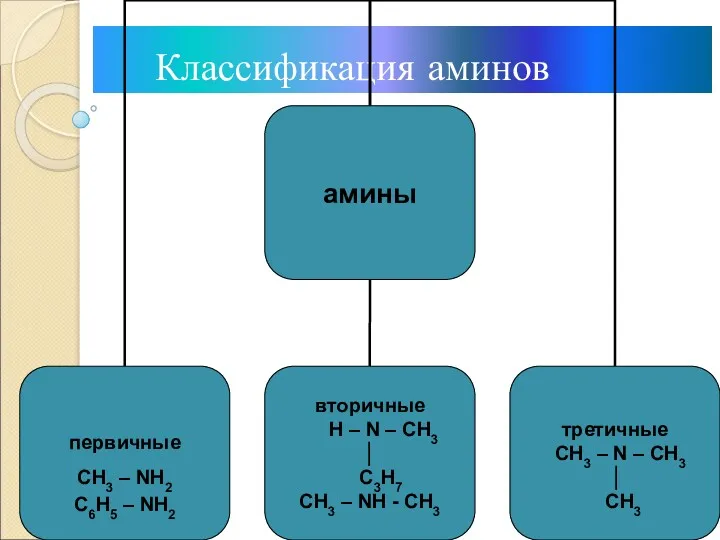
- 4. Классификация аминов
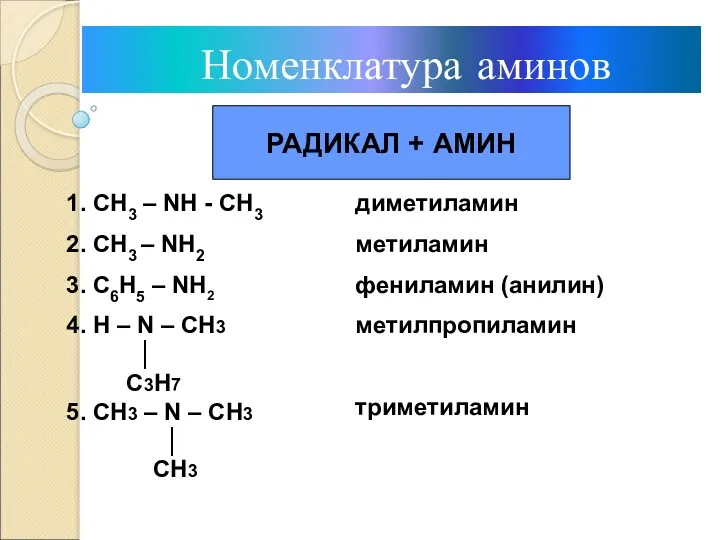
- 5. Номенклатура аминов РАДИКАЛ + АМИН 1. СН3 – NН - СН3 2. СН3 – NН2 3.
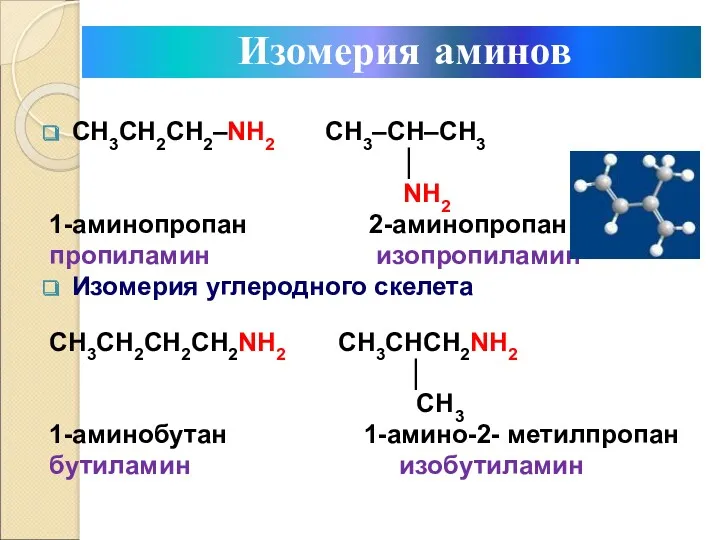
- 6. CH3CH2CH2–NH2 CH3–CH–CH3 │ NH2 1-аминопропан 2-аминопропан пропиламин изопропиламин Изомерия углеродного скелета CH3CH2CH2CH2NH2 CH3CHCH2NH2 │ CH3 1-аминобутан
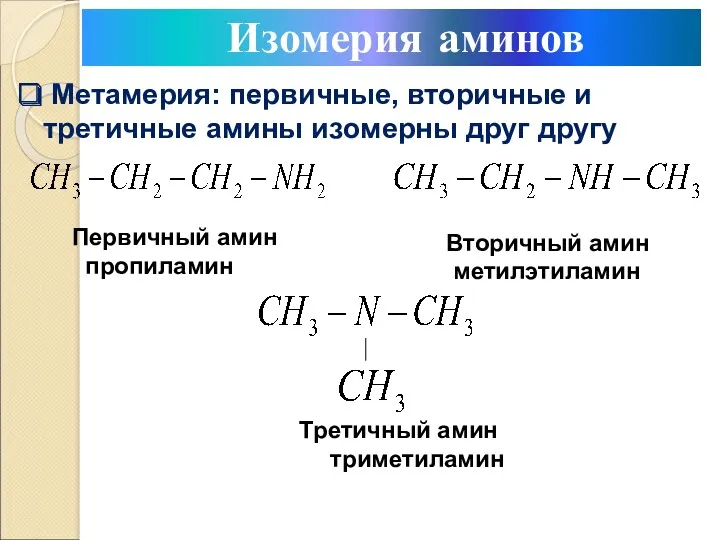
- 7. Метамерия: первичные, вторичные и третичные амины изомерны друг другу Первичный амин пропиламин Вторичный амин метилэтиламин Третичный
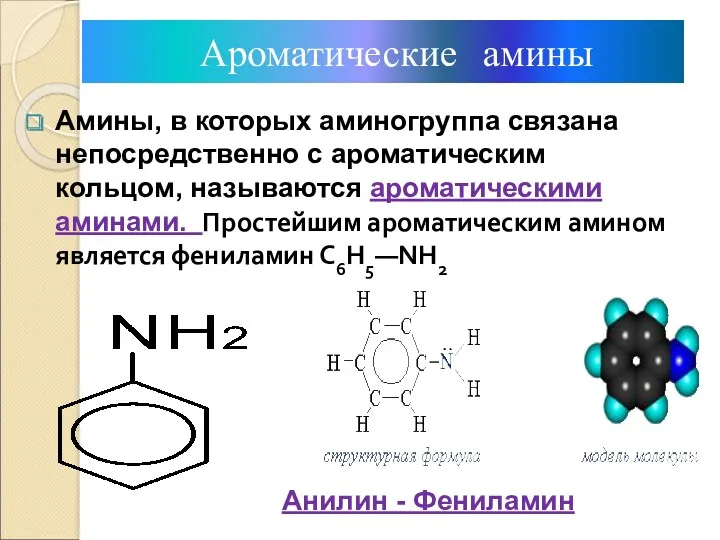
- 8. Амины, в которых аминогруппа связана непосредственно с ароматическим кольцом, называются ароматическими аминами. Простейшим ароматическим амином является
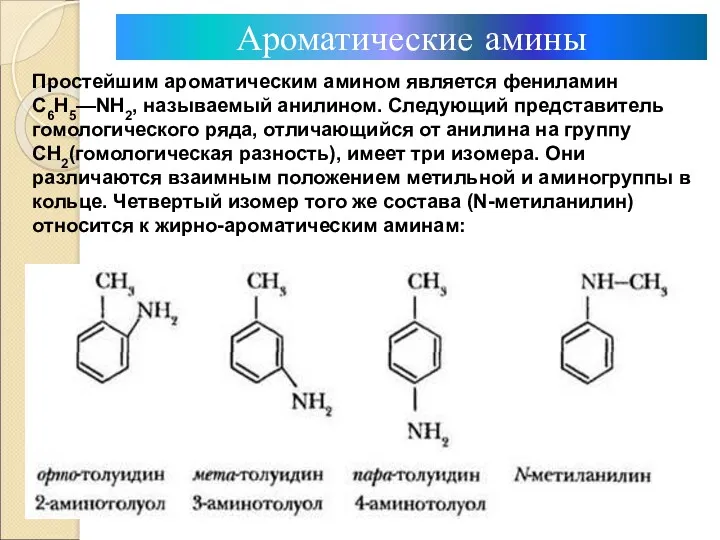
- 9. Ароматические амины Простейшим ароматическим амином является фениламин С6Н5—NH2, называемый анилином. Следующий представитель гомологического ряда, отличающийся от
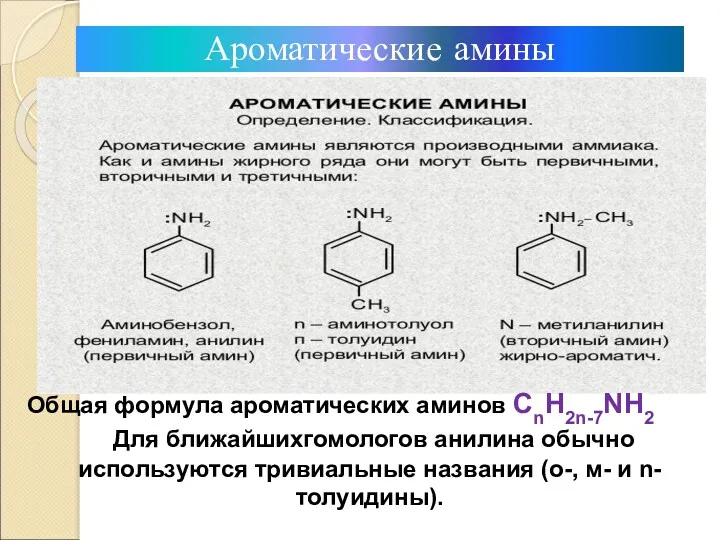
- 10. Ароматические амины Общая формула ароматических аминов СnН2n-7NH2 Для ближайшихгомологов анилина обычно используются тривиальные названия (о-, м-
- 11. Метиламин, диметиламин и триметиламин – газы; средние члены алифатического ряда – жидкости; высшие – твердые вещества.
- 12. Физические свойства анилина Анилин – маслянистая жидкость, ограниченно растворимая в воде, кипящая при температуре 184˚С
- 13. В результате этой реакции образуется соль амина (гидробромид этиламмония), из которой действием щёлочи можно выделить первичный
- 14. При взаимодействии полученного первичного амина и галогенопроизводного и последующей обработке щелочью получают вторичный амин (диэтиламин): Получение
- 15. Повторение процедуры приводит к образованию третичного амина: Получение
- 16. Третичный амин может ещё раз вступить в реакцию с бромэтаном. При этом образуется четвертичная аммонийная соль,
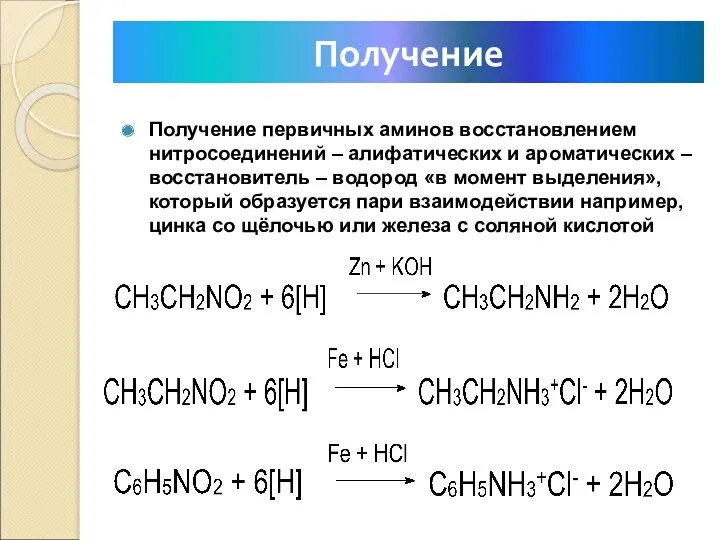
- 17. Получение Получение первичных аминов восстановлением нитросоединений – алифатических и ароматических – восстановитель – водород «в момент
- 18. В промышленности анилин (аминобензол) – получают восстановлением нитробензола, нагревая в присутствии железа с водяным паром: Способ
- 19. Получение анилина Зинин Николай Николаевич (1812 – 1880) Русский химик — органик, академик. «Если бы Зинин
- 20. ион аммония ион тетраэтиламмония Существуют ионы, которые являются продуктом формального замещения на углеводородный радикал всех атомов
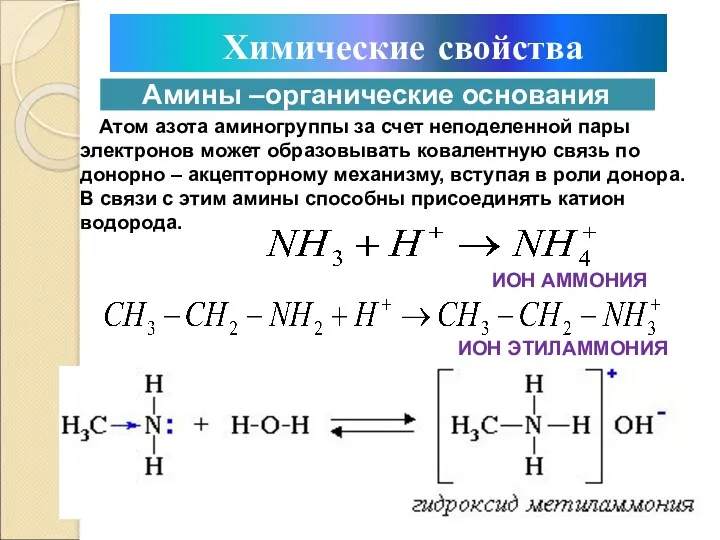
- 21. Атом азота аминогруппы за счет неподеленной пары электронов может образовывать ковалентную связь по донорно – акцепторному
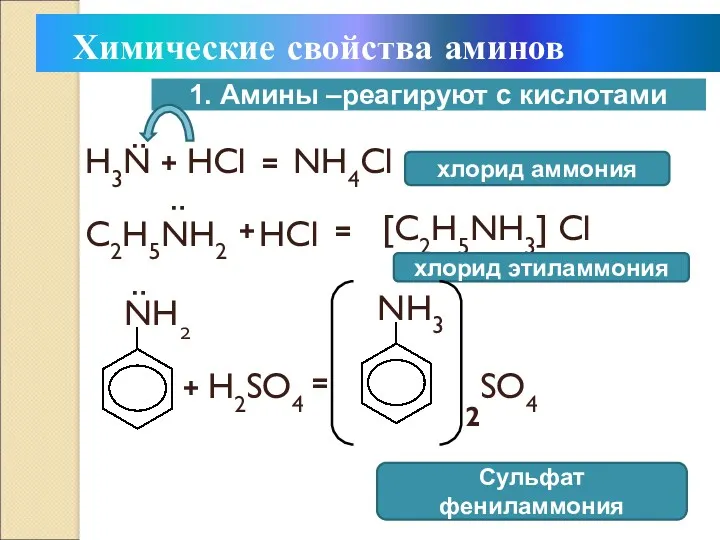
- 22. + H3N HCl = NH4Cl хлорид аммония C2H5NH2 : : + HCl = [C2H5NH3] Cl хлорид
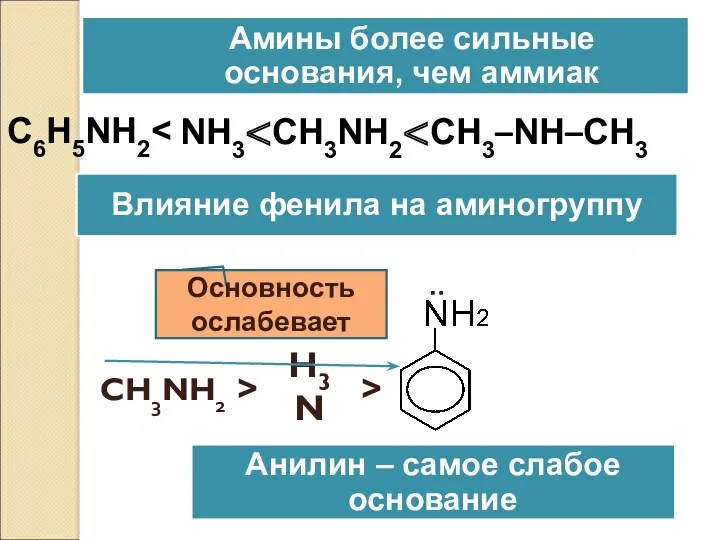
- 23. : CH3NH2 > H3N > Основность ослабевает NH3 C6H5NH2
- 24. На воздухе с образованием углекислого газа, воды и азота: Химические свойства аминов
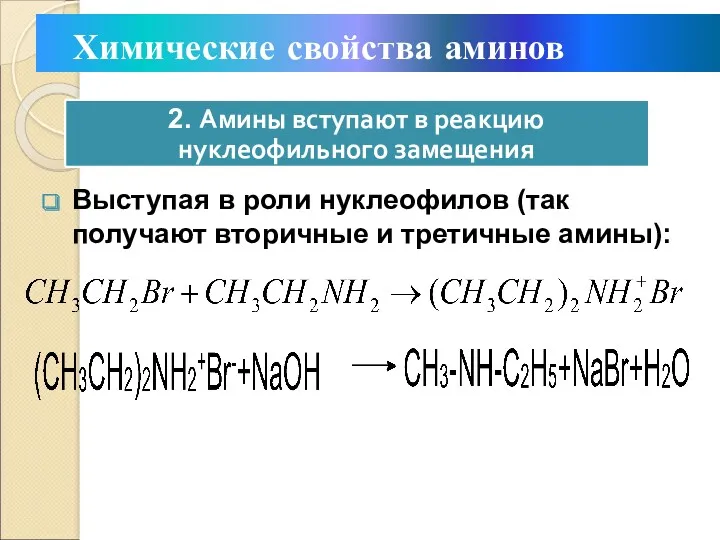
- 25. Выступая в роли нуклеофилов (так получают вторичные и третичные амины): Химические свойства аминов
- 26. Химические свойства аминов Образуя Амиды – важнейший класс органических соединений: этиламид уксусной кислоты метиламид уксусной кислоты
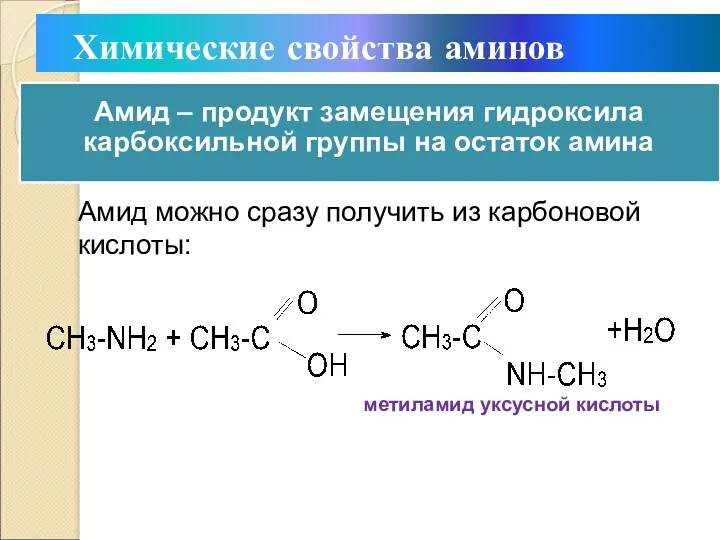
- 27. Химические свойства аминов Амид можно сразу получить из карбоновой кислоты: метиламид уксусной кислоты
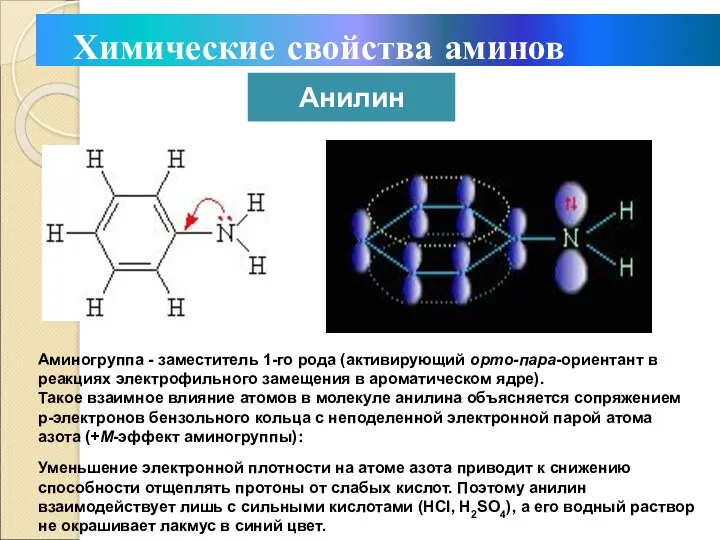
- 28. Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому
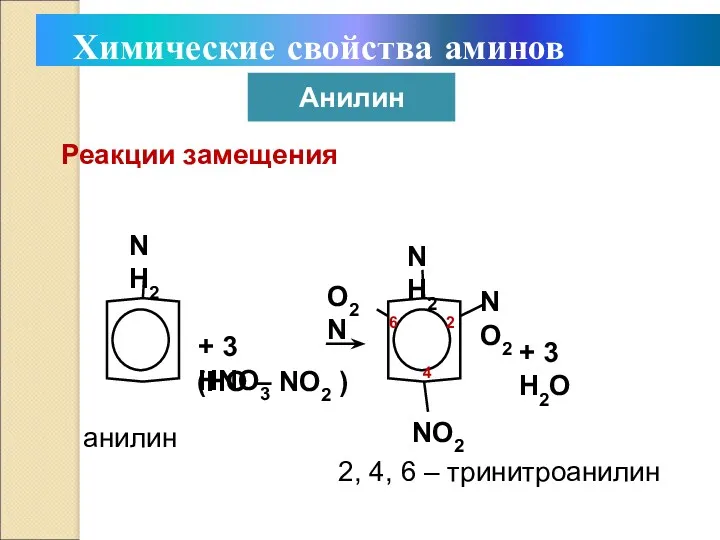
- 29. Реакции замещения NH2 + 3 HNO3 (HO – NO2 ) NH2 NO2 NO2 O2N + 3
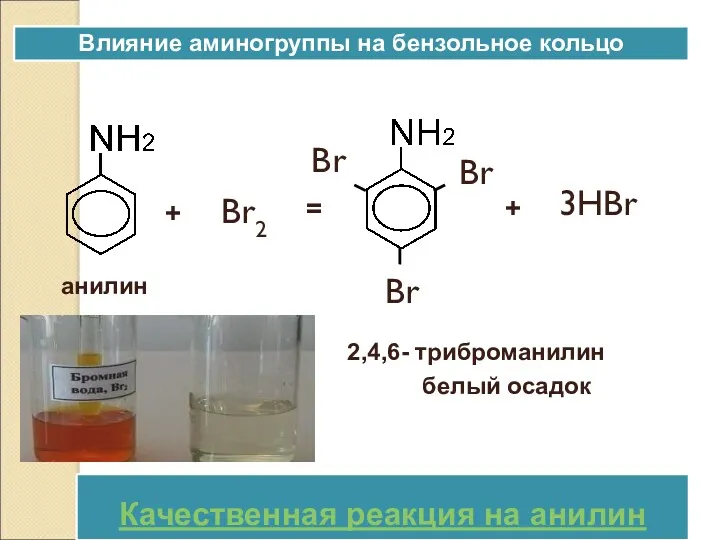
- 30. + Br2 = Br Br Br анилин 3HBr + 2,4,6- триброманилин белый осадокбелый
- 31. С6Н5NH2 + H+Cl- → [С6Н5NH3]+Cl- хлорид фениламмония Реакция анилина с соляной кислотой
- 32. Применение аминов Амины широко применяются для получения лекарств, полимерных материалов.
- 34. Скачать презентацию












![С6Н5NH2 + H+Cl- → [С6Н5NH3]+Cl- хлорид фениламмония Реакция анилина с соляной кислотой](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/27236/slide-30.jpg)

 Геометрические задачи практического содержания в вариантах ГИА
Геометрические задачи практического содержания в вариантах ГИА Дискуссионные проблемы. Задание 25 по истории
Дискуссионные проблемы. Задание 25 по истории Формы и виды публичной коммуникации
Формы и виды публичной коммуникации Роль нефти и углеводородных газов в мировом и российском топливно-энергетическом балансах
Роль нефти и углеводородных газов в мировом и российском топливно-энергетическом балансах Розвиток металургii
Розвиток металургii Сетевые черви и защита от них
Сетевые черви и защита от них Отправка заказа Avon
Отправка заказа Avon транспорт
транспорт Театрально- интегрированная деятельность для детей старше-подготовительного возраста
Театрально- интегрированная деятельность для детей старше-подготовительного возраста Наш коллектив
Наш коллектив Урок в 8 классе Генетическая связь веществ
Урок в 8 классе Генетическая связь веществ Гипертоническая болезнь
Гипертоническая болезнь Презентация Я здесь живу, и край мне этот дорог.История развития поселка Первомайский
Презентация Я здесь живу, и край мне этот дорог.История развития поселка Первомайский Образование СССР. Внешняя политика СССР в 1921-1927 годах
Образование СССР. Внешняя политика СССР в 1921-1927 годах Получение гидролизатов из пивной дробины и изучение условий культивирования на них разных видов дрожжей
Получение гидролизатов из пивной дробины и изучение условий культивирования на них разных видов дрожжей Фруктовый сад-загадки
Фруктовый сад-загадки Иудаизм в культуре
Иудаизм в культуре Фундаментальные физические явления наноэлектроники
Фундаментальные физические явления наноэлектроники Роль супервайзера в достижении лидерства ТМ Nemiroff в рознице в г. Одесса
Роль супервайзера в достижении лидерства ТМ Nemiroff в рознице в г. Одесса Грозова енергетика
Грозова енергетика Презентация к внеклассному мероприятию Здравствуй, Зимушка-зима
Презентация к внеклассному мероприятию Здравствуй, Зимушка-зима Мероприятия по раннему выявлению незаконного потребления наркотических средств и психотропных веществ
Мероприятия по раннему выявлению незаконного потребления наркотических средств и психотропных веществ e0ef78602e2a8994
e0ef78602e2a8994 Материаловедение. Технология конструкционных материалов. Материалы и материаловедение. (Тема 1)
Материаловедение. Технология конструкционных материалов. Материалы и материаловедение. (Тема 1) Оператор цикла For/Next
Оператор цикла For/Next Образ тургеневской девушки
Образ тургеневской девушки Интегрированное занятие Жили-были мама коза с козлятами
Интегрированное занятие Жили-были мама коза с козлятами Воспитательный процесс. Содержание воспитания
Воспитательный процесс. Содержание воспитания