Содержание
- 2. Строение молекулы аммиака Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине; Атом азота
- 3. Аммиак − слабое основание Аммиак − это слабое основание, водные растворы аммиака имеют слабощелочную среду и
- 4. Взаимодействие аммиака с хлороводородом и раствором соляной кислоты 2. При взаимодействии: а) газообразного аммиака с газообразным
- 5. Взаимодействие раствора аммиака с растворами кислот 3. Аммиак взаимодействует с кислотами, образуя соли аммония: а) с
- 6. Взаимодействие раствора аммиака с растворами солей 4. Аммиака или гидроксид аммония реагирует с растворами солей, образуя
- 7. Взаимодействие аммиака с соединениями меди (II) и другими солями 5. Комлексообразование – молекулы NH3 могут входить
- 8. Аммиак – сильный восстановитель Так как в аммиаке атом N−3 находится в низшей степени окисления, то
- 9. Свойства аммиака как восстановителя 1. Взаимодействие с галогенами: а) Фтор мгновенно окисляет аммиак до трифторида: N–3H3
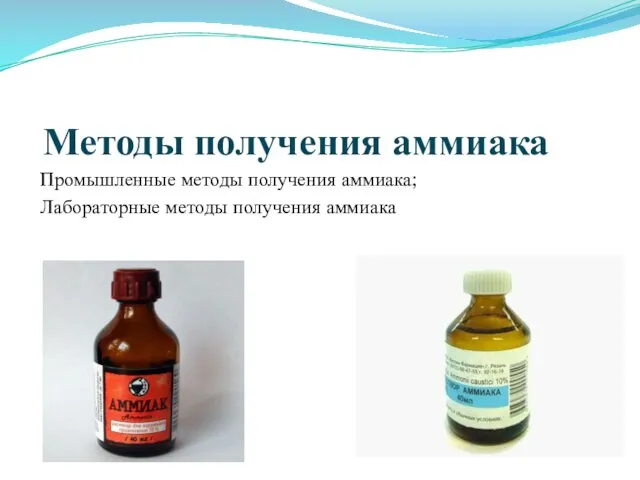
- 10. Методы получения аммиака Промышленные методы получения аммиака; Лабораторные методы получения аммиака
- 11. Промышленный метод получения аммиака Прямое взаимодействие водорода и азота (процесс Габера): р=200 атм N2(г) + 3H2(г)
- 12. Лабораторные методы получения Аммиака 1. Взаимодействие солей аммония со щелочами при нагревании: Ca(OH)2 + 2NH4Cl →
- 13. Получение и термолиз солей аммония Все соли аммония при нагревании разлагаются; При этом возможны: 1) Не
- 14. Термолиз солей аммония (не ОВР) 1.1. Карбонат аммония t°C (NН4)2СО3 → 2NН3↑+ СО2↑ + Н2О 1.2.
- 15. Термолиз солей аммония (ОВР) 2.1. Нитрит аммония t°C NН4NО2 → N2↑+ 2Н2О 2.2. Нитрат аммония t°C
- 17. Скачать презентацию













 Презентация Воздушный транспорт
Презентация Воздушный транспорт Инновационные подходы в преподавании физики и при подготовке к государственной итоговой аттестации в форме ЕГЭ и ОГЭ
Инновационные подходы в преподавании физики и при подготовке к государственной итоговой аттестации в форме ЕГЭ и ОГЭ Информация по сессии в Международном юридическом институте
Информация по сессии в Международном юридическом институте Презентация Информационно-коммуникационные технологии в процессе развития и обучения дошкольников
Презентация Информационно-коммуникационные технологии в процессе развития и обучения дошкольников Друзья-лицеисты Пушкина
Друзья-лицеисты Пушкина презентация Готовимся к школе
презентация Готовимся к школе Игровые технологии в ДОУ
Игровые технологии в ДОУ Великий канон cвятого Андрея Критского, читаемый в четверг пятой седмицы Великого поста
Великий канон cвятого Андрея Критского, читаемый в четверг пятой седмицы Великого поста Классный час Моя малая Родина.
Классный час Моя малая Родина. United Kingdom
United Kingdom Интегрированный урок (математика-география) Применение теоремы Пифагора в сельском хозяйстве
Интегрированный урок (математика-география) Применение теоремы Пифагора в сельском хозяйстве Анализ эмитента на примере ПАО ЛУКОЙЛ
Анализ эмитента на примере ПАО ЛУКОЙЛ Математика, как наука
Математика, как наука Технология сборки двутавровой балки
Технология сборки двутавровой балки ЛЕКЦИЯ 8. Электрические машины постоянного тока. Устройство электрической машины постоянного тока
ЛЕКЦИЯ 8. Электрические машины постоянного тока. Устройство электрической машины постоянного тока Информационная культура. Этические и правовые нормы информационной деятельности челове
Информационная культура. Этические и правовые нормы информационной деятельности челове Формирование и развитие философии науки
Формирование и развитие философии науки БЕЗОПАСНОСТЬ НА ДОРОГАХ
БЕЗОПАСНОСТЬ НА ДОРОГАХ 20 способов провалить интервью в Google
20 способов провалить интервью в Google Музеи мира. Лувр
Музеи мира. Лувр История основания города Петрозаводска
История основания города Петрозаводска Соуси
Соуси Типы и конструкции микроэлектромеханических систем. Сенсоры. Классификация сенсоров
Типы и конструкции микроэлектромеханических систем. Сенсоры. Классификация сенсоров ПЕДАГОГИЧЕСКИЙ СОВЕТ НА ТЕМУ: Формирование правовой компетентности учащихся – предупреждение подростковой преступности и правонарушений.
ПЕДАГОГИЧЕСКИЙ СОВЕТ НА ТЕМУ: Формирование правовой компетентности учащихся – предупреждение подростковой преступности и правонарушений. Учитель года-2012
Учитель года-2012 Преступления против собственности
Преступления против собственности Учимся рисовать вместе. Советы для родителей
Учимся рисовать вместе. Советы для родителей Сообщающиеся сосуды
Сообщающиеся сосуды