Содержание
- 2. Ароматичность как особое химическое качество характерно не только для бензола. Существуют соединения, не относящиеся к ряду
- 3. Соединения, содержащие 4n π-электронов в замкнутой сопряженной системе, являются антиароматическими. Соединения,в которых отсутствует циклическая система сопряженных
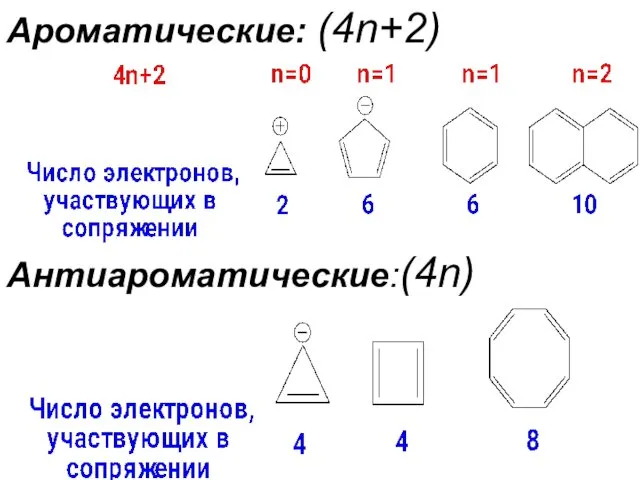
- 4. Ароматические: (4n+2) Антиароматические:(4n)
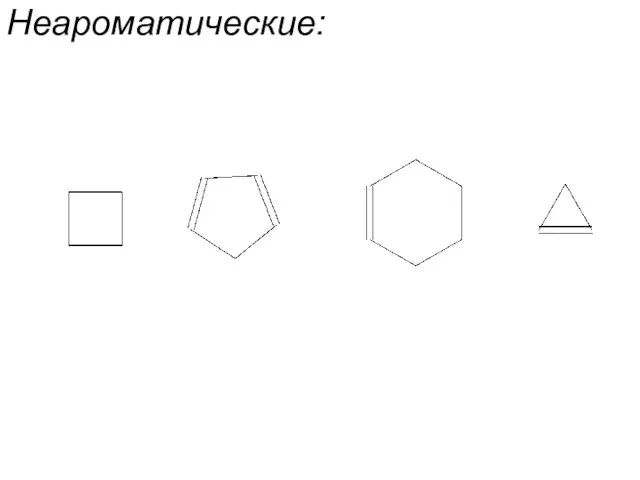
- 5. Неароматические:
- 6. Конденсированные арены
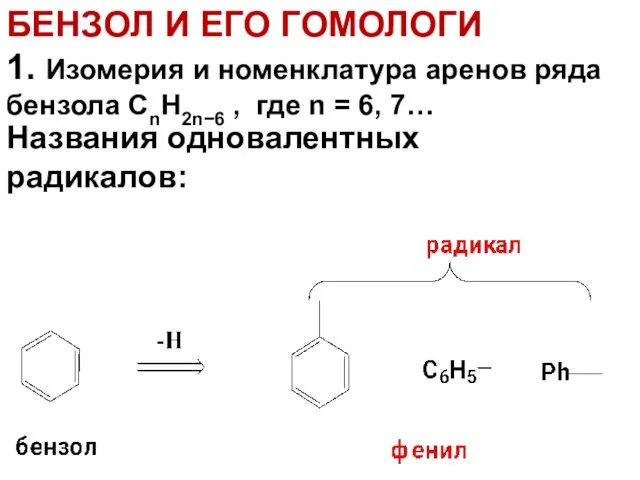
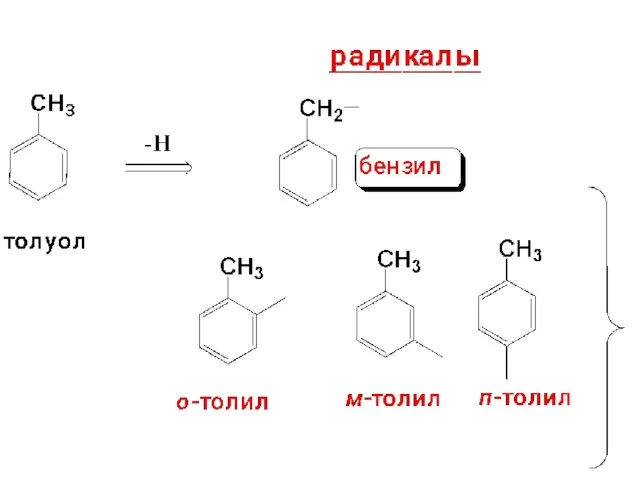
- 7. БЕНЗОЛ И ЕГО ГОМОЛОГИ 1. Изомерия и номенклатура аренов ряда бензола СnH2n−6 , где n =
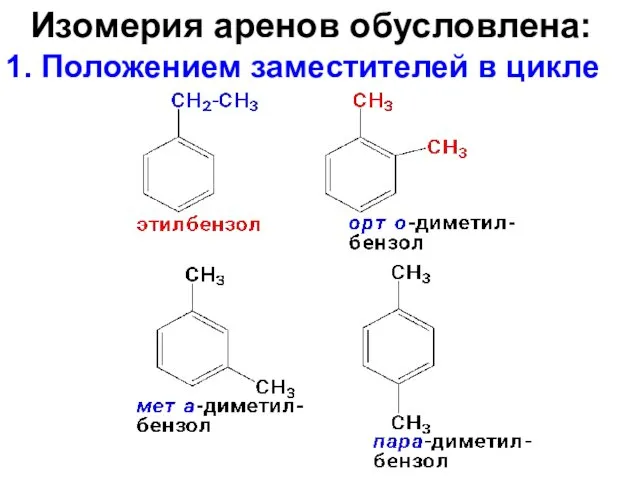
- 9. Изомерия аренов обусловлена: 1. Положением заместителей в цикле
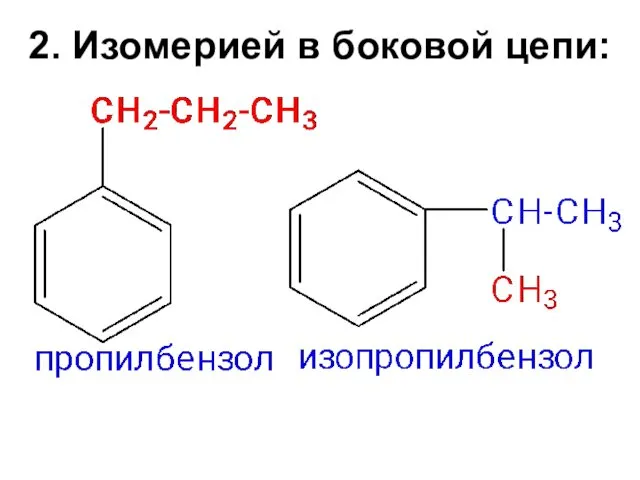
- 10. 2. Изомерией в боковой цепи:
- 11. СПОСОБЫ ПОЛУЧЕНИЯ Ряд промышленных способов основан на переработке угля и нефти. Из 1 т угля в
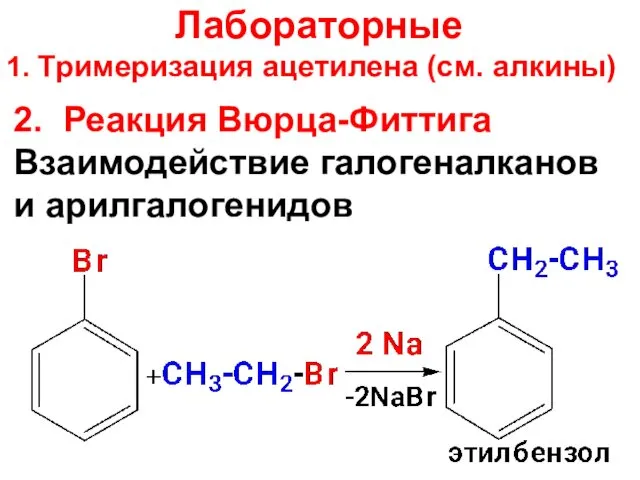
- 12. 2. Реакция Вюрца-Фиттига Взаимодействие галогеналканов и арилгалогенидов Лабораторные 1. Тримеризация ацетилена (см. алкины)
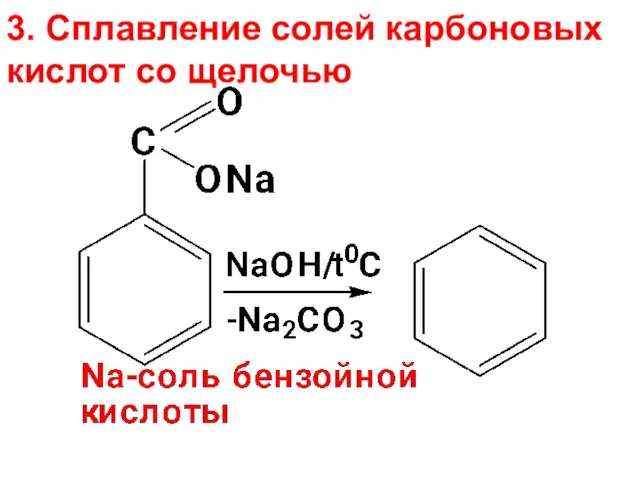
- 13. 3. Сплавление солей карбоновых кислот со щелочью
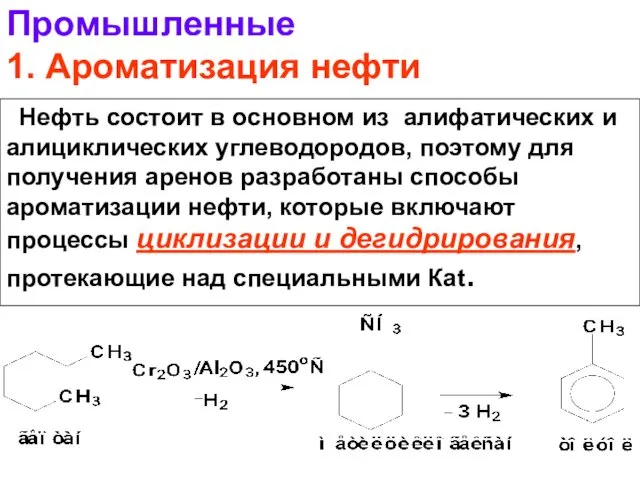
- 14. Промышленные 1. Ароматизация нефти Нефть состоит в основном из алифатических и алициклических углеводородов, поэтому для получения
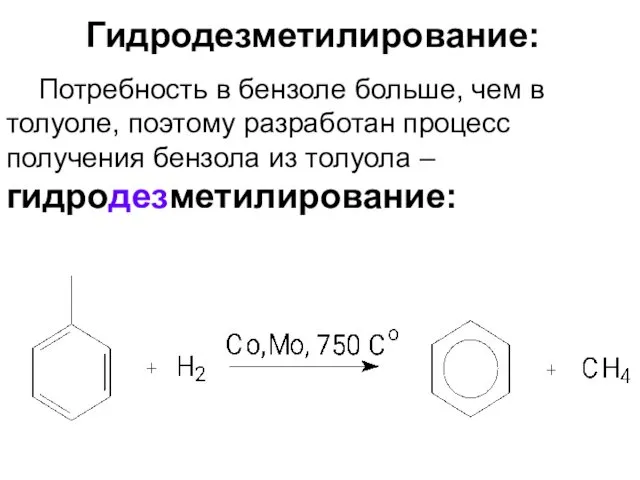
- 15. Гидродезметилирование: Потребность в бензоле больше, чем в толуоле, поэтому разработан процесс получения бензола из толуола –
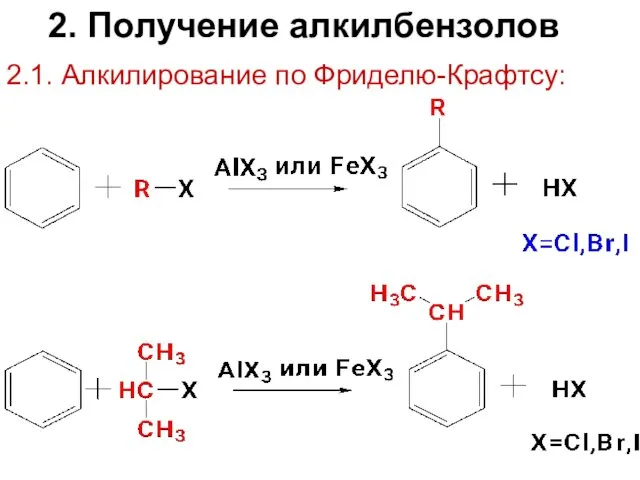
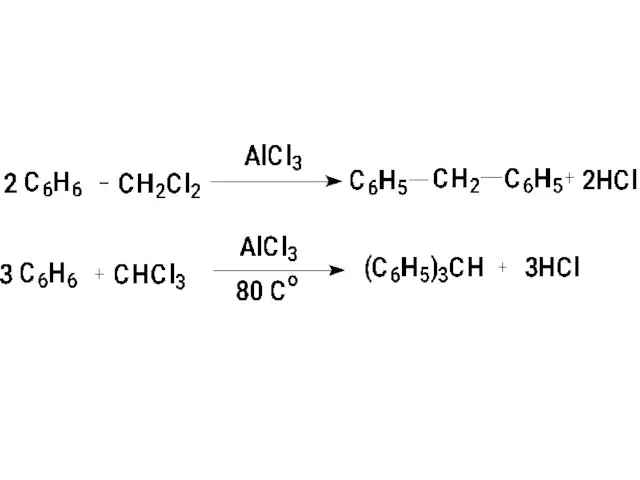
- 16. 2. Получение алкилбензолов 2.1. Алкилирование по Фриделю-Крафтсу:
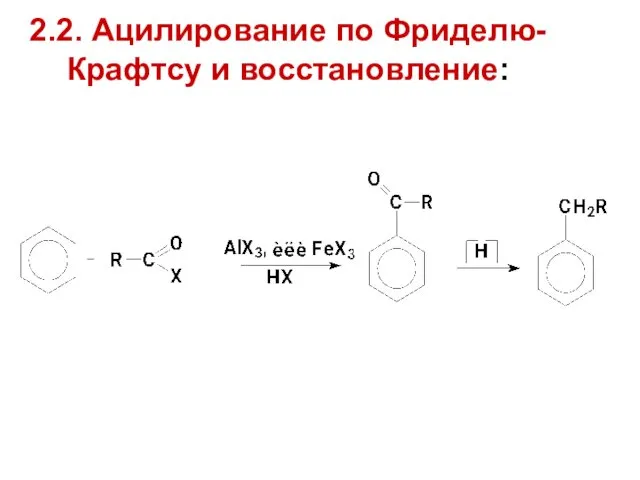
- 18. 2.2. Ацилирование по Фриделю-Крафтсу и восстановление:
- 19. ХИМИЧЕСКИЕ СВОЙСТВА Для аренов характерны: Реакции электрофильного замещения (SЕ). Реакции бензола с нарушением ароматической системы. Реакции
- 20. У аренов высокая степень ненасыщенности, но для аренов не характерны реакции присоединения, свойственные алкенам и алкинам.
- 21. Реакции галогенирования, нитрования и сульфирования осуществляются почти со всеми ароматическими соединениями, алкилирования и ацилирования – только
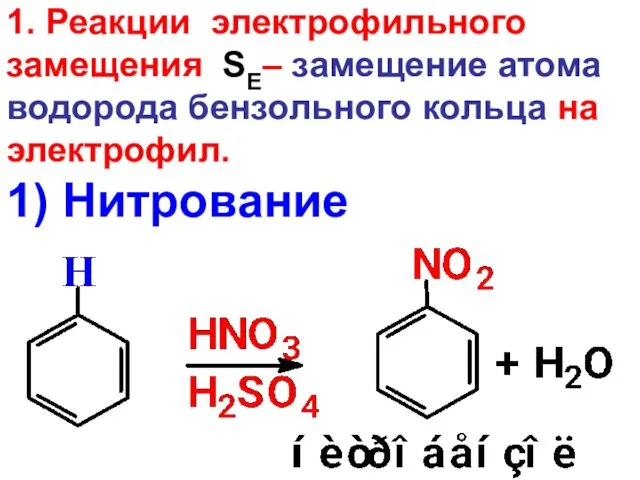
- 22. 1. Реакции электрофильного замещения SE– замещение атома водорода бензольного кольца на электрофил. 1) Нитрование
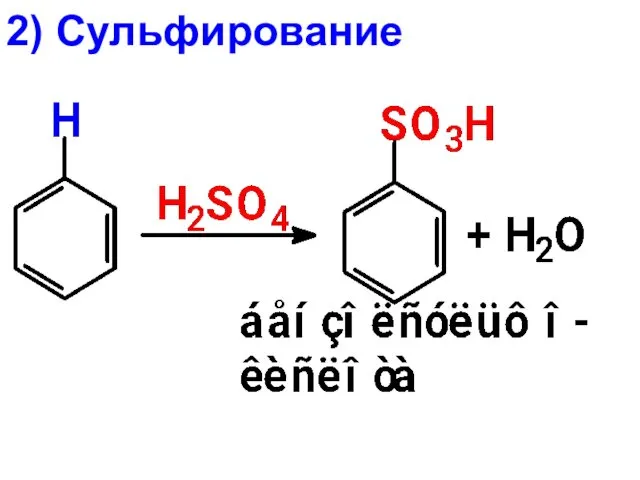
- 23. 2) Сульфирование
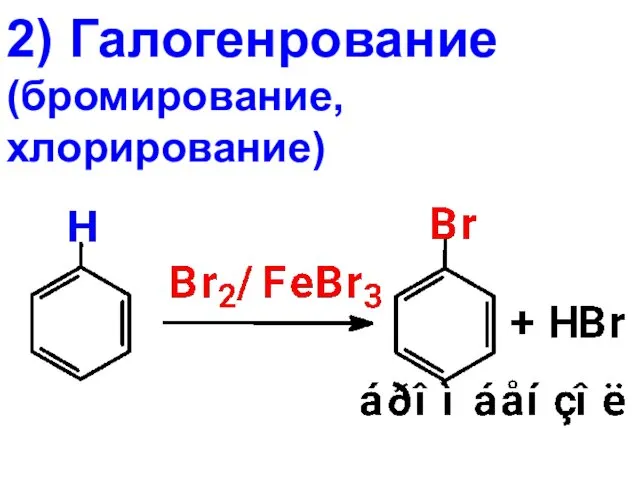
- 24. 2) Галогенрование (бромирование, хлорирование)
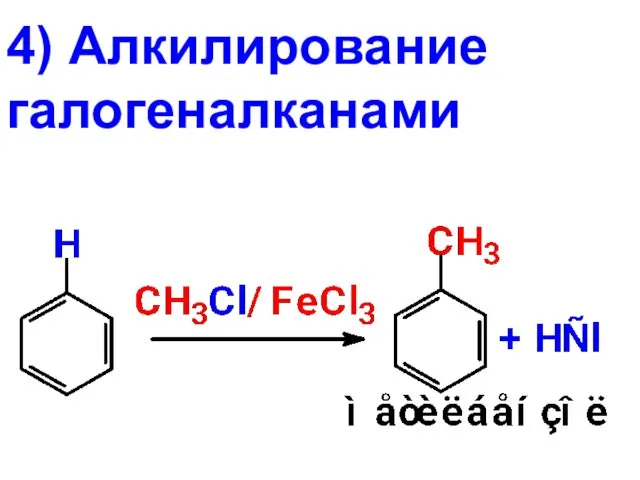
- 25. 4) Алкилирование галогеналканами
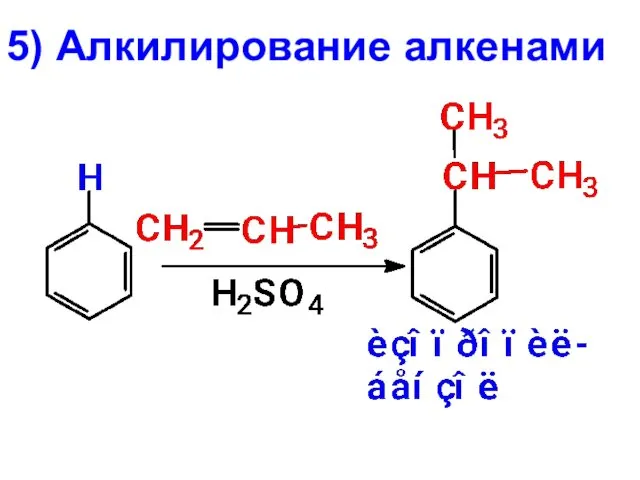
- 26. 5) Алкилирование алкенами
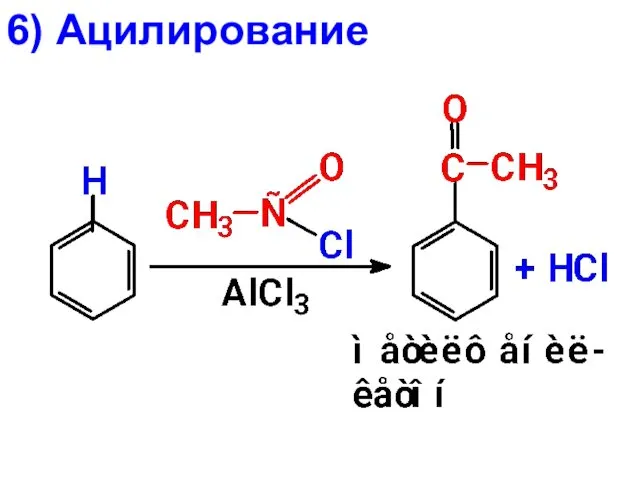
- 27. 6) Ацилирование
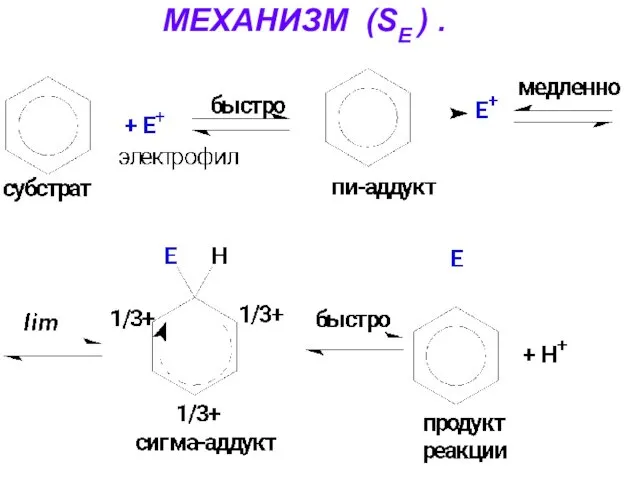
- 28. МЕХАНИЗМ РЕАКЦИЙ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ (SЕ). ( См. Учебник. С. 195-199). Стадии реакции: 1. Активация реагента 2.
- 29. МЕХАНИЗМ (SЕ ) .
- 30. ЗАМЕСТИТЕЛИ БЕНЗОЛЬНОГО КОЛЬЦА И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И НАПРАВЛЕНИЕ SЕ-реакций ( См. Учебник. С. 199-206).
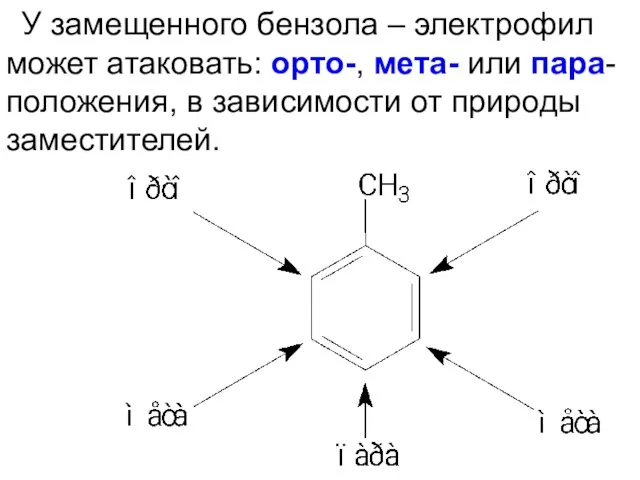
- 31. У замещенного бензола – электрофил может атаковать: орто-, мета- или пара-положения, в зависимости от природы заместителей.
- 33. При рассмотрении таких реакций надо решить два важных вопроса: 1) Какие изомеры преимущественно образуются в результате
- 34. Правила ориентации в монозамещенных аренах По влиянию на ориентацию в SE реакциях все заместители делятся, на:
- 35. Ориентирующее влияние заместителей обусловлено их электронными эффектами (статический фактор) и стабильностью σ-аддуктов, т.е. промежуточно образующихся аренониевых
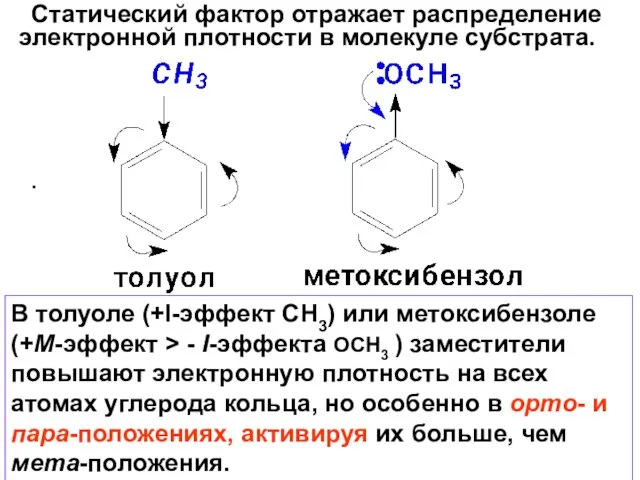
- 36. Статический фактор отражает распределение электронной плотности в молекуле субстрата. . В толуоле (+I-эффект СН3) или метоксибензоле
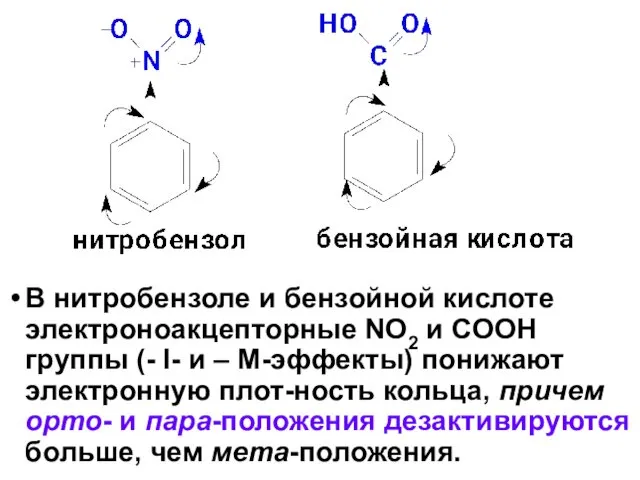
- 37. В нитробензоле и бензойной кислоте электроноакцепторные NO2 и COOH группы (- I- и – М-эффекты) понижают
- 38. Динамический фактор, то есть стабилизирующее или дестабилизирующее влияние заместителя на образующиеся в ходе реакции аренониевые ионы,
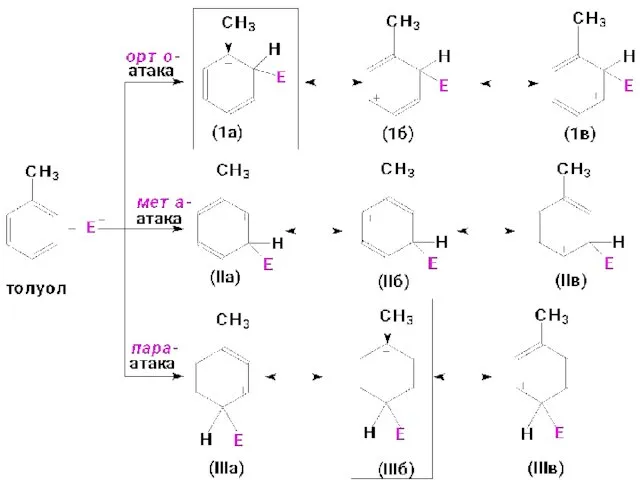
- 39. Граничные структуры σ-аддукта, вносящие вклад в его стабилизацию на примере толуола: В структурах (1а) и (IIIб)
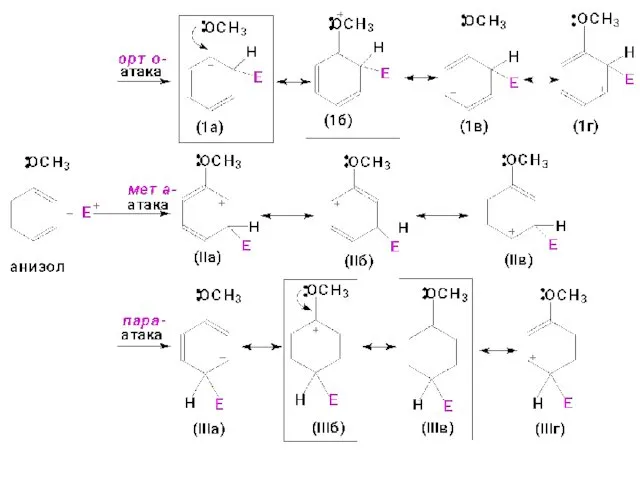
- 41. В анизоле (метоксибензоле) интермедиаты, образующиеся при атаке в орто- и пара – положения, стабилизированы больше
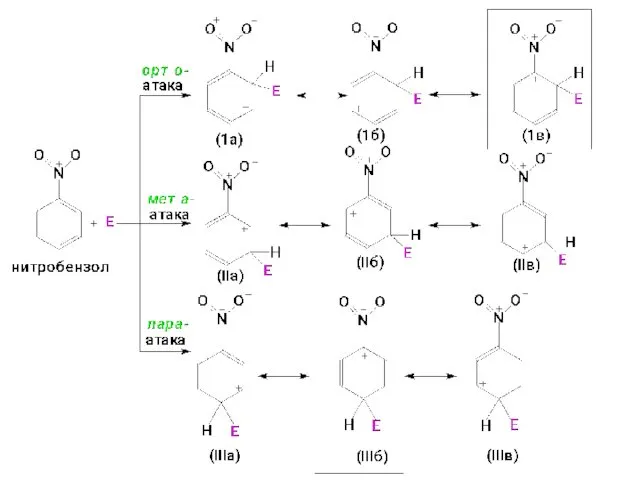
- 43. ЭА заместители дестабилизируют все три возможных σ-аддукта, но σ-аддукт, возникающий при атаке в мета-положение, дестабилизирован меньше.
- 45. По влиянию статических и динамических факторов на реакционную способность и ориентацию в реакциях электрофильного замещения все
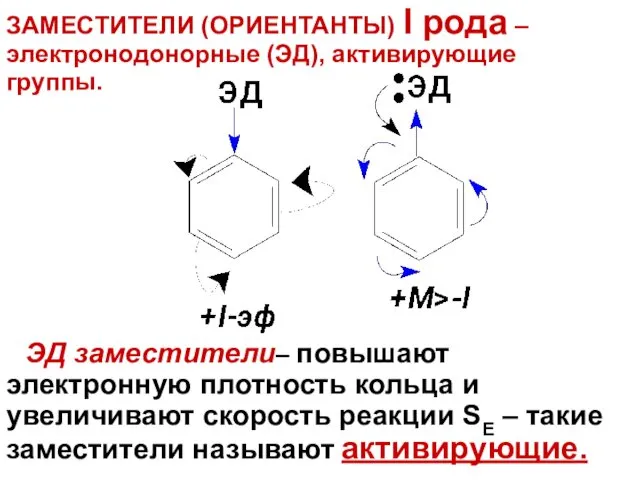
- 46. ЗАМЕСТИТЕЛИ (ОРИЕНТАНТЫ) I рода – электронодонорные (ЭД), активирующие группы. ЭД заместители– повышают электронную плотность кольца и
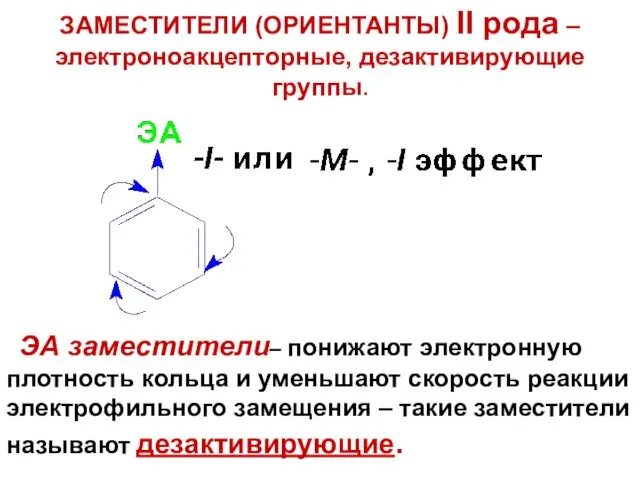
- 47. ЗАМЕСТИТЕЛИ (ОРИЕНТАНТЫ) II рода – электроноакцепторные, дезактивирующие группы. ЭА заместители– понижают электронную плотность кольца и уменьшают
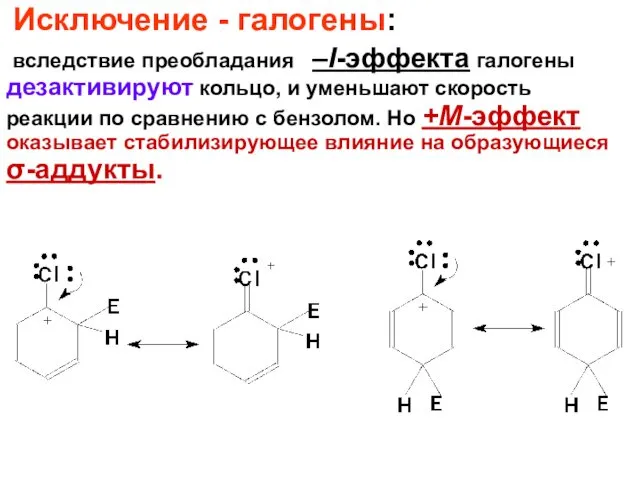
- 48. Исключение - галогены: вследствие преобладания –I-эффекта галогены дезактивируют кольцо, и уменьшают скорость реакции по сравнению с
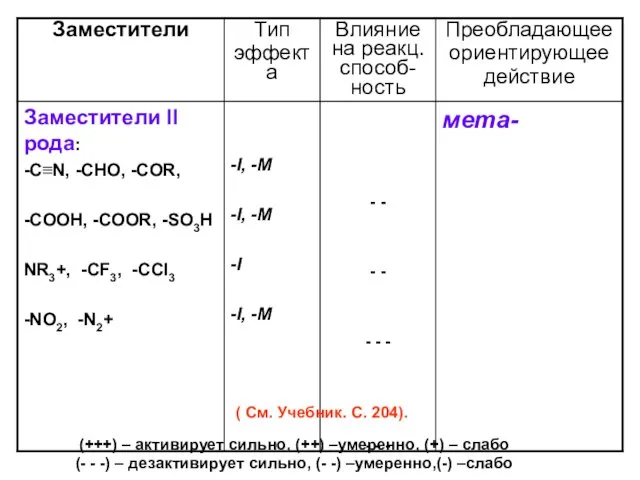
- 49. ВЛИЯНИЕ ЗАМЕСТИТЕЛЕЙ В БЕНЗОЛЬНОМ ЯДРЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ И ОРИЕНТАЦИЮ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ
- 50. (+++) – активирует сильно, (++) –умеренно, (+) – слабо (- - -) – дезактивирует сильно, (-
- 51. Правила ориентации позволяют предсказать преимущественное направление реакции и преобладание того или иного изомера в продуктах реакции.
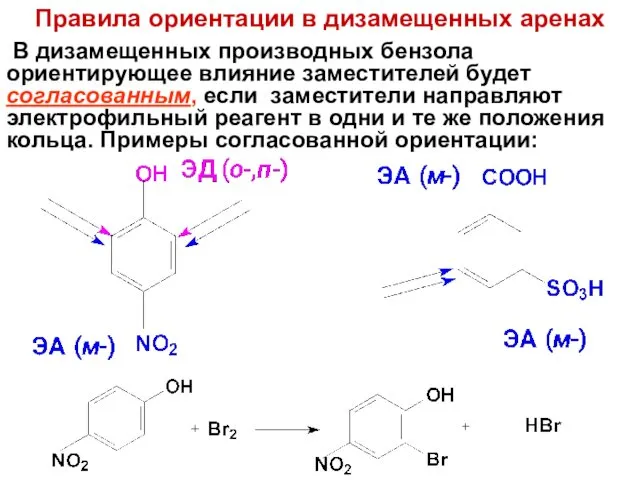
- 52. Правила ориентации в дизамещенных аренах В дизамещенных производных бензола ориентирующее влияние заместителей будет согласованным, если заместители
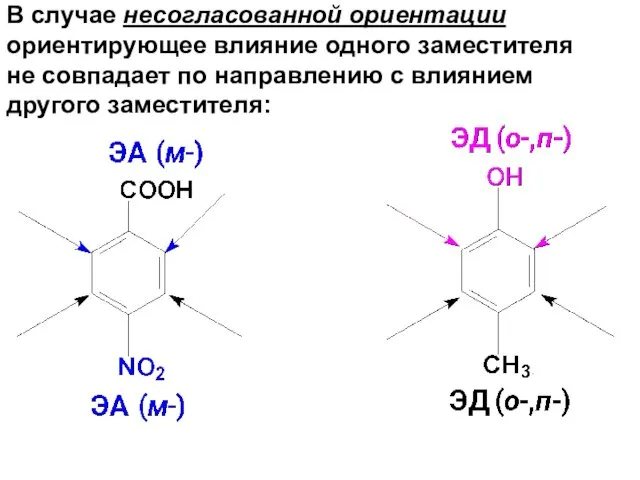
- 53. В случае несогласованной ориентации ориентирующее влияние одного заместителя не совпадает по направлению с влиянием другого заместителя:
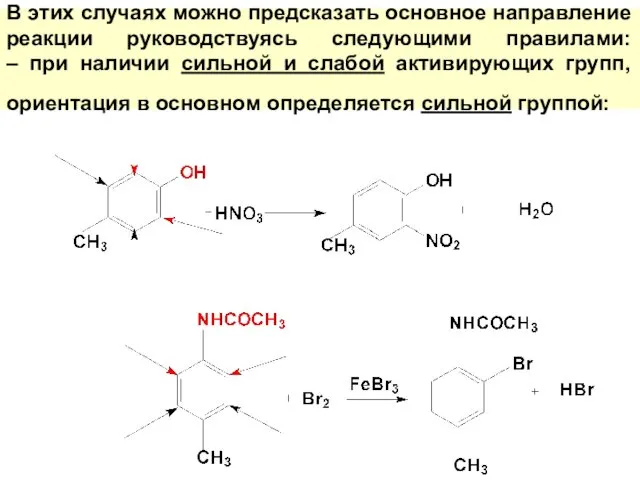
- 54. В этих случаях можно предсказать основное направление реакции руководствуясь следующими правилами: – при наличии сильной и
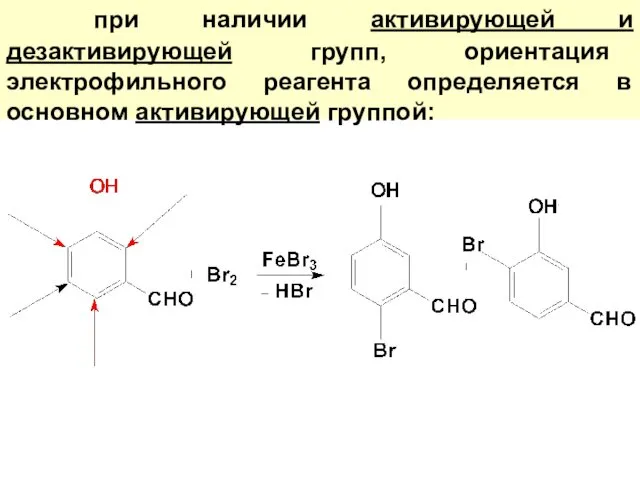
- 55. при наличии активирующей и дезактивирующей групп, ориентация электрофильного реагента определяется в основном активирующей группой:
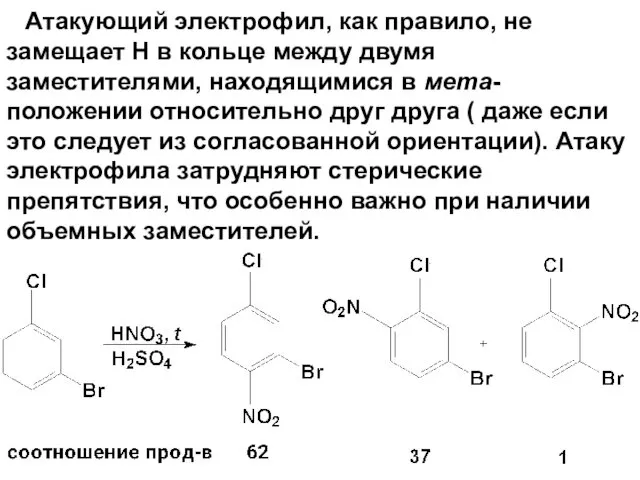
- 56. Атакующий электрофил, как правило, не замещает Н в кольце между двумя заместителями, находящимися в мета-положении относительно
- 57. Важнейшие реакции SE 1.1. Галогенирование. Бензол реагирует с Cl2 и Br2 в присутствии kаt – кислот
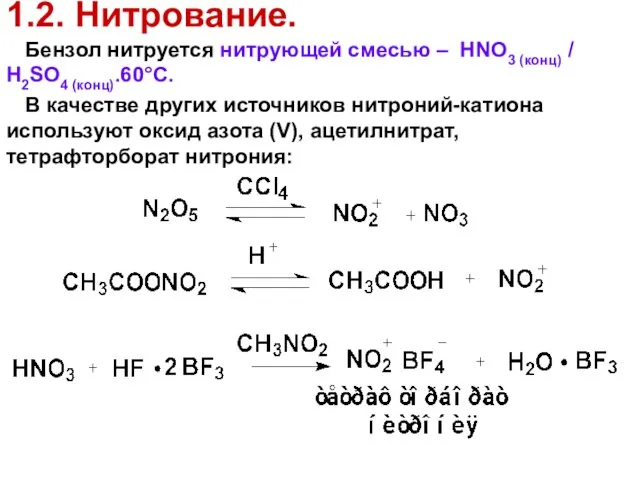
- 58. 1.2. Нитрование. Бензол нитруется нитрующей смесью – HNO3 (конц) / H2SO4 (конц).60°С. В качестве других источников
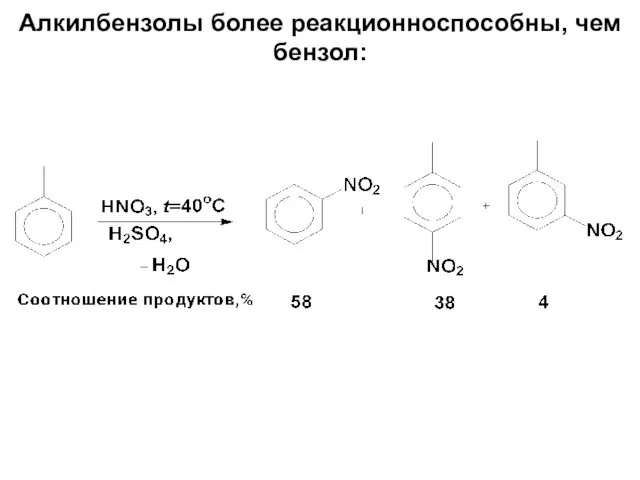
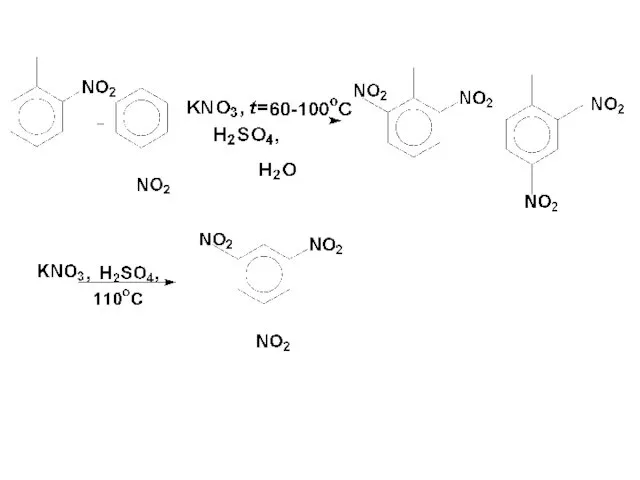
- 59. Алкилбензолы более реакционноспособны, чем бензол:
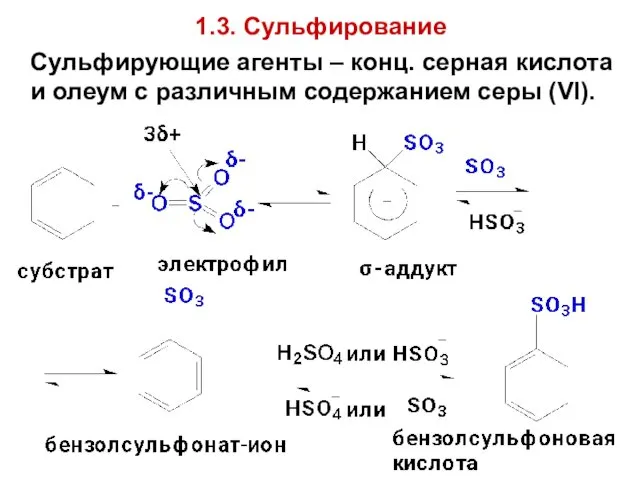
- 61. 1.3. Сульфирование Сульфирующие агенты – конц. серная кислота и олеум с различным содержанием серы (VI).
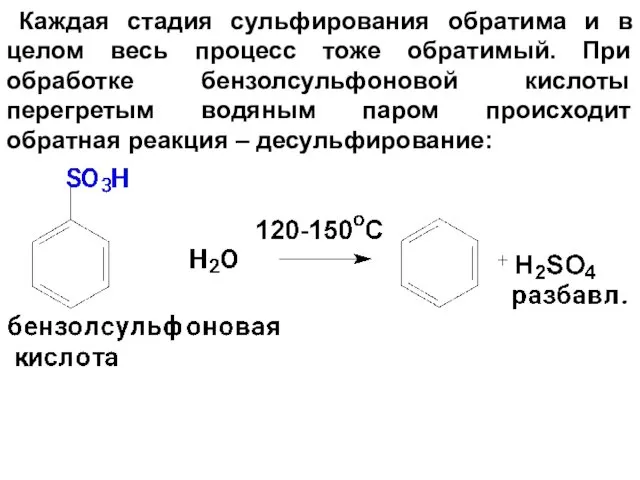
- 62. Каждая стадия сульфирования обратима и в целом весь процесс тоже обратимый. При обработке бензолсульфоновой кислоты перегретым
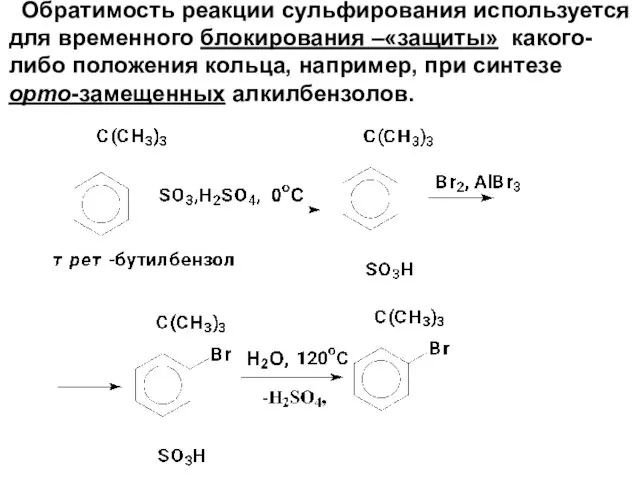
- 63. Обратимость реакции сульфирования используется для временного блокирования –«защиты» какого-либо положения кольца, например, при синтезе орто-замещенных алкилбензолов.
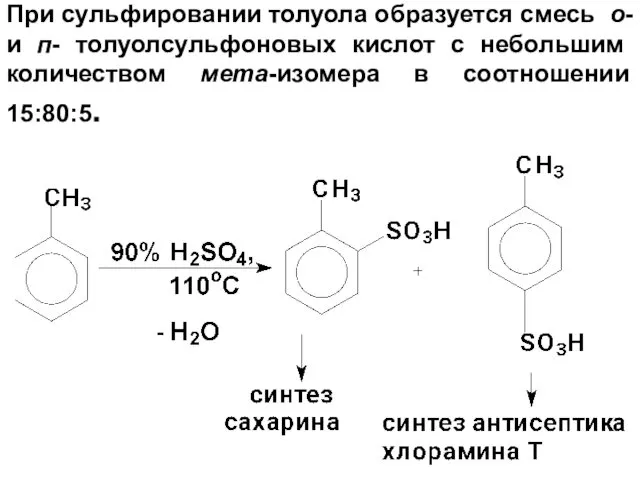
- 64. При сульфировании толуола образуется смесь о- и п- толуолсульфоновых кислот с небольшим количеством мета-изомера в соотношении
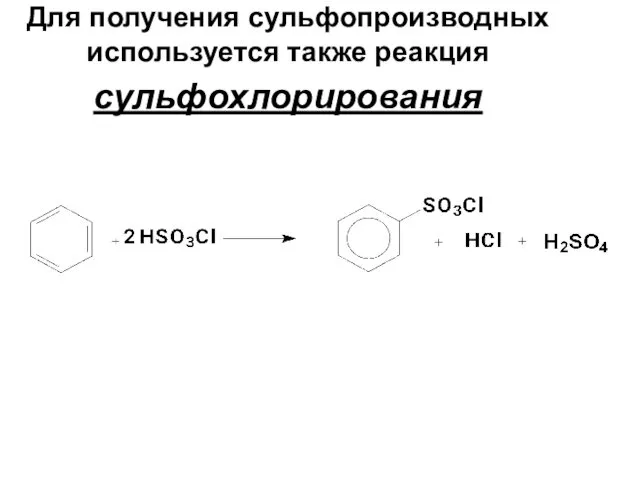
- 65. Для получения сульфопроизводных используется также реакция сульфохлорирования
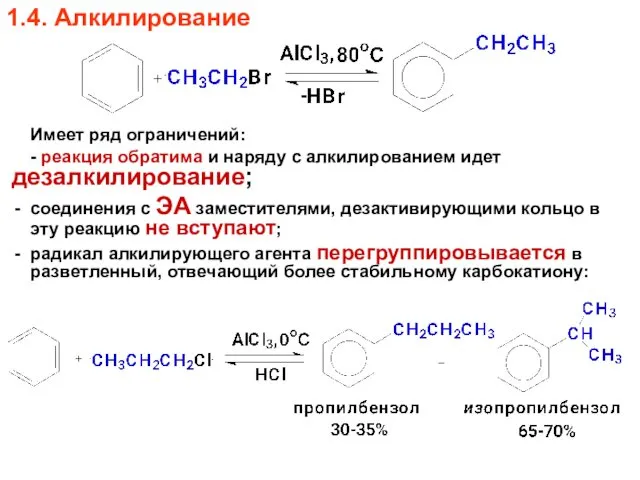
- 66. 1.4. Алкилирование Имеет ряд ограничений: - реакция обратима и наряду с алкилированием идет дезалкилирование; соединения с
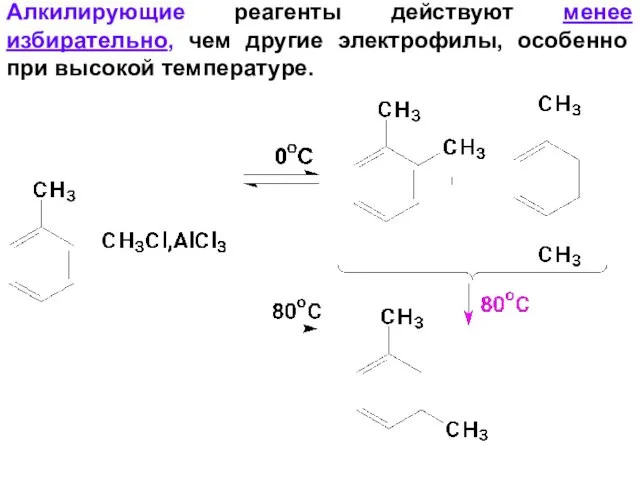
- 67. Алкилирующие реагенты действуют менее избирательно, чем другие электрофилы, особенно при высокой температуре.
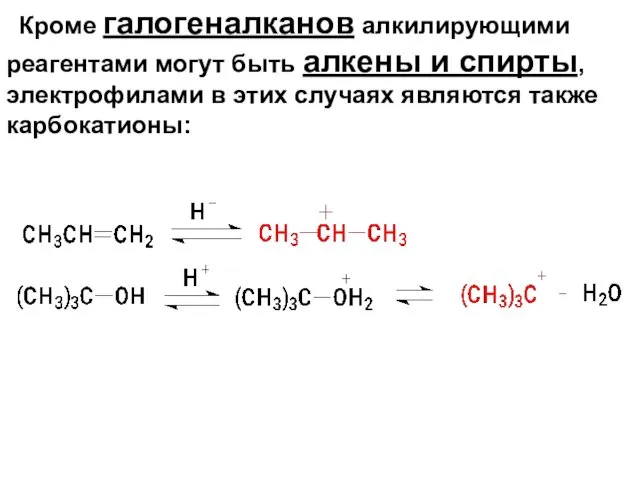
- 68. Кроме галогеналканов алкилирующими реагентами могут быть алкены и спирты, электрофилами в этих случаях являются также карбокатионы:
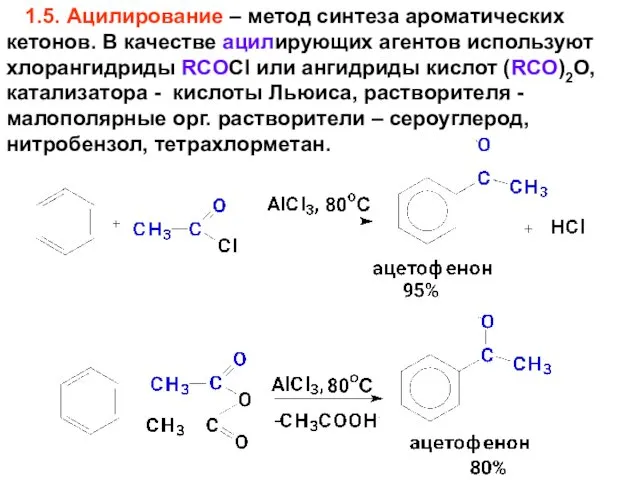
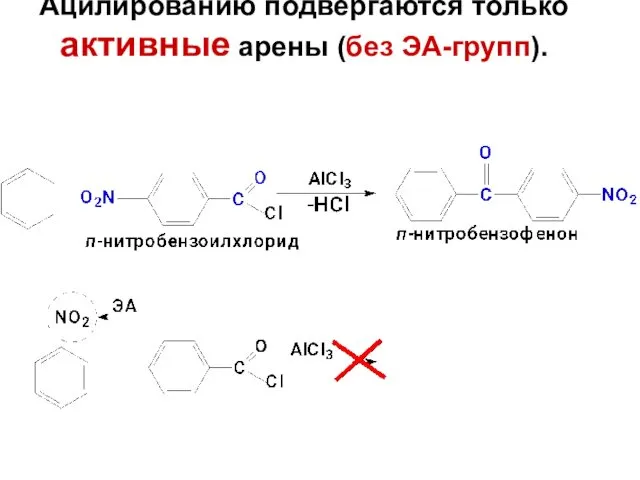
- 69. 1.5. Ацилирование – метод синтеза ароматических кетонов. В качестве ацилирующих агентов используют хлорангидриды RCOCl или ангидриды
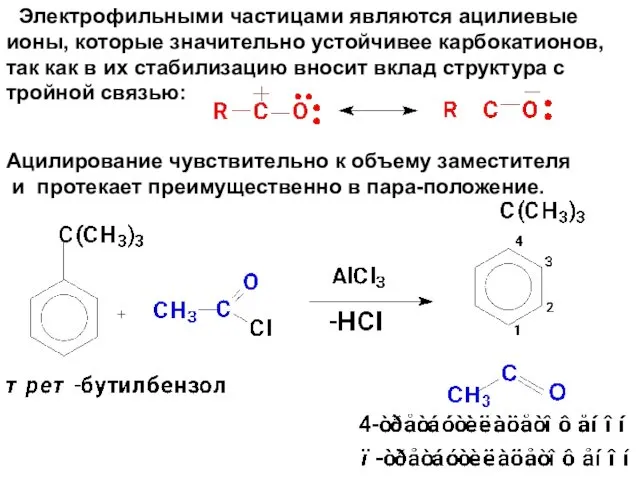
- 70. Электрофильными частицами являются ацилиевые ионы, которые значительно устойчивее карбокатионов, так как в их стабилизацию вносит вклад
- 71. Ацилированию подвергаются только активные арены (без ЭА-групп).
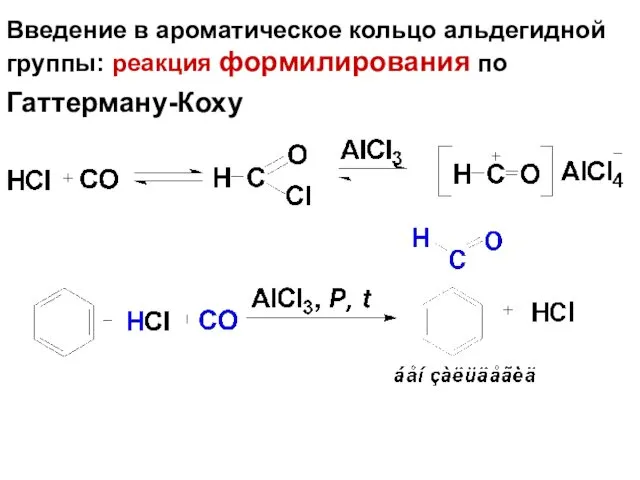
- 72. Введение в ароматическое кольцо альдегидной группы: реакция формилирования по Гаттерману-Коху
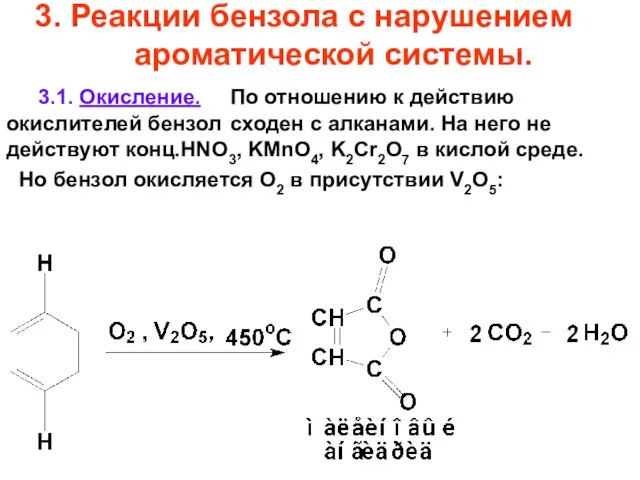
- 73. 3. Реакции бензола с нарушением ароматической системы. 3.1. Окисление. По отношению к действию окислителей бензол сходен
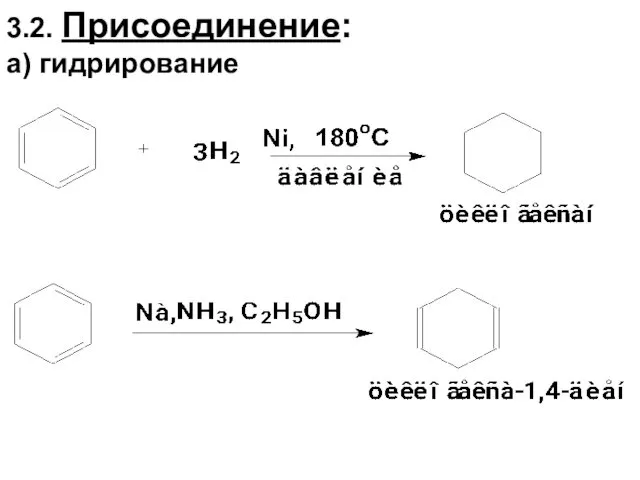
- 74. 3.2. Присоединение: а) гидрирование
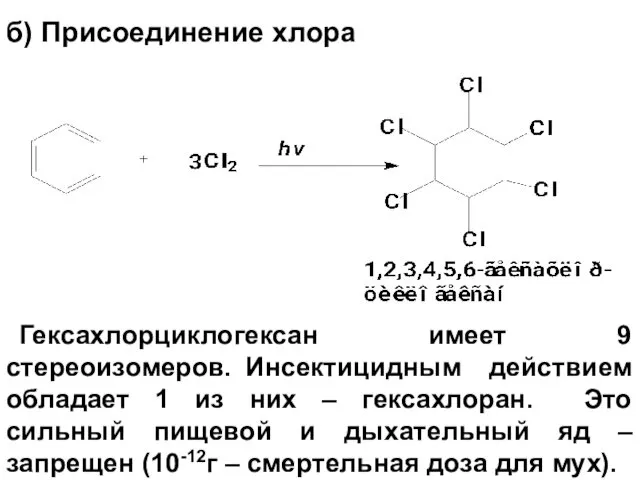
- 75. б) Присоединение хлора Гексахлорциклогексан имеет 9 стереоизомеров. Инсектицидным действием обладает 1 из них – гексахлоран. Это
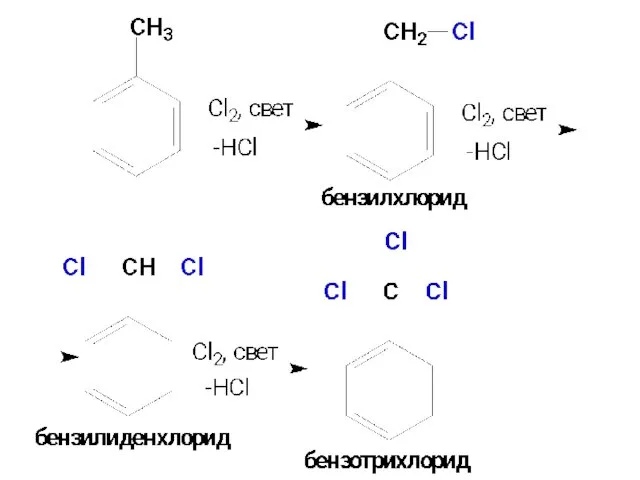
- 76. 3.3. Реакции боковых цепей в алкилбензолах а) Галогенирование.Алкилбензолы вступают в реакции радикального хлорирования и бромирования боковой
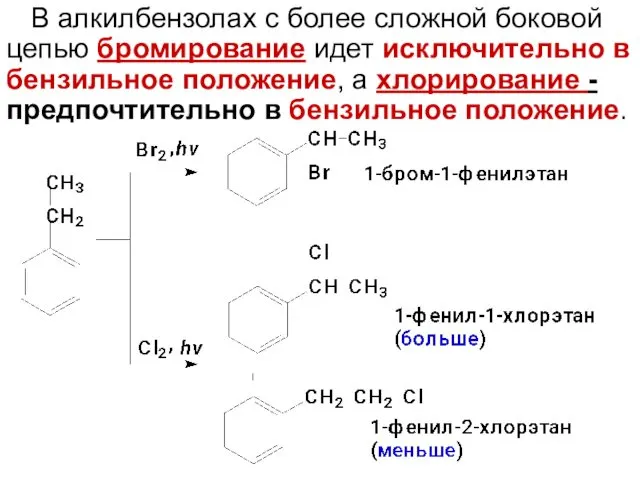
- 78. В алкилбензолах с более сложной боковой цепью бромирование идет исключительно в бензильное положение, а хлорирование -
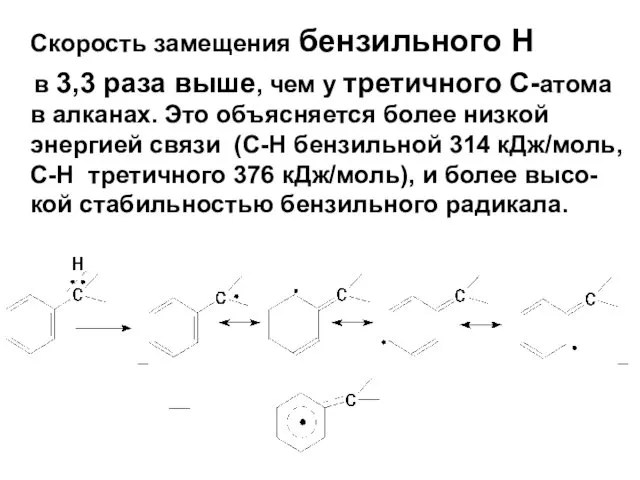
- 79. Скорость замещения бензильного Н в 3,3 раза выше, чем у третичного С-атома в алканах. Это объясняется
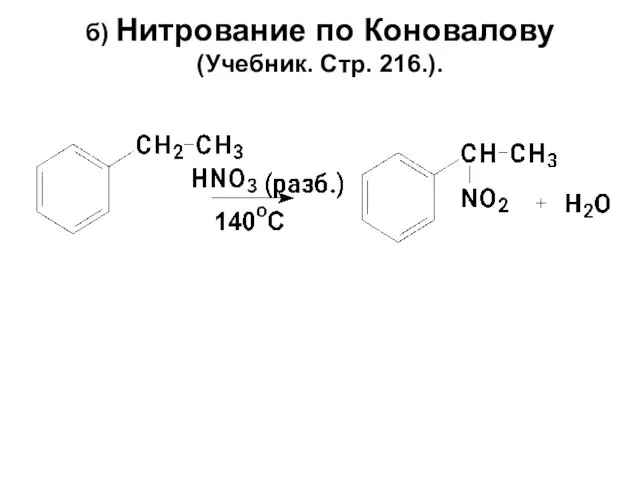
- 80. б) Нитрование по Коновалову (Учебник. Стр. 216.).
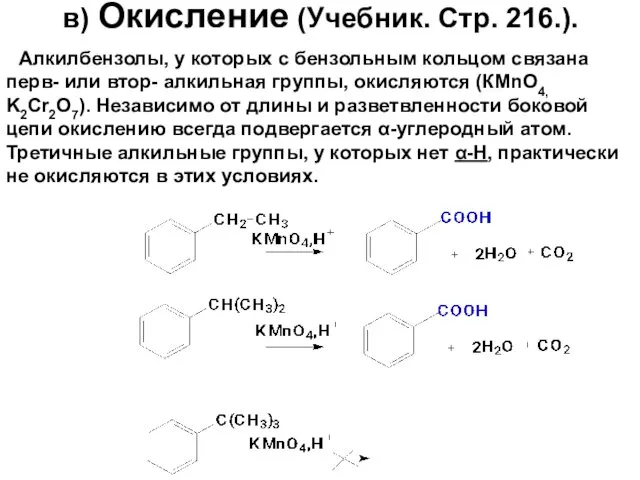
- 81. в) Окисление (Учебник. Стр. 216.). Алкилбензолы, у которых с бензольным кольцом связана перв- или втор- алкильная
- 83. Скачать презентацию






















 Гражданское право. Договор поставки
Гражданское право. Договор поставки Текстовые процессоры и текстовые редакторы
Текстовые процессоры и текстовые редакторы Презентация Африка
Презентация Африка Әлемдік діндер мәдениеті: буддизм, християндық исламдық
Әлемдік діндер мәдениеті: буддизм, християндық исламдық Системы счисления. Основные понятия систем счисления
Системы счисления. Основные понятия систем счисления Царство Грибы. Общая характеристика грибов
Царство Грибы. Общая характеристика грибов Коронавирус COVID-19
Коронавирус COVID-19 Представление технологии Диск
Представление технологии Диск Патофизиология красной крови
Патофизиология красной крови Из опыта работы по формированию у дошкольников представлений о правилах дорожного движения (презентация)
Из опыта работы по формированию у дошкольников представлений о правилах дорожного движения (презентация) Что такое доброта?
Что такое доброта? Автоматизация звука Ш. Артикуляционная гимнастика
Автоматизация звука Ш. Артикуляционная гимнастика Программа оценки навыков речи и социального взаимодействия для детей с аутизмом и другими нарушениями VB-MAPP
Программа оценки навыков речи и социального взаимодействия для детей с аутизмом и другими нарушениями VB-MAPP Влияние сотовых телефонов на здоровье человека
Влияние сотовых телефонов на здоровье человека Уинстон Леонард Спенсер Черчилль
Уинстон Леонард Спенсер Черчилль Безопасное поведение детей в сети
Безопасное поведение детей в сети Логический квадрат. Ложные, истинные и неопределенные суждения
Логический квадрат. Ложные, истинные и неопределенные суждения 2615Імунофлуорисцентний експрес аналізатор LS-1100
2615Імунофлуорисцентний експрес аналізатор LS-1100 Явление паразитизма
Явление паразитизма Музыкальная композиция
Музыкальная композиция Проектирование водопроводной насосной станции II подъема
Проектирование водопроводной насосной станции II подъема Доколе я в мире, я свет миру
Доколе я в мире, я свет миру Алгоритм ветвления. Условный оператор
Алгоритм ветвления. Условный оператор Электронное портфолио по предмету Окружающий мир
Электронное портфолио по предмету Окружающий мир презентация проекта по ПДД Нам на улице не страшно
презентация проекта по ПДД Нам на улице не страшно Школьный спортивный клуб Спасатель
Школьный спортивный клуб Спасатель My favorite paintings
My favorite paintings Родительское собрание Подготовка ребёнка ко 2 классу
Родительское собрание Подготовка ребёнка ко 2 классу