Содержание
- 2. Тема урока: Гомологи бензола. Толуол. Стирол.
- 3. Цель урока: Продолжить формирование понятий об ароматических углеводородах через: гомологический ряд и номенклатуру моноциклических аренов строение
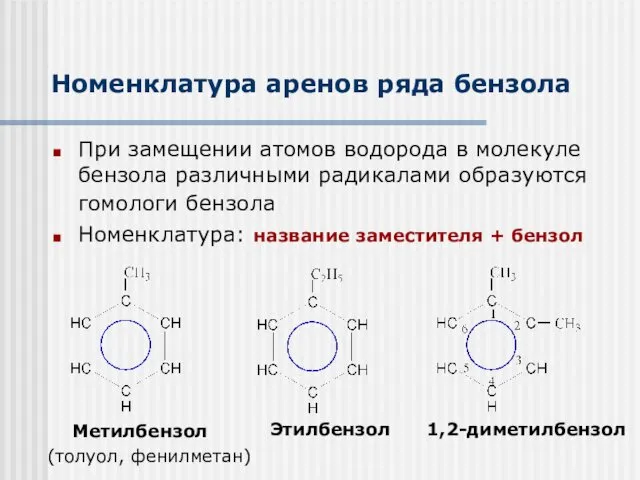
- 4. Номенклатура аренов ряда бензола При замещении атомов водорода в молекуле бензола различными радикалами образуются гомологи бензола
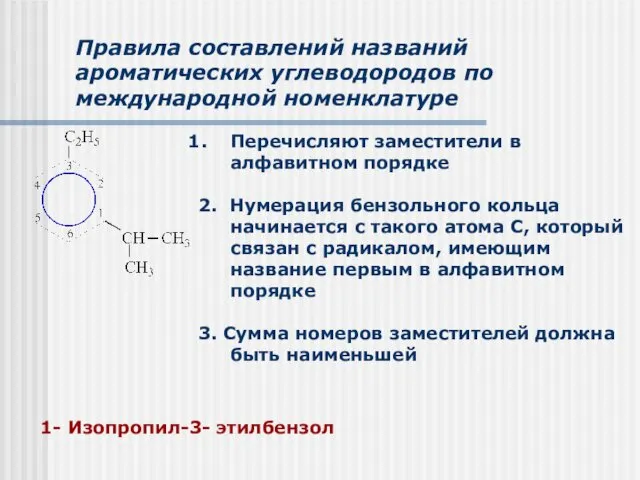
- 5. Правила составлений названий ароматических углеводородов по международной номенклатуре Перечисляют заместители в алфавитном порядке 2. Нумерация бензольного
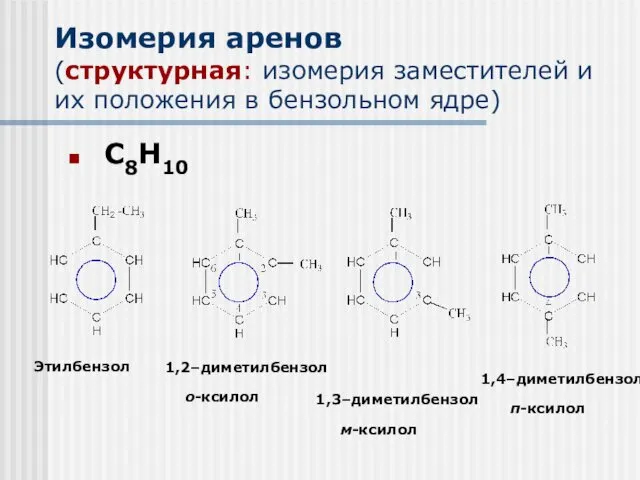
- 6. Изомерия аренов (структурная: изомерия заместителей и их положения в бензольном ядре) С8Н10 Этилбензол 1,2–диметилбензол о-ксилол 1,3–диметилбензол
- 7. Физические свойства толуола При обычных условиях-бесцветная жидкость с характерным запахом, температурой кип. 111 °С , не
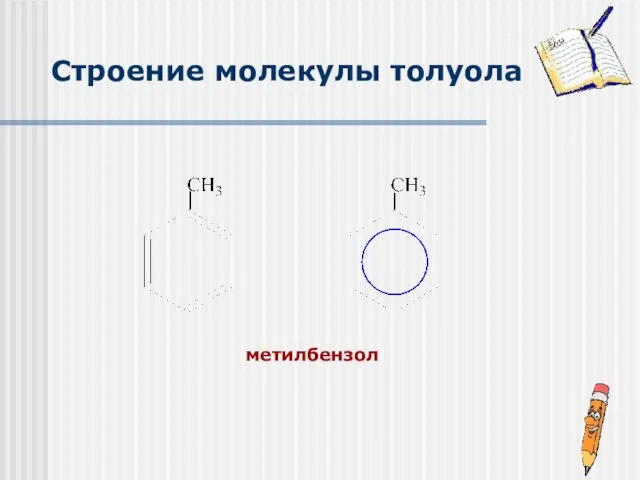
- 8. метилбензол Строение молекулы толуола
- 9. Химические свойства толуола Ароматическая связь бензольного кольца и метильная группа взаимно влияют друг на друга и
- 10. Взаимное влияние атомов в молекуле толуола Метилбензол вступает во все реакции замещения, в которых участвует бензол,
- 11. Правило ориентации в бензольном кольце Заместители I рода – электронодоноры (-OH, NH2, -R, Hal), находясь в
- 12. Правило ориентации в бензольном кольце Заместители II-рода (электроноакцепторы: -SО3Н, -NO2 , -СН=О, -СООН) оттягивают электроны от
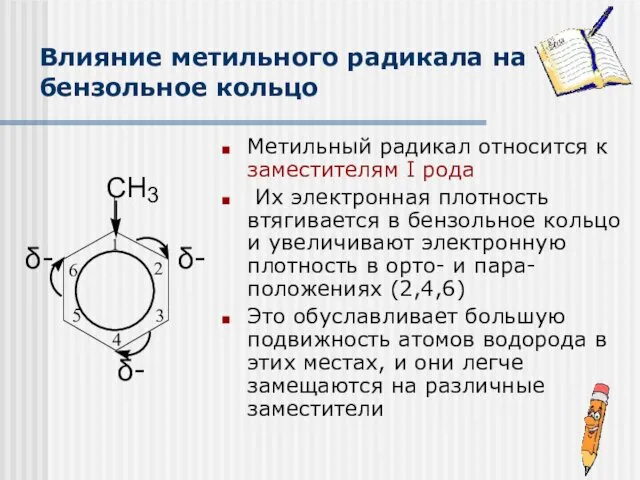
- 13. Влияние метильного радикала на бензольное кольцо Метильный радикал относится к заместителям I рода Их электронная плотность
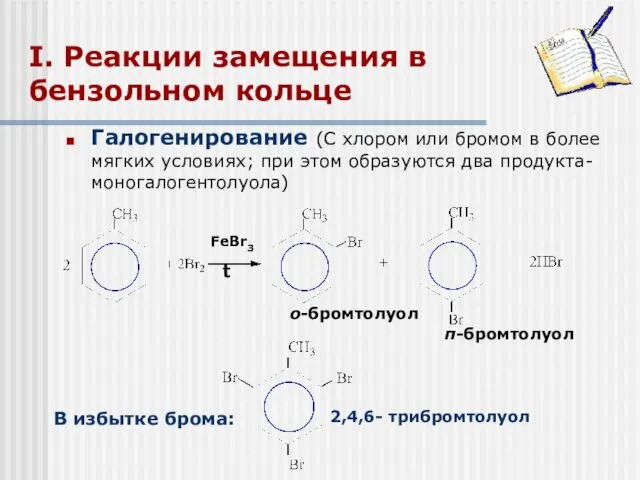
- 14. FeBr3 t о-бромтолуол I. Реакции замещения в бензольном кольце 2,4,6- трибромтолуол п-бромтолуол Галогенирование (С хлором или
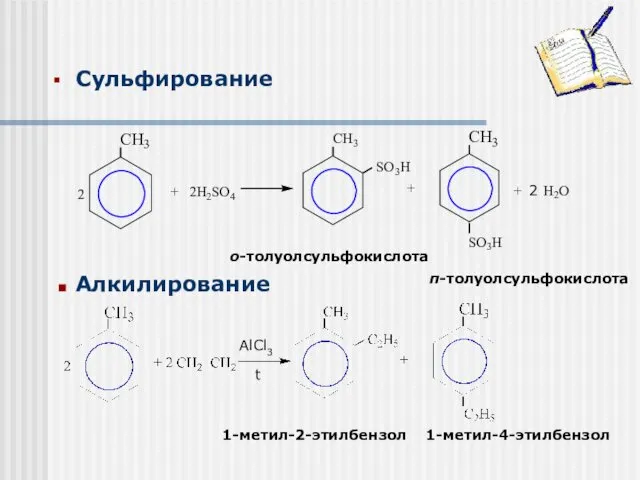
- 15. Алкилирование Сульфирование о-толуолсульфокислота
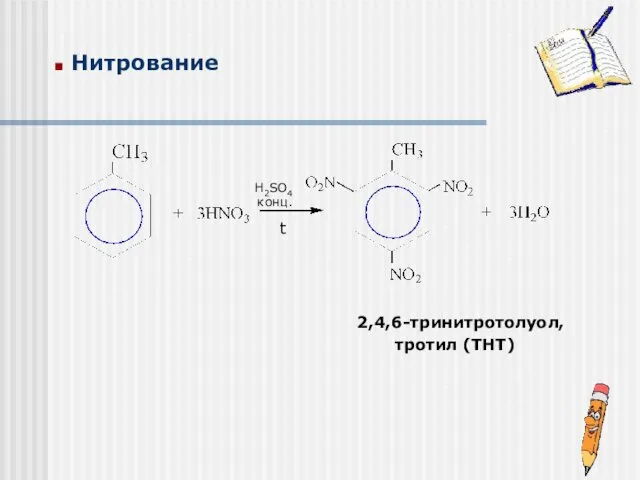
- 16. Нитрование
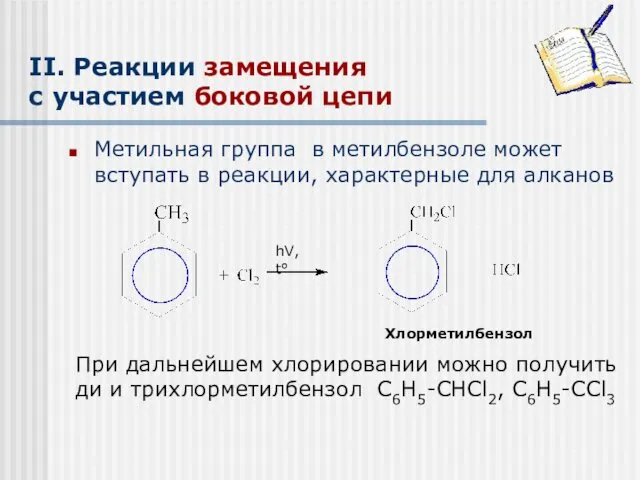
- 17. II. Реакции замещения с участием боковой цепи Метильная группа в метилбензоле может вступать в реакции, характерные
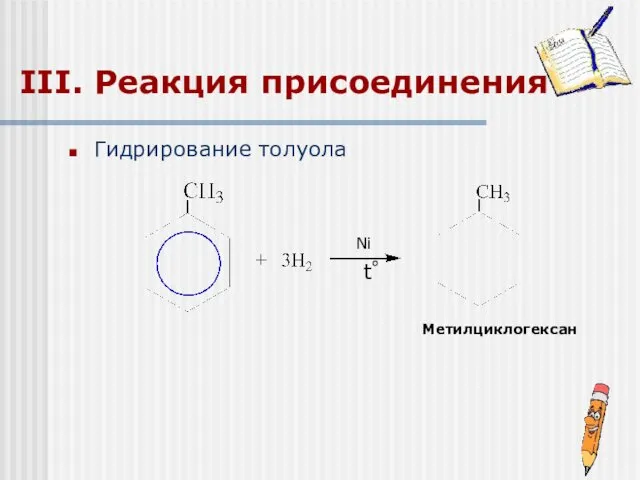
- 18. III. Реакция присоединения Гидрирование толуола
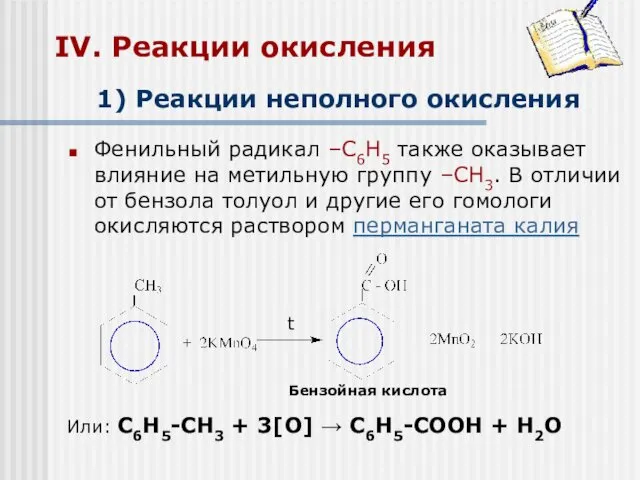
- 19. IV. Реакции окисления Фенильный радикал –С6Н5 также оказывает влияние на метильную группу –СН3. В отличии от
- 20. Взаимодействие толуола с перманганатом калия
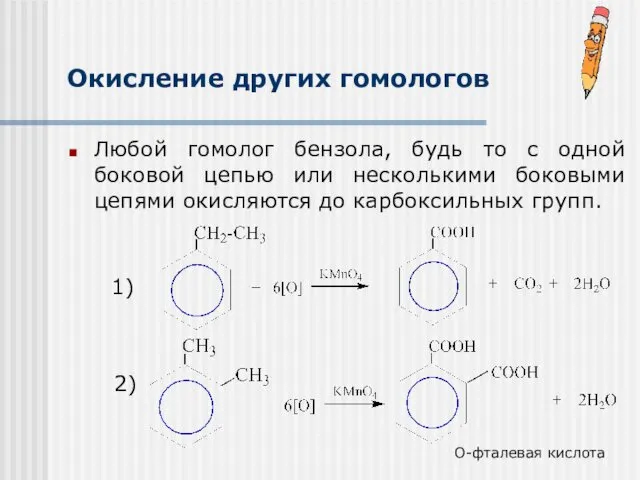
- 21. Окисление других гомологов Любой гомолог бензола, будь то с одной боковой цепью или несколькими боковыми цепями
- 22. 2) Реакции полного окисления C6H5-CH3 + 9O2 → 7CO2 + 4H2O Горение толуола в кислороде (на
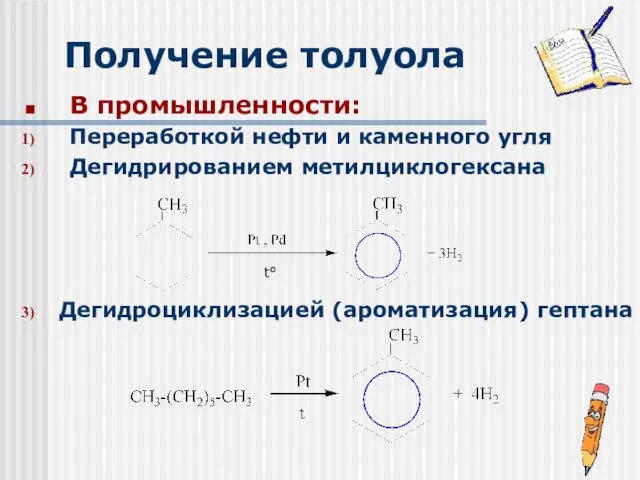
- 23. Получение толуола В промышленности: Переработкой нефти и каменного угля Дегидрированием метилциклогексана Дегидроциклизацией (ароматизация) гептана
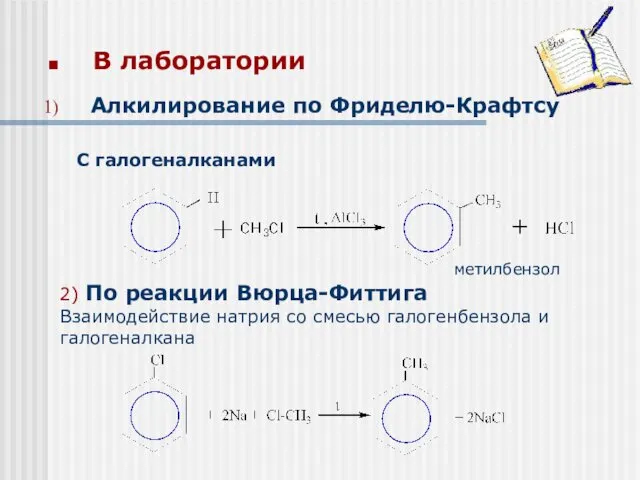
- 24. В лаборатории С галогеналканами метилбензол 2) По реакции Вюрца-Фиттига Взаимодействие натрия со смесью галогенбензола и галогеналкана
- 25. Применение толуола и его производных Толуол и его производные – важнейшее сырьё для химической промышленности В
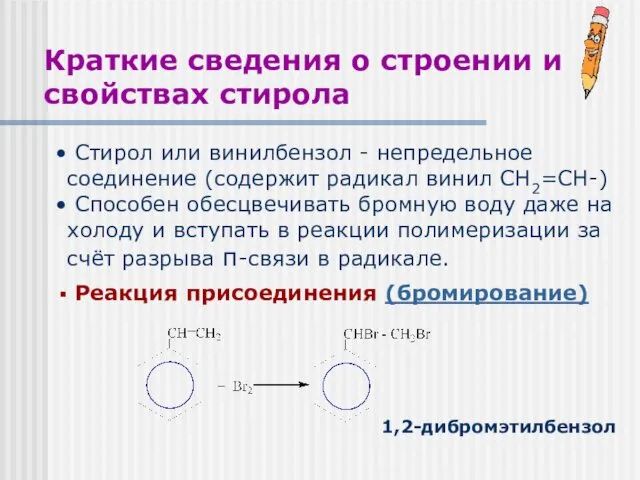
- 26. Краткие сведения о строении и свойствах стирола Стирол или винилбензол - непредельное соединение (содержит радикал винил
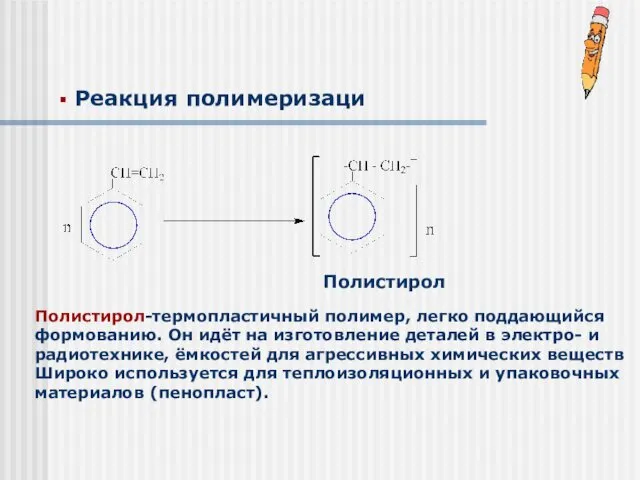
- 27. Реакция полимеризаци Полистирол Полистирол-термопластичный полимер, легко поддающийся формованию. Он идёт на изготовление деталей в электро- и
- 28. Вопросы для самоконтроля Приведите примеры реакций замещения с участием толуола. Объясните причины различий реакционной способности толуола
- 29. Приведите примеры реакций присоединения с участием толуола. Объясните, почему KMnO4 реагирует с толуолом, но не реагирует
- 30. Упражнения и задачи для самостоятельной работы Назовите следующие соединения: Ответы: а) 1-метил-4-пропилбензол (п-пропилтолуол) б) 1-бром-2-метилбензол (0-бромтолуол)
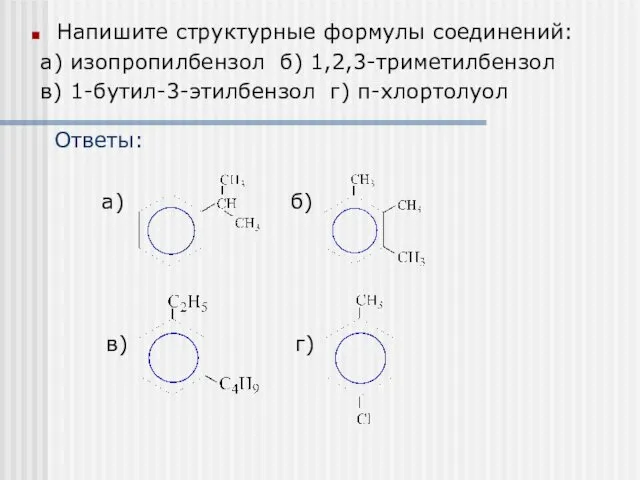
- 31. Напишите структурные формулы соединений: а) изопропилбензол б) 1,2,3-триметилбензол в) 1-бутил-3-этилбензол г) п-хлортолуол Ответы:
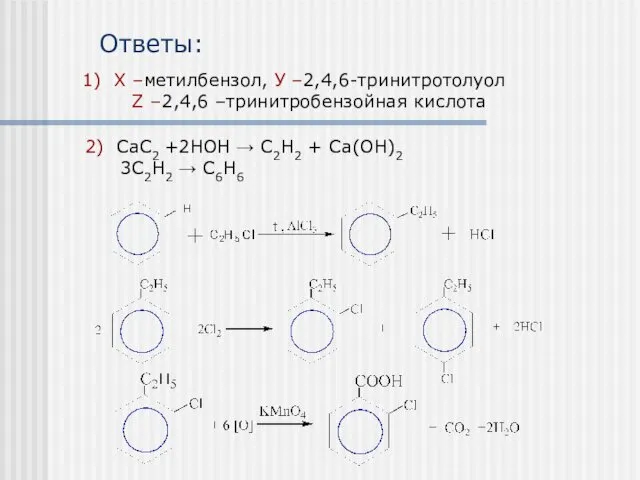
- 32. Напишите уравнения реакций следующих превращений
- 33. 2) СаС2 +2НОН → С2Н2 + Са(ОН)2 3С2Н2 → С6Н6 Ответы: 1) Х –метилбензол, У –2,4,6-тринитротолуол
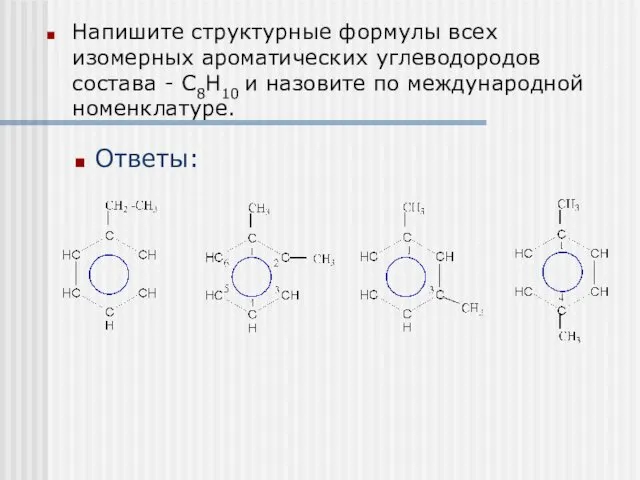
- 34. Напишите структурные формулы всех изомерных ароматических углеводородов состава - С8Н10 и назовите по международной номенклатуре. Ответы:
- 35. Задачи: При сжигании 2,12 г вещества выделилось 7,04 г оксида углерода (IV) и 1,80 г воды.
- 37. Скачать презентацию















 Перенаселение
Перенаселение Медико-социальные аспекты демографии
Медико-социальные аспекты демографии Проектная и исследовательская деятельность по технологии в рамках ФГОС
Проектная и исследовательская деятельность по технологии в рамках ФГОС презентация Аминокислоты
презентация Аминокислоты Перша Світова війна
Перша Світова війна Транспортная планировка городов
Транспортная планировка городов Современное состояние и перспективы развития нефтяной и газовой промышленности России
Современное состояние и перспективы развития нефтяной и газовой промышленности России Презентация к классному часу Что такое дружба.
Презентация к классному часу Что такое дружба. Ландшафтная организация территории жилого района
Ландшафтная организация территории жилого района История игрушек
История игрушек Классные часы на тематику Здоровый образ жизни
Классные часы на тематику Здоровый образ жизни Работа с одарёнными детьми в РФМЛИ.
Работа с одарёнными детьми в РФМЛИ. Электрическое оборудование и его обслуживание на модернизированных тепловозах 2ТЭ10Мк с УПУ
Электрическое оборудование и его обслуживание на модернизированных тепловозах 2ТЭ10Мк с УПУ Параметры пожаров. Открытые и внутренние пожары
Параметры пожаров. Открытые и внутренние пожары Я - маркетолог
Я - маркетолог В мире сказок
В мире сказок Радиоволны. Что такое радиоволны?
Радиоволны. Что такое радиоволны? Виброакустический метод диагностирования технического состояния колесно-моторного блока
Виброакустический метод диагностирования технического состояния колесно-моторного блока Построение сечения выработки сводчатой формы для самоходного оборудования
Построение сечения выработки сводчатой формы для самоходного оборудования Бет-жақ аймағының ауруы кезіндегі мрт диагностикасы
Бет-жақ аймағының ауруы кезіндегі мрт диагностикасы Глобальные экологические проблемы
Глобальные экологические проблемы География автомобильного транспорта РФ
География автомобильного транспорта РФ Современные системы отопления зданий и сооружений
Современные системы отопления зданий и сооружений Множественная регрессия
Множественная регрессия Общая характеристика грибов
Общая характеристика грибов City Tour Tbilisi 35 lari
City Tour Tbilisi 35 lari ОГЭ по обществознанию. Кодификатор, спецификация
ОГЭ по обществознанию. Кодификатор, спецификация любимое время года
любимое время года