Содержание
- 2. Окислительно-восстановительный (редокс-) потенциал 1. Реакции, при которых происходит перенос электронов от одних молекул к другим, называются
- 3. Редокс-потенциал Уравнение Нернста для редокс-потенциала: Е0׀ = Е0 + RT/nF •ln[Ox]/[Red] - Стандартный электрод сравнения (Е0)
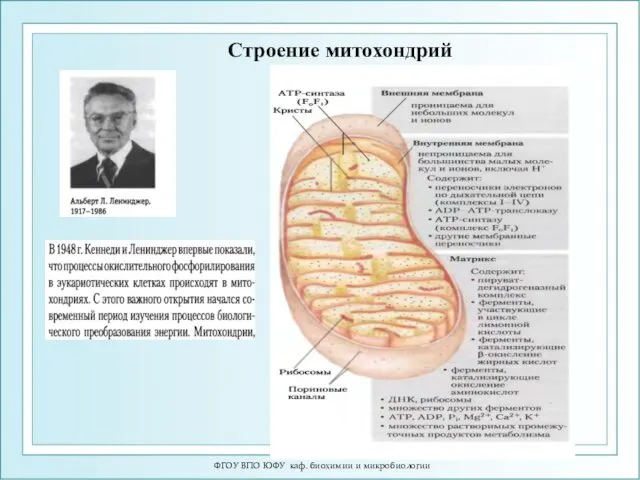
- 4. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Строение митохондрий
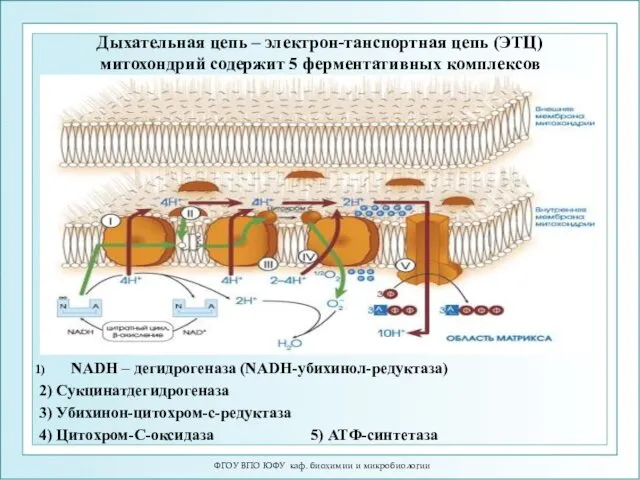
- 5. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Дыхательная цепь – электрон-танспортная цепь (ЭТЦ) митохондрий содержит 5
- 6. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Каскад переноса π-электронов по дыхательной цепи. 1.Каждый компонент дыхательной
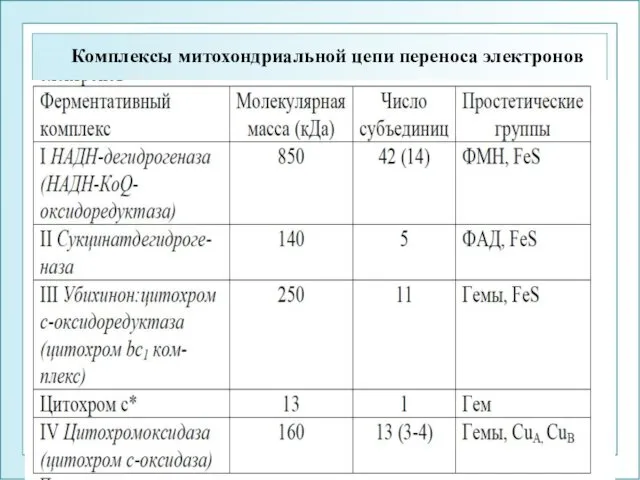
- 7. Комплексы митохондриальной цепи переноса электронов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
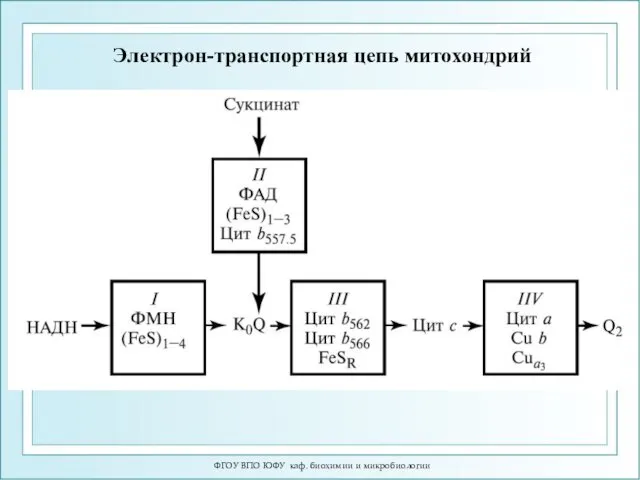
- 8. Электрон-транспортная цепь митохондрий ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
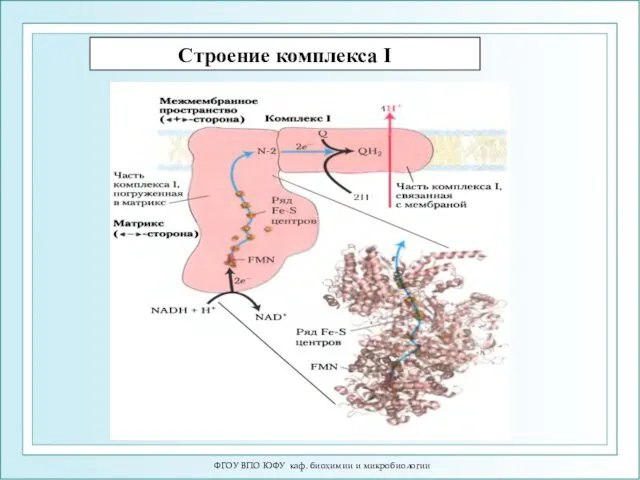
- 9. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Строение комплекса I
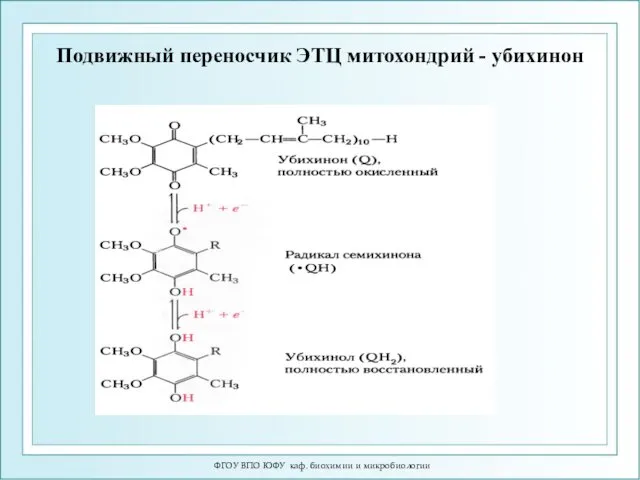
- 10. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Подвижный переносчик ЭТЦ митохондрий - убихинон
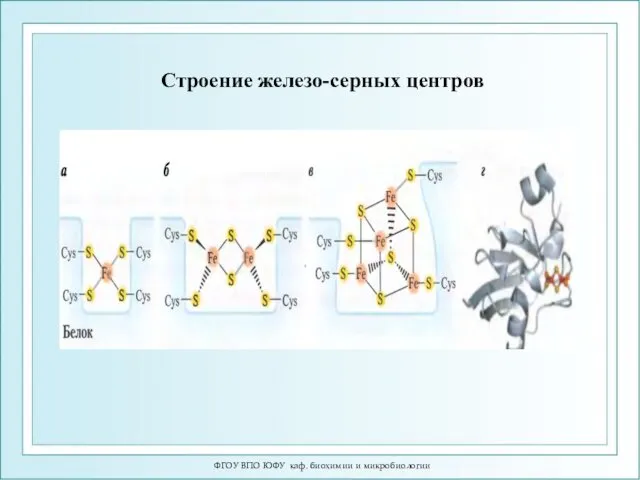
- 11. Строение железо-серных центров ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
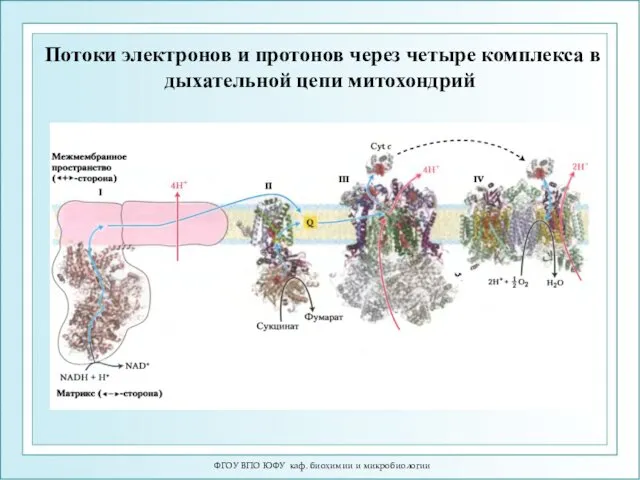
- 12. Потоки электронов и протонов через четыре комплекса в дыхательной цепи митохондрий ФГОУ ВПО ЮФУ каф. биохимии
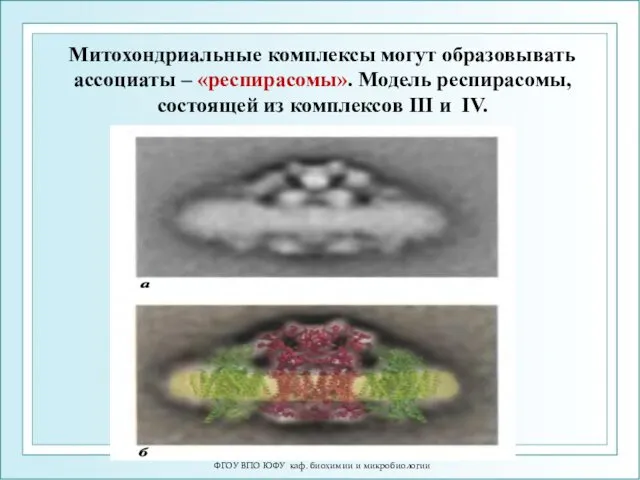
- 13. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Митохондриальные комплексы могут образовывать ассоциаты – «респирасомы». Модель респирасомы,
- 14. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Питер Митчелл (1920-1992) Нобелевская премия 1978 года «За вклад
- 15. Положения хемиосмотической теории П.Митчелла (1961) Ферментные реакции, в которых одновременно протекают химические превращения и транспорт частиц
- 16. Хемиосмотическая теория Митчелла. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Главный постулат – сопряжение окисления и
- 17. Положения хемиосмотической теории П.Митчелла Электрохимический градиент протонов включает две составляющих: осмотическую (∆рН) и электрическую (∆φ) ∆μн+
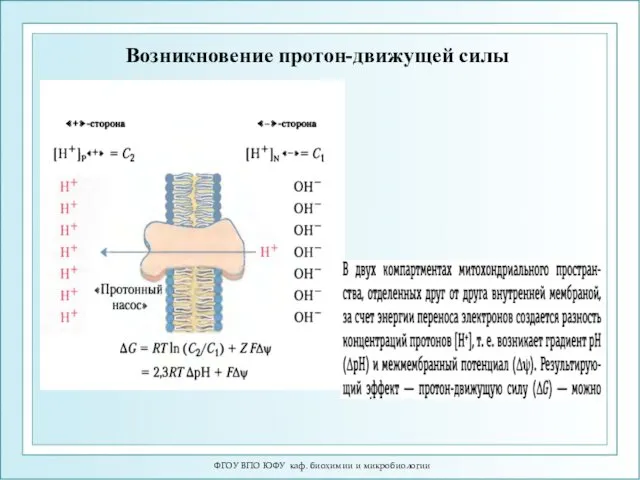
- 18. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Возникновение протон-движущей силы
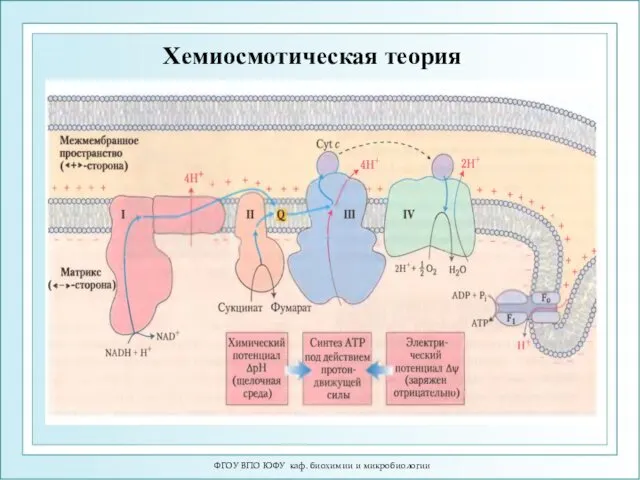
- 19. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Хемиосмотическая теория
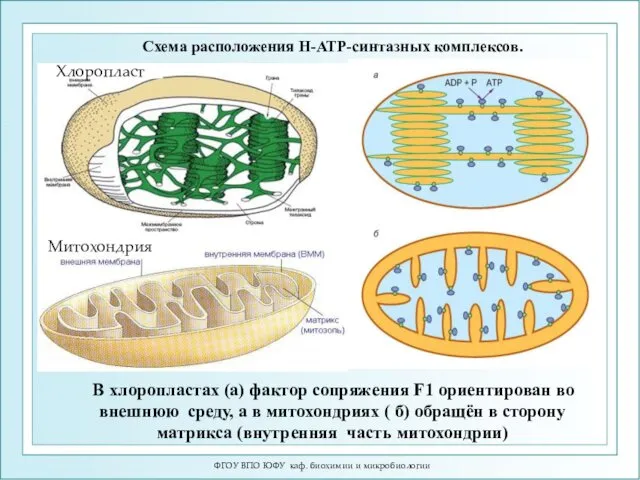
- 20. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Схема расположения H-ATP-синтазных комплексов. В хлоропластах (а) фактор сопряжения
- 21. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии «Все ферменты красивы, но АТФ-синтаза является одним из самых
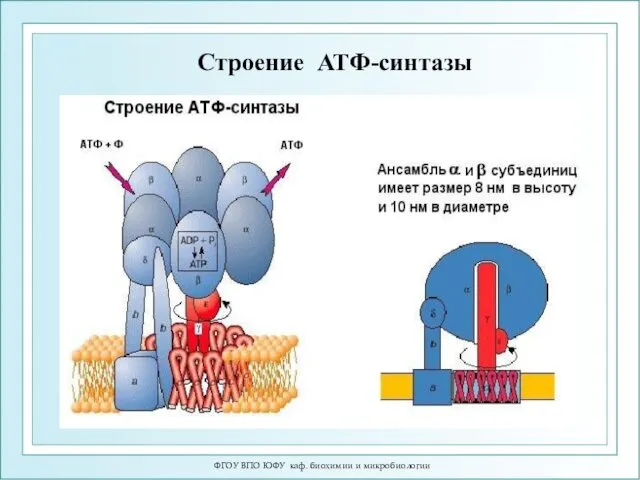
- 22. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Строение АТФ-синтазы
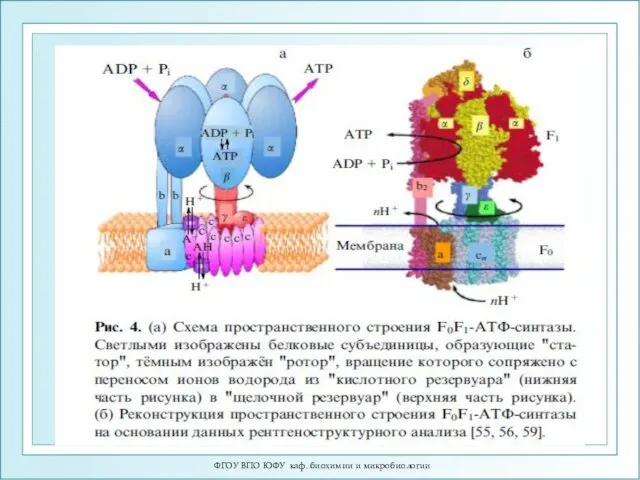
- 23. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
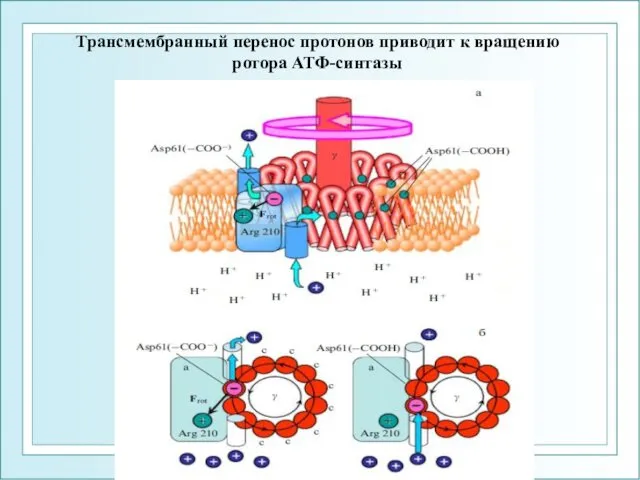
- 24. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Трансмембранный перенос протонов приводит к вращению ротора АТФ-синтазы
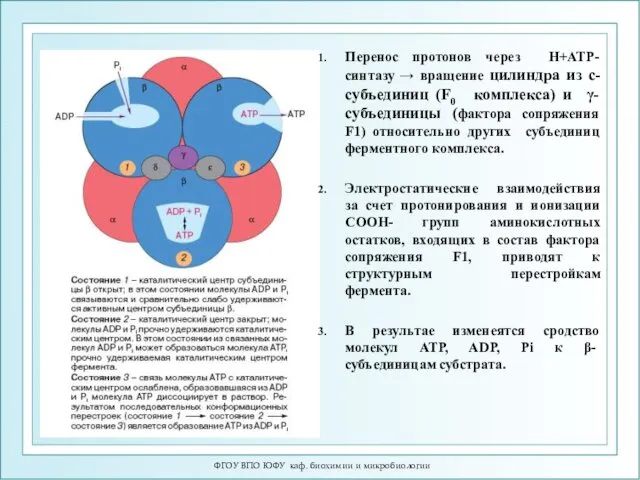
- 25. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Перенос протонов через H+ATP-синтазу → вращение цилиндра из с-субъединиц
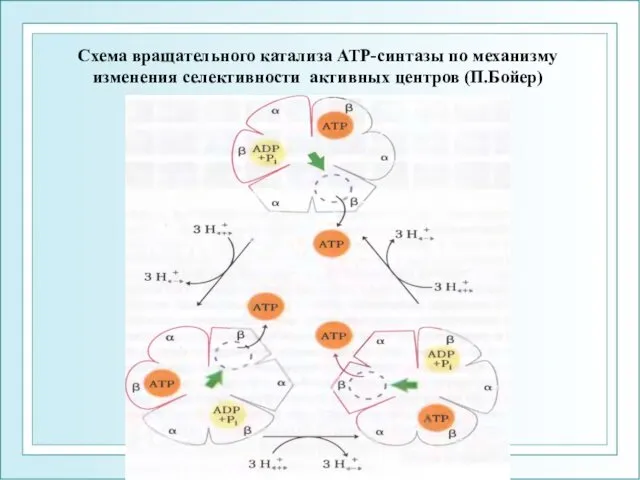
- 26. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Схема вращательного катализа АТР-синтазы по механизму изменения селективности активных
- 27. Механизм синтеза АТФ Механизм синтеза АТФ был предложен P. Boyer и включает 3 стадии, в результате
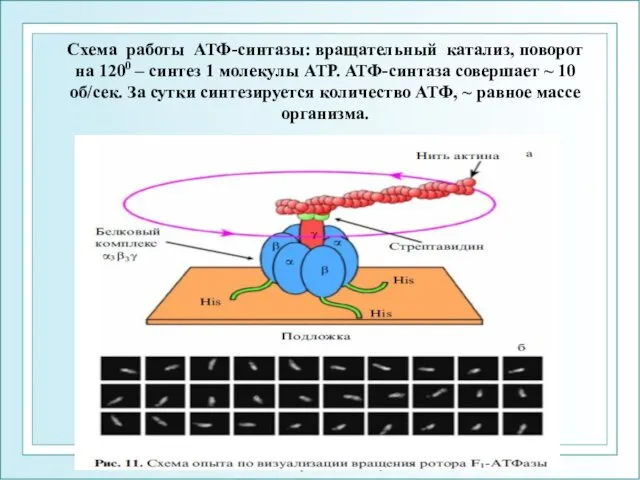
- 28. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Схема работы АТФ-синтазы: вращательный катализ, поворот на 1200 –
- 29. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии В сутки человек потребляет в среднем 27 моль кислорода.
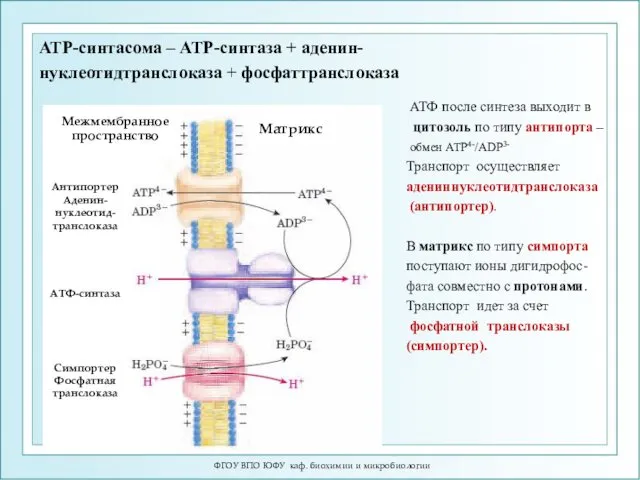
- 30. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии АТР-синтасома – АТР-синтаза + аденин- нуклеотидтранслоказа + фосфаттранслоказа АТФ
- 31. АТФ-синтасома Адениннуклеотидтранслоказа (антипортер) связывает АДФ3- в межмембранном пространстве и транспортирует его в матрикс в обмен на
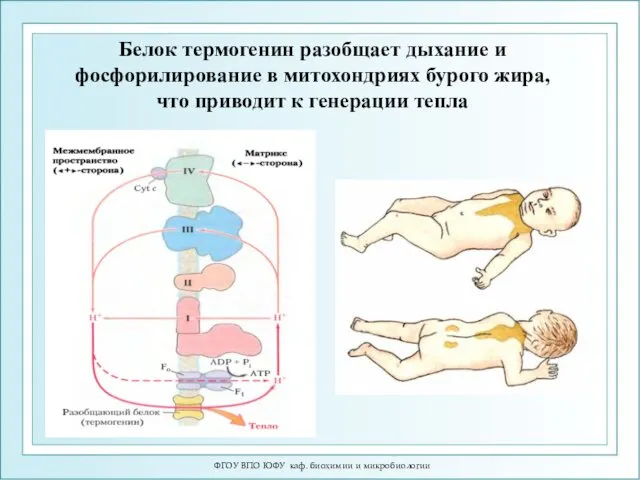
- 32. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Белок термогенин разобщает дыхание и фосфорилирование в митохондриях бурого
- 33. Разобщение дыхания и окислительного фосфорилирования На разобщении дыхания и фосфорилирования основана терморегуляторная функция тканевого дыхания. Тканевое
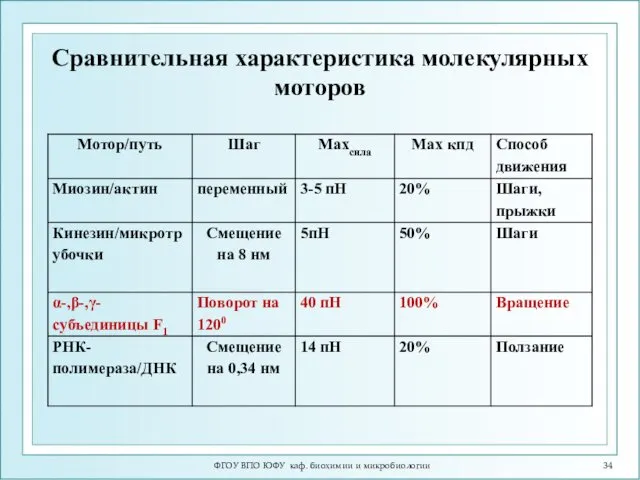
- 34. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Сравнительная характеристика молекулярных моторов
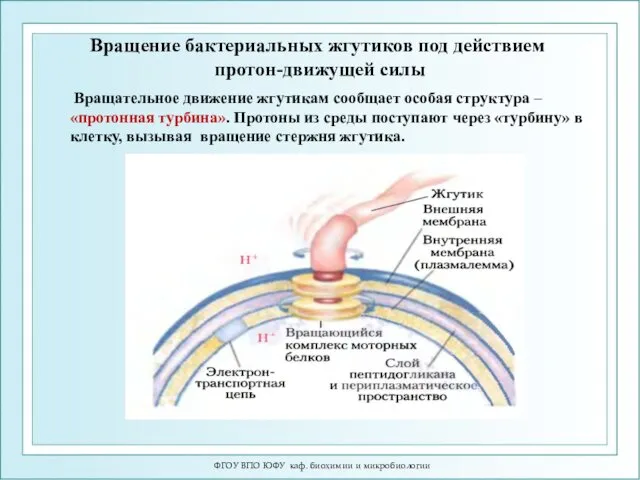
- 35. Вращение бактериальных жгутиков под действием протон-движущей силы Вращательное движение жгутикам сообщает особая структура – «протонная турбина».
- 36. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
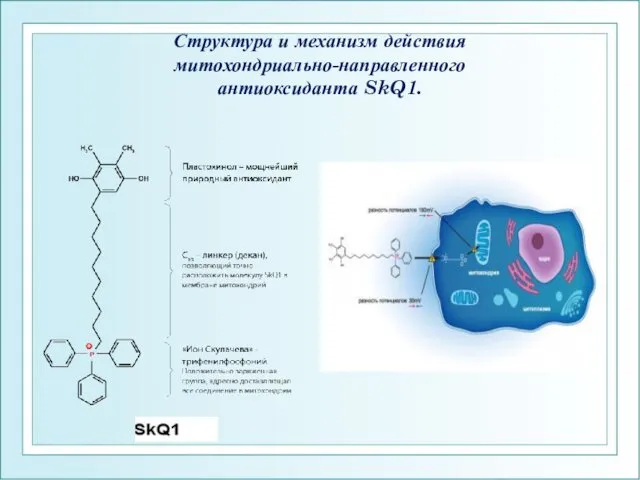
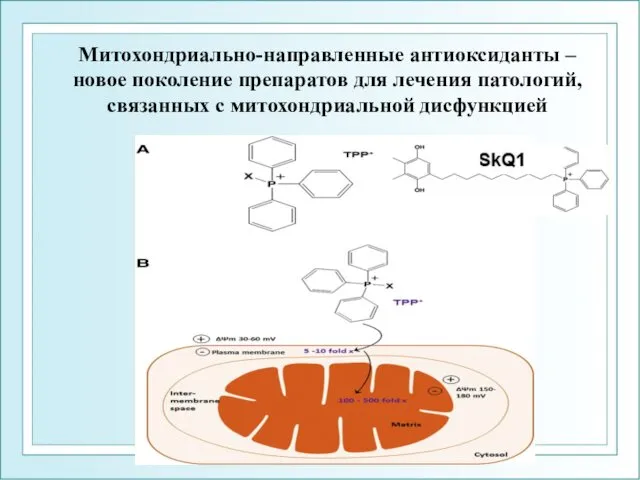
- 37. Структура и механизм действия митохондриально-направленного антиоксиданта SkQ1.
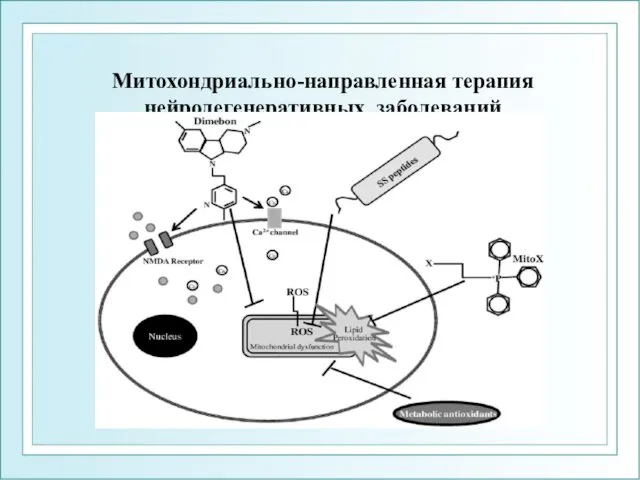
- 38. Митохондриально-направленная терапия нейродегенеративных заболеваний
- 39. Митохондриально-направленные антиоксиданты – новое поколение препаратов для лечения патологий, связанных с митохондриальной дисфункцией
- 41. Скачать презентацию













 Обследование зданий и сооружений (продолжение). Магнитные, электрические и электромагнитные методы
Обследование зданий и сооружений (продолжение). Магнитные, электрические и электромагнитные методы Управление развитием рынка потребителей газомоторного топлива в Московском регионе
Управление развитием рынка потребителей газомоторного топлива в Московском регионе Веб-камеры
Веб-камеры Багаторівнева організація пам'яті комп'ютера
Багаторівнева організація пам'яті комп'ютера Страны Европы и США в 1900 - 1914 годах
Страны Европы и США в 1900 - 1914 годах Особенности сестринского процесса при заболевании органов пищеварения у лиц старшей возрастной группы
Особенности сестринского процесса при заболевании органов пищеварения у лиц старшей возрастной группы Алгоритм разработки Адаптированной общеобразовательной программы (АООП)
Алгоритм разработки Адаптированной общеобразовательной программы (АООП) Сборка игрушки из помпонов
Сборка игрушки из помпонов Интегрированный урок математика + история
Интегрированный урок математика + история Круговорот веществ. 11 класс
Круговорот веществ. 11 класс Схемы. Виды схем
Схемы. Виды схем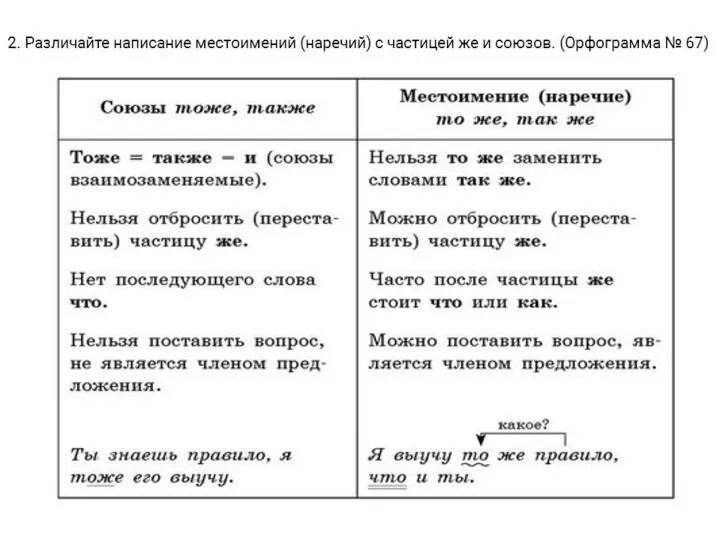 §65. Правило
§65. Правило Порядок предоставления субсидий из бюджета Пермского края бюджетам муниципальных образований Пермского края
Порядок предоставления субсидий из бюджета Пермского края бюджетам муниципальных образований Пермского края Неделя детской книги . Средняя группа.
Неделя детской книги . Средняя группа. Диагностика воспитанности учащихся
Диагностика воспитанности учащихся РЭР
РЭР Классификация конституций и их юридические свойства
Классификация конституций и их юридические свойства африка носорог
африка носорог Сочинение на ЕГЭ
Сочинение на ЕГЭ Языки и системы программирования
Языки и системы программирования Применениние наглядного моделирования в логопедической работе с детьми, имеющими ОНР.
Применениние наглядного моделирования в логопедической работе с детьми, имеющими ОНР. Родителям о ФГОС ДО
Родителям о ФГОС ДО Деревянное зодчество Древней Руси
Деревянное зодчество Древней Руси Технологические особенности управления режимом работы магистрального газопровода
Технологические особенности управления режимом работы магистрального газопровода Производство текстильных материалов. Технологии. 5 класс
Производство текстильных материалов. Технологии. 5 класс Иврит. Фестиваль языков 2019
Иврит. Фестиваль языков 2019 Малоугловое рентгеновское рассеяние
Малоугловое рентгеновское рассеяние Трансформаторы. Производство, передача и использование электрической энергии
Трансформаторы. Производство, передача и использование электрической энергии