Содержание
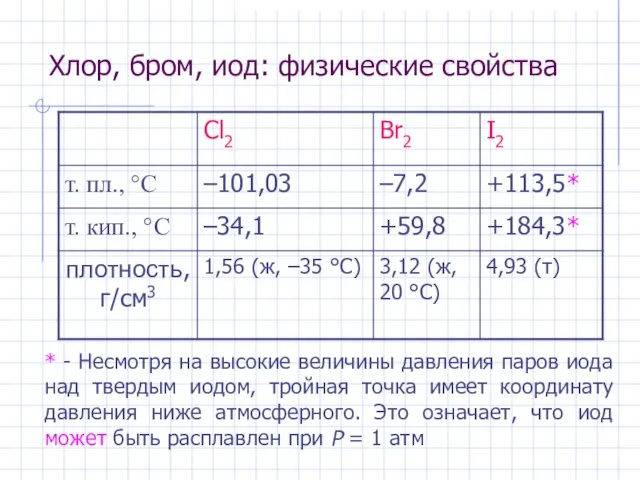
- 2. Хлор, бром, иод: физические свойства * - Несмотря на высокие величины давления паров иода над твердым
- 3. Г2: Cl Br I (At) Примеры: Cl2(Br2) + Cu → CuCl2 (CuBr2); ½ I2 + Cu
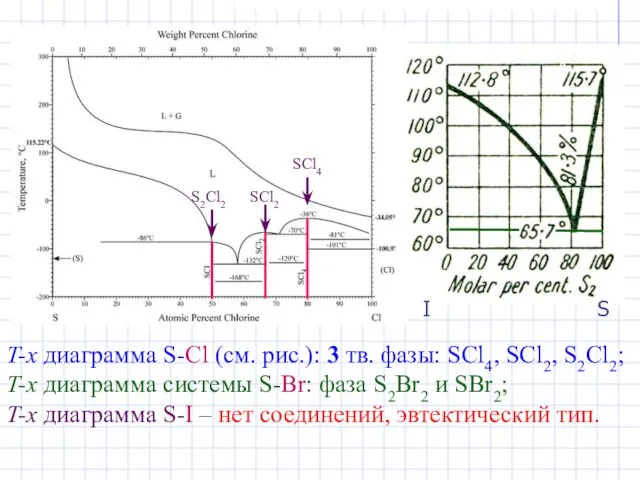
- 4. T-x диаграмма S-Cl (см. рис.): 3 тв. фазы: SCl4, SCl2, S2Cl2; T-x диаграмма системы S-Br: фаза
- 5. Г2: Cl Br I (At) Примеры (продолжение): 3. H2(г) + Cl2(г) ⮀ 2 HCl(г); ΔG °
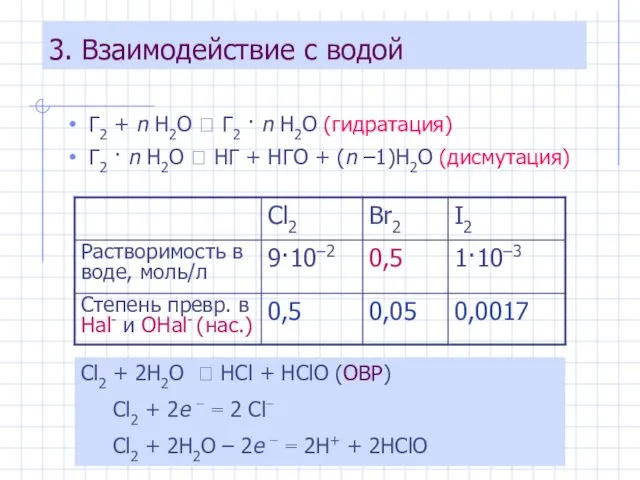
- 6. 3. Взаимодействие с водой Г2 + n H2O ⮀ Г2 · n H2O (гидратация) Г2 ·
- 7. В р-ре KI: KI + I2 (т) = K[I(I)2] I– + I2 (т) = [I(I)2]– дииодоиодат(I)-ион
- 8. В органических растворителях Органические растворители, не смешивающиеся с водой, используют для извлечения (экстракции) брома и иода.
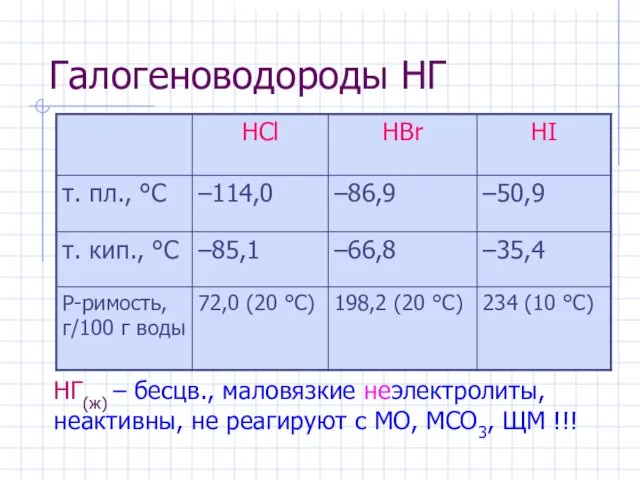
- 9. Галогеноводороды НГ НГ(ж) – бесцв., маловязкие неэлектролиты, неактивны, не реагируют c МО, МCO3, ЩМ !!!
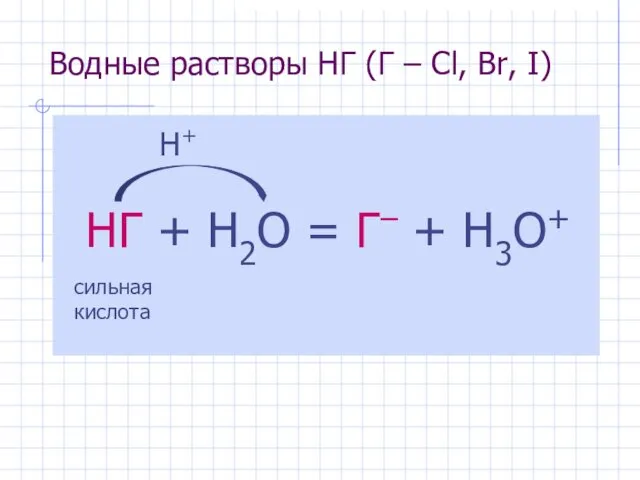
- 10. Водные растворы HГ (Г – Cl, Br, I) НГ + H2O = Г– + H3O+ сильная
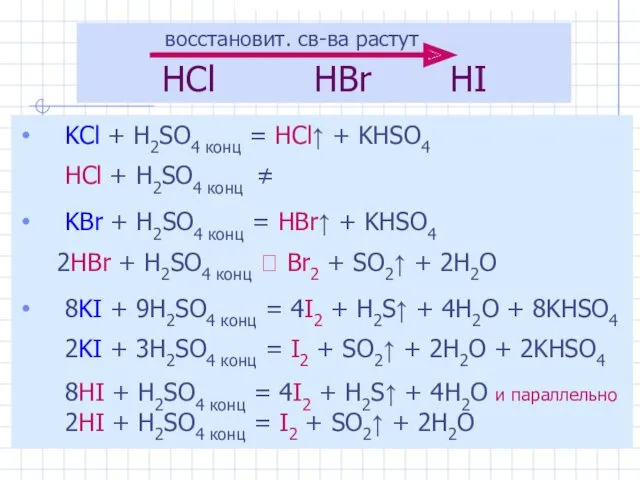
- 11. HCl HBr HI KCl + H2SO4 конц = HCl↑ + KHSO4 HCl + H2SO4 конц ≠
- 12. Получение НCl В промышл. – прямым синтезом: H2 + Cl2 = 2HCl В лаборатории: NaCl +
- 13. Получение НBr и HI В лаборатории и в промышл. усл. – синтез галогенидов фосфора с последующим
- 14. Положительные степени окисления галогенов: (в основном) +1, +3, +5, +7 +1: Г2 + NaOH ⇔ NaГ
- 15. В растворах щелочей Br2 + 2KOH = KBr + KBrO + H2O (на холоду) Br2 +
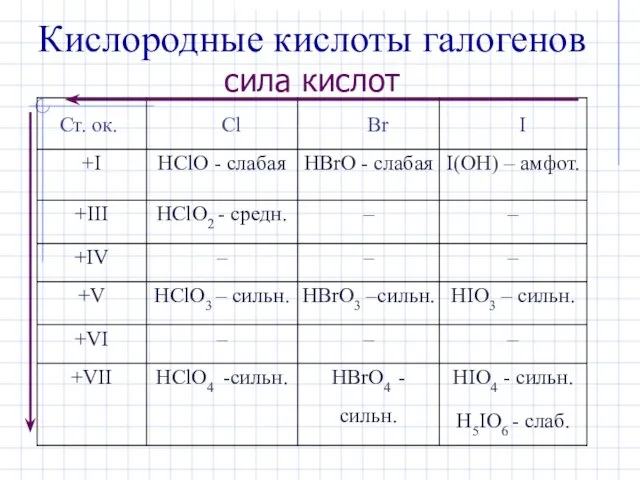
- 16. Кислородные кислоты галогенов сила кислот
- 17. Получение и реакции оксидов: Cl2 + Ag2O → Cl2O + 2AgCl (в неводн. р-ле); 3KClO3 +
- 18. В щелочной среде – диспропорционирование (дисмутация): 3Г2 + 6NaOH = 5NaГ + NaГO3 + 3H2O Г2
- 20. Скачать презентацию


![В р-ре KI: KI + I2 (т) = K[I(I)2] I–](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/55396/slide-6.jpg)







 Программа элективных курсов Химические реакции в аналитической химии
Программа элективных курсов Химические реакции в аналитической химии Послепечатные процессы. Способы послепечатной обработки
Послепечатные процессы. Способы послепечатной обработки . Большое путешествие
. Большое путешествие Усиление деревянных конструкций (2)
Усиление деревянных конструкций (2) Семинар формир. и оценка РУУД
Семинар формир. и оценка РУУД Анализ эффективного выбора УЭЦН на фонде скважин ЦДНГ 3, Филлиповского месторождения
Анализ эффективного выбора УЭЦН на фонде скважин ЦДНГ 3, Филлиповского месторождения Динамика развития и структура мирового автомобилестроения
Динамика развития и структура мирового автомобилестроения Ипотечное кредитование и перспективы его развития в России (на примере ПАО Сбербанк)
Ипотечное кредитование и перспективы его развития в России (на примере ПАО Сбербанк) Медицинская эвакуация. Объем мед. помощи в очагах катастроф
Медицинская эвакуация. Объем мед. помощи в очагах катастроф Регламент работы менеджера по продажам
Регламент работы менеджера по продажам Анализ качества образовательных результатов летней сессии 2019-2020 уч.г
Анализ качества образовательных результатов летней сессии 2019-2020 уч.г научно-практическая конференция
научно-практическая конференция Классный час Хлеб - всему голова
Классный час Хлеб - всему голова Резюме Ольги Ищук
Резюме Ольги Ищук Наклонение глагола
Наклонение глагола Производство электроэнергии. Передача и распределение электроэнергии
Производство электроэнергии. Передача и распределение электроэнергии Гигиена воды
Гигиена воды Игровое упражнение
Игровое упражнение Математическая модель реальной ситуации. 5 класс
Математическая модель реальной ситуации. 5 класс участники конкурса Город мастеров-2014г Диск
участники конкурса Город мастеров-2014г Диск Архитектурные сооружения Гатчины
Архитектурные сооружения Гатчины Идеальный конечный результат
Идеальный конечный результат Социальные отклонения и их классификация. Девиантное поведение
Социальные отклонения и их классификация. Девиантное поведение Единственное и множественное число глагола
Единственное и множественное число глагола Электротравма. Поражение атмосферным электричеством
Электротравма. Поражение атмосферным электричеством Чудеса Иисуса Христа Исцеление сына царедворца и воскрешение сына вдовы
Чудеса Иисуса Христа Исцеление сына царедворца и воскрешение сына вдовы Война с Польшей. Разгром Врангеля
Война с Польшей. Разгром Врангеля 100 шагов к здоровью
100 шагов к здоровью