Содержание
- 2. Содержание: Что изучает химическая кинетика ?; Скорость химической реакции ; Элементарные реакции; Молекулярность реакции; Механизм реакции;
- 3. Содержание: Реакции других порядков; Определение порядка реакций; Метод Вант-Гоффа; Метод подстановки; Метод Оствальда Нойеса; Метод полупревращения;
- 4. Что изучает химическая кинетика? Химическая кинетика изучает скорости протекания химических процессов и их механизм Основные задачи
- 5. Скорость химической реакции Скорость гомогенной химической реакции (в газовой фазе или в растворе) – это изменение
- 6. Скорость химической реакции Если химическая реакция описывается стехиометрическим уравнением aA + bB → rR + sS
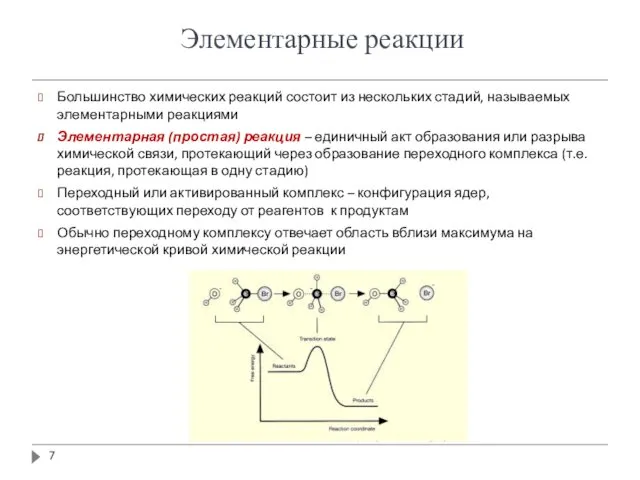
- 7. Элементарные реакции Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями Элементарная (простая) реакция –
- 8. Молекулярность реакции Молекулярностью реакции называют число частиц, участвующих в элементарной реакции. Молекулярность реакции бывает трех видов:
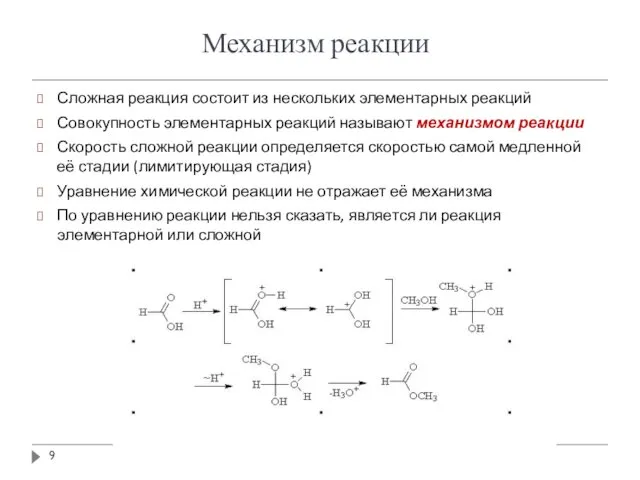
- 9. Механизм реакции Сложная реакция состоит из нескольких элементарных реакций Совокупность элементарных реакций называют механизмом реакции Скорость
- 10. Факторы, влияющие на скорость реакции Природа реагирующих веществ (тип химических связей в молекулах реагентов, прочность связей,
- 11. Постулаты химической кинетики Законы химической кинетики основаны на двух принципах (постулатах): скорость химической реакции пропорциональна концентрациям
- 12. Влияние концентрации реагирующих веществ на скорость реакции Функциональная зависимость скорости химической реакции от концентраций компонентов называется
- 13. Порядок сложной реакции Порядок сложной реакции по веществу в общем случае не совпадает с коэффициентами в
- 14. Реакции нулевого порядка Реакциями нулевого порядка по данному веществу являются реакции в закрытой системе про постоянном
- 15. Примеры реакций нулевого порядка Реакции нулевого порядка встречаются в гетерогенных процессах, гетерогенном катализе и всегда указывают
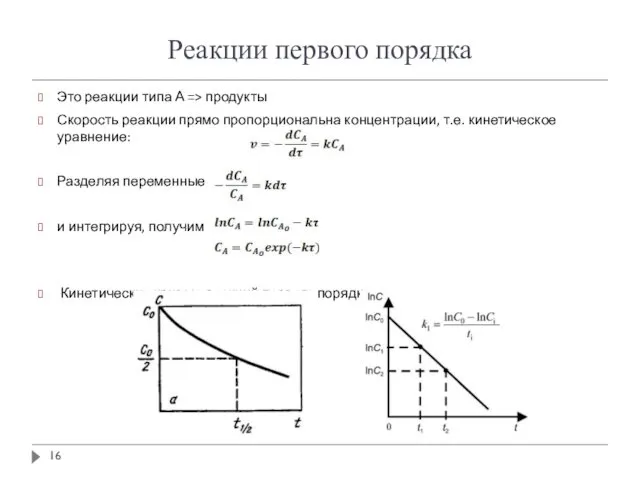
- 16. Реакции первого порядка Это реакции типа А => продукты Скорость реакции прямо пропорциональна концентрации, т.е. кинетическое
- 17. Реакции первого порядка Особенности реакций первого порядка: Скорость реакции экспоненциально зависит от концентрации График зависимости lnC
- 18. Реакции второго порядка В реакции участвуют два реагента Возможны два случая Случай 1. А+В→продукты, начальные концентрации
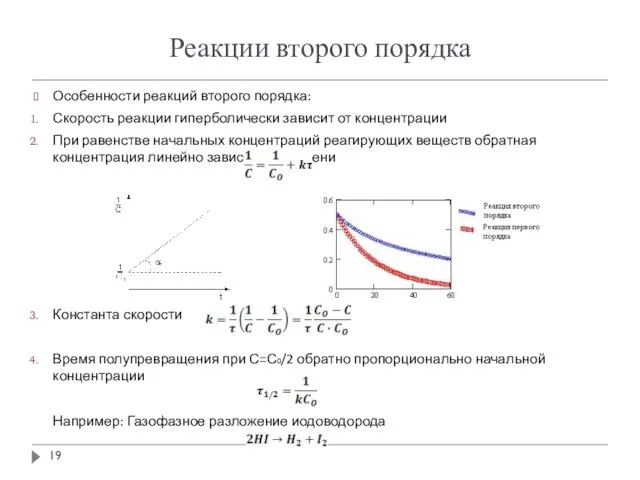
- 19. Реакции второго порядка Особенности реакций второго порядка: Скорость реакции гиперболически зависит от концентрации При равенстве начальных
- 20. Реакции второго порядка Случай 2. А+В→продукты, начальные концентрации веществ не равны, т.е. Кинетическое уравнение Разделяя переменные
- 21. Реакции n-го порядка Это реакции типа nА→продукты Кинетическое уравнение Решение уравнения: Время полупревращения
- 22. Реакции других порядков Необычный — дробный или отрицательный — порядок реакции однозначно указывает на её сложный
- 23. Определение порядка реакции Методы определения порядка реакции базируются на методах вычислительной математики, которые позволяют по кинетическим
- 24. Метод Вант-Гоффа Порядок реакции определяют по скоростям превращения Для реакции А+В→продукты записывают уравнение закона действующих масс:
- 25. Метод подстановки Заключается в том, что экспериментальные данные последовательно подставляют в интегральные кинетические уравнения для реакций
- 26. Метод Оствальда-Нойеса Порядок реакции определяют по времени достижения определённой доли превращения α: Отсюда порядок реакции
- 27. Метод полупревращения Частный случай метода Оствальда-Нойеса Порядок реакции определяют по периоду полупревращения (α=1/2) Метод Оствальда-Нойеса и
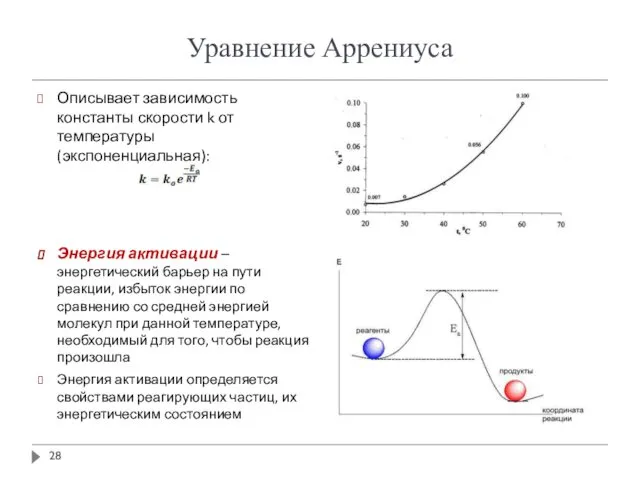
- 28. Уравнение Аррениуса Описывает зависимость константы скорости k от температуры (экспоненциальная): Энергия активации – энергетический барьер на
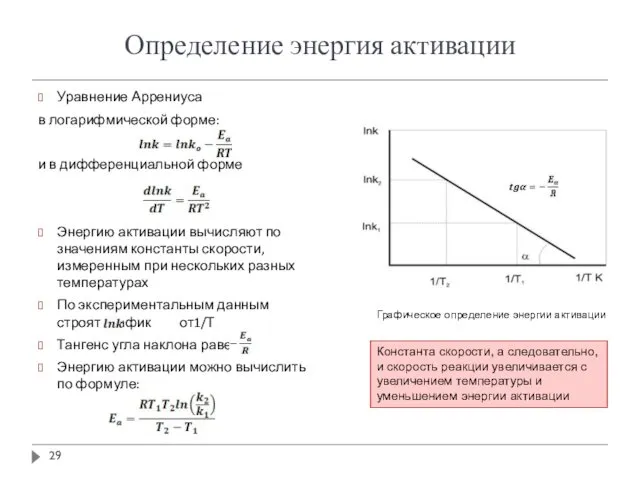
- 29. Определение энергия активации Уравнение Аррениуса в логарифмической форме: и в дифференциальной форме Энергию активации вычисляют по
- 30. Кинетика сложных реакций При изучении сложных реакций, включающих несколько элементарных стадий, используют принцип независимости химических реакций:
- 32. Скачать презентацию























 От пера до компьютера
От пера до компьютера Классный час Культура общения. Правила поведения в театре
Классный час Культура общения. Правила поведения в театре Патофізіологія системи крові. (Лекція 10)
Патофізіологія системи крові. (Лекція 10) bd3ccfe5c6d24bb9a8b4ece584a2830f
bd3ccfe5c6d24bb9a8b4ece584a2830f Планирование, исполнение и завершение проекта
Планирование, исполнение и завершение проекта Презентация урока Мира.
Презентация урока Мира. Презентация Использование приемов мнемотехники для развития речи детей старшего дошкольного возраста
Презентация Использование приемов мнемотехники для развития речи детей старшего дошкольного возраста Презентация Робот и человек на конкурс Я -исследователь
Презентация Робот и человек на конкурс Я -исследователь Әлемдік діндер: буддизм, христиан, ислам
Әлемдік діндер: буддизм, христиан, ислам О бездомных животных
О бездомных животных презентация подготовительной группы Колокольчики
презентация подготовительной группы Колокольчики География. Транспорт России
География. Транспорт России Презентация Рельеф Южной Америки
Презентация Рельеф Южной Америки Методическая разработка Своя игра по теме Кислород, 8 класс
Методическая разработка Своя игра по теме Кислород, 8 класс Урок-инструктаж Как подготовить реферат и презентацию по обществознанию
Урок-инструктаж Как подготовить реферат и презентацию по обществознанию Инструкция по работе в виртуальной образовательной среде
Инструкция по работе в виртуальной образовательной среде Ratownicze zestawy pneumatyczne podnoszące
Ratownicze zestawy pneumatyczne podnoszące Сенсорный контроль качества пищевых продуктов. Тема 3
Сенсорный контроль качества пищевых продуктов. Тема 3 Главный тормозной цилиндр
Главный тормозной цилиндр Особенности образовательного процесса в 5 классе в 2020-2021 учебном году
Особенности образовательного процесса в 5 классе в 2020-2021 учебном году выступ. проекты 2022
выступ. проекты 2022 Дарындылық, талант, данышпандық қабілетінің даму жағдайы
Дарындылық, талант, данышпандық қабілетінің даму жағдайы Экскурсия как средство духовно-нравственного развития и гражданско-патриотического воспитания подростков гимназии.
Экскурсия как средство духовно-нравственного развития и гражданско-патриотического воспитания подростков гимназии. Идентификация чулочно-носочных изделий заявленным производителем характеристикам
Идентификация чулочно-носочных изделий заявленным производителем характеристикам Ефекти радіаційного ураження
Ефекти радіаційного ураження Величины и действия с ними. 4 класс
Величины и действия с ними. 4 класс Компания Северсталь
Компания Северсталь 20190419_prezentatsiya-ekologiya1
20190419_prezentatsiya-ekologiya1