Содержание
- 2. Цель урока: познакомиться с общими химическими свойствами кислот.
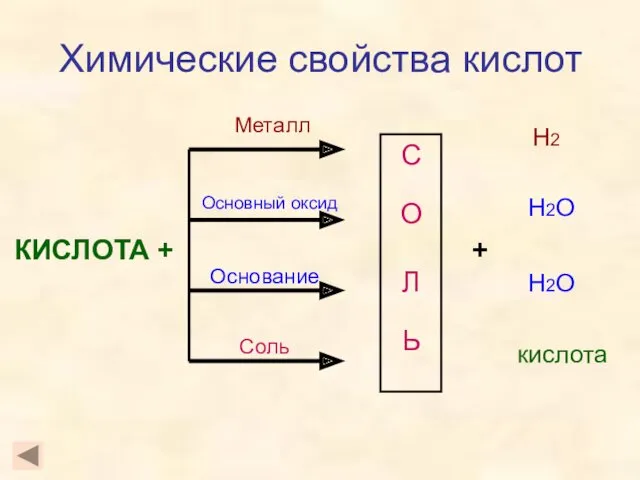
- 3. Химические свойства кислот КИСЛОТА + С О Л Ь Металл Основный оксид Основание Соль + Н2
- 4. Химические свойства кислот Кислота + металл = соль + водород Ряд активности металлов: Li K Ba
- 5. Химические свойства кислот Кислота + основный оксид = соль + вода Опыт. Взаимодействие оксида меди (Опыт.
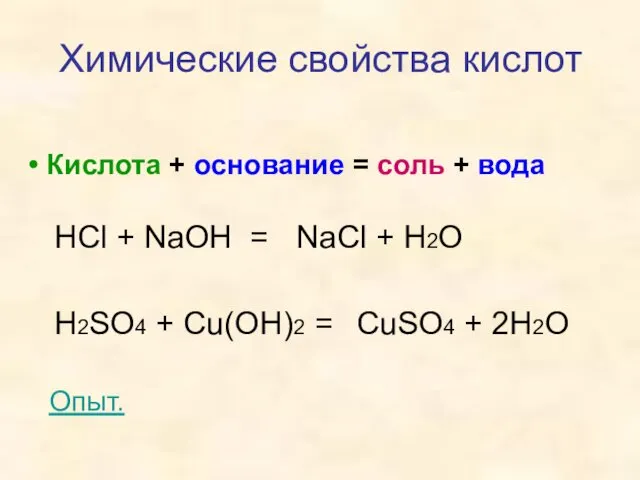
- 6. Кислота + основание = соль + вода Химические свойства кислот HCl + NaOH = H2SO4 +
- 7. Химические свойства кислот Кислота 1 + соль 1 = соль 2 + Кислота 2 Условия реакции:
- 8. Составьте возможные уравнения реакций взаимодействия перечисленных веществ с раствором серной кислоты.
- 10. Скачать презентацию





 Презентация Коллективная разработка ПО
Презентация Коллективная разработка ПО Невынашивание беременности
Невынашивание беременности Мікропроцесорна техніка (лекція 7)
Мікропроцесорна техніка (лекція 7)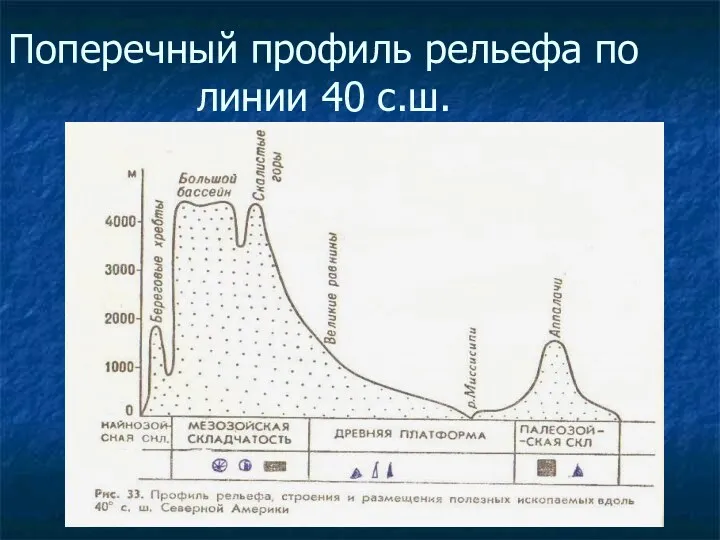 7 класс: Оледенение С.Америки
7 класс: Оледенение С.Америки Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого
Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого Functional styles of the english language: newspaper style
Functional styles of the english language: newspaper style Статус - отчет по ремонту Сормовский 3060
Статус - отчет по ремонту Сормовский 3060 К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР
К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР Планиметрия. Повторение. Часть 1
Планиметрия. Повторение. Часть 1 Мартеновский способ производства стали. Выплавка стали в электропечах
Мартеновский способ производства стали. Выплавка стали в электропечах How to present in English
How to present in English Интеллектуальные роботы состояние и перспективы
Интеллектуальные роботы состояние и перспективы Презентация С правом по жизни.
Презентация С правом по жизни. особенности изображения Земли на глобусе и на карте
особенности изображения Земли на глобусе и на карте Декоративные злаки
Декоративные злаки Мы вместе. Часть 2
Мы вместе. Часть 2 Рисуем пластилином
Рисуем пластилином Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей
Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей Философия Августина Блаженного
Философия Августина Блаженного Классный час 1сентября Эхо Бесланской печали
Классный час 1сентября Эхо Бесланской печали Конспект урока географии в 6 классе Тайны подземных бурь.
Конспект урока географии в 6 классе Тайны подземных бурь. Закрепление изученного в 4 классе
Закрепление изученного в 4 классе Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность
Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность презентация
презентация Биосфера Земли. Тест
Биосфера Земли. Тест Презентация Автоматизация звука Л в словах
Презентация Автоматизация звука Л в словах Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3)
Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3) Нарушения обмена хромопротеидов
Нарушения обмена хромопротеидов