Содержание
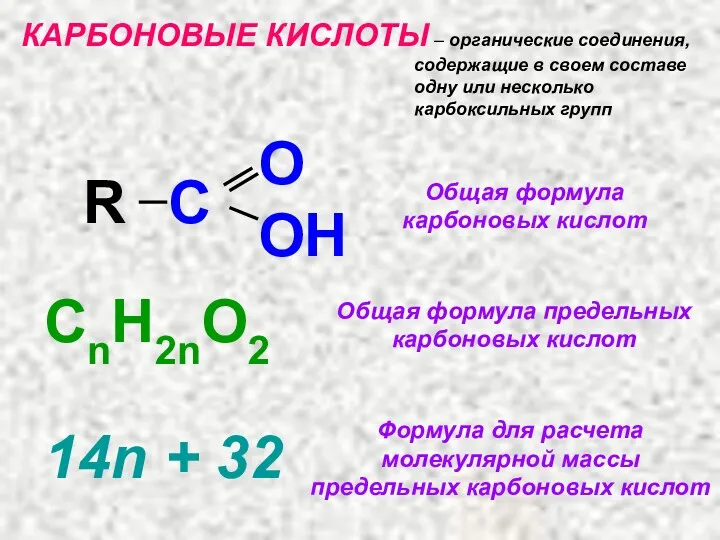
- 2. КАРБОНОВЫЕ КИСЛОТЫ – органические соединения, содержащие в своем составе одну или несколько карбоксильных групп R C
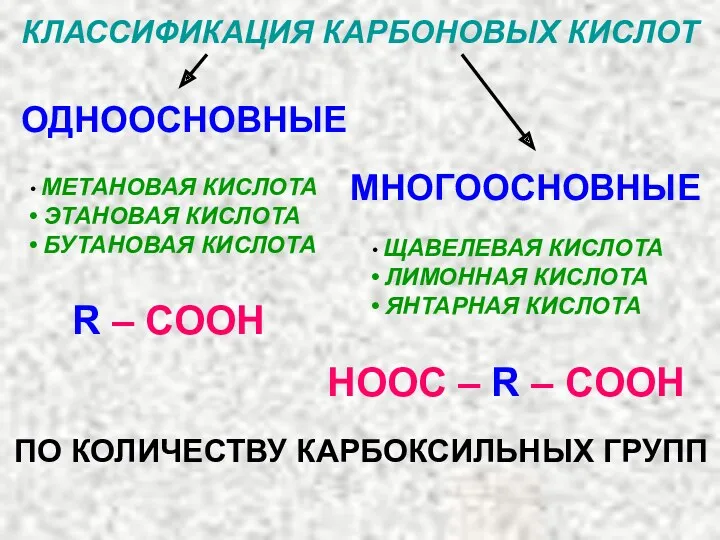
- 3. КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ ОДНООСНОВНЫЕ МНОГООСНОВНЫЕ МЕТАНОВАЯ КИСЛОТА ЭТАНОВАЯ КИСЛОТА БУТАНОВАЯ КИСЛОТА ЩАВЕЛЕВАЯ КИСЛОТА ЛИМОННАЯ КИСЛОТА ЯНТАРНАЯ
- 4. КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ ПРЕДЕЛЬНЫЕ НЕПРЕДЕЛЬНЫЕ АРОМАТИЧЕСКИЕ МЕТАНОВАЯ КИСЛОТА ЭТАНОВАЯ КИСЛОТА БУТАНОВАЯ КИСЛОТА ОЛЕИНОВАЯ КИСЛОТА ЛИНОЛЕВАЯ КИСЛОТА
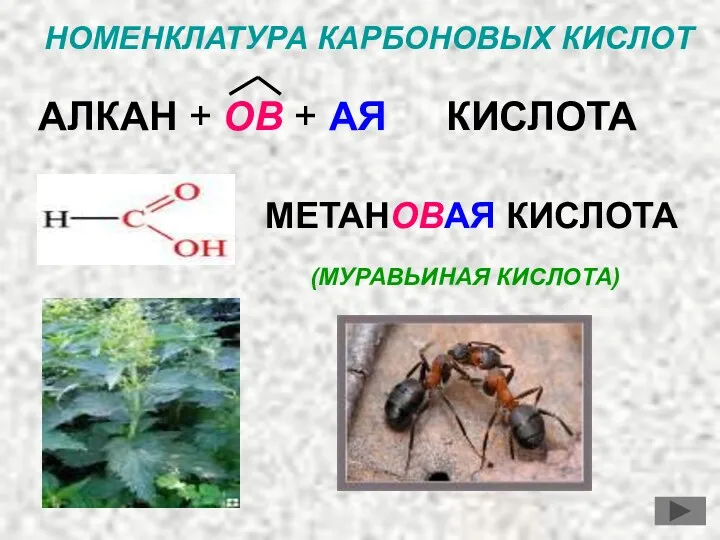
- 7. НОМЕНКЛАТУРА КАРБОНОВЫХ КИСЛОТ АЛКАН + ОВ + АЯ КИСЛОТА МЕТАНОВАЯ КИСЛОТА (МУРАВЬИНАЯ КИСЛОТА)
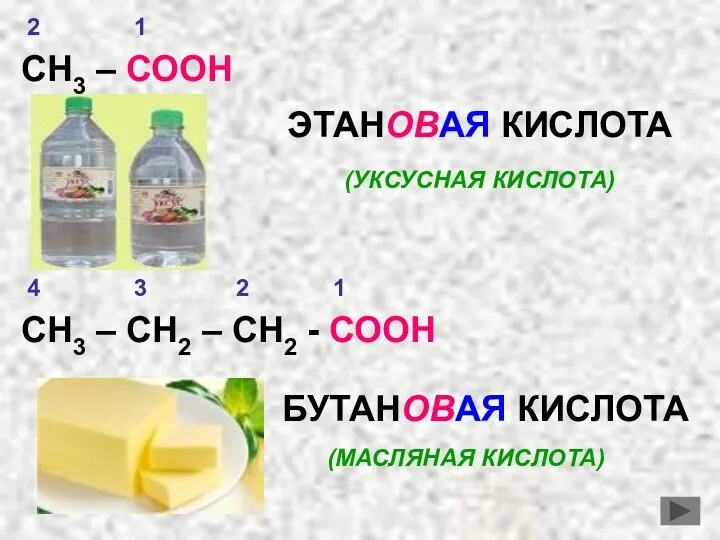
- 9. СН3 – СООН ЭТАНОВАЯ КИСЛОТА (УКСУСНАЯ КИСЛОТА) СН3 – СН2 – СН2 - СООН БУТАНОВАЯ КИСЛОТА
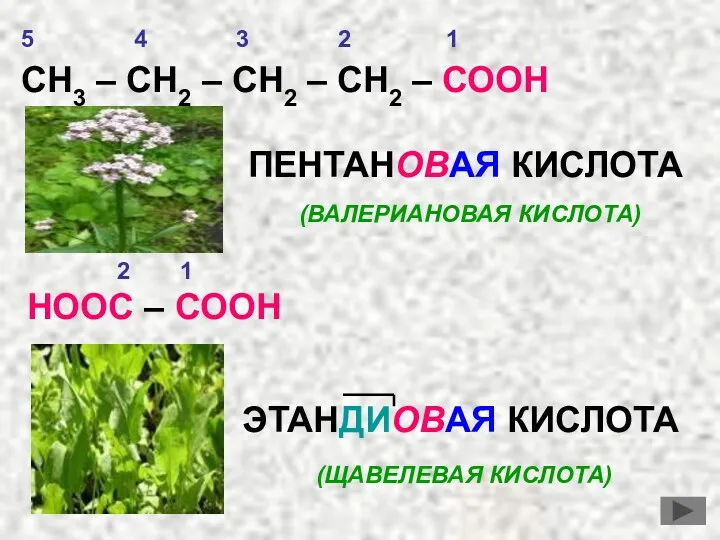
- 11. СН3 – СН2 – СН2 – СН2 – СООН ПЕНТАНОВАЯ КИСЛОТА (ВАЛЕРИАНОВАЯ КИСЛОТА) НООС – СООН
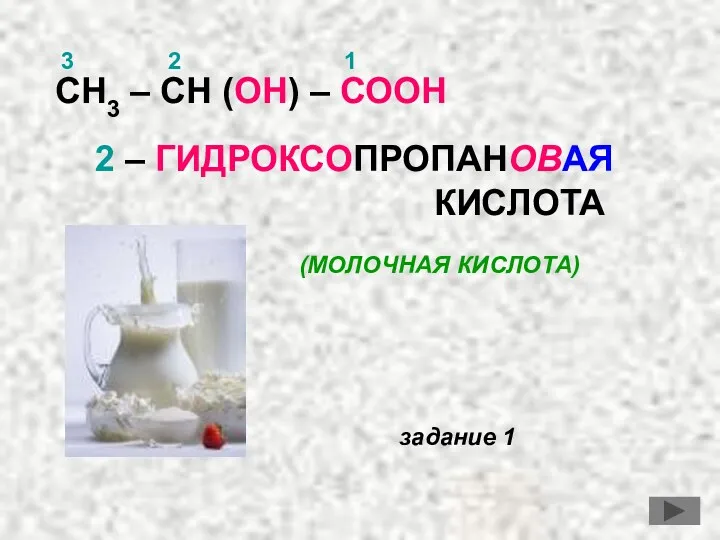
- 13. СН3 – СН (ОН) – СООН 1 2 3 2 – ГИДРОКСОПРОПАНОВАЯ КИСЛОТА (МОЛОЧНАЯ КИСЛОТА) задание
- 14. ДАЙТЕ НАЗВАНИЕ ВЕЩЕСТВАМ ПО МЕЖДУНАРОДНОЙ НОМЕНКЛАТУРЕ СН3 – СН(СН3) – СООН СН3 – СН2 – СН(СН3)
- 15. ОТВЕТЫ 2 – МЕТИЛПРОПАНОВАЯ КИСЛОТА 2, 3 – ДИМЕТИЛПЕНТАНОВАЯ КИСЛОТА 2 – МЕТИЛПЕНТЕН – 3 –
- 16. ИЗОМЕРИЯ КАРБОНОВЫХ КИСЛОТ Для предельных карбоновых кислот УГЛЕРОДНОГО СКЕЛЕТА МЕЖКЛАССОВАЯ (СЛОЖНЫЕ ЭФИРЫ) Для непредельных карбоновых кислот
- 17. ФИЗИЧЕСКИЕ СВОЙСТВА С1 – С3 С4 – С9 C10 и > Жидкости с характерным резким запахом,
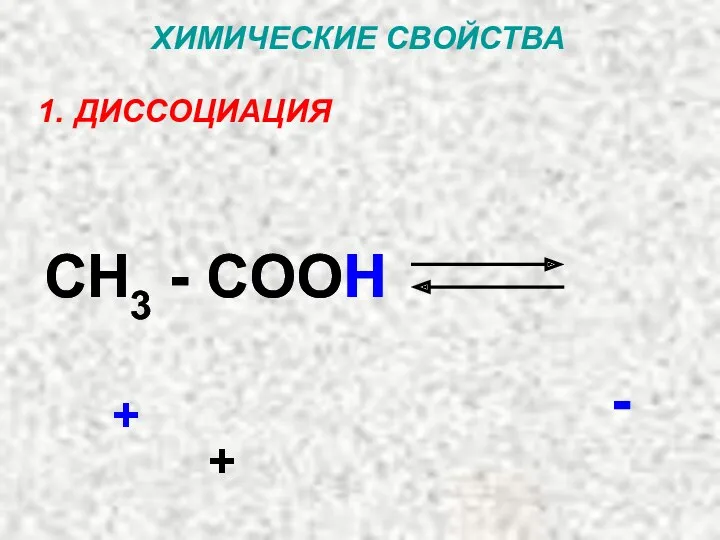
- 18. ХИМИЧЕСКИЕ СВОЙСТВА ДИССОЦИАЦИЯ CH3 - COO H + - + CH3 - COOH
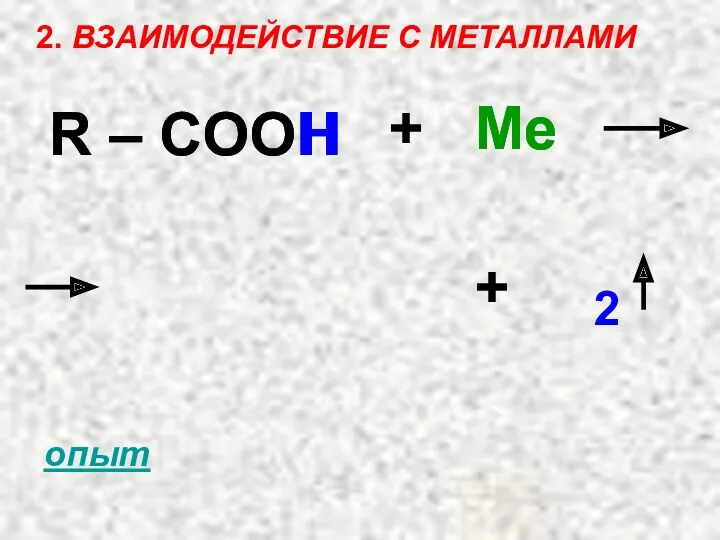
- 19. 2. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ R – COOH + Ме + 2 R – COO H Ме
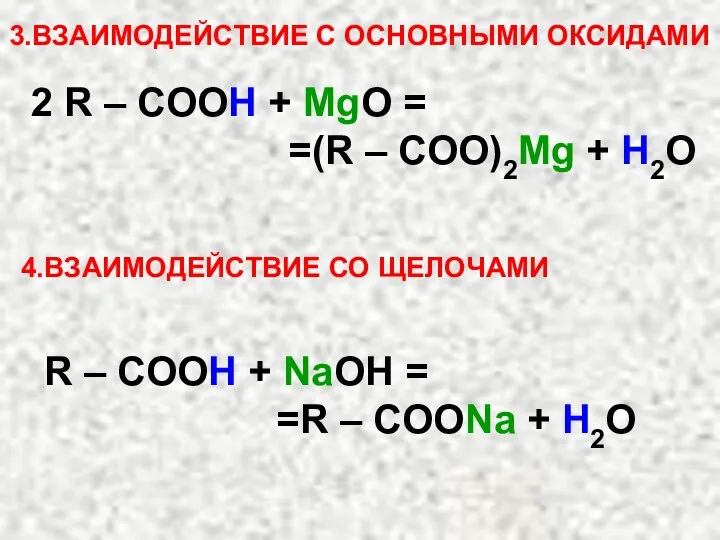
- 20. 3.ВЗАИМОДЕЙСТВИЕ С ОСНОВНЫМИ ОКСИДАМИ 2 R – COOH + MgO = =(R – COO)2Mg + H2O
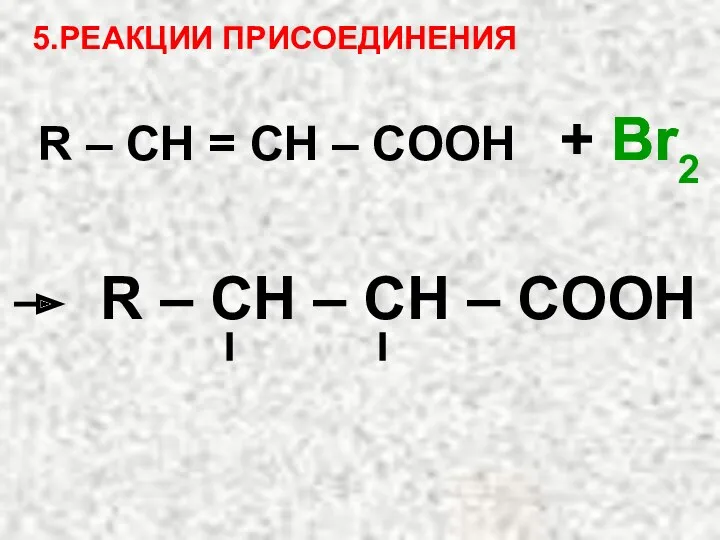
- 21. 5.РЕАКЦИИ ПРИСОЕДИНЕНИЯ R – CH = СH – COOH + Br2 Br Br R – CH
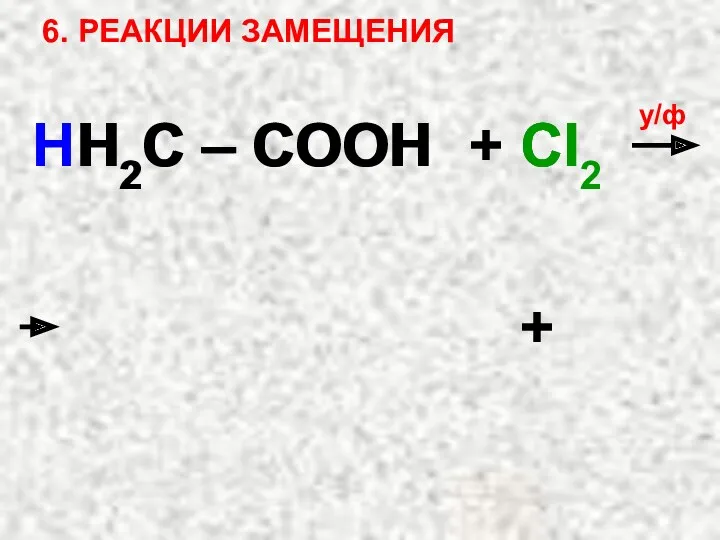
- 22. 6. РЕАКЦИИ ЗАМЕЩЕНИЯ HH2C – COOH + Cl2 у/ф + H2C – COOH Cl Cl H
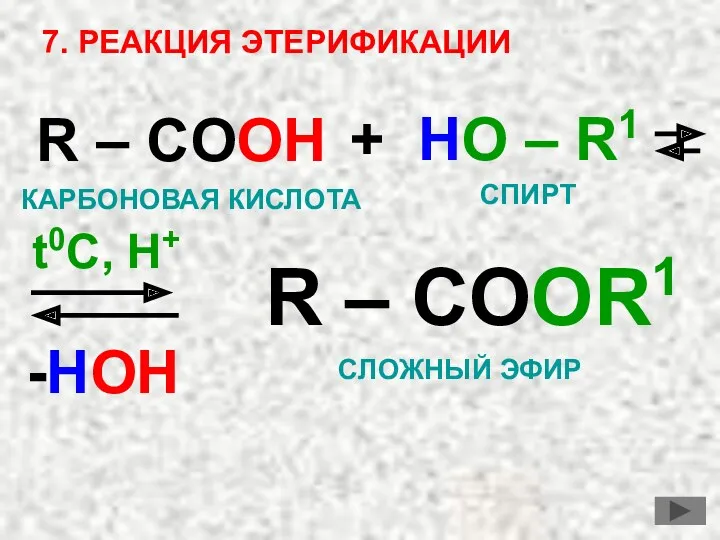
- 23. 7. РЕАКЦИЯ ЭТЕРИФИКАЦИИ R – COOH + HO – R1 R – COOR1 -HOH t0C, H+
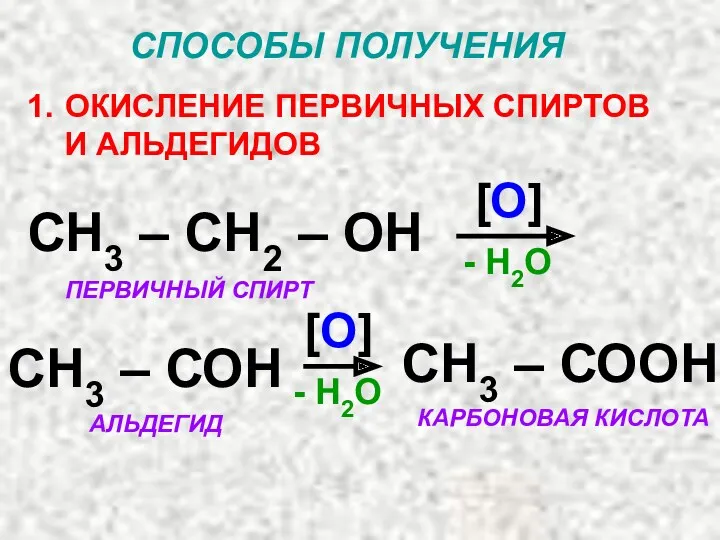
- 28. СПОСОБЫ ПОЛУЧЕНИЯ ОКИСЛЕНИЕ ПЕРВИЧНЫХ СПИРТОВ И АЛЬДЕГИДОВ СН3 – СН2 – ОН [О] - Н2О СН3
- 29. 2. ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ СН3 – СООС2Н5 + НОН Н+ СН3 – СООН + С2Н5ОН
- 30. ОБЛАСТИ ПРИМЕНЕНИЯ МУРАВЬИНАЯ КИСЛОТА УКСУСНАЯ КИСЛОТА ЩАВЕЛЕВАЯ КИСЛОТА ТЕСТ
- 35. Скачать презентацию



















 Классный час - виртуальная экскурсия На фабрике ёлочных игрушек
Классный час - виртуальная экскурсия На фабрике ёлочных игрушек Ветеринарно-санитарная экспертиза туш и органов животных при инфекционных болезнях
Ветеринарно-санитарная экспертиза туш и органов животных при инфекционных болезнях Деление на десятичную дробь. 5 класс
Деление на десятичную дробь. 5 класс Чорна металургія України
Чорна металургія України Живонись французеких импрессионистов и постимпрессионистов в собрании ГМИИ имени А.С.Пушкина
Живонись французеких импрессионистов и постимпрессионистов в собрании ГМИИ имени А.С.Пушкина Поэты и писатели Саратовской области
Поэты и писатели Саратовской области Город Подольск
Город Подольск Презентация факутальтива Эрудит 2
Презентация факутальтива Эрудит 2 Страны исламского мира. Саудовская Аравия
Страны исламского мира. Саудовская Аравия Лекція 2. Професіографічний аналіз інженерної діяльності
Лекція 2. Професіографічний аналіз інженерної діяльності Обустройство нефтяных месторождений
Обустройство нефтяных месторождений Магистерская программа Управленческий учет и контроллинг
Магистерская программа Управленческий учет и контроллинг Напряженно-деформированное состояние оболочечных конструкций, выполненных из материалов с усложненными механическими свойствами
Напряженно-деформированное состояние оболочечных конструкций, выполненных из материалов с усложненными механическими свойствами Опыт работы организации родительского просвещения РИМЦ Краснокамского муниципального района
Опыт работы организации родительского просвещения РИМЦ Краснокамского муниципального района презентация Заботимся о книгах Диск
презентация Заботимся о книгах Диск Образовательный проект Моя инициатива в сфере образования
Образовательный проект Моя инициатива в сфере образования Можно всё, друзья, найти в этой сказочной сети!
Можно всё, друзья, найти в этой сказочной сети! Презентация Безопасность на дорогах
Презентация Безопасность на дорогах Технические средства нейросетевого подхода к распознаванию информации
Технические средства нейросетевого подхода к распознаванию информации Дидактические игры по сенсорному воспитанию для детей раннего возраста.
Дидактические игры по сенсорному воспитанию для детей раннего возраста. Детали машин и основы конструирования. Механические передачи. Фрикционные передачи. (Лекция 4)
Детали машин и основы конструирования. Механические передачи. Фрикционные передачи. (Лекция 4) Фальсификации истории Великой Отечественной войны. Тезисы
Фальсификации истории Великой Отечественной войны. Тезисы Инфраструктура транспортных систем
Инфраструктура транспортных систем Захист нафтогазопромислового обладнання від корозії з використанням інгібіторів. Оцінка ефективності дії інгібіторів
Захист нафтогазопромислового обладнання від корозії з використанням інгібіторів. Оцінка ефективності дії інгібіторів Неорганические вяжущие вещества
Неорганические вяжущие вещества Крылатые слова
Крылатые слова Разработка ИТ-стратегии. (Лекция 7). Системы управления взаимоотношениями с клиентами (CRM-Client Relationship Management)
Разработка ИТ-стратегии. (Лекция 7). Системы управления взаимоотношениями с клиентами (CRM-Client Relationship Management) Микозы. Грибные заболевания кожи
Микозы. Грибные заболевания кожи