Содержание
- 2. вещества, избирательно подавляющие жизнедеятельность микроорганизмов. Это действие определяется специфичностью по отношению к возбудителям инфекционного процесса. АНТИБИОТИКИ
- 3. Антибактериальные Антимикобактериальные Противогрибковые Противовирусные Антипротозойные АНТИМИКРОБНЫЕ ЛС
- 4. Нарушение синтеза клеточной стенки (пенициллины, цефалоспорины, гликопептиды), Нарушение структуры клеточных мембран (полимиксины), Нарушение метаболизма фолиевой кислоты
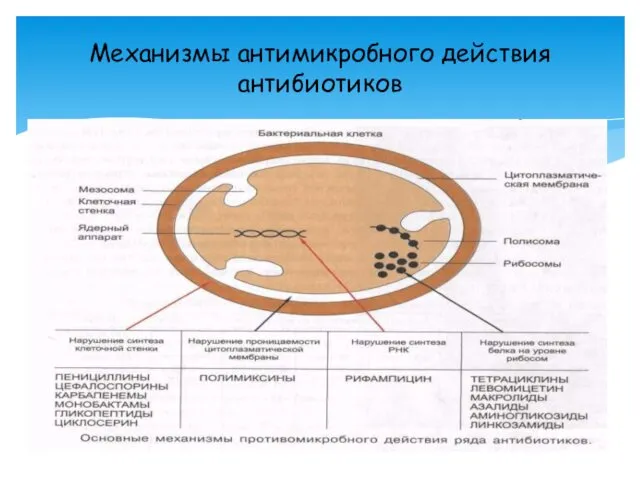
- 5. Механизмы антимикробного действия антибиотиков
- 6. Бета-лактамы ПЕНИЦИЛЛИНЫ ЦЕФАЛОСПОРИНЫ КАРБАПЕНЕМЫ МОНОБАКТАМЫ КЛАССИФИКАЦИЯ АНТИБАКТЕРИАЛЬНЫХ ПРЕПАРАТОВ
- 7. КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ – амоксициллин + клавулановая кислота тикарциллин + клавулановая кислота ампициллин + сульбактам цефаперазон +
- 8. ИНГИБИТОРЫ ДНК –ГИРАЗЫ Хинолоны - налидиксовая кислота, пипемидиевая кислота Фторхинолоны - норфлоксацин, пефлоксацин, ципрофлоксацин, офлоксацин, помефлоксацин,
- 9. ДРУГИЕ АНТИМИКРОБНЫЕ ПРЕПАРАТЫ - хлорамфеникол, фузидиевая кислота, спектиномицин, фосфомицин ПРОТИВОГРИБКОВЫЕ ПРЕПАРАТЫ - амфотерицин В, интраконазол, кетоконазол,
- 10. Изменение мишени действия. Ферментативную инактивацию антимикробного ЛС. Активное выведение антимикробного ЛС из микробной клетки. Нарушение проницаемости
- 11. Антибиотики с концентрационно-зависимой активностью -Аминогликозиды и фторхиноолоны Антибиотики время-зависимой активностью. -пеницилины и цефалоспорины Влияние фармакодинамики на
- 12. бактерицидные (вызывающие гибель микроба) антибиотики (целесообразно применять в тяжелых случаях) бактериостатические антибиотики, которые вызывают приостановку размножения
- 13. При чувствительной флоре: Биодоступность (при приеме внутрь) Способность проникать в инф очаг Состояние функции элим органов
- 14. Точная постановка диагноза. Уточнение показаний к АБ терапии Выбор оптимального антимикробного ЛС с учетом: - активности
- 15. Внебольничные инфекции-возникшие вне больницы и ставшие причиной госпитализации пациента-причина-ограниченный и стабильный круг возбудителей, зависящий от локализации
- 16. Streptococcus pneumonia. Резистентность пневмококков к бензилпенициллину -3-4%, к макролидам - 2-4%, тетрациклину - 56-63%. Почти все
- 17. Escherichia coli. Резистентность к пиперациллину - 44%, ампициллину 40%, гентамицину 13%, амикацину 1%, имипенему 0%, ципрофлоксацину
- 18. ВЗОМТ: тактика лечения (согласно международным рекомендациям) 1. Schindlbeck С, Dziura D, Mylonas I Diagnosis of pelvic
- 19. тяжесть состояния больного, обусловленной основным заболеванием; частое выделение из раны или брюшной полости двух и более
- 20. Proteus s.p.p. - резистентность к тазоцину 1%, цефтриаксону 10%, цефтазидиму 3%, цефепиму 2%, имипинему 0%, ципрофлоксацину
- 21. S.aureus и коагулазонегативные стафилококки. Устойчивость к оксациллину встречается у коагулазонегативных стафилококков в 66%, у S. aureus
- 22. Антибиотики и тип инфекции Внебольничные инфекции При грамм+ флоре -Бета-лактамные антиб -Защищенные пеницилины -Макролиды При грамм-
- 23. Эмпирический – выбор на основании предполагаемой этиологии заболевания в зависимости от первичной локализации очага инфекции. Целенаправленный
- 24. Выбранный режим терапии охватывает всех потенциальных возбудителей инфекции. При выборе антибактериального препарата учитывается риск селекции полирезистентных
- 25. Неправильный микробилогический диагноз и соотвественно, выбор ЛС. Взаимодействие с другим ЛС при комбинированной терапии Присоединение суперинфекции
- 26. Изменение мишени действия. Ферментативную инактивацию антимикробного ЛС. Активное выведение антимикробного ЛС из микробной клетки. Нарушение проницаемости
- 27. Обычные сроки 5 до 10 дней. Более длительная антибиотикотерапия не желательна из-за развития возможных осложнений лечения,
- 28. Обычные сроки 5 до 10 дней. При локализации инфекции в органах и тканях, в которых терапевтические
- 30. Скачать презентацию


























 Путешествие по сказке Колобок
Путешествие по сказке Колобок Витамины- чудесные вещества
Витамины- чудесные вещества 20231011_opora_i_dvizhenie
20231011_opora_i_dvizhenie Формирование действий самостоятельного создания, способов решения проблемы в процессе решения комбинированных задач в 11 классе
Формирование действий самостоятельного создания, способов решения проблемы в процессе решения комбинированных задач в 11 классе Презентации по ОБЖ
Презентации по ОБЖ Транспорт_спецтехника_1
Транспорт_спецтехника_1 Деление окружности на равные части. Геометрические построения – урок черчения в 8 классе
Деление окружности на равные части. Геометрические построения – урок черчения в 8 классе Презентация Как помочь подросткам подготовиться к экзаменам?
Презентация Как помочь подросткам подготовиться к экзаменам? Лазерная импульсная наплавка
Лазерная импульсная наплавка Восславим женщину-мать!
Восславим женщину-мать! Проект Как просыпаются деревья для детей младшей группы
Проект Как просыпаются деревья для детей младшей группы Информационные и коммуникационные технологии
Информационные и коммуникационные технологии Успешный руководитель
Успешный руководитель Устройство для производство профильных заготовок резинотехнических изделий
Устройство для производство профильных заготовок резинотехнических изделий Мой город Сургут
Мой город Сургут Формирование универсальных учебных действий при проведении уроков по физической культуре разных типов
Формирование универсальных учебных действий при проведении уроков по физической культуре разных типов Ваш ребенок пятиклассник
Ваш ребенок пятиклассник Отказы несущих и ограждающих конструкций
Отказы несущих и ограждающих конструкций Презентация проекта Школьная форма моего класса
Презентация проекта Школьная форма моего класса Госпошлина - новый банк 27.03.2015
Госпошлина - новый банк 27.03.2015 Родительское собрание для будущих первоклассников.
Родительское собрание для будущих первоклассников. Тренды развития ГИС и интеграция с цифровой экономикой РФ
Тренды развития ГИС и интеграция с цифровой экономикой РФ Презентация Письма с фронта
Презентация Письма с фронта Викторина Отгадай сказку
Викторина Отгадай сказку Понятие, классификация и процесс реализации коммерческих сделок
Понятие, классификация и процесс реализации коммерческих сделок Строительные конструкции. Сущность железобетона
Строительные конструкции. Сущность железобетона Презентация Классификация неорганических веществ
Презентация Классификация неорганических веществ Николай Васильевич Гоголь
Николай Васильевич Гоголь